Группы крови и иммунитет.. Группы крови и иммунитет. Системы групп крови
 Скачать 0.53 Mb. Скачать 0.53 Mb.
|
|
Системы групп крови Со временем, выяснилось, что для того чтобы кровь донора "прижилась" в организме реципиента, она должна быть с ней совместимой. Условия подобной совместимости были открыты лишь в 1901 г. венским исследователем Карлом Ландштейнером. Он предложил классификацию крови людей, состоящую из 3 групп. Современную классификацию АВ0 системы, состоящую из 4-х групп предложил чешский профессор Ян Янский в 1907 году. Крупным событием начала 20 в. следует считать предложение В.А. Юревича и Н.К. Розенгарта (1910), использовать цитрат натрия для предотвращения свертывания крови при переливаниях. Цитратный метод переливания крови получил всеобщее признание. Некоторые важнейшие системы групп крови Наиболее значимы системы АВ0 и Rh поскольку антигены этих систем широко распространены и высоко иммунологичны. Остальные системы либо мало распространены, либо их антигены мало иммунологичны. Особенности системы АВ0 100% - ная распространенность Наличие в плазме естественных антител (агглютининов) Агглютинины АВ0 системы – полные антитела – не проникают через плацентарный барьер. В крови новорожденных как правило нет антител системы АВ0. Они появляются в течении первого года жизни. По-видимому продукция антител вызывается веществами пищи или кишечной микрофлоры. Распределение групп крови системы АВ0 Антигены и антитела системы АВ0 В мембрану эритроцитов встроен ряд полисахаридно-аминокислотных комплексов, обладающих антигенными свойствами (агглютиногены). К антигенам в плазме находятся специфические антитела (агглютинины), которые представляют собой фракции γ—глобулинов. 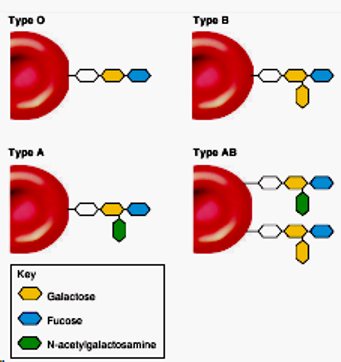 Антигены и антитела системы АВ0 Антигены и антитела системы АВ0Условия агглютинации: А + или В + 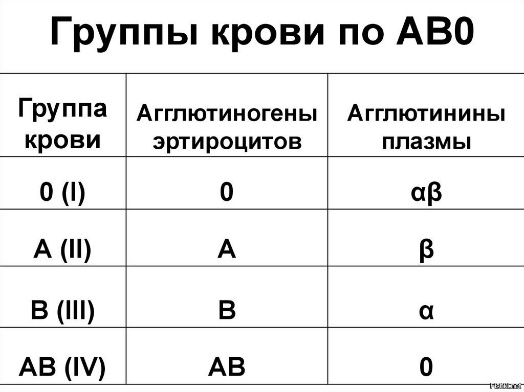 При реакции антиген-антитело молекула антитела образует связь между двумя эритроцитами, поскольку обладает как минимум двумя центрами связывания. В результате этого происходит склеивание большого числа эритроцитов, а затем гемолиз. Возникает явление гемотрансфузионного шока. Определение групп крови с помощью цолеклонов В цолеклонах находятся агглютинины (антитела): Наследование групп крови Система резус фактора (Rh) Rh-фактор был обнаружен в 1939 (Левин и Стетсон) и 1940 г. (Ландштайнер и Винер). Авторы у кроликов и морских свинок изучали образование АТ к эритроцитам обезьян из рода макак (Macaca rhesus). Оказалось, что сыворотка иммунизированных грызунов агглютинировала не только эритроциты макак, но также эритроциты 85% европейцев (их кровь Rh-положительна, у остальных 15% - Rh-отрицательна). Система Rh-фактора Является второй по значимости системой групп крови (клинически значимой). Система антигенов резус представлена пятью основными антигенами: D, C, с, Е, e (ранее считали, что их шесть, но позже было доказано, что аллельного гена d не существует). C и с, а также Е и e - аллельные антигены. Каждая из хромосом несёт только три гена из пяти: D, С или с, Е или е. Для простоты кровь, содержащую D-агглютиноген называют Rh-положительной (Rh+), а не содержащую - Rh-отрицательной (Rh-). Антигены появляются в возрасте 5-10 недель. Передаются по наследству. Rh-принадлежность в течении жизни не меняется, однако активность Rh-агглютиногена может меняться. Отличия от системы АВ0 Нет готовых антител (до 4-х раз можно перелить Rh+ кровь Rh- реципиенту). Rh-агглютинины – неполные антитела и могут проникать через плацентарный барьер. Переливание крови При переливании Rh+ крови Rh- реципиенту, в крови последнего образуются специфические антитела – агглютинины к резус агенту (d- агглютинины). Поэтому повторное введение этому человеку Rh+ крови может привести к агглютинации и гемотрансфузионному шоку. Rh-фактор при беременности Первая беременность Rh-отрицательной матери Rh-положительным плодом не приводит к резус конфликту. Проникновение в кровь матери D-агглютиногенов способствует началу наработки антител. Резус-конфликт может возникнуть при повторной беременности Rh-отрицательной матери Rh-положительным плодом, когда у матери имеются уже готовые антитела. В этом случае исход беременности зависит от титра антител. Профилактика резус-конфликта Образование антител в организме матери можно ограничить или полностью подавить путем D-профилактики. Введение анти-D-глобулина непосредственно после родов блокирует Rh+ эритроциты, попавшие в её кровь. Эритроциты разрушаются и наработки антител не происходит. Гемотрансфузия. Основные цели гемотрансфузии Заместительная (восстановление дыхания, кровообращения, водного баланса), Гемостатическая, Стимулирующая и иммунобиологическая, Дезинтоксикационная, Диуретическая, Питательная, Реологическая, Обменная. Общие правила переливания крови Перепроверить группу крови реципиента по системам АВ0 и Rh, сверить полученный результат с данными в истории болезни. Перепроверить группу крови по системе АВ0 и Rh донорского контейнера и сопоставить результат с данными на этикетке контейнера. Уточнить у реципиента Ф.И.О., год рождения и сверить их с указанными на титульном листе истории болезни. Данные должны совпадать, и реципиент должен их по возможности подтвердить. Необходимо переливать только одногруппную кровь. Однако при отсутствии одногруппной по системе АВ0 крови (за исключением детей) допускается: переливание Rh- 0(I) группы реципиенту с любой группой крови в количестве до 500 мл. Rh- эритроцитная масса или взвесь от доноров группы А(II) или В(III) могут быть перелиты реципиенту с AB(IV)-группой, независимо от его резус–принадлежности. при отсутствии одногруппной плазмы реципиенту м.б. перелита плазма группы АВ(IV). ГЛАВНОЕ! Плазма реципиента должна быть пригодна для жизни эритроцитов донора; Агглютинины донора в расчет не берутся – правило разведения – 200-500 мл донорской крови неродной группы может быть перелито реципиенту без последствий (агглютинации не происходит). Кровозаменители и плазмозаменители донорская кровь (с цитратом или гепарином) используется для восстановления ОЦК с сохранением физических и функциональных свойств при кровопотере), эритроцитарная масса применяется для восстановления кислородтранспортной функции крови при небольшом увеличении ОЦК, эритроцитарная взвесь (деплазмированный концентрат эритроцитов) переливается лицам с тяжелой аллергией в анамнезе с целью предупреждения анафилактических реакций, а также больным с дефицитом IgA или при обнаружении у реципиента антител к IgA тромбоцитарная масса (переливание тромбоцитарного концентрата стало в последние годы обязательным условием программной терапии опухолей системы крови, апластической анемии, проведения трансплантации костного мозга), Кровозаменители и плазмозаменители лейкоцитарная масса переливается при снижении абсолютного количества гранулоцитов у реципиента менее 0,5 х 109/л, при наличии неконтролируемой инфекции, эффективно при сепсисе новорожденных. плазма крови - компоненты плазмы поддерживают нормальный ОЦК, ее жидкое состояние, онкотическое давление, равновесное состояние системы свертывания и фибринолиза, баланс электролитов и кислотно-щелочное равновесие крови, препараты крови (отдельные белковые фракции) Альбумин - один из важнейших белков крови. По сравнению с плазмой в меньших дозах эффективнее увеличивает ОЦК, меньше содержит Na+, что имеет значение при борьбе с отеками. Фибриноген - один из белков свертывающей системы крови. Применяется для гемостаза). Кровозамещающие растворы гемодинамические (полиглюкин, реополиглюкин, желатиноль) дезинтоксикационные (гемодез, полидез) препараты для парентерального питания (гидролизат казеина, аминокровин, аминопептид) регуляторы водно-солевого обмена (физиологический раствор, маннитол, сорбитол) Запрещается переливание компонентов крови, предварительно не исследованных на ВИЧ, гепатиты В и С, сифилис!!! Иммунитет 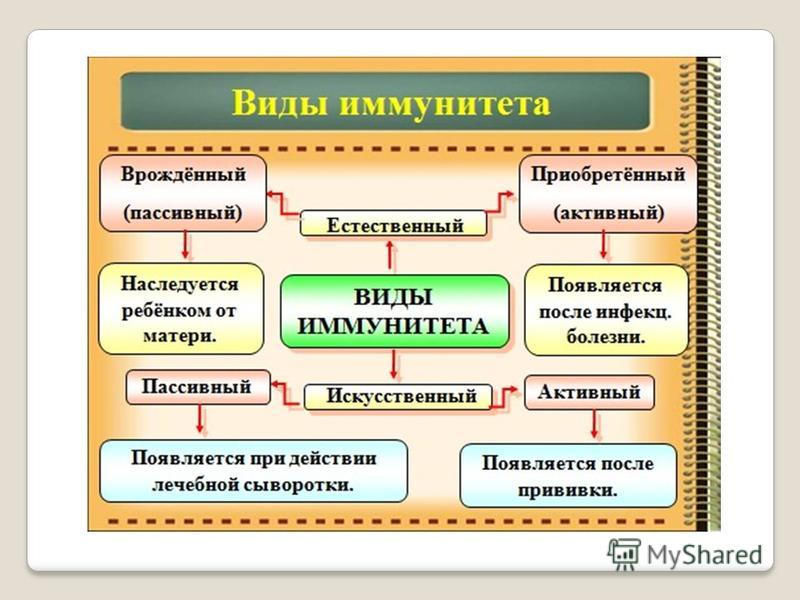 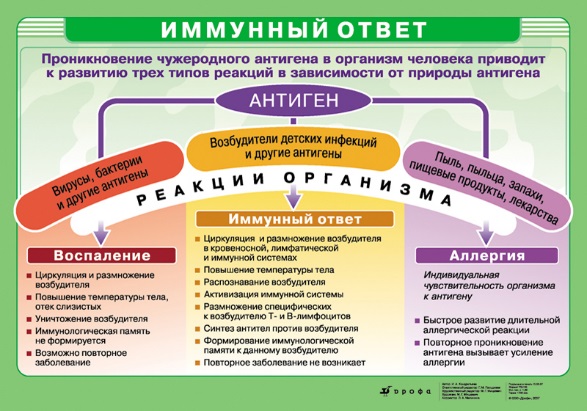 ИММУННАЯ СИСТЕМА состоит из: ИММУННАЯ СИСТЕМА состоит из:Неспецифической иммунной системы (способна обезвреживать организм от чужеродных агентов с которыми организм сталкивается впервые) Специфической иммунной системы (формируется лишь после первичного контакта с чужеродным фактором) Спектр иммунных ответов можно разделить на 3 типа: неспецифическая резистентность, врожденный иммунитет, приобретенный иммунитет. Неспецифическая иммунная система необходима для: уничтожения инородных частиц, разрушения комплексов антиген-антитело, активации клеток, участвующих в воспалительных реакциях. К этим системам относят: барьеры между внешней и внутренней средой организма, кининовая система, система комплемента, пропердиновая система, интерферон, неспецифические клеточные системы Барьеры 1. Кожа: - сальные секреты и пот создают слегка кислую рН уничтожающую грибки, - непрерывное шелушение способствует удалению бактерий 2. Слизистые оболочки содержат: - муцины, - антибактериальные факторы (лизоцим, лактоферрин, пероксидазы, компоненты комплемента и др.), - иммуноглобулины классов IgA, IgM и IgG, относящиеся к факторам иммунитета, - нейтрофилы и макрофаги, мигрирующие из кровеносного русла, - биение ресничек Кининовая система Кининовая система работает в очаге воспаления. Например: на занозе адсорбируется XII фактор свертывания (Хагемана) – один изначальных компонентов системы крови. В жидкой фазе крови он спонтанно диссоциирует на два фрагмента –ХIIа и XIIв. ХIIа адсорбируется на поверхности занозы, где стабилизируется и запускает синтез кининов. Генерация брадикинина: Брадикинин - является одним из главных медиаторов воспаления. Он вызывает “размыкание” краев клеток сосудистого эндотелия и открывает путь плазме в очаг воспаления. Т.о. кининовая система: 1. обнаруживает чужеродное тело по его отрицательно заряженной поверхности. 2. быстро активируема за счет каскадных усилений начальной реакции. Активированный XII индуцирует и систему свертывания крови, что способствует изоляции очага воспаления. Система комплемента В настоящее время к системе комплемента относят более 25 белков и их активных фрагментов, из которых девять — комплементные белки (С1-С9), а остальные — факторы комплемента (B, D, P, H и др.). Главной функцией системы комплемента является отличие «своего» от «чужого», что осуществляется за счет регуляторных молекул находящихся на клетках организма и подавляющих активацию комплемента. Функции системы комплемента: лизис клеток; растворение иммунных комплексов; участие в фагоцитозе; участие в воспалительной реакции; образование хемотаксинов; модуляция иммунного ответа; нейтрализация веществ. активация факторов комплемента за счет расщепления на: крупные фрагменты (обозначают буквой «b»): связываются с клеточными мембранами, активируют следующий фактор в системе комплемента мелкие фрагменты (обозначают буквой «a»): обладают хемотаксическим действием, увеличивают проницаемость мембран, активируют гранулоциты и макрофаги и вызывают воспалительную реакцию 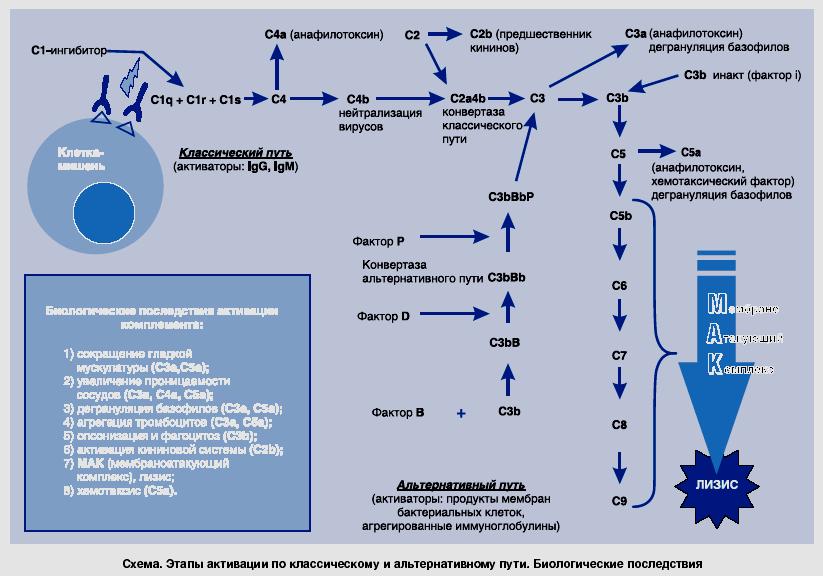 Пропердиновая система Пропердиновая система является своего рода «скорой помощью», которая включается в работу сразу же после попадания чужеродных агентов в организм, требует немедленной защиты до того, как образуются специфические иммуноглобулины и специфические иммунные комплексы. Она активирует систему комплемента по альтернативному пути Пропердиновая система представлена в организме группой белков, имеющих буквенное обозначение, – факторы D и В. При их участии происходит образование неустойчивого фермента СЗbВb. Белок пропердин (Р), соединяясь с ним, стабилизирует этот комплекс и обеспечивает его длительное функционирование. РС3bВb активирует белок С3 системы комплемента. Фактор В расщепляется на два фрагмента: Фрагмент Ва является хемотаксическим фактором для нейтрофилов. Фрагмент Вb активирует макрофаги и способствует их прикреплению и распластыванию на поверхности клеток. Система интерферона - важнейший фактор неспецифической резистентности организма человека. Функции интерферона: антивирусная, противоопухолевая, иммуномодулирующая, радиопротективная. Различают три типа интерферонов (ИФН): -интерферон синтезируют лейкоциты периферической крови (ранее был известен как лейкоцитарный ИФН); -интерферон синтезируют фибробласты (ранее известен как фибробластный ИФН); γ -интерферон - продукт стимулированных Т-лимфоцитов, NK-клеток и, возможно, макрофагов (ранее был известен как иммунный ИФН). Механизм антивирусного действия ИФН Интерферон индуцируют антивирусное состояние клетки благодаря угнетению трансляции вирусной мРНК. ИФН не обладают вирусоспецифичностъю (широкий спектр антивирусной активности). ИФН взаимодействует с неинфицированными клетками, препятствуя реализации репродуктивного цикла вирусов за счёт активации клеточных протеинкиназ. ИФН повышают цитотоксичность макрофагов, но подавляют размножение лимфоцитов, поэтому при вирусных инфекциях подавляют иммунитет. Неспецифические клеточные системы Эти системы включают лейкоциты и макрофаги, способные осуществлять фагоцитоз и благодаря этому уничтожающие болезнетворные агенты и комплексы антиген–антитело. Тканевые макрофаги играют также важную роль в распознавании инородных частиц специфической иммунной системой. Специфическая иммунная система Специфическая иммунная система отвечает на внедрение чужеродных клеток, частиц или молекул (антигенов) образованием: специфических защитных веществ, локализованных внутри клеток или на их поверхности (специфический клеточный иммунитет) специфических защитных веществ, растворенных в плазме (антитела, специфический гуморальный иммунитет). Эти вещества воздействуют на чужеродные частицы и соединяются с ними (реакции антиген–антитело). Специфичность иммунной реакции определяется лимфоцитами и продуцируемыми ими специфическими иммуноглобулинами. Имеются 3 типа лимфоцитов: В‑лимфоциты (10% всех лимфоцитов), обеспечивающие гуморальный иммунитет Т‑лимфоциты (80% и более всех лимфоцитов), обеспечивающие клеточный иммунитет NK‑клетки (около 5–10% всех лимфоцитов). В ответ на антигенное раздражение лимфоциты могут, оседая в лимфоидной ткани, активно размножаться и дифференцироваться в конечные эффекторные клетки (в плазматические клетки из В-лимфоцитов и цитотоксические — из Т-лимфоцитов). Клетки, участвующие в реакциях специфического иммунитета: антигенпредставляющие (презентирующие) клетки (АПК), захватывающие антигены, перерабатывающие их и представляющие соответствующие антигенные детерминанты другим иммунокомпетентным клеткам, (к АПК относятся дендритные АПК, моноциты и макрофаги, а также В-лимфоциты); эффекторные клетки, непосредственно осуществляющие реакции специфического иммунитета (к ним относятся цитотоксические T-лимфоциты и плазматические клетки); регуляторные клетки обеспечивают активацию или угнетение отдельных звеньев иммунных реакций: активаторы: индукторы T-хелперов, индукторы T-супрессоров, T-хелперы, макрофаги; ингибиторы: T-супрессоры; Т-контрсупрессоры делают T-хелперы нечувствительными к Т-супрессорам; клетки памяти, хранящие информацию о взаимодействии с конкретным антигеном и тем самым способствующие более активному развитию иммунного ответа при повторном его воздействии. Фазы специфического иммунного ответа: распознавание антигена; активацию лимфоцитов; эффекторное действие. Специфический клеточный иммунитет Этапы: Проникший в организм антиген захватывается АПК и выносится на поверхность клетки в комплексе с белками МНС-II* для распознавания Тх или с молекулами МНС-I, распознаваемом Тк. Для иммунного ответа необходимо одновременное распознавание как чужеродного антигена , так и собственного антигена МНС. Процесс распознавания активирует АПК, которые начинают секретировать сигнальные белки IL-1, стимулирующие пролиферацию этих Т-лимфоцитов. Активированные Тх продуцируют IL-2, стимулирующий пролиферацию Тх и Тк. (МНС (Major Hislocompatibility Complex) - гликопротеины гистосовместимости). Клонированные и активированные Тк способны узнавать и связывать инфицированные клетки организма, на поверхности которых есть вирусные фрагменты, связанные с МНС-I. (Тк секретируют перфорин, обеспечивая лизис. Активированные Тх распознают на поверхности В-клеток тот же комплекс: МНС II – антиген, который присутствует на АПК, запуская гуморальный иммунитет. Часть дочерних лимфоцитов образует группу клеток иммунологической памяти. Специфический гуморальный иммунитет За этот вид иммунитета отвечают В-лимфоциты. В-лимфоциты, в отличие от T-клеток, обладают слабой способностью к рециркуляции. В связи с этим В-клетки практически отсутствуют в лимфе грудного протока, в крови же их количество составляет не более 30%. Среди В-лимфоцитов преобладают короткоживущие, хотя встречаются и долгоживущие формы. Характерной особенностью В-лимфоцита является наличие на его поверхности иммуноглобулинового рецептора (IgM), а также рецептора к СЗ- компоненту комплемента. Этапы: Мембраносвязанные антитела В-лимфоцитов (IgM) выполняют функции антигенраспознающих рецепторов. После связывания антигена с рецептором происходит его фагоцитоз В-лимфоцитом и вынос антигенной детерминанты в комплексе с белками МНС-II на поверхность клетки. Т-лимфоциты распознают антиген только в комплексе с белками МНС. Связывание Т-хелперов, имеющих на своей поверхности рецептор, специфичный по отношению к данному антигену, стимулирует выработку в Т-хелперах медиаторов иммунного ответа – интерлейкинов. IL-2, воздействуя на В-лимфоцит, активируют процесс размножения и преобразования в плазматическую клетку. Часть дочерних клеток превращаются в клетки иммунологической памяти и разносятся по организму. Продукция антител может протекать без участия Т-клеток, если антигенами являются молекулы биополимеров с повторяющимися эпитопами, например белковые и липополисахаридные антигены бактерий, вирусов. Развивающийся при этом иммунный ответ идет по IgM-типу. Переключение на синтез иммуноглобулинов других типов в отсутствие кооперации с Т-клетками либо невозможно, либо длится непродолжительное время. Классы иммуноглобулинов IgM - антитела, которые первыми производятся в ответ воздействие антигена. IgG - самый многочисленный класс антител. Они производятся в ответ на повторное воздействие антигена (могут переходить через плацентарный барьер). IgA - антитела, которые защищают организма от вторжения микроорганизмов через слизистые оболочки. IgE - антитела, которые вызывают немедленные аллергические реакции, важны в борьбе против паразитарных заболеваний. IgD - антитела, присутствующие в очень небольшом количестве в циркулирующей крови. Их функция до конца не понятна. NK‑КЛЕТКИ NK‑клетки — лимфоциты, лишённые характерных для Т- и В‑клеток поверхностноклеточных детерминант. Эти клетки содержат цитолитические гранулы с перфорином, уничтожают трансформированные (опухолевые) и инфицированные вирусами, а также чужеродные клетки. Взаимосвязь неспецифического и специфического иммунитета Антитела подключают механизмы неспецифического иммунитета: фагоцитоз, комплемент и т. д. Т-хелперы, распознавая комплекс МНС-антиген, активируют секрецию цитокинов, стимулирующих синтез В-лимфоцитами антител, и последующее подключение воспаления и фагоцитоза к иммунному ответу через систему комплемента. Т.о. защита от инфекции включает 3 линии: Неспецифический иммунитет (сразу при внедрении микроба), Образование антител и специфических лимфоцитов (специфическое распознавания антигена) На заключительной стадии иммунного ответа снова подключается неспецифический иммунитет. Аллергия Выделяют 3 вида проявления аллергической реакции (измененной формы иммунного ответа): Гиперэргия Гипергия Анергия Ч 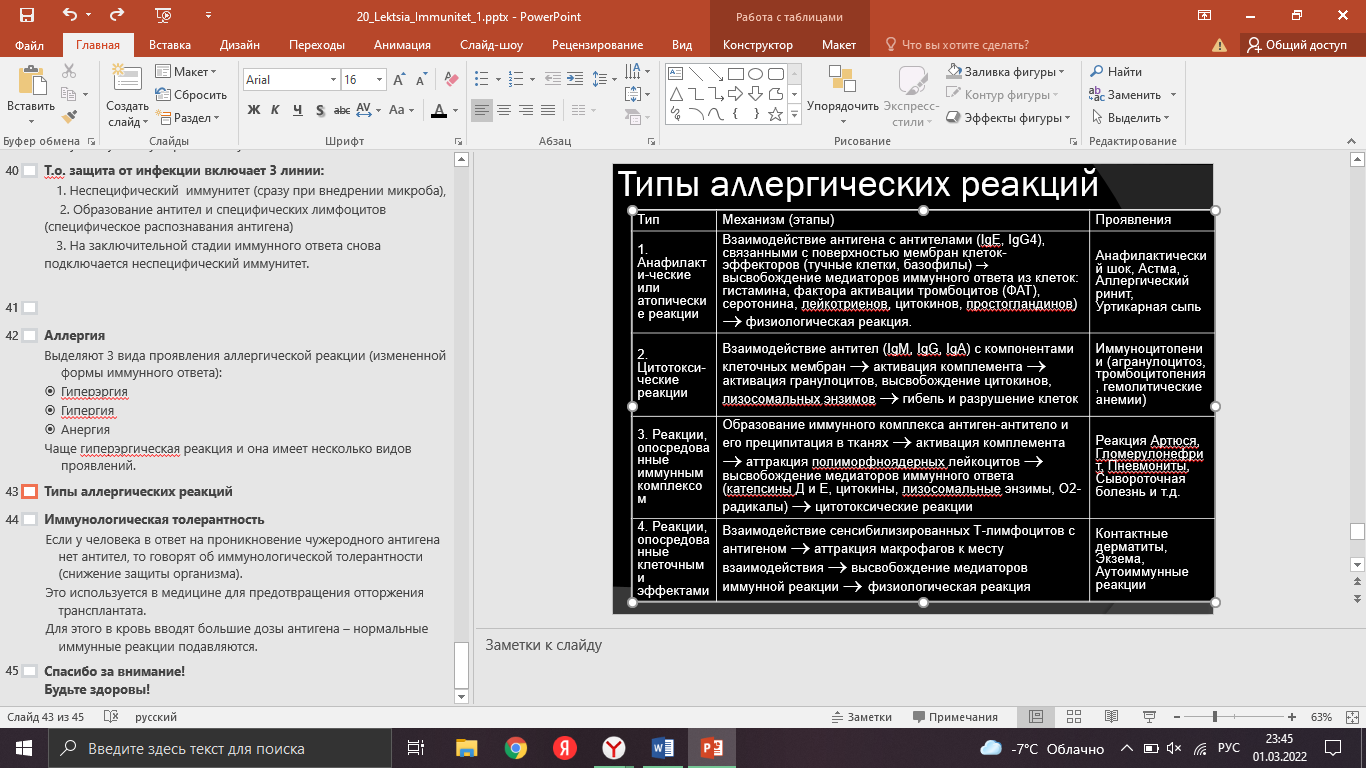 аще гиперэргическая реакция и она имеет несколько видов проявлений. аще гиперэргическая реакция и она имеет несколько видов проявлений.Иммунологическая толерантность Если у человека в ответ на проникновение чужеродного антигена нет антител, то говорят об иммунологической толерантности (снижение защиты организма). Это используется в медицине для предотвращения отторжения трансплантата. Для этого в кровь вводят большие дозы антигена – нормальные иммунные реакции подавляются. |
