Алканы. Реферат - Алканы. Содержание главы Строение алканов
 Скачать 136 Kb. Скачать 136 Kb.
|
АлканыСодержание главы: 1. Строение алканов. 2. Способы получения алканов. 3. Химические свойства алканов. Наиболее простыми органическими соединениями являются предельные углеводороды или алканы. В соответствии с названием, их молекулы состоят из атомов углерода, образующих скелет, и атомов водорода. Углеродный скелет представляет собой открытую линейную ("нормальные" алканы) или разветвленную цепь. В молекулах этих соединений все атомы углерода имеют максимальную валентность, равную четырем, поэтому их называют предельными, или насыщенными. Таким образом, в алканах реализуются только одинарные -связи. Алканы образуют гомологический ряд, и формула любого члена этого ряда имеет вид CnH2n+2. Гомологический ряд – это бесконечный ряд сходных по строению соединений, причем рядом стоящие представители этого ряда отличаются друг от друга на нефункциональную группу, которая мало влияет на свойства соединений. Она называется гомологической разностью (чаще всего это, как в алканах, группа СН2). Все представители гомологического ряда обладают сходными химическими свойствами. Гомологический ряд алканов начинается с метана, имеющего один углеродный атом. Первые четыре члена ряда имеют тривиальные (случайные или исторические) названия, названия же остальных представителей являются производными греческих и латинских числительных в соответствии с количеством атомов углерода в наиболее длинной цепи молекулы. Физические свойства гомологов плавно меняются с изменением молярной массы, что особенно заметно по температурам кипения алканов (С): СН4 метан (т. пл. = - 182.5, т. кип. = - 164.0) СН3-СН3 этан (т. пл. = - 183.3, т. кип. = - 88.6) СН3-СН2-СН3 пропан (т. пл. = - 189.7, т. кип. = - 42.1) СН3-СН2-СН2-СН3 бутан (т. пл. = - 138.4, т.кип = - 0.5) СН3-СН2-СН2-СН2-СН3 пентан (т. пл. = - 129.7, т. кип. = + 36.1) СН3(СН2)4СН3 гексан (т. пл. = - 95, т. кип. = + 69) СН3(СН2)5СН3 гептан (т. кип. = - 90.5, т. кип. = + 98.4) СН3(СН2)6СН3 октан (т. кип. = - 56.8, т. кип. = + 125.7) Начиная с бутана, алканы существуют в нескольких изомерных структурах, т.к. наличие в молекуле более чем трех атомов углерода открывает возможность для существования разветвленных цепей. Это явление называется структурной изомерией. Бутан имеет 2 изомера, пентан - три, гептан - 9, декан - 75 изомеров. Наиболее распространенные из разветвленных алканов имеют устоявшиеся названия, тогда как для остальных нужно применять номенклатуру IUPAC. Физические свойства разветвленных алканов зачастую отличаются от свойств их линейных изомеров. Особенно это касается температуры плавления, которая сильно зависит от симметрии молекулы: 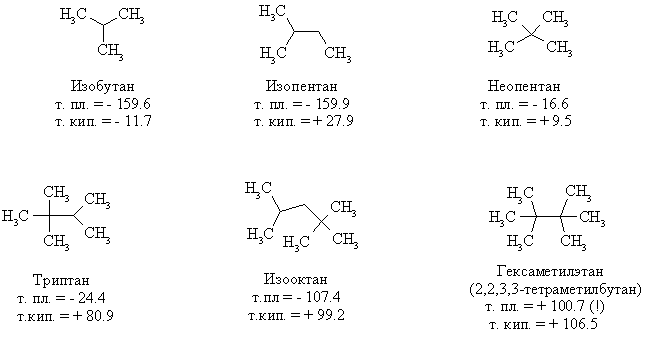 в начало страницы Строение алкановВсе атомы углерода в молекулах алканов имеют sp3-гибридизацию, оси орбиталей направлены к углам тетраэдра, валентный угол равен 109,5о. Длины связей С-С составляют 154 пм, С-Н – 109 пм. Молекула метана представляет собой правильный тетраэдр, в молекуле этана два тетраэдрических метила связаны между собой вершинами. -Связь позволяет структурным фрагментам вращаться вокруг ее оси, поэтому этан может существовать в виде двух конформаций: заторможенной и заслоненной. Заторможенная коформация на 15 кДж/моль выгоднее заслоненной. 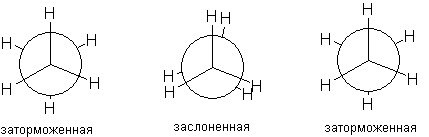 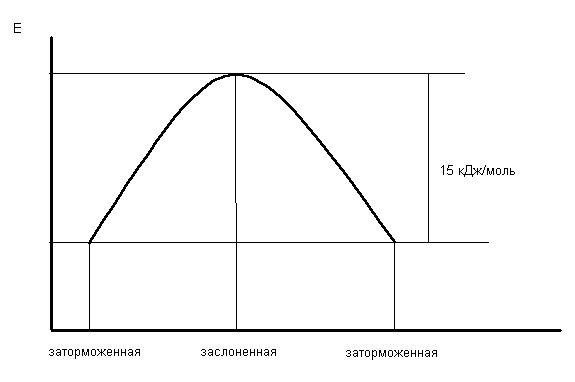 Для последующих гомологов метана число возможных конформаций значительно больше. в начало страницы Способы получения алкановВ промышленности предельные углеводороды получают из нефти фракционированием или крекингом. Перегонка позволяет выделить алканы, изначально присутствующие в нефти, при крекиге происходит разрыв С-С связей, в результате чего образуются углеводороды меньшей молекулярной массы, чем исходные. Низшие гомологи алканов зачастую получают из природного газа. Лабораторные способы можно разделить на три группы: образование алкана с сохранением углеродного скелета исходной молекулы 1. гидрирование непредельных углеводородов 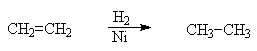 2. восстановление йодалканов 3. восстановление карбонильных соединений (реакции Кижнера-Вольфа и Клемменсена) 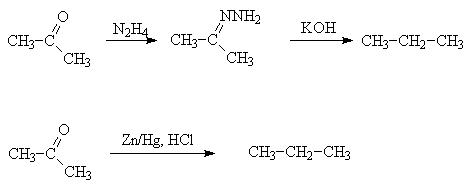 4. гидролиз (сольволиз) реактивов Гриньяра реакции, протекающие с укорочением углеродной цепи получение алканов с более длинной цепью, чем исходные соединения 1. взаимодействие галогеналканов с металлическим натрием или калием (реакция Вюрца) 2. электролиз солей карбоновых кислот (реакция Кольбе) 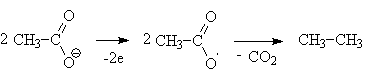 3. взимодействие диалкиллитийкупратов или других металлорганических соединений с активными алкилгалогенидами в начало страницы Химические свойства алкановРазница в электроотрицательностях водорода и углерода составляет 0,4 условных единицы, то есть связь С-Н малополярна. В ходе химических превращений алканов разрыв связей происходит, главным образом, гомолитически, то есть с образованием радикалов. Об этом же свидетельствуют экспериментальные данные, касающиеся энергии связей. Так, гомолиз связи С-Н в метане требует 435 кДж/моль, тогда как для образования пары ионов - карбкатиона СН3+ и гидрид-иона необходимо 878 кДж/моль. Рассмотрение возможности образования другой пары ионов: метильного аниона СН3- и протона показывает, что этот вариант еще более нецелесообразен, т.к. только для превращения атома водорода в катион нужно затратить 1305 кДж/моль. Аналогично, при гомолитическом разрыве связи С-С затрачивается 351 кДж/моль, тогда как гетеролиз требует 757 кДж/моль. Таким образом, наиболее характерными превращениями алканов являются такие, которые происходят в результате атаки частиц с неспаренным электроном (радикалов или атомов), называемые свободно-радикальные реакции. Самый простой пример – это взаимодействие метана с хлором на свету. Свободно-радикальные реакции были подробно изучены Семеновым. Согласно его представлениям, они протекают по цепному механизму, который можно описать следующим образом. Облучение заставляет молекулу хлора диссоциировать на два атома с неспаренным электроном (энергия диссоциации связи Cl-Cl 242,8 кДж/моль). Эта стадия называется инициированием цепи. Затем происходит рост цепи, то есть последовательный ряд стадий реакции, когда из уже имевшихся в системе свободных радикалов возникают новые. 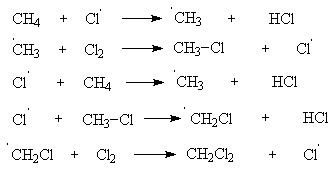 В тех случаях, когда два радикала сталкиваются, образуется новая молекула ( этот процесс называется рекомбинация радикалов), происходит обрыв цепи и реакция прекращается. 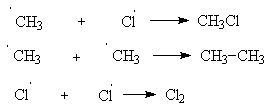 В зависимости от условий, действие галогенов на алканы может протекать либо как замещение атомов водорода атомами галогена, либо с разрывом связи С-С. Последнее превращение требует более жестких условий, несмотря на то, что энергия, необходимая для разрыва С-С-связи (351 кДж/моль) меньше, чем таковая для разрыва С-Н-связи (435 кДж/моль). Это несоответствие объясняется пространственными затруднениями для доступа реагента к углерод-углеродной связи, которая "заслонена" атомами водорода. Можно привести количественное объяснение, которое основано на расчете энергетического эффекта реакции по закону Гесса. Так, для реакции атома хлора с молекулой этана, для которой можно предположить три направления, наиболее выгодным оказывается то, в ходе которого образуется молекула HCl и этильный радикал (H = -21 кДж/моль). Два других направления имеют положительный тепловой эффект (т.е. протекают с поглощением тепла). Это связано с величиной термодинамической стабильности радикалов метила и этила, и энергии связей Н-Cl и C-Cl. 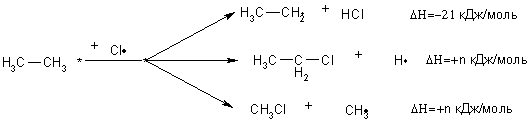 Такой подход позволяет оценить активность различных галогенов в реакциях замещения водорода в алканах (реакциях металепсии). Для получения полной энергетической картины реакции необходимо учитывать энергию разрыва и образования всех связей: диссоциацию молекулы галогена, разрыв С-Н-связи в алкане, а также образование связей C-Hal и H-Hal. Так, хлорирование протекает экзотермически с выделением 117 кДж/моль, бромирование идет также экзотермически, но с меньшим тепловым эффектом (H = -46 кДж/моль), при фторировании выделяется так много энергии, что происходит разрушение молекулы алкана, разрываются и С-Н, и С-С – связи (H = -485 кДж/моль). Реакция йодирования, напротив, эндотермична (H = 50 кДж/моль) и поэтому, несмотря на то, что молекула йода диссоциирует легче других галогенов, замещение не происходит. До сих пор мы рассматривали галогенирование алканов на примере метана и этана, т.е. когда замещение водорода происходит при первичном атоме углерода. Но, как мы видели, даже в столь простых случаях реакция приводит к целому ряду продуктов разной степени замещения. Иная картина наблюдается, когда в реакцию с хлором вступают алканы более сложного строения. Например, в пропане атомы водорода неэквивалентны (6 из них - первичные, остальные два – вторичные). На основании чистой статистики в реакции хлорирования среди продуктов монозамещения соотношение 1-хлорпропана и 2-хлорпропана должно быть 3 : 1. Действительно, при 500 оС это соотношение соблюдается, однако при более низких температурах повышается количество изо-пропилхлорида. h, 25 oC СН3СН2СН3 + Cl2 СН3СН2СН2Cl + СН3СН(Cl)СН3 43% 57% (статистически: 75% 25%) Таким образом, при понижении температуры замещение при вторичном атоме углерода идет с более высокой скоростью, т.е. процесс становится более избирательным. Аналогично, доминирующим продуктом реакции изобутана с хлором оказывается 2-метил-2-хлорпропан, т.е. замещение идет преимущественно при третичном атоме углерода: h, 25 oC СН3СН(СН3)СН3 + Cl2 СН3СН(СН3)СН2Cl + СН3С(СН3)(Cl)СН3 2-метилпропан 64% 36% (статистически 90% 10%) Поскольку в ходе реакции, независимо от ее ориентации, во всех случаях разрывается связь С-Н и образуется связь H-Cl, наблюдаемая региоселективность (преимущественная ориентация) галогенирования именно при третичном С-атоме должна объясняться свойствами промежуточного углеводородного радикала. Ввиду того, что простейшие алифатические радикалы весьма неустойчивы, экспериментальных данных об их геометрии не получено, а квантово-химические расчеты, в зависимости от используемого метода, дают различные результаты. Согласно одним результатам радикал CH3 совершенно плоский, атом углерода находится в sp2-гибридном состоянии, и неспаренный электрон размещен в основном на его p-орбитали. Альтернативный вариант постулирует пирамидальное строение этого радикала, причем пирамида сильно сплющена и легко инвертируется. Недавно были получены рентгеноструктурные данные для свободного радикала не имеющего резонансной стабилизации, т.е. в данной структуре неспаренный электрон принадлежит только одному атому. Согласно этим данным трехвалентный атом имеет плоское строение, т.е. наиболее выгодным для него является sp2-состояние.  Главное различие метильного и трет-бутильного радикалов заключается в следующем: в метиле спиновая плотность (т.е. область, в которой находится неспаренный электрон) принадлежит только атому углерода, тогда как в трет-бутильном радикале она делокализована с участием трех алкильных групп (+I-эффект каждой С-С- и С-Н-связи). Известно, что делокализация электронов снижает энергию частицы (т.к. энергия волны уменьшается с увеличением объема пространства, в котором она распространяется), поэтому трет-бутил-радикал намного выгоднее метильного радикала. Любая химическая реакция идет таким путем, чтобы на самой медленной стадии образовалась по возможности более стабильная промежуточная частица, поэтому в пропане замещение атомов водорода протекает более легко при вторичном атоме углерода. Измерение кинетики хлорирования показывает, что при 200оС скорости замещения при первичном, вторичном и третичном С-атомах относятся как 1:3,9:5,1 При бромировании относительные скорости различаются сильнее – 1:32:1600. К такому течению процесса применяют термин региоспецифичность, почти исключительная региоселективность. Последнее обстоятельство иллюстрирует известное правило химической кинетики: чем менее активна реагирующая частица, тем более она избирательна, т.к. ей труднее преодолеть более высокий потенциальный барьер. 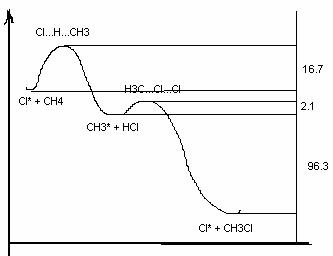 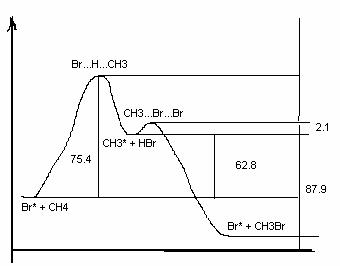 Большинство других реакций замещения водорода в алканах также имеют свободно-радикальный механизм. Сульфохлорирование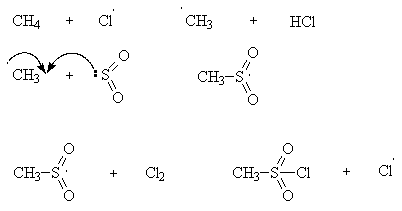 Эта реакция лежит в основе промышленного получения алкансульфокислот, соли которых используются как моющие средства. В промышленности применяют избыток сернистого газа для предотвращения хлорирования. Нитрование по Коновалову (20%-ная азотная кислота, 140 оС). 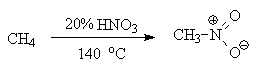 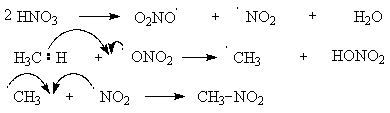 Горение алкановАлканы при высокой температуре на воздухе окисляются (сгорают) до углекислого газа и воды, их пары образуют взрывчатую смесь с воздухом . При сгорании углеводородов выделяется большое количество тепла (метан - 890 кДж/моль), поэтому они широко применяются как источники тепловой энергии, которую используют для нагревания или превращают в другие виды энергии. Реакция также носит свободно-радикальный характер, и для ее инициирования вместо нагревания можно применять источники свободных радикалов, т.е. легко диссоциирующие соединения, например, 2,2'-азодиизобутиронитрил ("химический поджиг"): 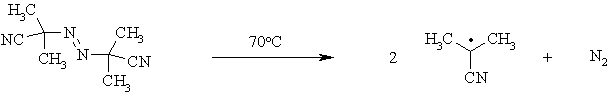 Каталитическое окислениеНа холоду кислород на алканы не действует, но в присутствии катализаторов (солей марганца, солей карбоновых кислот и т.д.) углеводороды окисляются, что приводит к образованию различных кислородсодержащих органических соединений. Роль катализаторов, вероятно, заключается в создании на стадии инициирования цепи высокой концентрации бирадикальной формы молекул кислорода, которые оказываются способными разорвать С-Н-связь. Возникающий алкильный радикал атакует молекулу кислорода и образующийся перекисный радикал реагирует со следующей молекулой алкана. В результате этого образуются новый алкильный радикал и молекула алкилгидропероксида. Если реакция проводится в кислой среде, то гидропероксиды превращаются в кетоны. 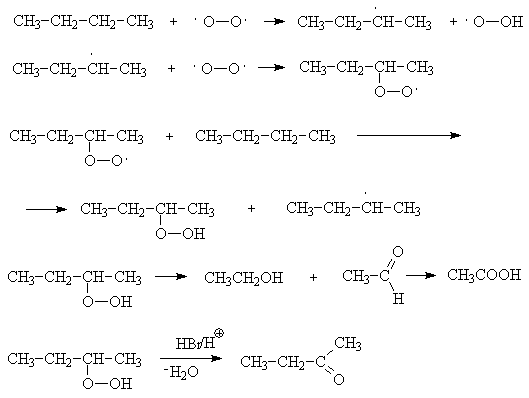 Каталитическое окисление алканов позволяет получать спирты, оксосоединения, карбоновые кислоты. 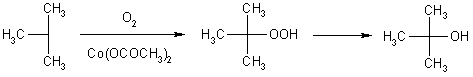 По свободно-радикальному механизму протекает расщепление молекул высших углеводородов под действием высоких температур (пиролиз, крекинг). При высокой температуре амплитуда валентных колебаний атомов превышает допустимые значения и связи гомолитически разрушаются. Образующиеся при этом радикалы реагируют далее в основном двумя путями: диспропорционированием и рекомбинацией. 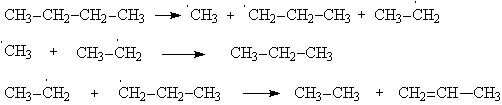 Диспропорционирование, то есть перенос атома водорода от одного радикала к другому приводит к алкану и алкену, рекомбинация - к сшиванию двух радикалов в молекулу алкана. При образовании связи за счет неспаренных электронов двух радикалов выделяется ровно столько энергии, сколько необходимо, чтобы эту связь разорвать. Поэтому рекомбинация возможна только в том случае, если поблизости с реагирующими частицами имеется либо какая-нибудь молекула, либо стенка реакционного сосуда, которая должна забрать хотя бы часть выделившейся энергии. Это обстоятельство объясняет, почему в условиях крекинга происходит уменьшение средней молекулярной массы алканов. Этот процесс имеет важное промышленное значение и широко используется для повышения качества углеводородного сырья. Ионные реакции алкановНаряду со свободнорадикальными реакциями, для алканов известны также некоторые превращения, имеющие ионный механизм. Выше было показано, что действие хлора на изобутан в различных условиях дает смесь продуктов хлорирования, среди которых преобладает третичный хлорид. В то же время, та же реакция в присутствии безводного хлорида алюминия протекает региоспецифично по третичному углеродному атому. Это объясняется тем, что на первой стадии реакции AlCl3, как сильная кислота Льюиса, отрывает гидрид-ион от третичного атома углерода, при этом генерируется чрезвычайно реакционноспособный карбокатион. Этот катион, реагируя с молекулой галогена, превращается в трет-бутилхлорид и освобождает катион хлорония. Последний разрушает комплекс гидрид-иона с кислотой Льюиса, регенерируя AlCl3. 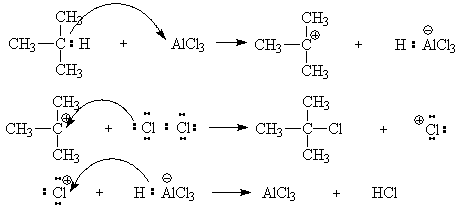 Не исключено, что реализуется другой механизм: гидрид-ион от третичного атома углерода отрывает катион хлорония, являющийся частью комплекса молекулы хлора и хлорида алюминия. Карбкатион, в свою очередь, реагирует с анионом тетрахлороалюминия. 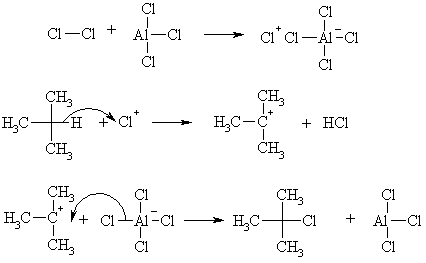 Тот факт, что в реакции изобутана с AlCl3 образуется не изо-, а только трет‑бутилкатион, объясняется аналогично реакции радикального хлорирования. Карбкатионы при третичном С-атоме более устойчивы, чем вторичные и еще более устойчивы, чем первичные. Это объясняется +I-эффектом алкильных заместителей при атоме углерода, несущем положительный заряд. Благодаря индуктивному эффекту происходит делокализация дефицита электронной плотности по -связям алкильных групп, и, чем их больше, тем она эффективнее а, следовательно, тем более устойчив карбкатион. Углеродцентрированные катионы бывают двух типов. Наиболее распространены катионы, образующиеся путем отщепления гидрида или (чаще) другой уходящей вместе с парой электронов группы. В таких катионах положительно заряженный атом связан с тремя заместителями, находится в sp2-гибридном состоянии и имеет вакантную p-орбиталь. Такие катионы называют карбениевыми ионами (формально их можно рассматривать как продукты протонирования карбенов), R2C: + H+ à R2HC+ но нередко можно встретить название карбкатион. Характерным свойством карбкатионов является способность к перегруппировкам с переносом атома водорода или заместителя. При этом образуется более устойчивая система (например, из первичного карбкатиона получается вторичный или из вторичного – третичный): 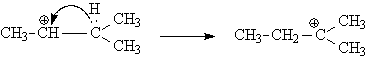 По ионному механизму протекает обмен алифатического водорода на дейтерий в суперкислых средах. В этих условиях промежуточно образуются ионы другого типа: карбониевые ионы с пятикоординированным углеродом, то есть протонированные алканы. Ввиду того, что формально максимальная валентность атома углерода равна четырем, такие частицы называют "гипервалентными". Для их образования требуется суперсильная кислота, которая способна протонировать алканы. К таким системам относится смесь фторсульфоновой кислоты и пятифтористой сурьмы в среде жидкого серного ангидрида (низкосоновный растворитель).  Расщепление карбониевого иона дает молекулу водорода и карбениевый ион, что наблюдалось экспериментально при нагревании растворов алканов с суперкислотах. Это позволяет рассматривать ион карбония как комплекс кислоты CH3+ и молекулы водорода, выполняющей роль -основания. Учитывая сказанное, для перегруппировок алканов в суперкислых средах предложен следующий механизм: 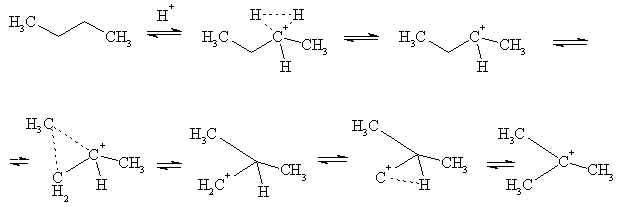 |
