Химическая и концентрационная поляризация. Потенциал разложения и перенапряжение. ФХ_ШевчукФД_р2. Содержание Концентрационная поляризация
 Скачать 0.5 Mb. Скачать 0.5 Mb.
|
СодержаниеКонцентрационная поляризация…………………………………………..3Потенциал разложения и перенапряжение……………………………….5 Список использованных источников……………………………………...6 Концентрационная поляризация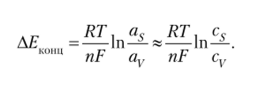 Изменение потенциала электрода вследствие изменения концентрации реагентов в при электродном пространстве при прохождении тока называется концентрационной поляризацией. В свою очередь, изменение концентрации реагирующих веществ в при электродном пространстве вызывается замедленностью подвода реагентов или отвода продуктов реакции. Так как по уравнению Нернста потенциал электрода пропорционален логарифму активности ионов (в разбавленных растворах концентрации ионов), то концентрационная поляризация должна быть пропорциональна разности логарифмов активностей (концентраций) ионов в при электродном пространстве as и в объеме раствора a v: С увеличением плотности тока растет разность между активностями (концентрациями) в приэлектродном пространстве и в объеме раствора и соответственно возрастает концентрационная поляризация: 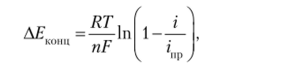 где I — предельная плотность тока; где cv — концентрация реагента в объеме раствора; I) — коэффициент диффузии реагента; 8 — толщина диффузного слоя. Как видно из приведенных уравнений, концентрационная поляризация снижается с увеличением коэффициента диффузии и концентрации реагента, а также с уменьшением толщины диффузного слоя. Толщина этого слоя и концентрационная поляризация уменьшаются при перемешивании раствора. 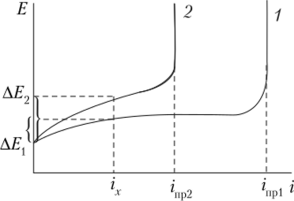 Кривые потенциал — плотность тока при концентрационной поляризации с перемешиванием (1) и без перемешивания (2) На рис. выше приведены типичные кривые зависимости потенциал — плотность тока для концентрационной поляризации, из которых следует, что перемешивание влияет на предельный ток и концентрационную поляризацию. Концентрационная поляризация имеет важное значение для окислительно-восстановительных процессов и меньшее значение — для разряда простых металлических ионов. Концентрационная поляризация не единственная причина отклонения потенциала электрода под током от его равновесного значения. Обычно изменение потенциала при наложении тока оказывается больше, чем концентрационная поляризация. Это является следствием торможения на стадии присоединения или отдачи электронов. Поляризация, вызванная замедленностью разряда или ионизации при протекании электрохимической реакции, называется химической поляризацией. Химическую поляризацию называют также перенапряжением. Потенциал разложения и перенапряжение Потенциал разложения - это минимальная необходимая разность потенциалов, при которой начинается электролиз данного вещества  Иногда они совпадают со стандартными потенциалами. Но на практике величина потенциала разложения равна большей величине. Разность между опытным (экспериментальным) и теоретическим значением потенциала разложения называют перенапряжением.  Список использованных источников Материалы интернет ресурса studizba.com. URL: https://studizba.com/lectures/107-himija/1424-lekcii-po-jelektrohimii/26262-9-jelektroliz-toki-obmena-poljarizacija-jelektroda-perenaprjazhenie-koncentracionnaja-i-jelektrohimicheskaja-poljarizacija.html (дата обращения 02.10.2020) Материалы интернет ресурса portal.tpu.ru. URL: https://portal.tpu.ru/SHARED/s/STRASHKOAN/rabota/Tab8/Tab/Основы%20электрохимических%20мет1.pdf (дата обращения 02.10.2020) Материалы интернет ресурса studopedia.ru. URL: https://studopedia.ru/15_90171_kontsentratsionnaya-i-himicheskaya-polyarizatsiya.html (дата обращения 02.10.2020) |
