Проводящий механизм биологических мембран. Сроп1 реферат тема Проводящий механизм биологических мембран Дисциплина Медицинская биофизика Специальность
 Скачать 205.43 Kb. Скачать 205.43 Kb.
|
СРОП№1 РЕФЕРАТ Тема: Проводящий механизм биологических мембран Дисциплина: Медицинская биофизика Специальность: Стоматология Курс: 1 Группа:113а Форма выполнения: реферат Подготовил:Тайфуров Айваз Проверено:Жумабекова Р. Алматы 2023 Содержание Введение Биологические мембраны. Основные функции биомембран. Общее представление о проницаемости биомембран. Перенос молекул через мембрану. Электрические характеристики биомембран. Строение и функции ионных каналов. Биологический электрогенез Заключение Литература Приложение ВВЕДЕНИЕ Мембранный транспорт – транспорт веществ сквозь клеточную мембрану в клетку или из клетки, осуществляемый с помощью различных механизмов – простой диффузии, облегченной диффузии и активного транспорта. Важнейшее свойство биологической мембраны состоит в ее способности пропускать в клетку и из нее различные вещества. Это имеет большое значение для саморегуляции и поддержания постоянного состава клетки. Такая функция клеточной мембраны выполняется благодаря избирательной проницаемости, т.е. способностью пропускать одни вещества и не пропускать другие. Легче всего проходят через липидный бислой неполярные молекулы с малой молекулярной массой (кислород, азот, бензол). Достаточно быстро проникают сквозь липидный бислой такие мелкие полярные молекулы, как углекислый газ, оксид азота, вода, мочевина. С заметной скоростью проходят через липидный бислой этанол и глицерин, а также стероиды и тиреоидные гормоны. Для более крупных полярных молекул (глюкоза, аминокислоты), а также для ионов липидный бислой практически непроницаем, так как его внутрення часть гидрофобна. Так, для воды коэффициент проницаемости (см/с) составляет около 10-2, для глицерина – 10-5, для глюкозы – 10-7, а для одновалентных ионов – меньше 10-10. Перенос крупных полярных молекул и ионов происходит благодаря белкам-каналам или белкам-переносчикам. Так, в мембранах клеток существуют каналы для ионов натрия, калия и хлора, в мембранах многих клеток – водные каналы аквапорины, а также белки-переносчики для глюкозы, разных групп аминокислот и многих ионов. Активный и пассивный транспорт. Мембраны формируют структуру клетки и осуществляют ее функции. Нарушение функций клеточной и внутриклеточной мембран лежит в основе необратимого повреждения клеток и, как следствие, развитие тяжелых заболеваний сердечно-сосудистой, нервной, эндокринной системы. Биологические мембраны. Основные функции биомембран. Элементарная живая система, способная к самостоятельному существованию, развитию и воспроизведению – это живая клетка – основа строения всех животных и растений. Важнейшими условиями существования клетки являются, с одной стороны, автономность по отношению к окружающей среде (вещество клетки не должно смешиваться с веществом окружения, должна соблюдаться автономность химических реакций в клетке и ее отдельных частях); с другой стороны, связь с окружающей средой (непрерывный, регулируемый обмен веществом и энергией между клеткой и окружающей средой). Живая клетка – открытая система. Единство автономности от окружающей среды и одновременно тесной связи с окружающей средой – необходимое условие функционирования живых организмов на всех уровнях их организации. Поэтому важнейшее условие существования клетки, и, следовательно, жизни – нормальное функционирование биологических мембран. Биологическая мембрана (БМ) – пространство между живыми клетками, которое способно защищать клетку, питать и т.д. Физические, химические и физико-химические свойства биомембран обеспечивают выполнение ими определенных функций, без которых невозможна жизнедеятельность организма. В самом общем виде применительно к мембранам всех типов многообразие этих функций можно свести к 3 основным: механической, барьерной и матричной. Механическая функция заключается в поддержании морфологической целостности и относительной автономности как клетки в целом, так и внутриклеточных органоидов. Она основана, прежде всего, на механических свойствах мембранных структур. Под барьерной функцией понимают создание биомембраной препятствий для свободного переноса веществ через нее. Для одних агентов биомембрана является непреодолимым препятствием, другие легко проходят сквозь нее, причем, как правило, только в определенном направлении, как того требуют векторные свойства мембраны. Матричная функция. Биомембрана служит матрицей для белков-рецепторов, ферментов и других физиологически активных веществ, обеспечивая пространственную организацию рецепторных взаимодействий, метаболических реакций, переноса энергии и других метаболических процессов. Так, биомембраны объединяют встроенные в них ферменты в единый конвейер, где каждый из них действует согласованно с остальными. Общее представление о проницаемости биомембран. Проницаемость биологических мембран - важнейшее свойство биологических мембран, заключающееся в их способности пропускать в клетку и из неё различные метаболиты (аминокислоты, сахара, ионы и т.п.). Проницаемость биомембран имеет большое значение для осморегуляции и поддержания постоянства состава клетки, её физико-химический гомеостаз; играет важную роль в генерации и проведении нервного импульса, в энергообеспечении клетки, сенсорных механизмах и др. процессах жизнедеятельности. Проницаемость биомембран обусловлена особенностями строения биомембран, являющихся осмотическим барьером между клеткой и средой, и служит характерным примером единства и взаимосвязи между структурой и функцией на молекулярном уровне. БМ проницаемы лишь для небольшого числа низкомолекулярных жирорастворимых веществ (глицерин, спирты, мочевина и др.). Такая проницаемость (простая диффузия) играет сравнительно малую роль в процессах переноса веществ через мембраны. Более важные процессы переноса (транслокации) веществ через БМ происходят с участием специфических систем транспорта. Предполагают, что эти системы содержат мембранные переносчики (белки или липопротеиды) и, возможно, ряд др. компонентов, осуществляющих связанные с транспортом функции (например, рецепторные). Переносчик (или их система) связывает переносимое вещество (субстрат) и может перемещаться в мембране. Если переносчики неподвижно фиксированы в БМ, то считают, что в БМ существуют специфические для переносимого вещества поры или каналы. Если переносчик связывается с субстратом путём невалентных взаимодействий (ионными, гидрофобными и др. силами), то такой процесс называется вторичной транслокацией; различают 3 её типа: облегчённая диффузия (унипорт), котранспорт (симпорт) и противотранспорт (антипорт). Механизм облегчённой диффузии не зависит от переноса др. веществ в клетку или из клетки. Этим способом переносится, например, глюкоза в эритроциты. Котранспорт — совместный транспорт двух (или более) веществ в одном направлении. Так, транспорт глюкозы и аминокислот через слизистые оболочки тонкого кишечника сопряжён с транспортом ионов Na+. Механизм противотранспорта подразумевает сопряжение переноса вещества в одном направлении с потоком др. вещества в противоположном направлении. Этим способом осуществляется противоположно направленный перенос ионов Na+ и К+ в нервных клетках. Процессы сопряжённого транспорта (симпорт и антипорт) имеют большое значение в тех случаях, когда переносимое вещество движется против градиента концентрации (из области меньшей в область большей концентрации). Такой активный транспорт, в отличие от пассивного транспорта (по концентрационному градиенту), требует затрат энергии. Энергообеспечение активного транспорта достигается за счёт сопряжения вторичной транслокации с ферментативными реакциями разрыва или образования химических связей. При этом энергия химического превращения расходуется на поддержание осмотического потенциала или асимметрии по обе стороны мембраны. Транспорт веществ через БМ, связанный с разрывом или образованием валентных связей, называется первичной транслокацией. Типичный пример такого процесса — работа «натриевого насоса», сопряжённая с химической реакцией гидролиза богатого энергией аденозинтрифосфата (АТФ), катализируемого ферментом аденозинтрифосфатазой. Гидролиз АТФ сопровождается переносом ионов Na+ из клетки и поступлением в клетку ионов К+; предполагают, что переносчиком ионов К+ является свободный фермент, а ионов Na+ — фосфорилированный фермент, образующийся в ходе гидролиза АТФ. До сих пор не удалось выделить переносчиков из БМ клеток животных. У бактерий четко доказано (главным образом генетическими методами) существование переносчиков — т. н. пермеаз, некоторые из них (например, М-белок — переносчик лактозы у кишечной палочки) выделены в чистом виде. Имеются данные, показывающие, что активный транспорт сахаров и аминокислот у бактерий сопряжён с окислением D-молочной комитеты. У некоторых бактерий обнаружено большое число «связывающих белков», которые, возможно, являются рецепторными компонентами соответствующих транспортных систем. Проницаемость биомембран регулируется гормонами и другими биологически активными веществами. Так, некоторые стероидные гормоны, инсулин и др. увеличивают проницаемость мембран эритроцитов, мышечных и жировых клеток. Проницаемость биомембран возбудимых клеток (например, нервных) зависит от особых веществ — медиаторов (ацетилхолин и др.). На проницаемость биомембран для ионов сильно влияют антибиотики (валиномицин, грамицидин, нонактин), а также некоторые синтетические полиэфиры. В исследованиях П. б. м. — одной из важнейших проблем молекулярной биологии - большое значение имеют модельные мембраны: липидные монослои, искусственные двухслойные мембраны, многослойные замкнутые мембраны (липосомы) и т.п. Для изучения проницаемости биомембран широко применяются электро- химические, физические и химические методы. Уравнение Фика Знак «–» показывает, что суммарная плотность потока вещества при диффузии направлена в сторону уменьшения плотности, D –коэффициент диффузии. Формула показывает, что плотность потока вещества J пропорциональна коэффициенту диффузии D и градиенту концентрации. Это уравнение выражает первый закон Фика (Адольф Фик — немецкий физиолог, установивший законы диффузии в 1855 г.). Перенос молекул через мембрану. Так как внутренняя часть липидного слоя гидрофобна, он представляет собой практически непроницаемый барьер для большинства полярных молекул. Вследствие наличия этого барьера, предотвращается утечка содержимого клеток, однако из-за этого клетка была вынуждена создать специальные механизмы для транспорта растворимых в воде веществ через мембрану. Перенос малых водорастворимых молекул осуществляется при помощи специальных транспортных белков. Это особые трансмембранные белки, каждый из которых отвечает за транспорт определенных молекул или групп родственных молекул. В клетках существуют также механизмы переноса через мембрану макромолекул (белков) и даже крупных частиц. Процесс поглощения макромолекул клеткой называется эндоцитозом. В общих чертах механизм его протекания таков: локальные участки плазматической мембраны впячиваются и замыкаются, образуя эндоцитозный пузырек, затем поглощенная частица обычно попадает в лизосомы и подвергается деградации. 3.1 Диффузия (лат. diffusio — распространение, растекание, рассеивание) — процесс переноса материи или энергии из области с высокой концентрацией в область с низкой концентрацией (против градиента концентрации). Самым известным примером диффузии является перемешивание газов или жидкостей (если в воду капнуть чернил, то жидкость через некоторое время станет равномерно окрашенной). Другой пример связан с твёрдым телом: если один конец стержня нагреть или электрически зарядить, распространяется тепло (или соответственно электрический ток) от горячей (заряженной) части к холодной (незаряженной) части. В случае металлического стержня тепловая диффузия развивается быстро, а ток протекает почти мгновенно. Если стержень изготовлен из синтетического материала, тепловая диффузия протекает медленно, а диффузия электрически заряженных частиц — очень медленно. Диффузия молекул протекает в общем ещё медленнее. Например, если кусочек сахара опустить на дно стакана с водой и воду не перемешивать, то пройдёт несколько недель, прежде чем раствор станет однородным. Ещё медленнее происходит диффузия одного твёрдого вещества в другое. Например, если медь покрыть золотом, то будет происходить диффузия золота в медь, но при нормальных условиях (комнатная температура и атмосферное давление) золотосодержащий слой достигнет толщины в несколько микрометров только через несколько тысяч лет. Все виды диффузии подчиняются одинаковым законам. Скорость диффузии пропорциональна площади поперечного сечения образца, а также разности концентраций, температур или зарядов (в случае относительно небольших величин этих параметров). Так, тепло будет в четыре раза быстрее распространяться через стержень диаметром в два сантиметра, чем через стержень диаметром в один сантиметр. Это тепло будет распространяться быстрее, если перепад температур на одном сантиметре будет 10 °C вместо 5 °C. Скорость диффузии пропорциональна также параметру, характеризующему конкретный материал. В случае тепловой диффузии этот параметр называется теплопроводность, в случае потока электрических зарядов — электропроводность. Количество вещества, которое диффундирует в течение определённого времени, и расстояние, проходимое диффундирующим веществом, пропорциональны квадратному корню времени диффузии. Диффузия представляет собой процесс на молекулярном уровне и определяется случайным характером движения отдельных молекул. Скорость диффузии в связи с этим пропорциональна средней скорости молекул. В случае газов средняя скорость малых молекул больше, а именно она обратно пропорциональна квадратному корню из массы молекулы и растёт с повышением температуры. Диффузионные процессы в твёрдых телах при высоких температурах часто находят практическое применение. Например, в определённых типах электронно- лучевых трубок (ЭЛТ) применяется металлический торий, продиффундировавший через металлический вольфрам при 2000 °C. Электрические характеристики мембран. Особая морфология клеточных мембран определяет их электрические характеристики, среди которых наиболее важными являются емкость и проводимость. Емкостные свойства в основном определяются фосфолипидным бислоем, который непроницаем для гидратированных ионов и в то же время достаточно тонок (около 5 нм), чтобы обеспечивать эффективное разделение и накопление зарядов и электростатическое взаимодействие катионов и анионов. Кроме того, емкостные свойства клеточных мембран являются одной из причин, определяющих временные характеристики электрических процессов, протекающих на клеточных мембранах. Проводмость (g) — величина, обратная электрическому сопротивлению и равная отношению величины общего трансмембранного тока для данного иона к величине, обусловившей его трансмембранной разности потенциалов. Через фосфолипидный бислой могут диффундировать различные вещества, причем степень проницаемости (Р), т. е. способность клеточной мембраны пропускать эти вещества, зависит от разности концентраций диффундирующего вещества по обе стороны мембраны, его растворимости в липидах и свойств клеточной мембраны. Скорость диффузии для заряженных ионов в условиях постоянного поля в мембране определяется подвижностью ионов, толщиной мембраны, распределением ионов в мембране. Для неэлектролитов проницаемость мембраны не влияет на ее проводимость, поскольку неэлектролиты не несут зарядов, т. е. не могут переносить электрический ток. Проводимость мембраны является мерой ее ионной проницаемости. Увеличение проводимости свидетельствует об увеличении количества ионов, проходящих через мембрану. Строение и функции ионных каналов. Ионы Na+, K+, Са2+, Сl- проникают внутрь клетки и выходят наружу через специальные, заполненные жидкостью каналы. Размер каналов довольно мал (диаметр 0,5—0,7 нм). Расчеты показывают, что суммарная площадь каналов занимает незначительную часть поверхности клеточной мембраны. Функцию ионных каналов изучают различными способами. Наиболее распространенным является метод фиксации напряжения, или «voltage- clamp». Сущность метода заключается в том, что с помощью специальных электронных систем в процессе опыта изменяют и фиксируют на определенном уровне мембранный потенциал. При этом измеряют величину ионного тока, протекающего через мембрану. Если разность потенциалов постоянна, то в соответствии с законом Ома величина тока пропорциональна проводимости ионных каналов. В ответ на ступенчатую деполяризацию открываются те или иные каналы, соответствующие ионы входят в клетку по электрохимическому градиенту, т. е. возникает ионный ток, который деполяризует клетку. Это изменение регистрируется с помощью управляющего усилителя и через мембрану пропускается электрический ток, равный по величине, но противоположный по направлению мембранному ионному току. При этом трансмембранная разность потенциалов не изменяется. Совместное использование метода фиксации потенциала и специфических блокаторов ионных каналов привело к открытию различных типов ионных каналов в клеточной мембране. В настоящее время установлены многие типы каналов для различных ионов. Одни из них весьма специфичны, вторые, кроме основного иона, могут пропускать и другие ионы. Изучение функции отдельных каналов возможно методом локальной фиксации потенциала «path-clamp». Стеклянный микроэлектрод (микропипетка) заполняют солевым раствором, прижимают к поверхности мембраны и создают небольшое разрежение. При этом часть мембраны подсасывается к микроэлектроду. Если в зоне присасывания оказывается ионный канал, то регистрируют активность одиночного канала. Система раздражения и регистрации активности канала мало отличается от системы фиксации напряжения. Ток через одиночный ионный канал имеет прямоугольную форму и одинаков по амплитуде для каналов различных типов. Длительность пребывания канала в открытом состоянии имеет вероятностный характер, но зависит от величины мембранного потенциала. Суммарный ионный ток определяется вероятностью нахождения в открытом состоянии в каждый конкретный период времени определенного числа каналов. Наружная часть канала сравнительно доступна для изучения, исследование внутренней части представляет значительные трудности. П. Г. Костюком был разработан метод внутриклеточного диализа, который позволяет изучать функцию входных и выходных структур ионных каналов без применения микроэлектродов. Оказалось, что часть ионного канала, открытая во внеклеточное пространство, по своим функциональным свойствам отличается от части канала, обращенной во внутриклеточную среду. Именно ионные каналы обеспечивают два важных свойства мембраны: селективность и проводимость. Селективность, или избирательность, канала обеспечивается его особой белковой структурой. Большинство каналов являются электроуправляемыми, т. е. их способность проводить ионы зависит от величины мембранного потенциала. Канал неоднороден по своим функциональным характеристикам, особенно это касается белковых структур, находящихся у входа в канал и у его выхода (так называемые воротные механизмы). Рассмотрим принцип работы ионных каналов на примере натриевого канала. Полагают, что в состоянии покоя натриевый канал закрыт. При деполяризации клеточной мембраны до определенного уровня происходит открытие m-активационных ворот (активация) и усиление поступления ионов Na+ внутрь клетки. Через несколько миллисекунд после открытия m-ворот происходит закрытие п-ворот, расположенных у выхода натриевых каналов (инактивация). Инактивация развивается в клеточной мембране очень быстро и степень инактивации зависит от величины и времени действия деполяризующего стимула. Работа натриевых каналов определяется величиной мембранного потенциала в соответствии с определенными законами вероятности. Рассчитано, что активированный натриевый канал пропускает всего 6000 ионов за 1 мс. При этом весьма существенный натриевый ток, который проходит через мембраны во время возбуждения, представляет собой сумму тысяч одиночных токов. При генерации одиночного потенциала действия в толстом нервном волокне изменение концентрации ионов Na+ во внутренней среде составляет всего 1/100000 от внутреннего содержания ионов Na гигантского аксона кальмара. Однако для тонких нервных волокон это изменение концентрации может быть весьма существенным. Кроме натриевых, в клеточных мембранах установлены другие виды каналов, избирательно проницаемых для отдельных ионов: К+, Са2+, причем существуют разновидности каналов для этих ионов. Ходжкин и Хаксли сформулировали принцип «независимости» каналов, согласно которому потоки натрия и калия через мембрану независимы друг от друга. Свойство проводимости различных каналов неодинаково. В частности, для калиевых каналов процесс инактивации, как для натриевых каналов, не существует. Имеются особые калиевые каналы, активирующиеся при повышении внутриклеточной концентрации кальция и деполяризации клеточной мембраны. Активация калий-кальцийзависимых каналов ускоряет реполяризацию, тем самым восстанавливая исходное значение потенциала покоя. Особый интерес представляют кальциевые каналы. Входящий кальциевый ток, как правило, недостаточно велик, чтобы нормально деполяризовать клеточную мембрану. Чаще всего поступающий в клетку кальций выступает в роли «мессенджера», или вторичного посредника. Активация кальциевых каналов обеспечивается деполяризацией клеточной мембраны, например входящим натриевым током. Процесс инактивации кальциевых каналов достаточно сложен. С одной стороны, повышение внутриклеточной концентрации свободного кальция приводит к инактивации кальциевых каналов. С другой стороны, белки цитоплазмы клеток связывают кальций, что позволяет поддерживать длительное время стабильную величину кальциевого тока, хотя и на низком уровне; при этом натриевый ток полностью подавляется. Кальциевые каналы играют существенную роль в клетках сердца. Биологический электрогенез Под биологическим электрогенезом, или биоэлектрогенезом, понимают комплекс механизмов, приводящих к генерации биоэлектрических потенциалов. Основы современной мембранной концепции биоэлектрогенеза были заложены, главным образом, Ходжкиным и сотрудниками . В основе этой концепции лежат следующие главные положения: Местом электрогенеза является поверхностная мембрана (на внутриклеточных мембранах тоже могут возникать разности электрических потенциалов, но электрические свойства клетки определяются преимущественно электрогенезом на поверхностной мембране). Разность потенциалов на поверхностной мембране имеет ионную природу (а не электронную, как в металлах). Генерация разностей потенциалов на поверхностной мембране обусловлена возникновением ионной асимметрии, то есть неодинаковым распределением по обе ее стороны катионов и анионов. Основной вопрос в происхождении БЭП - это вопрос о том, как возникает ионная асимметрия на поверхностной мембране. По современным представлениям, здесь действуют активный и пассивный механизмы. Пассивный механизм работает без затрат энергии. В его основе лежат два фактора: 1) разница концентраций ионов по обе стороны мембраны; 2) разная проницаемость мембраны для разных ионов. Оба фактора приводят к тому, что некоторые ионы, двигаясь по градиенту концентрации наружу или внутрь клетки, лучше проникают через мембрану, а другие хуже. Наиболее легко проникает через мембрану в покое К+. Поскольку его концентрация обычно больше внутри клетки, чем снаружи, то он выходит по градиенту концентрации из клетки и заряжает наружную сторону мембраны положительно. Соответственно, внутренняя сторона мембраны оказывается заряженной отрицательно. Так как другие ионы, хотя и в меньшей степени, также могут проникать через мембрану, то возникающий мембранный потенциал будет по своей величине меньше того, который создавался бы только выходом К+, то есть равновесного калиевого потенциала. Например, в излюбленном объекте электрофизиологов - аксоне кальмара - мембранный потенциал, рассчитанный исходя из разности концентраций К+ по обе стороны мембраны, составляет около -90 мВ (внутреннее содержимое заряжено отрицательно), а измеренный потенциал оказался близким к - 60 мВ. Это связано с тем, что мембрана аксона проницаема не только для ионов К, но и в определенной степени для других катионов и анионов. Кроме пассивного, генерация разности потенциалов на мембране связана также с активным механизмом. Последний работает с потреблением энергии и связан с работой особых ферментов - транспортных аденозинтрифосфатаз. Они представляют своего рода молекулярные машины, обладающие удивительными свойствами. Гидролизуя АТФ, эти ферменты одновременно используют освобождающуюся энергию для переноса ионов через мембрану. В результате такого транспорта и создается активная компонента мембранного потенциала. Не менее интересен и тот факт, что, несмотря на огромное разнообразие живых объектов, они имеют, в основном, две электрогенные транспортные АТФазы - Na+, K+-АТФазу (преимущественно у животных) и H+-АТФазу (у грибов и растений). Первая выкачивает из клетки 3Na+ и одновременно закачивает 2K+, вторая выкачивает из клетки H+. Нетрудно видеть, что работа этих ферментов приводит к зарядке мембраны, а именно созданию активной компоненты мембранного потенциала со знаком плюс снаружи и знаком минус внутри. В настоящее время транспортные АТФазы хорошо изучены. Показано, что это интегральные белки, то есть белки, молекулы которых пронизывают мембрану. Полипептидная цепь АТФаз несколько раз пересекает мембранный матрикс. АТФазы включают две части - каталитическую, взаимодействующую с АТФ и обращенную внутрь клетки, и канальную, направленную наружу. Na+, K+-АТФаза состоит из четырех полипептидов, называемых ее субъединицами, - двух больших (a) и двух малых (b). Ее общая молекулярная масса около 280 кD. H+-АТФаза имеет молекулярную массу 104 кD. В процессе работы эти АТФазы ведут себя как настоящие молекулярные машины. Они совершают определенные конформационные движения (то есть изменения пространственной ориентации структуры молекул), переходя из состояния Е1 в состояние Е2 и обратно. В результате этого происходит трансмембранный перенос ионов и создание активной компоненты мембранного потенциала. Вклад пассивного и активного механизмов в генерацию БЭП у разных биологических объектов может быть различным. Так, в аксонах доля активного механизма относительно невелика, в то время как, по нашим данным, в клетках высших растений она может достигать 60 - 70%. Рассмотрим теперь, как ведет себя мембранный потенциал во время возбуждения. Этот процесс происходит практически во всех животных и растительных клетках, но приобретает черты высокоспециализированной функции в нервных волокнах. Его природа была раскрыта благодаря исследованиям Ходжкина и сотрудников на гигантских аксонах головоногих моллюсков, в частности, на гигантском аксоне кальмара. Эти аксоны не покрыты миелиновой оболочкой (многослойным образованием, защищающим мембрану аксона от окружающей среды) и имеют очень большой диаметр (0,5 - 1 мм), что значительно облегчает проведение с ними микроэлектродных исследований. При возбуждении нервного волокна увеличивается проницаемость его мембраны для ионов Na. Поскольку ионов Na всегда больше снаружи и меньше внутри волокна, то они устремляются внутрь и вызывают деполяризацию мембраны, то есть уменьшение ее мембранного потенциала. Возникает восходящая ветвь ПД. Процесс деполяризации мембраны ионами Na идет до установления некоторого равновесного состояния, после чего резко увеличивается проницаемость мембраны для K+. В отличие от Na+, ионов K больше внутри волокна, чем в окружающей среде, поэтому они начинают выходить наружу. Это приводит к реполяризации мембраны, то есть восстановлению ее исходного потенциала. Возникает нисходящая ветвь ПД. Таким образом, генерация ПД в нерве непосредственно не связана с затратами энергии и происходит за счет уже имеющихся на мембране ионных градиентов. Почему же при возбуждении вначале увеличивается проницаемость мембраны для Na+, а лишь затем для K+? Это связано с работой особых белковых образований в мембране - натриевых и калиевых каналов. Каналы - это своеобразные отверстия в мембране. Они имеют диаметр около 0,7 - 0,8 нм и заполнены водой. Две особенности примечательны в их строении: наличие селективного фильтра и ворот. Селективный фильтр - это та часть канала, которая позволяет в силу своего строения и физико-химических свойств производить отбор ионов. Например, натриевый канал пропускает преимущественно ионы Na, в то время как калиевый канал проницаем в основном для ионов K. Однако наиболее важная часть рассматриваемых каналов - ворота, то есть конформирующий, меняющий свою пространственную ориентацию участок канала, способный закрывать или открывать канал. Состояние ворот зависит от потенциала в мембране. При одних его значениях они открываются, при других становятся закрытыми. Генерация ПД как раз и возможна потому, что ворота натриевых и калиевых каналов по разному зависят от величины мембранного потенциала. В процессе генерации ПД при деполяризации мембраны под влиянием раздражителя вначале открываются натриевые каналы и возникает входящий внутрь волокна натриевый ток. И лишь позднее в условиях более глубокой деполяризации, вызванной входящим натрием, происходит закрывание (инактивация) натриевых каналов и открываются калиевые каналы, что приводит к возникновению выходящего потока ионов K и реполяризации мембраны. Процесс возбуждения, связанный с генерацией ПД, наблюдается не только в нервных волокнах, но и во многих других образованиях, в том числе и в тканях растений. При этом механизм генерации ПД является по существу во всех случаях одинаковым. Отличия наблюдаются лишь в некоторых особенностях. Так, если у всех возбудимых объектов роль реполяризующего иона играет K+, то деполяризующий ион может быть разным. В нервных волокнах это Na+, в некоторых гладких мышцах Ca2+, а в клетках высших растений, как показали наши исследования, таким ионом является Cl. В сильной степени может меняться сопряженность генерации ПД с метаболизмом. Их генерация в нервных волокнах, как мы видели, носит пассивный характер. Такой механизм вполне успешно функционирует, поскольку длительность одного импульса всего несколько миллисекунд, и за единичный импульс внутрь волокна входит Na+ и, соответственно, из него выходит K+ в количестве около 3 - 4 " 10-12 моль на 1 см2 поверхности мембраны. Следовательно, генерация одного импульса вызывает ничтожное нарушение имеющегося по обе стороны мембраны градиента концентраций ионов Na и K. Этого градиента хватает на генерацию очень многих импульсов. Не случайно в связи с этой особенностью выдающийся отечественный физиолог Н.Е. Введенский говорил, что нерв может работать в долг. Но, как принято говорить, долг платежом красен. И нарушенные градиенты ионов Na и K восстанавливаются в нерве путем работы ионного насоса - Na+, K+-АТФазы, работающей за счет энергии АТФ. Она выкачивает обратно из нерва Na+ и закачивает в него K+. Иная ситуация в клетках растений. Длительность ПД здесь достигает нескольких секунд (или даже нескольких десятков секунд), и за это время происходит значительное нарушение существующих ионных градиентов. Поэтому ионному насосу, роль которого играет H+-АТФаза, приходится здесь восстанавливать ионный гомеостаз в большинстве случаев после каждого импульса. Более того, как оказалось, фаза реполяризации, то есть восстановления исходного потенциала, у высших растений также частично связана с работой H+-АТФазы. Наконец, есть организмы (например, водоросль ацетабулярия), у которых генерация ПД обусловлена преимущественно временным уменьшением активности метаболического ионного насоса. Таковы в общих чертах механизмы клеточного электрогенеза. ЗАКЛЮЧЕНИЕ Таким образом, изменения электрических свойств возбудимых биомембран осуществляется с помощью ионных каналов. Это белковые макромолекулы, пронизывающие липидный бислой, которые могут находиться в нескольких дискретных состояниях. Свойства каналов, селективных для ионов калия, натрия и кальция могут по-разному зависеть от мембранного потенциала, что и определяет динамику потенциала действия в мембране, а также отличия таких потенциалов в мембранах разных клеток.Нельзя преувеличить роль проницаемости плазматической мембраны в жизнедеятельности клетки. Большинство процессов, связанных с обеспечением клетки энергией и избавлением ее от продуктов распада, основаны на вышеописанных механизмах. Кроме того, специальные функции клеточной мембраны заключаются в получении клеткой внешних сигналов (примером этому могут служить описанные взаимодействия клетки с гормонами). Литература В. Ф. Антонов, А. М.Черныш, В. И. Пасечник, Биофизика, Москва,2006 г. В. О. Самойлов, Медицинская биофизика, Санкт-Петербург, 2007 г. Сайт https://www.bestreferat.ru/referat-235865.html Сайт http://www.bibliotekar.ru/447/7.htm Приложения Элементарная живая система, способная к самостоятельному существованию, развитию и воспроизведению – это живая клетка – основа строения всех животных и растений. Важнейшими условиями существования клетки являются, с одной стороны, автономность по отношению к окружающей среде (вещество клетки не должно смешиваться с веществом окружения, должна соблюдаться автономность химических реакций в клетке и ее отдельных частях); с другой стороны, связь с окружающей средой (непрерывный, регулируемый обмен веществом и энергией между клеткой и окружающей средой). Живая клетка – открытая система. 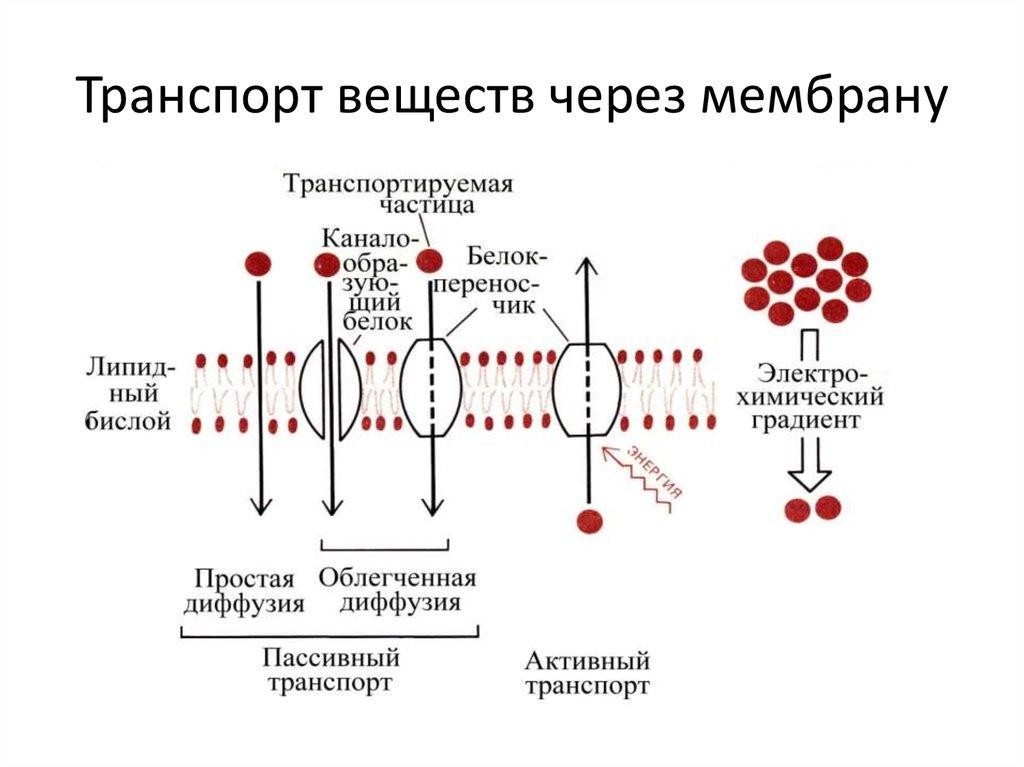 |
