Лекция. Дыхание. Стадии дыхания
 Скачать 240.05 Kb. Скачать 240.05 Kb.
|
|
Дыхание - обмен газов между атмосферой и клетками организма. Периодическое обновление воздуха в легких позволяет организму поддерживать дыхательный гомеостазис — состояние, характеризующееся оптимальным для жизнедеятельности относительным постоянством газового состава в крови и тканях организма. Жизнь организма невозможна без поддержания оптимального уровня дыхательных показателей рН, РСО2, РО2 в тканях организма. Несмотря на факторы, способные нарушить дыхательный гомеостазис, организм способен при различных условиях существования поддерживать оптимальное содержание этих показателей в крови и тканях. Система внешнего дыхания в каждом дыхательном цикле обеспечивает необходимый объем легочной вентиляции. Стадии дыхания: 1. Легочное или внешнее дыхание — связано с поступлением и удалением воздуха из легких, т.е. вдохом и выдохом. 2. Газообмен в легких между альвеолярным воздухом и легочными капиллярами. 3. Транспорт газов кровью: кислород — из легких к тканям, углекислота — из тканей в легкие. 4. Газообмен в тканях. 5. Тканевое дыхание (внутреннее): метаболические процессы утилизации кислорода клетками и образование углекислоты. Внешнее дыхание — одна из важнейших функций организма. Прекращение дыхания влечет за собой неминуемую гибель человека уже через 3-5 минут. Запасы кислорода в организме очень незначительны, поэтому необходимо его постоянное поступление через систему внешнего дыхания. В основе деятельности системы регуляции дыхания лежит поддержания константного уровня таких показателей организма, как РСО2, РО2 и рН. Основным принципом регуляции является принцип саморегуляции: отклонение вышеуказанных показателей от нормального уровня немедленно вызывает цепь процессов, направленных на их восстановление. Кроме того, дыхание участвует в речеобразовании, в выражении эмоций (смех), а также взаимосвязано с рядом других функций организма (пищеварение, терморегуляция и т.п.). В системе регуляции дыхания можно выделить внутренние и внешние звенья саморегуляции. Внутренние — связаны с состоянием крови (буферные свойства, содержание гемоглобина) и сердечно-сосудистой системы. Внешние звенья связаны с механизмами внешнего дыхания. Регулируемыми параметрами системы внешнего дыхания являются глубина и частота дыхательных движений. Основным регулируемым объектом являются дыхательные мышцы, относящиеся к скелетной мускулатуре. Кроме них к объекту регуляции дыхания должны быть отнесены гладкие мышцы глотки, трахеи и бронхов, влияющие на состояние дыхательных путей. Транспорт газов кровью и газообмен в тканях осуществляют образования сердечнососудистой системы. Дыхание регулируется рефлекторным путем, включающим три составных элемента: рецепторы, воспринимающие информацию, и афферентные пути, передающие ее нервным центрам; нервные центры; эффекторы — пути передачи команд от центров и сами регулируемые объекты. Дыхательный центр расположен в области ствола мозга. Он состоит из нескольких отделов, именуемых нередко отдельными дыхательными центрами. В обеих половинах продолговатого мозга имеется не менее двух скоплений нейронов, проявляющих свою активность в момент совершения вдоха или выдоха — дорсальное и вентральное ядра. Если возбуждение нейронов совпадает с вдохом, то такие нейроны относят к инспираторным, если с выдохом — к экспираторным. Нейроны этих ядер широко контактируют с ретикулярной формацией ствола, через которую к дыхательному центру поступают афферентные сигналы от периферических рецепторов (рис. 9). Главной особенностью дыхательного центра является периодичность, при которой возбуждение нейронов попеременно сменяется их торможением. В основе периодической активности лежит функция бульбарного отдела. В нем решающая роль принадлежит нейронам дорсального ядра. Полагают, что своеобразным «водителем ритма» являются I – альфа – нейроны. От них возбуждение распространяетсяк трем отделам ЦНС: к мотонейронам шейного отдела спинного мозга; к инспираторным нейронам вентрального ядра; к I-бета нейронам, расположенным здесь же, в дорсальном ядре. Функция I-бета нейронов заключается в торможении I-альфа нейронов путем обратной связи. Однако для «выключения» I-альфа нейронов необходимо, чтобы уровень возбуждения I-бетта нейронов достиг определенного критического предела. 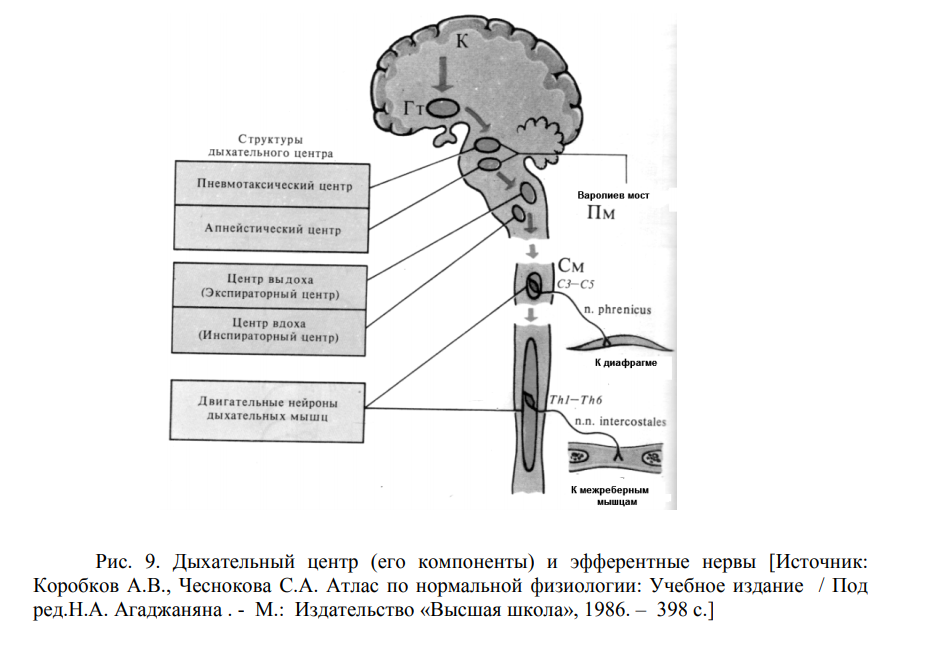 Рефлекторное возбуждение дыхания. В продолговатом мозге расположен дыхательный центр. Он представляет собой совокупность групп нейронов, аксоны которых идут к мотонейронам спинного мозга, иннервирующим межреберные мышцы и мышцы диафрагмы. При периодическом возбуждении так называемых инспираторных нейронов (отвечающих за вдох) возбуждение достигает дыхательных мышц, они сокращаются, и происходит вдох. При вдохе легкие растягиваются, и возбуждаются механические рецепторы, расположенные в их стенках. От них импульсы поступают в продолговатый мозг, и активность инспираторных нейронов резко тормозится. Происходит выдох. Стенки легких расслабляются, возбуждение механических рецепторов прекращается, возобновляется возбуждение инспираторных нейронов, и начинается следующий дыхательный цикл. Для того чтобы произошел глубокий выдох, необходимо возбуждение экспираторных нейронов дыхательного центра, которые вызывают сокращение мышц, приводящих к уменьшению объема грудной клетки. Дыхательный центр обладает автоматией и возбуждается периодически, в среднем 15 раз в минуту. При физических и эмоциональных нагрузках частота дыхания резко возрастает, чтобы обеспечить возросшие потребности организма в кислороде и, соответственно, удаление увеличенных количеств СO2 Во многих зонах сосудистого русла расположены рецепторы, возбуждающиеся при повышении содержания СO2 в крови. От этих рецепторов импульсы следуют в инспираторную часть дыхательного центра, стимулируя вдох. Кроме того, сами нейроны дыхательного центра очень чувствительны к увеличению концентрации углекислого газа в крови и реагируют на него учащением дыхания.
Когда применяются аналептики? Препараты этой группы используют при угнетении дыхания в условиях некоторых отравлений - окисью углерода, барбитуратами и наркотическими анальгетиками (легкой степени тяжести), в постнаркозном периоде (бемегрид, кофеин), при удушении, утоплении, асфиксии новорожденных (этимизол). Почему аналептики не являются препаратами выбора? Наряду с аналептической проявляют пробуждающую и судорожную активность. В связи с сопутствующей судорожной активностью большинство препаратов данной группы применяется редко; во всех перечисленных ситуациях им предпочитают искусственную вентиляцию легких Противокашлевые препараты – средства, которые ослабляют или полностью устраняют кашель, благодаря торможению кашлевых рефлексов. Кашлевой рефлекс,как и др. рефлексы, состоят из 3 звена: Афферентное звено (рецепторы гортани, глотки, трахеи) Центральное звено (центр продолговатого мозга, др. зоны коры и подкорки) Эфферентное звено (мускулатура бронхов, трахеи, диафрагмы) Исходя из этого, возможны следующиепути воздействия на кашлевой рефлекс: Периферические точки приложения действия. Это предусматривает влияние на: Афферентное звено – за счет уменьшения чувствительности рецепторов гортани, глотки и трахеи Эфферентное звено – дренаж бронхов или применение средств облегчающих отхождение мокроты Центральные точки приложения. Это влияние на центр продолговатого мозга, коры и подкорковых образований. Что такое прямое действие на кашлевой центр? Это центр в продолговатом мозге, препараты снижают раздражение рецепторов или активность кашлевого центра в головном мозге, и тем самым, предотвращают сухой, раздражающий кашель. Противокашлевые средства центрального действия
NB! В чем существенное отличие наркотических и ненаркотических препаратов? В отличие от препаратов предшествующей группы угнетают кашлевой центр, не влияя на дыхание (наркотические препараты в высоких дозах способны приводить к сильному угнетению дыхания) и не вызывая лекарственной зависимости. Противокашлевые средства периферического действия Либексин (Преноксдиазин) - механизм заключается в способности подавлять кашлевые толчки за счет снижения чувствительности эпителиальной оболочки, выстилающей бронхиальное дерево, и воздействовать на центральные звенья без угнетения центров дыхания в продолговатом мозге. В фармакологии препарат относят к противокашлевым средствам с периферическим и частично центральным действиями. Механизм действия направлен на ингибирование афферентного звена, при этом не возникает угнетения дыхания с опасностью апноэ и привыкания к основному компоненту, что допускает применение у ребенка. Преноксдиазин обладает мягким противовоспалительным и местноанестезирующим действиями. Отхаркивающие средства Рефлекторного действия - содержащиеся в растительных препаратах рефлекторного действия алкалоиды (в термопсисе - сапонины) при введении внутрь вызывают раздражение рецепторов слизистой желудка и двенадцатиперстной кишки. При этом рефлекторно (по блуждающему нерву) усиливается секреция бронхиальных желез. Повышается перистальтика бронхов, повышается активность мерцательного эпителия (происходит стимуляция мукоцилиарного транспорта). Мокрота становится более обильной, жидкой, с меньшим содержанием белка, ее отделение с кашлем облегчается. Прямого действия – после приема внутрь всасываются, попадают в кровь и доставляются к бронхам, где выделяются слизистой оболочкой, стимулируют секрецию бронхиальных желез, попадая в мокроту, разжижают и облегчают ее отделение. Усиливают перистальтику бронхов. Препараты хлорида аммония, гидрокарбоната натрия подщелачивают содержимое бронхов, что способствует разжижению и лучшему отхождению мокроты. Применение: Отхаркивающие средства используют при воспалительных заболеваниях верхних дыхательных путей и в комплексной терапии (совместно с антибиотиками, бронхолитиками и др.) больных с пневмонией, туберкулезом легких, бронхоэктатической болезнью, бронхиальной астмой (при повышении вязкости мокроты, присоединении гнойной инфекции). Кроме того, оправдано назначение этих средств для профилактики постоперационных осложнений после оперативных вмешательств на органах дыхательной системы и послинтратрахеального наркоза. Муколитические средства Средства ферментной структуры Ферментные муколитические средства, препараты протеолитических ферментов, нарушают пептидные связи в молекуле белков мокроты (кристаллические ТРИПСИН и ХИМОТРИПСИН), вызывают деполимеризацию нуклеиновых кислот (дезоксирибонуклеаза, рибонуклеаза), снижая вязкость мокроты. Средства неферментной структуры АЦЕТИЛ- и МЕТИЛЦИСТЕИН разжижают мокроту, разрывая дисульфидные связи мукополисахаридов, уменьшая тем самым вязкость мокроты, способствуют лучшему ее отхождению. Назначают по 2-5 мл 20% раствора на 3-4 ингаляции в день или промывают трахею, бронхи; возможно внутримышечное применение. Мукорегуляторы АМБРОКСОЛ - стимулирующее мукоцилиарную активность (реснитчатый эпителий) и оказывающее отхаркивающее действие. Показано при острых и хронических заболеваниях дыхательных путей, сопровождающихся образованием вязкой мокроты (острый и хронический бронхит, пневмония, бронхиальная астма с затруднением отхождения мокроты, бронхоэктатическая болезнь, муковисцидоз легких, трахеит, ларинготрахеит), воспалительных заболеваниях носоглотки и придаточных пазух, при которых необходимо разжижение слизи. БРОМГЕКСИН - неферментное муколитическое средство (секретолитик) приводит к деполимеризации и разжижению мукопротеинов и мукополисахаридных волокон мокроты, обладая, таким образом, муколитическим действием. Также выражено отхаркивающее действие препарата. Бромгексин повышает синтез сурфактанта, обладает слабым противокашлевым эффектом. NB! Одновременно принимать противокашлевые и отхаркивающие препараты не только необоснованно, но и опасно! Противокашлевые средства из-за ослабленного кашлевого рефлекса могут вызывать застой или скопление мокроты в дыхательных путях, и эвакуация слизи из дыхательных путей будут нарушена (эффект «заболачивания»). Бронхолитические средства Адреномиметики Эпинефрин - Адреналин воздействует на β2-адренорецепторы бронхиальных гладкомышечных клеток, что приводит к расслаблению мышечного слоя и расширению бронхов с облегчением дыхания. Для того, чтобы бронхолитический эффект адреналина не сопровождался выраженным прессорным действием, препарат следует вводить подкожно. В 1859 английский врач Генри Солтер (Henry Salter) сообщил о любопытном наблюдении: приступы бронхиальной астмы быстро проходят в условиях внезапной опасности или очень сильного эмоционального возбуждения. Возможно, это первое описание лечебного воздействия эндогенного, т.е. вырабатываемого самим организмом, адреналина. В основе астматического приступа лежит сокращение гладкомышечных клеток бронхов, что приводит к их спазму (сужению). В результате возникает затрудненное свистящее дыхание. Эфедрин - в малой степени непосредственно стимулирует адренорецепторы. В основном он действует на окончания адренергических нервов и усиливает выделение из них норадреналина, который возбуждает а- и b1-адренорецепторы. По фармакол. эффектам и применению эфедрин сходен с адреналином, но в отличие от него оказывает стимулирующее влияние на ц. н. с. и эффективен не только при парентеральном введении, но и при приеме внутрь. Длительность действия эфедрина при парентеральном введении 1-1.5 ч, при назначении внутрь - 3-4 ч. Применяют эфедрин при бронхиальной астме, аллергических реакциях (анафилактические реакции, сывороточная болезнь и др.), ринитах (капли в нос), снижении АД, миастении. Побочное действие препарата проявляется возбуждением, тремором, тахикардией, экстрасистолией, нарушениями сна и др. Эфедрин не следует назначать больным с повышенным АД, выраженным атеросклерозом, сердечными аритмиями, бессонницей. Салбутамол и Фенотерол - Бета-адреномиметик. Действует преимущественно на β2-адренорецепторы (действуют избирательно). Механизм действия связан с активацией сопряженной с рецептором аденилатциклазы, что приводит к увеличению образования ц-АМФ, который стимулирует работу кальциевого насоса, в результате этого снижается концентрация кальция в миофибриллах. При применении в качестве бронхолитика расширяет бронхи, увеличивает частоту и объем дыхания, улучшает функцию мерцательного эпителия бронхов. Профилактика и купирование бронхообструктивного синдрома: при бронхиальной астме, хроническом бронхите (в т.ч., осложненном эмфиземой), спастическом бронхите у детей; бронхолегочных заболеваниях (силикоз, бронхоэктазы, туберкулез). Препараты длительного действия Формотерол/ Сальметерол/ Индакатерол/ Олодатерол - селективный стимулятор β 2 -адренорецепторов. У пациентов с обратимой обструкцией дыхательных путей он оказывает бронхорасширяющее действие (вновь за счет цАМФ и механизма адреноподобных реакций). М-холиноблокаторы Атропин/Ипратропия бромид/Тиотропия бромид/Гликопиррония бромид – все блокируют М-холинорецепторы. Как бронхолитики М-холиноблокаторы уступают по эффективности β2-адреномиметикам. Это связано с несколькими причинами. Во-первых, распределение М-холинорецепторов в бронхиальном дереве таково, что чем дистальнее расположен бронх, тем меньше в нем М-холинорецепторов (таким образом, М-холиноблокаторы мало устраняют спазм мелких бронхов и бронхиол). Во-вторых, снижение тонуса бронхов является результатом блокады М3-холинорецепторов гладкомышечных клеток бронхов, в то же время на пресинаптической мембране холинергических синапсов находятся М2-холинорецепторы, блокада которых приводит к усилению выделения ацетилхолина в синаптическую) щель. При повышении концентрации ацетилхолина в синаптической щели он конкурентно вытесняет М-холиноблокаторы из связи с М3-холинорецепторами на мембране гладкомышечных клеток, препятствуя его бронхолитическому действию. Кроме того, М-холиноблокаторы уменьшают секрецию бронхиальных желез, что при бронхиальной астме нежелательно (снижение объема секреции мокроты делает ее более вязкой и трудноотделяемой, что усиливает бронхообструктивный синдром). В связи с вышеизложенным блокаторы М-холинорецепторов рассматриваются как вспомогательные средства. Ипратропия бромид (Атровент, Итроп) имеет в структуре четвертичный атом азота, в связи, с чем обладает низкой липофильностью. При ингаляционном применении практически не всасывается в системный кровоток. Бронхо-лйтический эффект развивается через 30 мин после ингаляции и достигает максимума через 1,5—2 ч и продолжается 5—6 ч. Побочные эффекты: сухость во рту, системных побочных (атропиноподобных) эффектов практически не вызывает. Тиотропий отличается от ипратропия тем, что не блокирует пресинаптические М2-холинорецепторы, в связи с чем не вызывает усиления выброса ацетилхолина из пресинаптических окончаний. Тиотропий оказывает более быстрое (максимальный эффект развивается через 1,5-2 ч) и более продолжительное Действие (около 12ч), чем ипратропий. Назначают ингаляционно 1 раз в сутки. Миотропные спазмолитики Аминофиллин (Эуфиллин)/ Теофиллин - не уступают β2-адреномиметикам по эффективности как бронхолитические средства, но в отличие от β2-адреномиметиков они не используются для ингаляционного введения. Механизм бронхолитического действия метилксантинов связывают с блокадой аденозиновых α1-рецепторов гладкомышечных клеток, а также с ингибированием фосфодиэстеразы цАМФ. Угнетение фосфодиэстеразы в гладкомышечных клетках бронхов приводит к накоплению в клетках цАМФ и снижению внутриклеточной концентрации Са2+, в результате в клетках уменьшается активность киназы легких цепей миозина и нарушается взаимодействие актина и миозина. Это приводит к расслаблению гладких мышц бронхов (спазмолитическое действие). Бронхиальная астма - в основе астматического приступа лежит сокращение гладкомышечных клеток бронхов, что приводит к их спазму (сужению). В результате возникает затрудненное свистящее дыхание. Присутствует и аллергический компонент. Противоаллергические средства (стабилизаторы мембран тучных клеток) Кромоглициевая кислота – стабилизирует мембраны тучных клеток, препятствуя входу в них ионов кальция. В связи с этим уменьшается дегрануля-ция сенсибилизированных тучных клеток (прекращается высвобождение лейкот-риенов, фактора активации тромбоцитов, гистамина и других медиаторов воспаления и аллергии). В связи с таким механизмом действия, препараты кромоглициевой кислоты эффективны как средства профилактики (но не купирования) бронхоспазма. При ингаляционном применении кромоглициевой кислоты в системный кровоток всасывается 5—15% от введенной дозы. t]/2 составляет 1—1,5 ч. Действие после однократного ингаляционного применения продолжается около 5 ч. При систематическом применении эффект нарастает постепенно, достигая максимума через 2—4 нед. Недокромил-натрий – выпускается в виде кальциевой и ди-натриевой соли (недокромил натрий). По свойствам сходен с кромоглициевой кислотой, но имеет отличную химическую структуру. Применяется ингаляционно, в системный кровоток всасывается 8—17% вещества. Используется как средство профилактики (но не купирования) бронхоспазма. Эффект нарастает постепенно, достигая максимума к концу 1-й недели регулярного применения. Назначают по 4 мг 4 раза в сутки. Кетотифен – имеет свойства стабилизатора мембран тучных клеток и блокатора гистаминовых Н,-рецепторов. Практически полностью всасывается из кишечника. Не очень высокая биодоступность (около 50%) объясняется эффектом первого прохождения через печень; t 3—5 ч. Применяется внутрь по 1 мг 2 раза в сутки (во время еды). Побочные эффекты: седативное действие, замедление психомоторных реакций, сонливость, сухость во рту, увеличение массы тела, тромбоцитопения. Противовоспалительные средства. Глюкокортикоиды. Глюкокортикоиды имеют сложный механизм антиастматического действия, в котором можно выделить несколько компонентов: Глюкокортикоиды стимулируют продукцию липокортинов (за счет индукции экспрессии соответствующего гена), которые являются естественными ингибиторами фосфолипазы А2, что приводит к уменьшению продукции в тучных клетках фактора активации тромбоцитов, лейкотриенов и простагландинов (см. рис. 17.1) Глюкокортикоиды подавляют синтез циклооксигеназы-2 (за счет репрессии соответствующего гена), что также приводит к снижению синтеза простагландинов в очаге воспаления. Глюкокортикоиды подавляют синтез молекул межклеточной адгезии, что затрудняет проникновение моноцитов и лейкоцитов в очаг воспаления. Все это приводит к уменьшению воспалительной реакции, препятствует развитию гиперреактивности бронхов и возникновению бронхоспазма Глюкокортикоиды оказывают иммуносупрессивное действие, угнетая продукцию интерлейкинов (за счет репрессии соответствующих генов), в том числе интерлейкинов-1, 4 и др. В связи с этим они подавляют пролиферацию и дифференцировку В-лимфоцитов и препятствуют образованию антител, в том числе IgE. Таким образом, глюкокортикоиды препятствуют дегрануляции тучных клеток и выходу в кровь лейкотриенов, фактора активации тромбоцитов, гистамина, простагландина D2 и других медиаторов воспаления и аллергии (см. рис. 17.1). Это приводит к подавлению иммунной реакции немедленного типа. Кроме того, глюкокортикоиды сенсибилизируют β2-адренорецепторы бронхов к циркулирующему в крови адреналину, в результате чего они усиливают бронхолитическое действие адреналина и бронхолитических средств, стимулирующих β2-адренорецепторы. 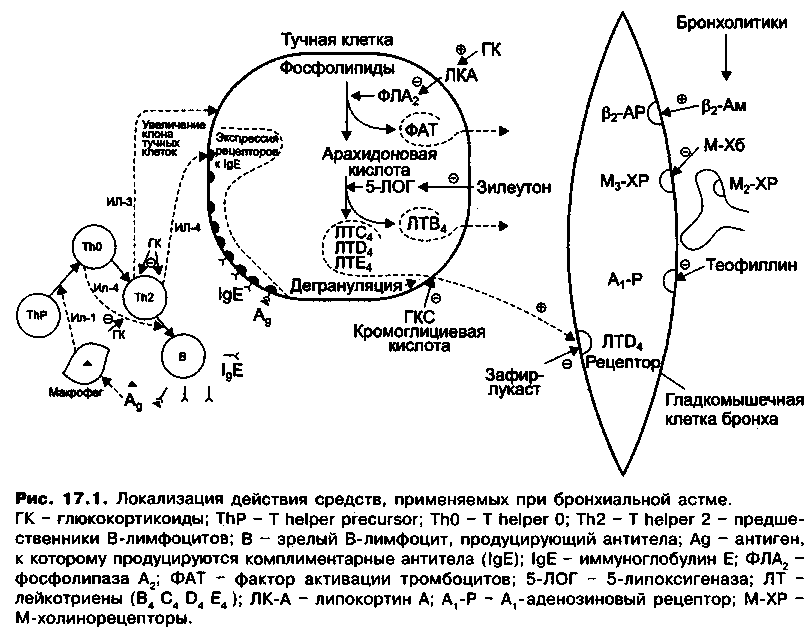 Почему данные препараты применяются ингаляционно при бронхиальной астме? Минимизация побочных эффектов Беклометазона дипропионат – применяется главным образом для профилактики приступов бронхоспазма. Эффективен только при регулярном применении. Эффект развивается постепенно и достигает максимума на 5—7-е сутки от начала использования. Обладает выраженным противоаллергическим, противовоспалительным и противоотечным действием. Побочное действие: дисфония (изменение или охриплость голоса), чувство жжения в зеве и гортани, крайне редко — парадоксальный бронхоспазм. При длительном применении может развиться кандидамикоз ротовой полости и глотки. Флутиказона пропионат / гидрокортизона ацетат. Будесонид – по фармакологическим свойствам и применению сходен с беклометазоном, но имеет ряд отличий. Будесонид имеет более продолжительное действие, в связи с этим применяется 1-2 раза в сутки. Нарастание эффекта до максимума происходит более продолжительное время (в течение 1-2 нед). При ингаляционном введении около 28% препарата попадает в системный кровоток. Будесонид применяется не только при бронхиальной астме, а также в дерматологии в составе мазей и кремов Апулеин. Блокаторы лейкотриеновых рецепторов Зафирлукаст - не только устраняет бронхоспазм, вызываемый ци-стеинилпептидолейкотриенами (LTC4 LTD4 LTE4), но и оказывает противовоспалительное действие, уменьшая проницаемость сосудов, экссудацию и отек слизистой оболочки бронхов. Из кишечника всасывается медленно и неполно. t1/2 -около 10 ч. Применяется внутрь натощак (за 1 ч до еды) или через 2 ч после последнего приема пищи, 2 раза в сутки. Действие препарата развивается медленно, около суток, поэтому зафирлукаст применяется для профилактики приступов бронхиальной астмы, при длительном лечении бронхиальной астмы. Применяют его также при аллергическом рините. Побочные эффекты: диспепсия, фарингит, гастрит, головная боль. Зафирлукаст ингибирует микросомальные ферменты печени, поэтому удлиняет действие некоторых лекарственных средств. Монтелукаст - вляется избирательным агонистом LTD4-peuen-торов. В отличие от зафирлукаста не ингибирует микросомальные ферменты печени (не изменяет продолжительность действия других лекарственных веществ). Зачем блокировать лейкотриеновые рецепторы? Бронхоспазм, вызываемый медленно реагирующей субстанцией анафилаксии, является результатом стимуляции специфических лейкотриеновых рецепторов бронхиол (ЦГО4-рецепторы). Устраняют бронхоконстрикторное действие лейкотриенов конкурентные блокаторы лейкотриеновых рецепторов (см. рис. 17.1) К ним относятся: зафирлукаст, монтелукаст Моноклональные антитела Омализумаб - ингибирует связывание IgE с высокоаффинными рецепторами IgE (FcεRI), расположенными на поверхности тучных клеток и базофилов. Снижение количества поверхностно-связанного IgE на клетках, имеющих рецепторы FcεRI, лимитирует степень высвобождения медиаторов аллергического ответа. При лечении омализумабом пациентов с атопической бронхиальной астмой отмечается уменьшение количества FcεRI-рецепторов на поверхности базофилов. Нарушение внешнего дыхания, или дыхательная недостаточность (ДН) – патологический процесс, при котором система внешнего дыхания не обеспечивает нормального газового состава артериальной крови или его поддержание на нормальном уровне достигается за счет чрезмерного функционального напряжения этой системы. Следует учитывать, что дополнительным фактором, определяющим уровень оксигенации артериальной крови, является содержание кислорода в венозной крови, поступающей в легкие. Этот параметр зависит от механизмов, определяющих доставку и потребление кислорода тканями. Поэтому снижение напряжения кислорода в крови может быть следствием не только изменения легочных функций, но и результатом патологии сердца, анемии, лихорадки и др. ДН может возникнуть и у практически здорового человека при изменении газового состава вдыхаемого воздуха. Дыхательная или легочная недостаточность бывает как острая, так и хроническая. Рассмотрим одну из разновидностей острой легочной недостаточности – отек легких. Отек легких - острая легочная недостаточность, связанная с массивным выходом транссудата из капилляров в легочную ткань, что приводит к инфильтрации альвеол и резкому нарушению газообмена в легких. Какие причины отека легких? Острая сердечная недостаточность, поражения легких химическими веществами, сильная интоксикация, ряд инфекционных заболеваний, заболевания почек и др. В результате застоя крови в легких происходит переход плазмы крови через стенки альвеол в просвет альвеол, где может скапливаться до 100-200 мл жидкости, которая при дыхании вспенивается (образуется до 3-4 л пены) и возникает гипоксия. Гипотензивные препараты – для уменьшения отека легких при высоком артериальном давлении используются ганглиоблокирующие (бензогексоний и др.) и альфа-адреноблокирующие (фентоламин и др.) средства. Снижая давление, они способствуют уменьшению кровенаполнения легкого. При низком АД противопоказаны Наркотические анальгетики – например, морфин, обладает свойством угнетать дыхательный центр и снижать частоту дыхательных движений. Кроме того, анальгетик снижает давление в малом кругу кровообращения. Этот механизм действия позволяет использовать морфин при отеке легких. Морфин снижает артериальное давление. Это действие основано на расширении периферических сосудов и снижении частоты сердечного ритма. Пеногасители – спирт этиловый. Концентрированные растворы спирта обладают прижигающим действием, способны свернуть кровь в ранее а также «вытянуть» из отекших тканей воду. Почему пеногаситель? Откуда пена? Самый концентрированный раствор можно использовать в роли противоотечного средства для оказания экстренной помощи-при отеке легких и заполнении дыхательных путей пеной из слизи. Спирт в этом случае применяют ингаляционно. Для этого вдыхаемый воздух (или кислород) предварительно пропускают через раствор спирта. Пары этилового спирта снижают поверхностное натяжение экссудата и предупреждают его вспенивание. |
