ФС_Дифенгидрамина_гидрохлорид. Статья дифенгидрамина гидрохлорид
 Скачать 50.27 Kb. Скачать 50.27 Kb.
|
|
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ ФАРМАКОПЕЙНАЯ СТАТЬЯ
2-(Дифенилметокси)-N,N-диметилэтан-1-амина гидрохлорид 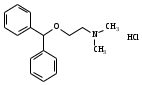
Cодержит не менее 99,0 % и не более 101,0 % дифенгидрамина гидрохлорида C17H21NO·HCl в пересчете на сухое вещество. Описание. Белый или почти белый кристаллический порошок. Растворимость. Очень легко растворим в воде, легко растворим в спирте 96 % и хлороформе. Подлинность. 1. ИК-спектрометрия. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру фармакопейного стандартного образца дифенгидрамина гидрохлорида. 2. Спектрофотометрия. Спектр поглощения испытуемого раствора в области длин волн от 230 до 350 нм должен иметь максимум при 253 нм, 258 нм и 264 нм. Испытуемый раствор. 50 мг (точная навеска) субстанции растворяют в спирте 96 % и доводят объём раствора спиртом 96 % до 100,0 мл. 3. Качественная реакция. На часовое стекло наносят 0,2 мл концентрированной серной кислоты и прибавляют 20 мг субстанции; должно появиться ярко-жёлтое окрашивание, постепенно переходящее в кирпично-красное; от прибавления нескольких капель воды окраска должна исчезнуть. 4. Качественная реакция. 20 мг субстанции растворяют в 2 мл воды. Раствор должен давать характерную реакцию на хлориды (ОФС «Общие реакции на подлинность»). Температура плавления. От 168 до 172 ºС (ОФС «Температура плавления»). *Прозрачность раствора. 1 % раствор субстанции в воде должен быть прозрачным (ОФС «Прозрачность и степень мутности жидкостей»). *Цветность раствора. Окраска раствора, полученного в испытании «Прозрачность раствора», должна выдерживать сравнение с эталоном ВY6 (ОФС «Степень окраски жидкостей», метод 2). рН. От 5,0 до 6,5 (1 % раствор, ОФС «Ионометрия», метод 3). *Кислотность или щелочность. К 10 мл раствора, полученного в испытании «Прозрачность раствора», прибавляют 0,15 мл раствора метилового красного и 0,25 мл 0,01 М соляной кислоты. Появившееся розовое окрашивание должно перейти в желтое от прибавления не более 0,5 мл 0,01 М раствора гидроксида натрия. Родственные примеси. Определение проводят методом ВЭЖХ (ОФС «Высокоэффективная жидкостная хроматография»). Подвижная фаза (ПФ). Ацетонитрил–буферный раствор 35:65. Буферный раствор. Фосфатный буферный раствор рН 3,0 (2). Испытуемый раствор. В мерную колбу вместимостью 20 мл помещают около 70 мг (точная навеска) субстанции, растворяют в ПФ и доводят объём раствора ПФ до метки. 2,0 мл полученного раствора доводят ПФ до 10,0 мл. Раствор сравнения. В мерную колбу вместимостью 10 мл помещают 1,0 мл испытуемого раствора и доводят объём раствора ПФ до метки. 1,0 мл полученного раствора доводят ПФ до 20,0 мл. Раствор для проверки разделительной способности хроматографической системы. В мерную колбу вместимостью 10 млпомещают 5 мг (точная навеска) фармакопейного стандартного образца примеси А (2-(дифенилметокси)-N-метилэтан-1-амин, CAS 53499-40-4) и 5 мг (точная навеска) дифенилметанола, растворяют в ПФ и доводят объём раствора ПФ до метки. К 2,0 мл полученного раствора прибавляют 1,5 мл испытуемого раствора и доводят ПФ до 10,0 мл. Раствор для проверки чувствительности хроматографической системы. В мерную колбу вместимостью 100 мл помещают 1,0 мл испытуемого раствора и доводят объём раствора водой до метки. В мерную колбу вместимостью 20 мл помещают 1,0 мл полученного раствора и доводят объём раствора водой до метки. Примечание: примесь A 2-дифенилметокси-N-метилэтанамин, CAS 53499-40-4; примесь В 2-[( RS )-(4-метилфенил)фенилметокси] -N,N - диметилэтанамин, CAS 19804-27-4; примесь C 2-[( RS )-(4-бромфенил)фенилметокси] -N,N -диметилэтанамин, CAS 1808-12-4; примесь D дифенилметанол (бензгидрол), CAS 91-01-0; примесь E дифенилметанон (бензофенон), CAS 119-61-9. Хроматографические условия
Хроматографируют раствор для проверки чувствительности хроматографической системы, раствор для проверки разделительной способности хроматографической системы, раствор сравнения и испытуемый раствор. Относительное время удерживания соединений. Дифенгидрамин – 1 (около 6 мин); примесь A – около 0,9; примесь В – около 1,5; примесь C – около 1,8; примесь D – около 2,6; примесь E - около 5,1. Пригодность хроматографической системы На хроматограмме раствора для проверки чувствительности хроматографической системы: ˗ отношение сигнал/шум (S/N) для пика дифенгидрамина должно быть не менее 10. На хроматограмме раствора для проверки разделительной способности хроматографической системы: ˗ разрешение (RS) между пиками дифенгидрамина и примеси A должно быть не менее 2,0. ˗ фактор асимметрии (AS) пика дифенгидрамина должен быть не более 2,0; ˗ относительное стандартное отклонение площади пика дифенгидрамина должно быть не более 2,0 % (6 введений); Поправочные коэффициенты. Для расчета содержания примеси D площадь пика умножают на соответствующий поправочный коэффициент - 0,7. Допустимое содержание примесей. На хроматограмме испытуемого раствора: – площадь пика примеси A должна быть не более площади основного пика на хроматограмме раствора сравнения (не более 0,5 %); – площадь пика любой примеси должна быть не более 0,6 площади основного пика дифенгидрамина на хроматограмме раствора сравнения (не более 0,3 %); – суммарная площадь пиков всех примесей не должна более чем в 2 раза превышать площадь основного пика на хроматограмме раствора сравнения (не более 1,0 %). Не учитывают пики, площадь которых менее 0,1 площади основного пика на хроматограмме раствора сравнения А (менее 0,05 %). Потеря в массе при высушивании. Не более 0,5 % (ОФС «Потеря в массе при высушивании», способ 1). Для определения используют около 1 г (точная навеска) субстанции. Сульфатная зола. Не более 0,1 %. (ОФС «Сульфатная зола»). Для определения используют около 1 г (точная навеска) субстанции. Тяжёлые металлы. Не более 0,001 %. Определение проводят в соответствии с ОФС «Тяжёлые металлы», метод 3А или 3Б, в зольном остатке, полученном после сжигания 1,0 г субстанции, с использованием эталонного раствора 1. Остаточные органические растворители. В соответствии с ОФС «Остаточные органические растворители». *Бактериальные эндотоксины. Не более 3,4 ЕЭ на 1 мг субстанции (ОФС «Бактериальные эндотоксины»). Для проведения испытания готовят исходный раствор субстанции (концентрация 10 мг/мл), а затем разбавляют его ЛАЛ водой не менее чем в 60 раз. Микробиологическая чистота. В соответствии с ОФС «Микробиологическая чистота». Количественное определение. Определение проводят методом титриметрии. Около 0,25 г (точная навеска) субстанции растворяют в 50 мл спирта 96% и добавляют 5,0 мл 0,01 М соляной кислоты. Титруют 0,1 М раствором натрия гидроксида. Конечную точку титрования определяют потенциометрически. 1 мл 0,1 М раствора натрия гидроксида соответствует 29,18 мг C17H21NO·HCl. Хранение. В защищённом от света месте. *Контроль по показателям качества «Прозрачность раствора», «Цветность раствора», «Кислотность или щелочность» и «Бактериальные эндотоксины» проводят в субстанции, предназначенной для производства лекарственных препаратов для парентерального применения. |
