аааааааа. 3. строение мет и спл. Тема Строение и свойства металлов
 Скачать 246.52 Kb. Скачать 246.52 Kb.
|
|
Тема: Строение и свойства металлов. Металлы в твердом состоянии — кристаллические тела, атомы которых располагаются в геометрически правильном порядке, образуя кристаллы, в отличие от аморфных тел (например, смола), атомы которых находятся в беспорядочном состоянии. Располагаясь в металлах в строгом порядке, атомы в плоскости образуют атомную сетку, а в пространстве — атомно-кристаллическую решетку. Наименьшую геометрическую фигуру называют элементарной ячейкой. Типы кристаллических решеток у различных металлов различные. Наиболее часто встречаются решетки: кубическая объемно-центрированная (рис.1 а), кубическая гранецентрированная (рис.1.б) и гексагональная плотноупакованная (рис.1 с). В кубической объемно-центрированной решетке (а) атомы расположены в вершинах куба и в центре куба; такую решетку имеют хром, ванадий, вольфрам, молибден и др. В кубической гранецентрированнойрешетке (б) атомы расположены в вершинах и в центре каждой грани куба; такую решетку имеют алюминий, никель, медь, свинец и др. В ячейкегексагональнойрешетки (с) атомы расположены в вершинах шестиугольных оснований призмы, в центре этих оснований и внутри призмы; гексагональную решетку имеют магний, титан, цинк и др. 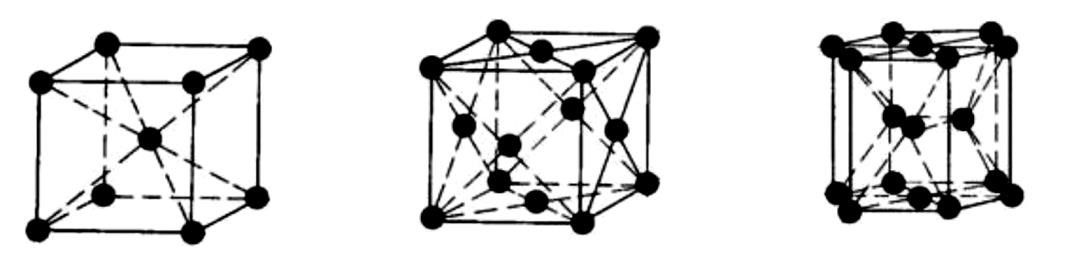 а) б) с) Рис.1. Элементарные ячейки кристаллических решеток. В реальном металле кристаллическая решетка состоит из огромного количества ячеек. Особенностями расположения атомов в кристалле объясняется явление анизотропии, т.е. неодинаковости свойств кристалла в разных кристаллографических направлениях. Кристаллизация – это процесс образования кристаллов при переходе металла из жидкого состояние в твердое. Первичной кристаллизацией называют образование кристаллов при переходе металла из жидкого состояния в твердое. Кристаллизация протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию с меньшей энергией Гиббса (свободной энергией). Кристаллизация состоит из двух процессов: зарождения мельчайших частиц кристаллов (зародышей или центров кристаллизации) и роста кристаллов из этих центров (рис.2). 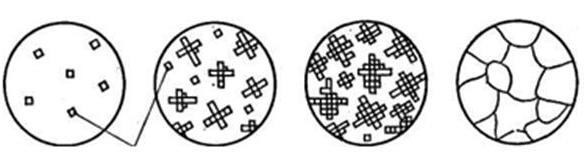 Центры кристаллизации Рис.2. Последовательные этапы процесса кристаллизации. Рост кристаллов заключается в том, что к их зародышам присоединяются все новые атомы жидкого металла. Сначала кристаллы растут свободно, сохраняя правильную геометрическую форму, но это происходит только до момента встречи растущих кристаллов. В месте соприкосновения кристаллов рост отдельных их граней прекращается и развиваются не все, а только некоторые грани кристаллов. В результате кристаллы не имеют правильной геометрической формы. Такие кристаллы называют кристаллитами или зернами. Величина зерен зависит от числа центров кристаллизации и скорости роста кристаллов. Чем больше центров кристаллизации, тем больше кристаллов образуется в данном объеме и каждый кристалл (зерно) меньше. На образование центров кристаллизации влияет скорость охлаждения. Чем больше скорость охлаждения металла, тем больше возникает в нем центров кристаллизации, и зерна получаются мельче. Это подтверждается на практике — в тонких сечениях литых деталей, охлаждающихся более быстро, металл всегда получается более мелкозернистым, чем в толстых массивных литых деталях, охлаждающихся медленнее. Однако не всегда можно регулировать скорость охлаждения. Методом получения мелкого зерна при затвердевании металла является создание искусственных центров кристаллизации. Для этого в расплавленный металл вводят специальные вещества, называемые модификаторами; процесс искусственного регулирования размеров зерен получил название модифицирования. Форма растущих кристаллов определяется не только условиями их столкновений между собой, но и составом сплава, наличием примесей и условиями охлаждения. В большинстве случаев при кристаллизации металлов механизм образования кристаллов носит так называемый дендритный характер. Дендритная кристаллизация характеризуется тем, что рост зародышей происходит с неравномерной скоростью. После образования зародышей их развитие идет главным образом в тех направлениях решетки, которые имеют наибольшую плотность упаковки атомов (минимальное межатомное расстояние). В этих направлениях образуются длинные ветви будущего кристалла — так называемые оси первого порядка (1 на рис. 3). В дальнейшем от осей первого порядка под определенными углами начинают расти новые оси, которые называют осями второго порядка (2), от осей второго порядка растут оси третьего порядка (3) и т. д. По мере кристаллизации образуются оси более высокого порядка (четвертого, пятого, шестого и т. д.), которые постепенно заполняют все промежутки, ранее занятые жидким металлом. 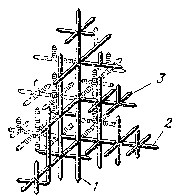 Рис.3. Схема дендритного строения. Дендритное строение характерно для литого металла. Рис.3. Схема дендритного строения. Дендритное строение характерно для литого металла. Вторичная кристаллизация – это превращения в затвердевшем металле при его дальнейшем остывании. Аллотропия - способность металлов в твердом состоянии иметь различное кристаллическое строение, а, следовательно, и свойства при различных температурах. Процесс перехода из одной кристаллической формы в другую называется аллотропическим (полиморфным) превращением. Многие металлы в зависимости от температуры могут существовать в разных кристаллических формах или, как их называют, в разныхполиморфных модификациях. В результате полиморфного превращения атомы кристаллического тела, имеющие решетку одного тина, перестраиваются таким образом, что образуется кристаллическая решетка другого типа. Полиморфную модификацию, устойчивую при более низкой температуре, для большинства металлов принято обозначать буквой α, а при более высокой — β, затем - γ и т. д.  Полиморфное превращение сопровождается скачкообразным изменением всех свойств металлов или сплавов: удельного объема, теплоемкости, теплопроводности, электрической проводимости, магнитных свойств, механических и химических свойств и т. д. Рассмотрев атомно-кристаллическое строение металлов, нельзя не отметить, что реальный кристалл имеет структурные несовершенства. Эти нарушения идеальной структуры твердых тел оказывают влияние на их свойства. Дефекты кристаллического строения классифицируются по геометрической форме и размерам на точечные (вакансии, межузельные и примесные атомы), линейные (дислокации), поверхностные (границы зерен) и объемные (поры, трещины). Чистые металлы применяются для изготовления изделий редко, т.к. они в большинстве случаев не обеспечивают требуемых свойств. Металлический сплав – это вещество, состоящее из двух или более элементов, обладающее металлическими свойствами. Химический элемент, входящий в состав металла или сплава, называется компонентом. По числу компонентов сплавы делятся на двухкомпонентные (двойные), трехкомпонентные (тройные) и т. д. Большинство сплавов получают сплавлением компонентов в жидком состоянии. Сплавы превосходят простые металлы по прочности, твердости, обрабатываемости и т. д. Вот почему они применяются в технике значительно шире простых металлов. Например, железо — мягкий металл, почти не применяющийся в чистом виде. Зато самое широкое применение в технике имеют сплавы железа с углеродом — стали и чугуны. При изучении явлений, протекающих в сплавах в процессе их превращений, пользуются понятиями «фаза», «система», «компонент». В зависимости от взаимодействия компонентов сплава могут образовываться следующие фазы: жидкие растворы, твердые растворы, химические соединения и механические смеси.
|
