Ферменты. Тема занятия 1
 Скачать 390.74 Kb. Скачать 390.74 Kb.
|
Кирьянова Дарья 19 группа ЛФФерменты.Тема занятия 1. Строение, функции и общие свойства ферментов. Классификация ферментов.Дайте определение следующих понятий: Фермент - это белковые молекулы (биологически активные вещества) синтезируемые живыми клетками. С их помощью многочисленные реакции протекают быстрее (выступают в роли катализаторов), а сами ферменты в ходе реакции не расходуются Активный центр – это уникальная комбинация аминокислотных остатков, обеспечивающая непосредственное связывание с молекулой субстрата и осуществляющая катализ. Аминокислотные радикалы в акт. центре могут находиться в любом сочетании, при этом рядом располагаются аминокислоты, значительно удалённый друг от друга в линейной цепи Аллостерический центр это центр регуляции активности ферментов, который пространственно отделён от активного центра и имеется не у всех ферменов. Связывание с аллостреческим центром какой-либо молекулы вызывает изменение конфигурации белка-фермента и скорости ферментативной реакции. Апофермент это белковая часть ферментов, для проявления каталитической активности которых необходимо присутствие и небелкового компонента - кофермента. Кофермент – это органические природные соединения небелковой природы Выберите правильный ответ: 1.В катализируемой реакции: Катализатор изменяет состояние равновесия системы; Катализатор изменяет значение константы равновесия; Катализатор не смещает положения равновесия; Изменение свободной энергии полной реакции зависит от концентрации катализатора; Нет правильного ответа. 2. Функции металлов в ферментативном катализе: Стабилизация определенной конформации фермента; Формирование истинного субстрата; Участие в связывании фермента с коферментом; Формирование активного центра; Верно 1,3; Все верно. 3.Удельную активность ферментов выражают: Числом единиц ферментативной активности на 1 моль фермента; Числом единиц ферментативной активности на 1 моль превращенного субстрата; Какую активность ферментов выражают числом единиц ферментативной активности на 1 мг белка? Удельная активность фермента 4.Об активности фермента судят по: Количеству образовавшегося продукта; Скорости убывания субстрата; Убыли фермента; Количеству превращенного субстрата; Скорости образования продукта; Верно 2 и 5; Все верно. 5. Формирование активного центра происходит на уровне… Первичной структуры белка; Вторичной структуры белка; Третичной структуры белка. 6.Аллостерический центр служит для связывания… Субстрата; Лиганда-эффектора, не изменяющегося в ходе реакции; Кофермента. Установите соответствия:
8. Установите соответствие между буквами и цифрами на графике (рис1.1):  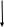 Энергетический барьер реакции; 4 Энергия активации в присутствии фермента;7 Энергия активации в отсутствие катализатора;2 Свободная энергия исходного субстрата;6 Свободная энергия конечного продукта;5 Свободная энергия активированного фермент-субстратного комплекса;1 Изменение свободной энергии в ходе реакции.3 9.Выберите из предложенного списка о6означения осей координат (1 и 2) на графике:
Что такое лабильность ферментов? Каталитическая эффективность фермента, как и любой белковой молекулы, зависит от его конформации, и в частности от конформации активного центра. Конформационная лабильность - способность к небольшим изменениям нативной конформации в следствии разрыва слабых связей. Поэтому воздействие денатурирующих агентов, способных изменять конформацию молекулы фермента, приводит к изменению конформации активного центра и снижению способности присоединять субстрат. В результате этого уменьшается каталитеческая эффективность фермента. 12.Укажите последовательность событий при ферментативном катализе: Перераспределение электронной плотности в химических связях субстрата; Сближение фермента и субстрата; Образование новых химических связей в молекулах, превращаемых под действием фермента; Связывание субстрата в активном центре фермента; Улучшение комплементарности между субстратом и активным центром фермента; Образование продуктов. OТВЕТ: 254136 Выполните следующие задания: 1.Нарисуйте графики зависимости скорости реакции от рН среды для пепсин, α-амилазы и щелочной фосфатазы. 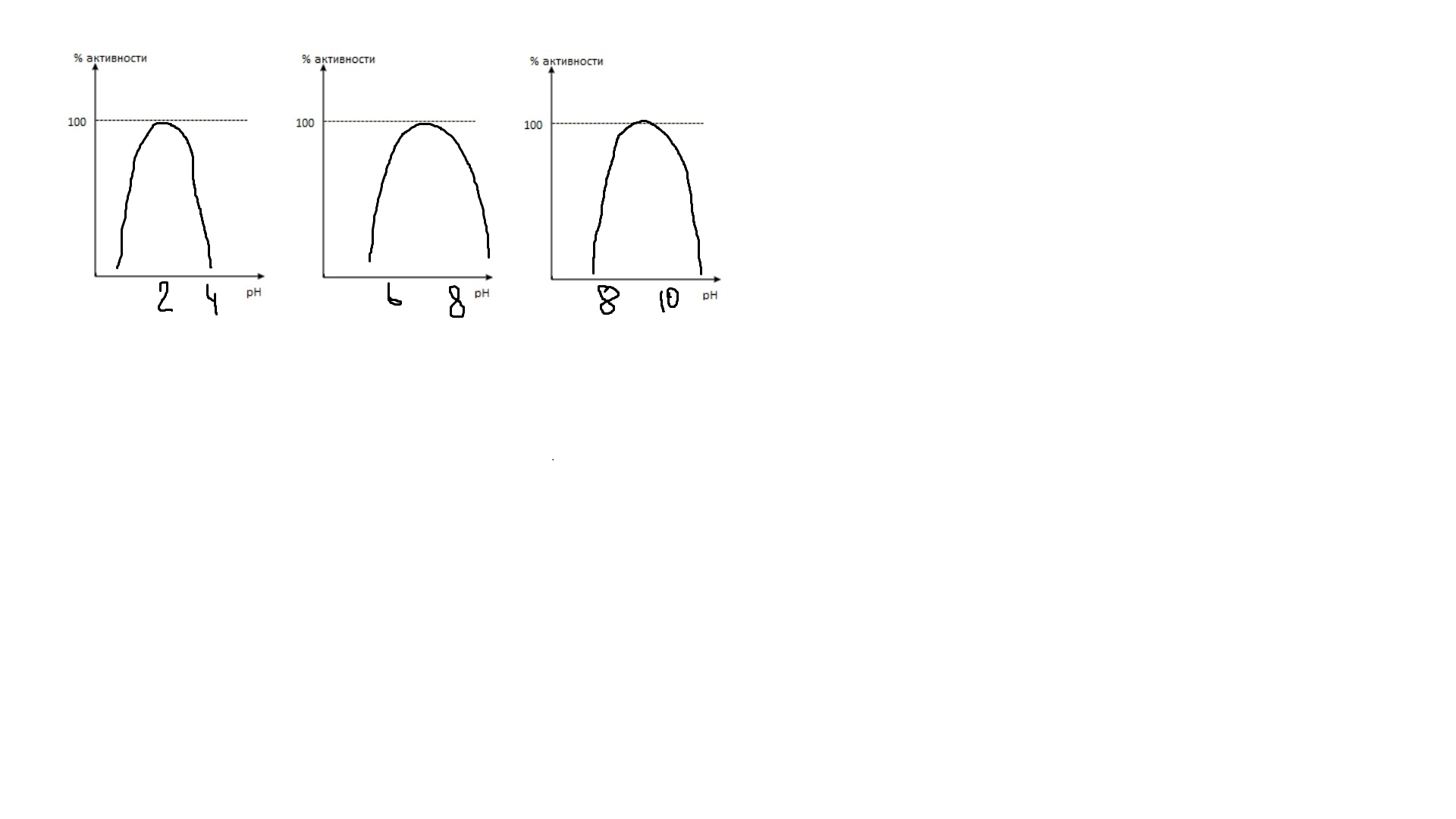 2. Укажите класс (а) и дайте название (б) ферментам, катализирующим следующие реакции: 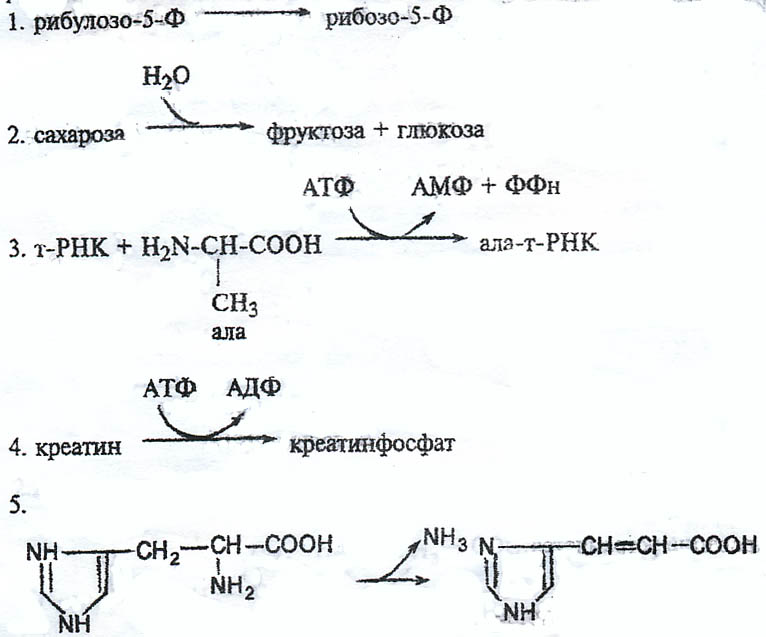 1._а) изомераза б) фосфорибоизомераза 2._а) гидролазы б) сахараза 3._а)лигазы б) аланин-тРНК-синтетаза 4._а) трансфераза б) креатинкиназа 5._а) лиазы б)гистидаза Установите и аргументируйте истинность утверждения. Ответ должен быть ДА или НЕТ (писать рядом с вопросом) А.Увеличение температуры реагирующей смеси повышает энергию активации молекул субстрата. НЕТ Энергия активации зависит от природы реагирующих веществ. Б. При этом уменьшается константа равновесия реакции. НЕТ Константа равновесия реакции не зависит от температуры А. После связывания белкового субстрата в активном центре химотрипсина пептидная связь в субстрате разрывается. ДА Б. Одновременно освобождаются оба продукта реакции. НЕТ Так как неодновременно. А. В ниже приведенной реакции участвует вода. ДА Б. Фермент, катализирующий эту реакцию, относится к классу гидролаз. ДА 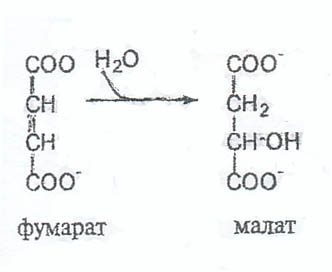 Определите класс ферментов. Попробуйте назвать ферменты, участвующие в реакциях пируват + СО2 + АТФ→ оксалоацетат + АДФ + Фн глюкоза-6-фосфат + Н2О →глюкоза + Н3РО4. сукцинат + ФАД → фумарат + ФАДН2 аспартат + 2-оксоглутарат → оксалоацетат + глутамат аденилосукцинат → АМФ + фумарат гистидин → гистамин + СО2 глюкоза + АТФ → глюкозо-6-фосфат + АДФ глюкозо-6-фосфат → фруктозо-6-фосфат ацетил-КоА + СО2 + АТФ→ малонил-КоА + АДФ + Фн глюкозо-6-фосфат + НАДФ+→ 6-фосфоглюконолактон +НАДФН + Н+ . малат + НАД+→ оксалоацетат + НАДН + Н+ аланин + 2-оксоглутарат → пируват+ глутамат лактоза + Н2О → галактоза + глюкоза глицеральдегид-3-фосфат → дигидроксиацетонфосфат _а)лигаза б) пируваткарбоксилаза _а)изомераза б) триозофосфатизомеразы _а) гидрогеназа б) сукцинатдегидрогеназа _а) трансфераза б) аспарат аминотрафераза _а) гидратаза б) фумарат _а) лиаза б) декарбоксилаза _а) трансфераза б) гексокиназа _а) изомераза б) глюкозо-6-фосфатизомераза _а) лигаза б) ацетил-КоА-карбоксилаза _а) гидрокеназа б) глюкозо-6-фосфатдегидрогеназа _а) оксидоредуктаза б) малатдегидрогеназа _а) трансфераза б) аланинаминотрансфераза _а) гидрогеназа б) лактаза _а) изомераза б) триозофосфатизомераза V. Решите ситуационную задачу: Лаборант поставил пробирку с кровью в термостат для скорейшего образования сгустка и выставил температуру 70оС. При анализе сыворотки крови активность исследованных ферментов равнялась нулю. 1. Что произошло с ферментами сыворотки крови? ДЕНАТУРАЦИЯ 2. Что называют активностью фермента? Количество субстрата, превращённого в единицу времени. 3. В каких единицах выражают активность фермента? В международных единицах или каталах . 4. Как меняется активность ферментов при повышении температуры? Сначала повышается, а после достижение оптимальной температуры снижается. 5. Какие еще действия с сывороткой крови могут привести к потере активности ферментов? Замораживание, добавление кислот, щелочей и другие действия, приводящие к денатурации белков. |