курсач. Теоретическая часть Практическая часть
 Скачать 63.31 Kb. Скачать 63.31 Kb.
|
|
Содержание Введение Теоретическая часть Практическая часть 1.1 2.1 Основные методы определения 2.2 Обоснование методов определения 2.3 Полное описание метода (оборудование, устройства, реактивы) 2.4 Обработка результатов 2.5 Выводы по обработке результатов 3. Техника безопасности при выполнении работы 3.1 Характеристика веществ по степени опасности (предельно допустимые концентрации ПД ; влияние вредных факторов; класс опасности) 3.2 Пожаробезопасность в лаборатории (категория пожароопасности, первичные средства пожаротушения) 3.3 Электробезопасность (работа с электроприборами; заземление; защита от статического электричества) 3.4 Средства индивидуальной защиты ( спец обувь, очки, перчатки х/б и резиновые) Заключение (что рассмотрено, предложено, представлено) Цель выполнена Выбор метода определения иона кальция в МИНЕРАЛЬНЫХ, ПИТЬЕВЫх ЛЕЧЕБНЫх и лЕЧЕБНО-СТОЛОВЫх водах. Введение К минеральным водам относят природные воды, оказывающие на организм человека лечебное действие, обусловленное основным ионно-солевым и газовым составом, повышенным содержанием биологически активных компонентов и специфическими свойствами (радиоактивность, температура, реакция среды). Минерализация - сумма всех растворимых в воде веществ — ионов, биологически активных элементов (исключая газы), выражается в граммах на 1 л воды. По показателю общей минерализации (М) различают: слабоминерализованные (1—2 г/л), малой (2—5 г/л), средней (5—15 г/л), высокой (15—30 г/л) минерализации, рассольные минеральные воды (35—150 г/л) и крепкорассольные (150 г/л и выше). В зависимости от общей минерализации минеральные воды классифицируются на: пресные (минерализация до 1 г на дм³ включительно); слабоминерализованные (минерализация более 1 до 2 г на дм³ включительно); маломинерализованные (минерализация более 2 до 5 г на дм³ включительно); среднеминерализованные (более 5 до 10 г на дм³ включительно); высокоминерализованные (более 10 до 15 г на дм³ включительно). В зависимости от назначения питьевые минеральные воды классифицируют на: столовые — минеральные воды с минерализацией менее 1 г на дм³ и с содержанием биологически активных компонентов менее установленной концентрации; столовые воды пригодны для ежедневного применения здоровыми людьми без ограничений; лечебно-столовые — минеральные воды с минерализацией более 1 г и до 10 г на дм³ включительно при концентрации биологически активных компонентов менее установленных норм или минеральные воды с минерализацией менее 1 г на дм³, но при превышении некоторыми биологически активными компонентами установленных норм; лечебно-столовые воды допускаются для столового потребления здоровыми людьми без ограничений непродолжительный период или нерегулярно; лечебные — минеральные воды с минерализацией более 10 г на дм³ или с меньшей минерализацией, но при превышении концентрации некоторых биологически активных компонентов установленных норм, эти минеральные воды не рекомендованы для обычного столового питья. Основной химический состав минеральных вод определяется содержанием наиболее распространенных трех анионов — НСО3, S04, Сl и трех катионов — Са, Mg, Na. Соотношение указанных шести элементов определяет основные свойства подземных вод — щелочность, соленость и жесткость. Одним из важнейших компонентов в минеральной воде являются ионы кальция. Ионы кальция (Ca2+) в минеральной воде имеют антисептические и вяжущие свойства, способны активировать ряд ферментов, улучшают обмен за счёт усиления выработки печеночных фосфолипидов, снижают проницаемость клеточных мембран (в том числе и гепатоцитов), усиливают выделительную функцию почек, стимулируют диурез, что делает целесообразным использование минеральных вод с содержанием кальция больным с патологией почек и мочевыделительной системы. Кальций имеет выраженные антисностические свойства. Воды, содержащие ионы кальция, улучшают липидный обмен в результате усиления под их влиянием выработки фосфолипидов, что способствует восстановлению печёночных клеток у людей с заболеваниями печени. Актуальность Объект- Предмет- Цели- Задачи: 1) Провести сравнительный анализ потенциометрического и титриметрического метода иона кальция; 2) 1. Теоретическая часть 1.1 Классификация минеральных вод Минеральные воды по назначению подразделяют на столовые, лечебно-столовые и лечебные. Минеральные воды по минерализации подразделяют на пресные, слабоминерализованные, маломинерализованные, среднеминерализованные и высокоминерализованные. Зависимость назначения минеральной воды от ее минерализации представлена в таблице 1. Таблица 1- Классификация минеральных вод по минерализации
В зависимости от химического состава минеральные воды подразделяют на группы и на гидрохимические типы в соответствии с таблицей 2. Минеральные воды по степени насыщения двуокисью углерода подразделяют на негазированные и газированные. 1.2 Требование к минеральным водам по содержанию ионов кальция. Требования к химическим показателям групп, гидрохимических типов минеральных вод и их лечебному применению приведены в таблице 2. Таблица 2
1.3 Методы отбора единиц продукции в выборку Для получения объективных результатов по содержанию ионов кальция важно правильно произвести выборку единиц продукции. Согласно ГОСТ 18321-73 СТАТИСТИЧЕСКИЙ КОНТРОЛЬ КАЧЕСТВА. Методы случайного отбора выборок штучной продукции, отбор проб может проводится способами описанными ниже. В зависимости от способа представления продукции на контроль применяются следующие методы отбора единиц продукции в выборку: - отбор с применением случайных чисел; - многоступенчатый отбор; - отбор "вслепую"; 1) Отбор с применением случайных чисел применяется для однородной продукции, представленной на контроль способом "ряд". 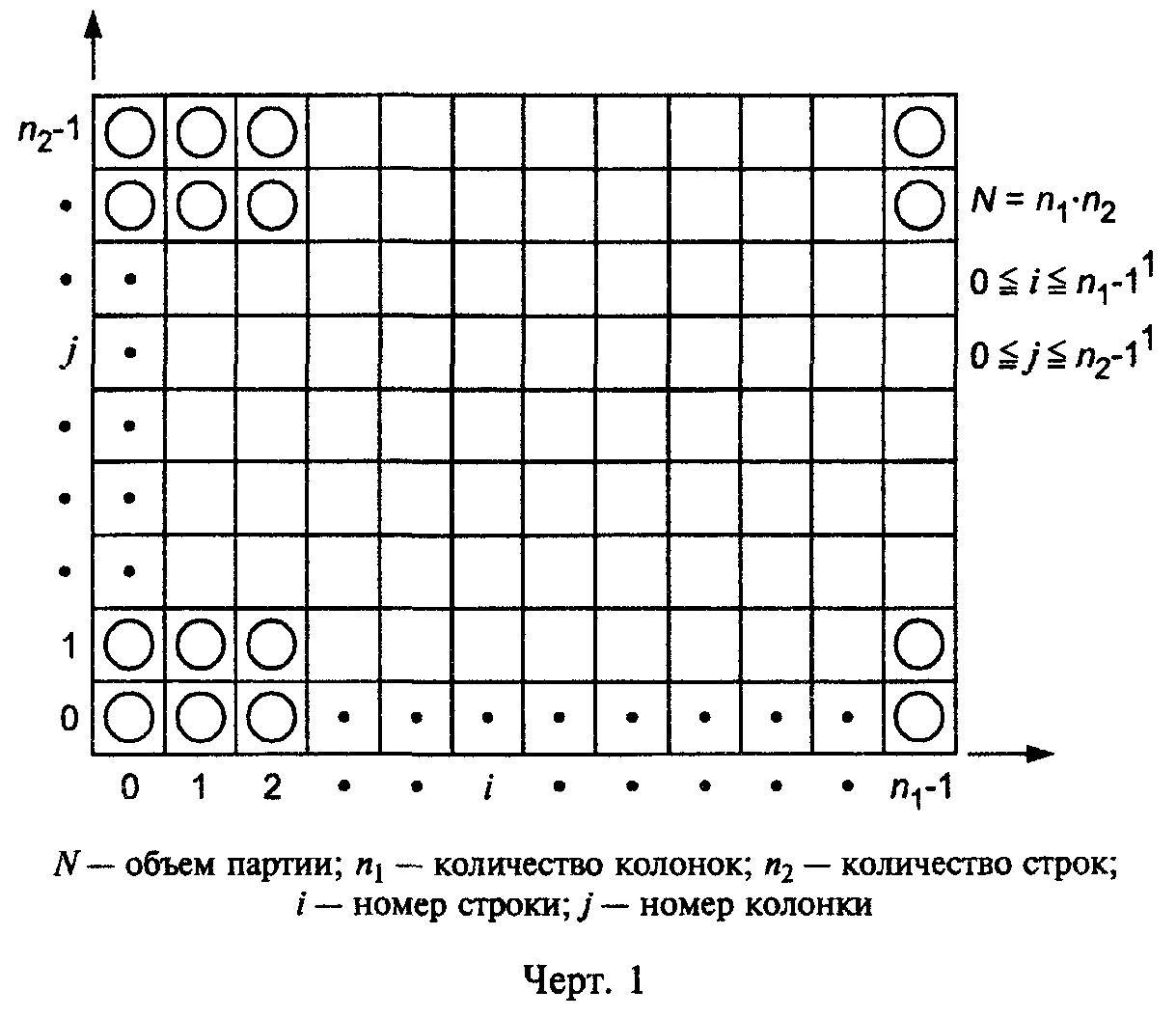 Метод отбора с применением случайных чисел используется и при всех остальных способах представления однородной продукции (если это не ведет к большим трудностям экономического или технического порядка). Метод предполагает предварительную сплошную нумерацию единиц продукции. Все номера должны иметь одно и то же количество цифр. Существующие номера с разным количеством цифр следует в начале дополнять слева нулями. При методе отбора единиц продукции в выборку с применением случайных чисел используют: - таблицы случайных чисел по СТ СЭВ 546-77* Многоступенчатый отбор Метод многоступенчатого отбора единиц продукции применяют для однородной продукции, представленной на контроль в упаковке, т.е. в упаковочных единицах, содержащих одинаковое количество единиц продукции. При многоступенчатом отборе выборку образуют по ступеням и единицы продукции в каждой ступени отбирают случайным образом из единиц, отобранных в предыдущей ступени. Кроме объема выборки, следует предварительно указывать и количество упаковочных единиц (первичных, вторичных и т.д.), выбранных для составления выборки. Из этих отобранных упаковочных единиц отбирается выборка. . Выборку составляют из примерно одинаковых объемов продукции, взятых из отобранных упаковочных единиц. Если первичные упаковочные единицы содержат вторичные и т.д. упаковочные единицы, то сначала отбирают первичную, затем вторичную и т.д. упаковочные единицы. Допускается единицы продукции паковать в первую (вторую и т.д.) упаковочную единицу россыпью. Для упаковочных единиц следует применять метод отбора с применением случайных чисел. Если продукция находится в "россыпи", то следует применять метод "вслепую". 3) Отбор "вслепую" (метод наибольшей объективности) Для осуществления контроля качества минеральной воды, разлитой в бутылки от каждой партии отбирают выборку единиц продукции методом отбора наибольшей объективности "вслепую". Метод "вслепую" применяется для продукции, в случае, когда применение метода отбора с применением случайных чисел технически затруднительно или экономически невыгодно. Метод "вслепую" не следует применять в тех случаях, когда бракованные единицы продукции можно определить органолептически. В выборку должны быть включены единицы продукции из разных частей контролируемой партии. Единицы продукции следует отбирать независимо от субъективных предположений контролера относительно качества отбираемой единицы продукции. В курсовой работе отбор объектов исследования (бутилированной минеральной воды) условно проводился методом «вслепую». 1.4 Требования минеральной воды по органолептическим показателям По органолептическим показателям минеральные воды должны соответствовать требованиям, указанным в таблице 3. Таблица 3
https://docs.cntd.ru/document/1200085076 - ВОДЫ МИНЕРАЛЬНЫЕ ПРИРОДНЫЕ ПИТЬЕВЫЕ. Общие технические условия https://docs.cntd.ru/document/1200022236?marker=7D20K3 Технические условия https://docs.cntd.ru/document/1200022288?marker методы отбора проб https://docs.cntd.ru/document/1200012873?marker=7D20K3 Методы случайного отбора выборок штучной продукции Практическая часть 2.1 Обоснование методов определения В ГОСТе 23268.5-78 « Воды минеральные питьевые лечебные и лечебно-столовые» были представлены два метода: титриметрический и потенциометрический метод. Эти два метода будут рассмотрены и сравнены между собой. Потенциометрический метод определения кальция даёт, как правило точные результаты, поэтому он применяется довольно часто при анализе объектов. Титриметрический метод 2.2 Описание титриметрического метода Метод основан на способности комплексона 3 образовывать в щелочной среде в интервале рH=12-13 комплексные соединения с ионами кальция. Метод позволяет определить более 1 мг ионов кальция в пробе с пределом погрешности измерений 0,02 мг при числе определений n=5 с доверительной вероятностью P=0,95. Аппаратура, материалы и реактивы: Бюретки мерные вместимостью 10, 25 см3; Пипетки мерные вместимостью 1, 2, 5, 10, 25, 50см3; Колбы мерные вместимостью 100, 500, 1000 см3; Цилиндры мерные вместимостью 50, 100 см3; Колбы стеклянные лабораторные конические вместимостью 250 см3; Капельницы; Стекло часовое; Холодильник стеклянный лабораторный; Весы лабораторные Плитка электрическая Воронки стеклянные Ступка фарфоровая Шпатель Кислота соляная, фиксанал, раствор концентрацией 0,1 моль/дм3 Метиловый красный Кислота кальконкарбовая Натрия гидроокись Гидроксиламина гидрохлорид Комплексон 3, фиксанал, раствор концентрацией 0,05 моль/дм3 Спирт этиловый ректификованный Вода дистиллированная Глицерин Мурексид Натрий хлористый Все реактивы должны быть квалификации х.ч или ч.д.а Подготовка к анализу Приготовление раствора комплексона 3 Раствор готовят из фиксанала. Содержимое ампулы количественно переносят в мерную колбу вместимостью 1000 см3 , растворяют в дистиллированной воде и объём раствора доводят дистиллированной водой до метки концентрацией 0,05 моль/дм3 Приготовление раствора соляной кислоты Раствор готовят из фиксанала. Содержимое ампулы количественно переносят в мерную колбу вместимостью 1000 см3 и объём раствора доводят дистиллированной водой до метки концентрацией 0,1 моль/дм3. Приготовление индикатора метилового оранжевого 0,1 г метилового красного взвешивают с погрешностью не более 0,01 г и растворяют в 100 см3 горячей дистиллированной воды. Приготовление раствора гидроокиси натрия 80 г гидроокиси натрия взвешивают с погрешностью не более 0,01 г, помещают в мерную колбу вместимостью 1000 см3, растворяют в дистиллированной воде, охлаждают до температуры 20С и доводят объём раствора дистиллированной водой до метки концентрацией 2 моль/дм3. Приготовление раствора гидроксиламина 4,5 г гидрохлорид гидроксиламина взвешивают с погрешностью не более 0,01 г и растворяют в 100 см3 этиловогоспирта. Приготовление раствора с массовой долей кальконкарбоновой кислоты 0,025%. 0,025 г кальконкарбоновой кислоты взвешивают с погрешностью не более 0,0002 г и растворяют в 100 см3 водно-глицериновой смеси 1:1. Приготовление индикатора мурексида 0,1-0,2 г индикатора мурексида смешивают с 10 г хлористого натрия и тщательно растирают смесь в фарфоровой ступке. Проведение анализа В коническую колбу вместимостью 250см3 отмеривают от 10 до 100 см3 минеральной воды, разбавляют дистиллированной водой до 100 см3, нейтрализуют раствором соляной кислоты концентрацией 0,1 моль/дм3 по индикатору метиловому красному до розового окрашивания раствора, добавляют ещё 1 см3 соляной кислоты, кипятят 5 минут с обратным холодильником для удаления двуокиси углерода ( холодильник можно заменить перевёрнутой воронкой). Раствор охлаждают до температуры 20 С. Добавляя 2 см3 раствора гидроокиси натрия концентрацией 2 моль/ дм3, устанавливают рH от 12 до 13. В качестве индикатора вводят 1 см3 раствора кальконкарбоновой кислоты и пробу медленно титруют раствором комплексона 3 концентрацией 0,05 моль/дм3 до изменения цвета раствора в синий. При определении ионов кальция в железистых минеральных водах железо маскируют 2-3 каплями раствора гидроксиламина. рнописанной методике пробу вводят на кончике шпателя индикатор, приготовленный по п.7(приготовление индикатора мурексида), и пробу медленно титруют раствором комплексона 3 концентрацией 0,05 моль/дм3 до изменения цвета раствора из малинового в красно-фиолетовый. 2.3 Обработка результатов Массовую концентрацию ионов кальция (х), мг/дм3, вычисляют по формуле: 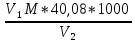 Где V1- объём раствора комплексона 3, пошедший на титрование, см3; M- молярная концентрация; 40,08- молярная масса иона кальция, г/моль; V2-объём воды, взятый на анализ, см3. За окончательный результат анализа принимают среднее арифметическое значение результатов двух параллельных определений, допускаемые относительные расхождения между которыми не должны превышать 2%. 2.4 Выводы по обработке результатов 2.5 Полное описание потенциометрического метода Метод основан на прямом определении ионов кальция с использованием ионоселективного кальциевого электрода. Метод позволяет определять от 4 мг до 100 мг ионов кальция в пробе. В диапазоне 4-20 мг с пределом погрешности измерений +0,3 -0,6 мг; в диапазоне20-100 мг с пределом погрешности +100 -0,3 мг при числе определений n=5 с доверительной вероятностью P=0,95. Аппаратура, материалы и реактивы: Прибор для измерения величины потенциала, типа рН-метр-милливольтметр (рН-340, рН-121) или иономер типа ЭВ-74. Электрод сравнения хлорсеребряный насыщенный образцовый 2-го разряда Электрод "Квант" ионоселективный кальциевый. Весы лабораторные, не ниже второго класса точности, с наибольшим пределом взвешивания до 200 г или другие весы, обеспечивающие необходимую точность взвешивания. Весы лабораторные, не ниже четвертого класса точности, с наибольшим пределом взвешивания до 500 г или другие весы, обеспечивающие необходимую точность взвешивания. Шкаф сушильный. Секундомер механический по НТД. Стаканы лабораторные, вместимостью 250 см3 Колбы конические, вместимостью 500 см3 Колбы мерные, вместимостью 100, 1000 см3 Цилиндры мерные с притертой пробкой, вместимостью 50 см3 Пипетки мерные вместимостью 1, 5, 10, 25 см3 Палочки стеклянные. Стаканчики для взвешивания (бюксы) Бутыль полиэтиленовая. Анионит АВ-17 Натрий уксуснокислый 3-водный Кальций углекислый Кислота соляная Бумага фильтровальная лабораторная Бумага индикаторная универсальная. Все реактивы должны быть квалификации х.ч. или ч.д.а. Подготовка к анализу Приготовление основного стандартного раствора хлористого кальция. Углекислый кальций прокаливают в сушильном шкафу при температуре(110+-2)С до постоянной массы. 10,000 г прокалённого углекислого кальция взвешивают с погрешностью не более +0,0002 г. Навеску переносят в стакан вместимостью 250 см3 и растворяют в 216 см3 раствора соляной кислоты концентрацией 1 моль/дм 3, затем содержимое стакана перемешивают стеклянной палочкой и после растворения соли раствор количественно переносят в мерную колбу вместимостью 1 дм3 и доводят объём раствора до метки дистиллированной водой. Полученный раствор хранят в полиэтиленовой бутыли. 1см3 раствора содержит 1*10-4 молей хлористого кальция. Приготовление раствора хлористого кальция. В мерную колбу вместимостью 100 см3 приливают 1 см3 основного стандартного раствора, отмеренного пипеткой вместимостью 1см3 , и объём раствора доводят дистиллированной водой до метки концентрацией 0.001 см3. 1 см3 раствора содержит 1*10-6 молей хлористого кальция. Приготовление буферного раствора 136,00 г трёхводного уксуснокислого натрия взвешивают с погрешностью не более +-0,01 г. Навеску помещают в колбу вместимостью 1000 см3, растворяют в 100-150 см3 дистиллированной воды и объём раствора доводят дистиллированной водой до метки. Подготовка прибора к испытанию Новый измерительный ионоселективный кальциевый электрод перед работой выдерживают в основном стандартном растворе не менее 24 ч. Перед началом работы ионоселективный электрод присоединяют к клемме прибора для измерения величины потенциала и промывают дистиллированной водой, а остатки воды с электрода удаляют фильтрованной бумагой. В качестве электрода сравнения используют хлорсеребряный электрод. По окончании работы ионоселективный электрод и наконечник электролитического ключа обмывают дистиллированной водой. Между анализами ионоселективный кальциевый электрод хранят в стаканчике с раствором хлористого кальция концентрацией 0,0001 моль/дм3. Проведение анализа На характер градуировочного графика влияют ионная сила раствора и присутствующие в воде гидрокарбонат ионы. Влияние ионной силы устраняют добавлением буферного раствора. Для устранения влияния гидрокарбонат-ионов анализируемую воду пропускают через колонку, наполненную ионообменной смолой марки АВ-17 в C1-форме. Первые 10-20 см фильтрата для анализа не используют. В мерный цилиндр с притертой пробкой вместимостью 50см3отмеривают пипетками от 5 до 25 см3фильтрата для того, чтобы в отобранной пробе содержалось от 4 до 100 мг ионов кальция, пробу фильтрата разбавляют дистиллированной водой до 25 см3и добавляют 25 см3буферного раствора. Раствор перемешивают. Подготовленную пробу используют для трех параллельных измерений. Для этого в стаканчик вместимостью 50 см3отливают около одной трети полученного раствора, погружают в него ионоселективный кальциевый электрод и наконечник электролитического ключа. Потенциал электрода измеряют при помощи прибора для измерения величины потенциала. Показания прибора снимают через 30 с после погружения электрода. Построение градуировочного графика В мерные цилиндры с притертыми пробками вместимостью по 50 см3каждый вносят при помощи пипеток вместимостью 1, 5, 10, 15, 25 см3 соответственно 1, 5, 10, 15, 25 см3основного стандартного раствора и доводят растворы до 25 см3дистиллированной водой. Полученные эталонные растворы содержат соответственно ионов кальция 1,0·10моль/дм3 (4,0 мг/; 5,0·10 моль/дм3(20,0 мг/дм3; 1,0·10) моль/дм3(40,0 мг/дм3; 1,5·10) моль/дм3(60,0 мг/дм3; 2,5·10 моль/дм3(100 мг/дм3). Затем к эталонным растворам добавляют пипеткой вместимостью 25 см3 по 25 см3буферного раствора. Растворы перемешивают и измеряют их потенциалы, как указано в п.4.4, в порядке возрастания концентрации ионов кальция в эталонных растворах. На основании полученных данных строят градуировочный график зависимости потенциала электрода, от концентрации ионов кальция. Для его построения на миллиметровой бумаге на оси абсцисс откладывают отрицательные логарифмы значений концентраций ионов кальция в эталонных растворах, выраженные в моль/дм3, а на оси ординат - величины измеренных потенциалов. 2.6 Обработка результатов При составлении таблицы использована зависимость C=40*103-pC Где C- концентрация ионов кальция, Моль/дм3 40- молярная масса иона кальция, г/моль pC-отрицательный логарифм концентрации ионов кальция, выраженной в моль/дм3 Если при подготовке пробы к анализу минеральную воду разбавляют дистиллированной водой, то массовую концентрацию ионов кальция (х) вычисляют по формуле 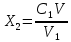 , ,Где С1-массовая концентрация ионов кальция в разбавленной пробе, мг/дм3 V-объём разбавленного раствора см3 V1-объём минеральной воды, взятый на анализ, см3 Выводы по обработке результатов 3.Техника безопасности при выполнении работ При работе с небольшими объемами веществ достаточно использование пробирок. При проведении экспериментов в пробирках необходимо соблюдать ряд правил: Категорически запрещается встряхивать пробирку, при этом закрывая отверстие пальцем. Попадание, каких-либо химических на кожные покровы может быть опасным. Так же, в используемую пробирку могут проникнуть посторонние вещества. Данные вещества могут повлиять на ход эксперимента, впоследствии, полученный результат может оказаться неверным. Перемешивать растворы необходимо быстрыми постукиваниями по стенкам пробирки. При проведении экспериментов с большими объемами веществ необходимо использовать колбы или стаканы и при работе с такой посудой рекомендуется соблюдать ряд правил: Содержимое колбы необходимо перемешивать, совершая круговые движения. Содержимое специального стакана необходимо перемешивать с помощью стеклянной палочки. На палочку следует надеть отрезок резиновой трубки. Данная трубка позволит не повредить стенку стакана. При переливании веществ из сосудов, имеющих широкое горлышко, в сосуд с узким горлышком, например, из большой колбы в пробирку, требуется использовать воронку в случае пролива вещества. При фильтровании веществ требуется использовать воронки, при этом бумажный фильтр после вкладывания в воронку должен смачиваться водой. Фильтруемую жидкость необходимо выливать на фильтр небольшой струей по стеклянной палочке, которую направляют на стенки воронки. При выпаривании растворов необходимо использовать выпарительные чаши, которые нужно закреплять на кольце штатива и нагреваться над пламенем спиртовки. Для закрепления посуды применяется лабораторный штатив. Штатив состоит из массивной металлической подставки. В данную подставку ввинчен стержень. На стержне присутствуют лапка и кольцо. При помощи муфты, появляется возможность перемещать лапку и кольцо по стрежню. Возможно регулировать высоту их закрепления. Положение муфты и кольца требуется закрепить специальными винтами. Пробирки и колбы укрепляются в лапке и при этом они должны находиться только в вертикальном положении отверстием вверх. Сосуды закрепляются возле отверстия. 3.1 Правила пожарной безопасности в лаборатории Все помещения лаборатории должны соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения. Лаборатория должна быть оснащена пожарными кранами (не менее одного на этаж) с пожарными рукавами. В каждом рабочем помещении должны быть в наличии огнетушители и песок, а в помещениях с огнеопасными и легковоспламеняющимися веществами (спички, карбид кальция, целлюлоза, вещества, содержащие нитрат, металлический магний, пленка на базе нитроцеллюлозы, фосфор, калий, натрий, гидрид натрия, порошок цинка, гидрид циркония и т.п.) - дополнительные средства пожаротушения. Таблица 4
В помещении лаборатории на видном месте должен быть вывешен план эвакуации сотрудников в случае возникновения пожара. Распоряжением по лаборатории из числа сотрудников назначается группа (3 - 5 человек), которая организует все противопожарные мероприятия, получив инструктаж местной пожарной команды. Все сотрудники лаборатории должны быть обучены правилам обращения с огне- и взрывоопасными веществами, газовыми приборами, а также должны уметь обращаться с противогазом, огнетушителем и другими средствами пожаротушения, имеющимися в лаборатории. В помещениях лаборатории и в непосредственной близости от них (в коридорах, под лестницами) запрещается хранить горючие материалы и устанавливать предметы, загромождающие проходы и доступ к средствам пожаротушения. Без разрешения начальника лаборатории и лица, ответственного за противопожарные мероприятия, запрещается установка лабораторных и нагревательных приборов, пуск их в эксплуатацию, переделка электропроводки. Все нагревательные приборы должны быть установлены на термоизолирующих подставках. Запрещается эксплуатация неисправных лабораторных и нагревательных приборов. После окончания работы необходимо отключить электроэнергию, газ и воду во всех помещениях. Каждый сотрудник лаборатории, заметивший пожар, задымление или другие признаки пожара обязан: - немедленно вызвать пожарную часть по номеру телефона 101; - принять меры по ограничению распространения огня и ликвидации пожара; - поставить в известность начальника лаборатории, который в свою очередь должен известить сотрудников, принять меры к их эвакуации и ликвидации пожара. 3.2 Правила электробезопасности в лабораторииВсе помещения лаборатории должны соответствовать требованиям электробезопасности при работе с электроустановками по ГОСТ 12.1.019-79. Все электрооборудование с напряжением свыше 36 В, а также оборудование и механизмы, которые могут оказаться под напряжением, должны быть надежно заземлены. . Для отключения электросетей на вводах должны быть рубильники или другие доступные устройства. Отключение всей сети, за исключением дежурного освещения, производится общим рубильником. . В целях предотвращения электротравматизма запрещается: - работать на неисправных электрических приборах и установках; - перегружать электросеть; - переносить и оставлять без надзора включенные электроприборы; - работать вблизи открытых частей электроустановок, прикасаться к ним; - загромождать подходы к электрическим устройствам. О всех обнаруженных дефектах в изоляции проводов, неисправности рубильников, штепсельных вилок, розеток, а также заземления и ограждений следует немедленно сообщить электрику. В случае перерыва в подаче электроэнергии электроприборы должны быть немедленно выключены. Запрещается использование в пределах одного рабочего места электроприборов класса "0" и заземленного электрооборудования. Категорически запрещается прикасаться к корпусу поврежденного прибора или токоведущим частям с нарушенной изоляцией и одновременно к заземленному оборудованию (другой прибор с исправным заземлением, водопроводные трубы, отопительные батареи), либо прикасаться к поврежденному прибору, стоя на влажном полу. При поражении электрическим током необходимо как можно быстрее освободить пострадавшего от действия электрического тока, отключив электроприбор, которого касается пострадавший. Отключение производится с помощью отключателя или рубильника. При невозможности быстрого отключения электроприбора необходимо освободить пострадавшего от токоведущих частей деревянным или другим не проводящим ток предметом источник поражения. Во всех случаях поражения электрическим током необходимо вызвать врача. 3.3 Правила использования средств индивидуальной защиты и коллективной защиты. К средствам индивидуальной защиты персонала лаборатории от вредных химических веществ и реактивов относятся такие средства гигиены, как мыло и другие моющие средства, специальные вещества антагонисты для снятия с кожи вредных веществ (например: раствор соды для нейтрализации попавшей на кожу кислоты), резиновые перчатки, лабораторные халаты, шапочки и т.п. К коллективным средствам защиты от воздействия вредных химических веществ относятся: лабораторные вытяжки и др. системы вентиляции воздуха. Для устранения возможного возгорания каждая ихтиологическая лаборатория должна быть оснащена стандартными газовыми огнетушителями. Для предотвращения возможного распространения огня от огнеопасных предметов и агрегатов (например, спиртовых и газовых горелок) используют огнеупорные прокладки и щиты из асбеста. К средствам индивидуальной защиты персонала лаборатории относится также аптечка, которая должна входить в комплект каждой ихтиологической лаборатории и должна содержать следующие предметы первой необходимости: вату гигроскопическую (стерилизованную), бинты марлевые, раствор йода, нашатырный спирт, пероксид водорода, борную кислоту (2%-ный раствор), вазелин или крем для рук. Заключение В ходе проделанной работе провели анализ минеральных питьевых вод на содержание катионов кальция | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

