|
|
Квантовая физика 17. Теория к разделу элементы содержания 17 (Радиоактивность. Опыты Резерфорда. Состав атомного ядра. Ядерные реакции)
Теория к разделу «ЭЛЕМЕНТЫ СОДЕРЖАНИЯ № 17»
(Радиоактивность. Опыты Резерфорда. Состав атомного ядра. Ядерные реакции)
|
|
|
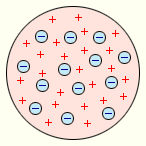
Модель атома Томсона
|
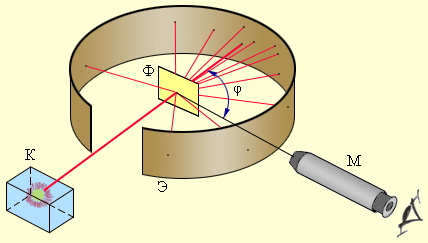
Схема опыта Резерфорда по рассеянию α-частиц. K – свинцовый контейнер с радиоактивным веществом, Э – экран, покрытый сернистым цинком, Ф – золотая фольга, M – микроскоп
|
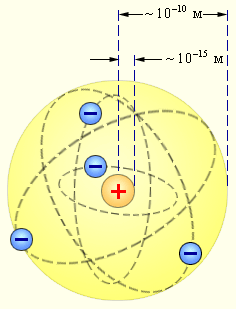
Планетарная модель атома Резерфорда
| Первая попытка создания модели атома (1903 г.) Он считал, что атом – электронейтральная система формы шара радиусом, примерно равным 10–10 м. «+» заряд атома равномерно распределен по всему объему шара, а «-« заряженные электроны находятся внутри него. Через несколько лет в опытах Э. Резерфорда было доказано, что модель Томсона неверна.
|
(1909–1911 г.) Резерфорд предложил применить зондирование атома с помощью α-частиц. Масса α-частиц примерно в 7300 раз больше массы электрона, а «+» заряд равен удвоенному заряду электрона, скорость порядка 107 м/с. Резерфорд бомбардировал атомы тяжелых элементов. Электроны, входящие в состав атомов из-за малой массы не могут заметно изменить траекторию α-частицы. Рассеяние, т. е. изменение направления движения α-частиц, может вызвать только тяжелая «+» часть атома. Рассеянные частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться под ударами быстрых заряженных частиц. Сцинтилляции (вспышки) на экране наблюдались с помощью микроскопа. Было обнаружено, что большинство α-частиц проходит через тонкий слой металла, практически не испытывая отклонения. Однако небольшая часть частиц отклоняется на значительные углы, превышающие 30°. Очень редкие α-частицы (приблизительно одна на десять тысяч) испытывали отклонение на углы, близкие к 180°.
|
- весь «+» заряд атома сосредоточен в малом объеме, в центре атома находится плотное «+» заряженное ядро, диаметр которого не превышает 10–14–10–15 м;
- это ядро занимает только 10–12 часть полного объема атома, но содержит весь «+» заряд и не менее 99,95 % его массы;
- заряд ядра должен быть равен суммарному заряду всех электронов, входящих в состав атома.
Так возникла ядерная (планетарная) модель атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, под действием кулоновских сил со стороны ядра вращаются электроны. Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро.
|
Радиоактивность - явление испускания атомами невидимых проникающих излучений. Атомы радиоактивных веществ испускают три вида излучений различной физической природы - альфа-, бета- и гамма-лучи.
α-лучи - поток ядер гелия «+»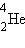
|
β-лучи – это поток электронов «-»
|
γ-лучи - коротковолновое э/м излучение с чрезвычайно малой длиной волны λ < 10–10 м «0»
|
Min проникающая способность, в воздухе α-лучи проходят путь в несколько см.
|
β-лучи способны пройти через слой алюминия толщиной в несколько мм.
|
Max проникающая способность, способны проходить через слой свинца толщиной 5–10 см.
|
Атом - электронейтральная система, носителями «-» заряда атомов являются электроны, «+» - ядро.
«-» ион – это атом, присоединивший электрон.
«+» ион – это атом, потерявший электрон.
Атомные ядра состоят из частиц двух видов – протонов и нейтронов.
Нуклоны – общее название протонов и нейтронов.
Ядра химических элементов - 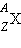 ,где X – химический символ элемента. ,где X – химический символ элемента.
Z – зарядовое число или атомный номер (это порядковый номер в периодической таблице Менделеева) - число протонов, входящих в состав атомного ядра.
N- число нейтронов
А - массовое число - общее число нуклонов, т. е. протонов и нейтронов: A = Z + N.
Изотопы – это ядра одного и того же химического элемента с разным числом нейтронов.
Ядерные силы - силы, удерживающие нуклоны в ядре.
Энергия связи ядра - минимальная энергия, которую необходимо затратить для полного расщепления ядра на отдельные частицы, равна той энергии, которая выделяется при образовании ядра из отдельных частиц.
Альфа-распад - испускание в процессе самопроизвольного радиоактивного распада ядер гелия 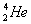 . . 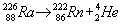
Бета-распад - радиоактивный распад атомного ядра, сопровождающийся вылетом из ядра электрона. 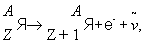
T – период полураспада – время, за которое распадается половина первоначального количества радиоактивных ядер.
Я́дерная реа́кция — это процесс взаимодействия атомного ядра с другим ядром или элементарной частицей, который может сопровождаться изменением состава и строения ядра.
При ядерных реакциях выполняются все законы сохранения классической физики.
Радий-226 претерпевает α-распад, в результате распада образуется нуклид 222Rn, также известный как радиоактивный газ радон или эманация радия. Выделяемая энергия 4 870,62(25) кэВ:
{\displaystyle \mathrm {^{226}_{88}Ra} \rightarrow \mathrm {^{222}_{86}Rn} +\mathrm {^{4}_{2}He} ,}
|
|
|
 Скачать 62.85 Kb.
Скачать 62.85 Kb.


