БЖД. Учебное пособие Санкт Петербург 2014 удк 355. 58 0758 ббк 68. 9 я 73 б 69 Рецензенты
 Скачать 7.93 Mb. Скачать 7.93 Mb.
|
|
Окись этилена (C2H4O) - бесцветный газ с запахом эфира, в 1,5 раза тяжелее воздуха, хорошо растворяется в воде, спиртах и других органических растворителях. Температура кипения -10,7°С, температура плавления -113,3°С. В жидком состоянии пожароопасна, в парообразном состоянии - взрывоопасна. Концентрационные пределы взрываемости от 3,2 до 100% по объему. Применяется при получении многих органических веществ (эфиров гликолия и полигликолей, акрилонитрила и т.д.); как инсектицид, фунгицид и дезинфицирующее средство в сельском хозяйстве. ПДК в воздухе рабочей зоны - 0,001 г/м3. Концентрация 0,3 г/м3 может вызвать острое отравление. Сернистый ангидрид (сернистый газ, двуокись серы, SO2) - бесцветный газ с резким раздражающим запахом, в 2,2 раза тяжелее воздуха, на воздухе дымит; хорошо растворяется в воде (при этом образуется сернистая кислота), а также в спиртах, эфире, бензоле. Температура кипения -10,1°С, температура плавления -75,5°С. Негорюч, взрывоопасен при нагревании емкостей. Сернистый ангидрид используется в производстве серной кислоты, серного ангидрида, солей серной и серноватистой кислот. Находит применение в бумажном и текстильном производстве; для дезинфекции помещений; для предохранения вин от скисания. Жидкий сернистый ангидрид применяется как хладоагент и растворитель. Опасен при вдыхании. ПДК в воздухе рабочей зоны - 0,01 г/м3. Соляная кислота (концентрированная, HCl) - концентрированный раствор хлористого водорода в воде с максимальной его концентрацией 38-39%. Кипит при 110°С. Негорючая агрессивная жидкость, реагирует с металлами с выделением водорода. ПДК рабочей зоны - 0,005 г/м3. Широко используется в промышленности. По масштабам использования из АХОВ после аммиака и хлора занимает прочное третье место. Обладая высокими токсическими свойствами, при поливах соляной кислоты возможно образование очагов химического поражения на значительных территориях. Для нейтрализации концентрированной соляной кислоты рекомендуется использовать 5% раствор щелочи, гашеную известь, аммиачную воду, щелочные отходы промышленного производства и др. В отсутствие щелочных компонентов может использоваться вода. Формальдегид (НСОН) - бесцветный газ с резким удушливым запахом, немного тяжелее воздуха (относительная плотность паров - 1,03), хорошо растворяется в воде (40% водный раствор формальдегида - формалин). Температура кипения -19,2°С, температура плавления -92°С. В смеси с воздухом и кислородом взрывоопасен, воспламеняется от огня (концентрационные пределы воспламенения от 7 до 73% по объему). Формальдегид используется для получения феноло-формальдегидных смол, изопрена, красителей, взрывчатых веществ, лекарств, а также как дубящее, антисептическое и дезодорирующее средства. Пары формальдегида раздражают слизистые оболочки глаз и дыхательных путей. При попадании на кожу вызывает покраснение, образование пузырей. ПДК рабочей зоны - 0,001 г/м3. Фосген (COCl2) - бесцветный газ с запахом прелого сена, в 3,4 раза тяжелее воздуха, на воздухе дымит, образуя соляную кислоту, плохо растворим в воде, хорошо - в органических растворителях, горючих и смазочных материалах. Температура кипения -8,2°С, температура плавления -118°С, негорюч, взрывобезопасен, но пожароопасен. Используется при получении красителей трифенилметанового ряда, поликарбонатных полимеров, полиуретанов; при производстве мочевины и других химических продуктов. Поражает легочную систему организма. Обладает кумулятивным действием. В ряде западных стран фосген находился на вооружении в качестве запасно-табельного отравляющего вещества. ПДК рабочей зоны - 0,0005 г/м3. При длительном воздействии считается уже опасной концентрация, равная 0,005 г/м3, десятикратное превышение этой концентрации опасно при 30-60 минутном воздействии. Хлор (Cl2) – зеленовато-желтый гах с резким раздражающим запахом, в 2,5 раза тяжелеее воздуха. Облако зараженного воздуха вследствие этого может скапливаться в подвальных помещениях и низких участках местности. Мало растворяется в воде (0,07%), хорошо – в некоторых органических растворителеях. Температура кипения –34,1С, температура плавления -101С. Хлор не горюч, но пожароопасен в контакте с горючми материалами. Хлор широко используется в промышленности: отбелевание тканей и бумажной массы, производства пластмасс, каучуков, растворителей, в цветной металлургии, а также в коммунально-бытовом хозяйстве для обеззараживания питьевой воды. На ряде объектов промышленности его запасы составляют сотни и даже тысячи тонн. Сотни тысяч тонн сжиженного хлора постоянно находятся в железнодорожных транспортных средствах. Хлор в первую мировую войну использовался в качестве отравляющего вещества. ПДК в рабочих помещениях – 0,001 г/м3. Раздражающее действие хлора проявляется при концентрации 0,01 г/м3, смертельные отравления возможны при концентрации 0,25 г/м3 при экспозиции в течении 5 минут. Первые признаки отравления – резкая загрудинная боль, резь в глазах, слезотечение, сухой кашель, рвота, нарушение координации, отдышка. При утечке хлора используют распыленный раствор кальцинированной соды или воду с целью осадить газ (водяные завесы). Места разлива заливают аммиачной водой, известковым молоком, раствором кальцинированной соды или каустика. Хлорпикрин (CCl3NO2) - бесцветная маслянистая жидкость с резким раздражающим запахом, его пары в 5,7 раза тяжелее воздуха, плохо растворим в воде, хорошо - в органических растворителях, горючих и смазочных материалах. Температура кипения -112,3°С, температура плавления -69°С. Пожароопасен, при нагревании разлагается с образованием фосгена. Используется главным образом для борьбы с вредителями сельского хозяйства, а также в качестве учебного опасного химического вещества для подгонки средств индивидуальной защиты органов дыхания. Поражает организм при поступлении через органы дыхания, вызывает сильное поражение легких и раздражение глаз. В капельно-жидком состоянии хлорпикрин может вызвать тяжелые поражения кожи. ПДК рабочей зоны - 0,0007 г/м3. При концентрации 0,0002 г/м3 слезотечение начинается через несколько секунд. Смертельная концентрация при 10-минутном воздействии 2 г/м3. Токсические свойства АХОВ, общий характер их действия и признаки поражения человека представлены в табл. 2.4. Таблица 2.4 Токсические свойства, общий характер действия и признаки поражения аварийно химически опасных веществ
2.3. Процесс протекания аварии на химически опасном объекте. Химическая авария – это авария, сопровождающаяся утечкой и выбросом опасных химических веществ из технологического оборудования или поврежденной тары, способная привести к гибели или заражению людей, сельскохозяйственных животных и растений, либо заражению химическими веществами окружающей природной среды в опасных для людей, животных и растений концентрациях. Способ хранения АХОВ во многом определяет их поведение при авариях. Анализ имеющих место аварийных ситуаций показывает, что объекты с химически опасными компонентами могут быть источником: - залповых выбросов АХОВ в атмосферу; - сброса АХОВ в водоемы; - «химического» пожара с поступлением токсичных веществ в окружающую среду; - заражения объектов и местности в очаге аварии и на следе распространения облака; - обширных зон задымления в сочетании с токсичными продуктами. Следует отметить, что особенностью химически опасных аварий являются высокая скорость формирования и действия поражающих факторов Зоной химического заражения называется территория или акватория, в пределах которого расположены или привнесены опасные химические вещества в концентрациях или количествах, создающих угрозу для жизни и здоровья людей, с/х животных и растений в течении определенного времени. Зона химического заражения включает в себя территорию непосредственного разлива АХОВ и территорию, над которой распространилось облако зараженного воздуха с поражающими концентрациями. Величина зоны заражения зависит от физико-химических свойств, токсичности, количества пролившегося (выброшенного в атмосферу) АХОВ, метеоусловий и характера местности. Размеры зоны заражения характеризуются глубиной и шириной распространения облака зараженного воздуха с поражающими концентрациями и площадью пролива АХОВ. Внутри зоны могут быть районы со смертельными концентрациями. В зависимости от физико-химических свойств и агрегатного состояния АХОВ зоны заражения определяются по первичному и (или) вторичного облаку, при этом: - для сжиженных газов – по первичному облаку, - для сжатых газов – по первичному облаку, - для жидкостей – по вторичному облаку. Первичное облако – облако зараженного воздуха, образующееся при разрушении (повреждении) емкости в результате мгновенного (1-3 мин.) перехода в атмосферу всего количества или части содержимого в ней АХОВ. Вторичное облако – облако зараженного воздуха, образующееся в результате испарения разлившегося АХОВ с подстилающей поверхности. Первичное облако образуется лишь при разрушении емкостей, содержащих АХОВ под давлением. Оно характеризуется высокими концентрациями АХОВ, превышающими на несколько порядков смертельные концентрации при кратковременной экспозиции. Особенностью поражающего действия вторичного облака по сравнению с первичным является то, что концентрация в нем паров АХОВ в 10-100 раз ниже. Продолжительность действия вторичного облака определяется временем испарения АХОВ и временем сохранения устойчивого направления ветра. В свою очередь скорость испарения АХОВ зависит от его физико-химических свойств, температуры окружающей среды, площади разлива и скорости ветра в приземном слое. Учитывая пространственную неопределенность направления и скорости ветра следует отметить, что площадь зоны возможного заражения представляет собой площадь территории, в пределах которой под воздействием ветра может перемешаться облако АХОВ. От скорости ветра в значительной мере зависит форма и размеры зоны заражения. При скорости ветра от 0 до 0,5 м\с прогнозируемая зона заражения представляет окружность с радиусом равным глубине распространения облака, от 0,6 м\с до 1 м\с – полукруг, от 1,1м\с до 2 м\с – сектор с углом в 900 и при скорости ветра более 2,1 м\с – сектор с углом в 450 (рис. 2.1). Этот сектор характеризует территорию, на которой должны приниматься меры по обеспечению безопасности производственного персонала и населения. Глубина зоны заражения зависит от скорости переноса переднего фронта зараженного облака. В свою очередь скорость переноса зависит не только от скорости ветра, но и от метеорологических условий, вертикальной устойчивости атмосферы. Различают три степени вертикальной устойчивости атмосферы: инверсию, изотермию и конвекцию. Инверсия – состояние приземного слоя воздуха, при котором температура нижнего слоя меньше температуры верхнего слоя (устойчивое состояние атмосферы). Наблюдается примерно за 1 час до захода солнца, разрушается примерно за 1 час после восхода солнца. Возникает при ясной погоде, малых (до 4 м\с) скоростях ветра. Изотермия – состояние приземного слоя воздуха, при котором температура нижнего и верхнего слоев одинаковы (безразличное состояние атмосферы). Характерна в утренние и вечерние часы (температура воздуха в пределах 20-30м от земной поверхности практически одинакова). Конвекция – состояние приземного слоя воздуха, при котором температура нижнего воздуха выше температуры верхнего слоя (неустойчивое состояние воздуха). Наблюдается примерно через 2 часа после восхода солнца, разрушается примерно за 2-2,5 часа после захода солнца. Возникает при ясной погоде, малых (до 4 м\с) скоростях ветра. Инверсия и изометрия обеспечивают сохранение высокой концентрации АХОВ в приземном слое воздуха и распространение зараженного облака на значительные расстояния. Конвекция вызывает рассеивание зараженного облака, что приводит к снижению концентрации паров АХОВ. 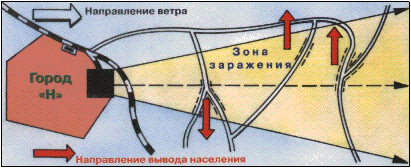 |
