РАСЧЁТ ГАЗИФИКАЦИИ. Расчёт газификации Вождаев Д.В.. "Уральский федеральный университет имени первого Президента России Б. Н. Ельцина"
 Скачать 484.87 Kb. Скачать 484.87 Kb.
|
2.3. Материальный баланс пиролизаПроцесс пиролиза проходит без доступа паровоздушной смеси, поэтому продуктами пиролиза являются: пиролизные газы, балласт – зола, смола и коксовый остаток. Таблица 6 – Материальный баланс пиролиза
2.4. Расчет процесса газификацииНекоторая часть углерода, поступившего в зону газификации, остается в шлаке. Содержание углерода в шлаке принимается 10 % от веса шлака. В шлак, кроме углерода, переходят зола и 20 % серы топлива: 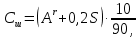 (7) (7)где Сш – содержание углерода в шлаке, кг. Сш = (14,93 + 0,2 ‧ 0,73) ‧ 10/90 = 1,68 кг. Выход шлака: mш = (Ar + 0,2S) + Сш (8) mш = (14,93 + 0,2 ‧ 0,73) + 1,68 = 16,756 кг Принимается, что на 100 кг топлива вводится 20 кг пара (νп = 1,11 моль). Уравнения для расчета состава газа по основному генераторному процессу: СО + СО2 = 3,658; Н2 + Н2О = 1,11; 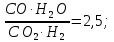 2 СО2 + СО = 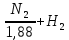 ; ;Пятое уравнение составляется на основе уравнения теплового баланса всего генераторного процесс, при условии, что температура газа при выходе из генератора в 250 °С. Приход тепла Теплота сгорания топлива: Q = 4,19 ‧ (81‧C + 300‧H - 26‧O + 26‧S) = 23285,21 кДж/кг. На 100 кг топлива: Q1= 23285,21 ‧ 100 = 2328521 кДж. Физическое тепло с углем: Q2 = cy ‧ t‧ m, (9) где cy – теплоемкость угля, cy = 0,2; t – температура угля, t = 15 °С. Q2 = 4,19 ‧ (0,2 ‧ 15 ‧ 100) = 1257 кДж. Теплосодержание пара паровоздушного дутья: Q3 = Wr ‧ cп, (10) где сп – теплосодержание насыщенного пара, cп = 622 ккал/к Q3 = 4,19 ‧ (12,2 ‧ 622) = 31795 кДж. Теплосодержание подаваемого в генератор воздуха: Q4 = cв‧ t‧ ν, (11) где св – теплоемкость воздуха, св = 0,312 ккал/м3; ν–расход воздуха на дутье, ν = 133 м3. Q4 = 4,19 ‧ (0,312 ‧ 15 ‧ 133) = 2608 кДж. Общий приход тепла в генератор на 100 кг топлива: Qпр = 2328521 + 1257 + 52123 + 2608 = 2384509 кДж. Расход тепла Теплота сгорания газов: Qi = qi‧ νi, (12) где qi– теплота сгорания i-го газа; νi – количество вещества i -го газа, кг/моль. QCH4 = 4,19‧ (213000 ‧ 0,287) = 256139 кДж. QC2H4 = 4,19‧ (341500 ‧ 0,038) = 54373 кДж. QH2 = 4,19‧ (68350 ‧ 0,739) = 211639 кДж. QCO = 4,19‧ (67700 ‧ 0,136) = 38578 кДж. QH2S = 4,19‧ (123920 ‧ 0,018) = 9346 кДж. Q1’ = 570075 кДж. Теплота сгорания смолы: Q = 4,19‧ (81C + 300H – 26O). (13) Q = 4,19‧ (81‧ 78,8 + 300 ‧ 7,8 – 26 ‧ 12,1) = 35230 кДж/кг. Q2 = 4,19 ‧ (4,853 ‧ 8408,2) = 170973 кДж. Теплосодержание смолы: Q3 = (Q0 + ccм ‧ t) ‧ mcм, (14) где ccм – теплосодержание смолы,ccм = 0,5 ккал/кг; Q0 – скрытая теплота испарения, Q0 = 80 ккал/кг. Q3 = 4,19‧ (80 + 0,5‧ 250)‧ 4,853 = 4168 кДж. Теплота сгорания углерода шлака: Q4 = Cш Qc, (15) где Cш – содержание углерода в шлаке, кг; Qc – теплота сгорания углерода, кДж. Q4 = 4,19 ‧ (1,68 ‧ 7800) = 54905 кДж. Физическое тепло шлака: Q5’ = tcш mш, (16) где t– температура шлака, t = 300 °; cш – теплосодержание шлака, cш = 0,2 ккал/кг; mш – масса шлака. Q5’ = 4,19 ‧ (0,2 ‧ 300 ‧ 162) = 4223 кДж. Расход тепла на потери в окружающую среду и получение пара в рубашке принимается равным 5 % от теплотворной способности топлива: Q6’ = 0,05Q1 (17) Q6’= 4,19 ‧ (0,05 ‧ 555732) = 116426 кДж. Теплосодержание продуктов пиролиза: Q7’= 22,4 ‧ ci‧ νi‧ t, (18) где ci – теплоемкость i –го газа; t – температура газов. Q’CO2 = 4,19 ‧ (0,063 ‧ 22,4 ‧ 250 ‧ 0,426) = 630 кДж. Q’CH4 = 4,19 ‧ (0,287 ‧ 22,4 ‧ 250 ‧ 0,414) = 2787 кДж. Q’C2H4= 4,19 ‧ (0,038 ‧ 22,4 ‧ 250 ‧ 0,518) = 462 кДж. Q’CО = 4,19 ‧ (0,136 ‧ 22,4 ‧ 250 ‧ 0,313) = 999 кДж. Q’H2= 4,19 ‧ (0,739 ‧ 22,4 ‧ 250 ‧ 0,31) = 5375 кДж. Q’H2S= 4,19 ‧ (0,018 ‧ 22,4 ‧ 250 ‧ 0,393) = 166 кДж. Q’H2О = 4,19 ‧ (595 + 0,48 ‧ 250) ‧ 17.6 = 52727 кДж. Q’г = 63146 кДж. Химическое тепло уноса пыли: Q’8 = my Qrв. (19) Q’8 = 4,19 ‧ (2 ‧ 4558,8) = 38203 кДж. Физическое тепло уноса: Q’9= ty‧ cy‘ ‧ my, (20) где ty – температура пыли, ty = 200 °С; cy’ – теплосодержание пыли, cy’ = 0,23 ккал/(кг °С). Q’9= 4,19 ‧ (200 ‧ 2 ‧ 0,23) = 386 кДж. Расход тепла: Qp’ = 386 + 38203 + 91778 + 96780 + 4072 + 52944 + 4123 + 169105 + 544379 = 1022505 кДж. Разность между приходом и расходом тепла, составляющая теплоту сгорания и теплосодержание продуктов основного генераторного процесса, равна: 2384509– 1022505 =1362004 кДж. Теплота сгорания продуктов основного генераторного процесса: 4,19 ‧ (67700 ‧ CO + 68350 ‧ H2). Теплосодержание при 250 °С: CO2 ‧ 4,19 ‧ 22,4 ‧ 250 ‧ 0,426 = 9996 ‧ CO2. (CO + N2) ‧ 22,4 ‧ 4,19 ‧ 250 ‧ 0,313 = 7341 ‧ (CO + N2). H2 ‧ 22,4 ‧ 4,19 ‧ 250 ‧ 0,31 = 7274 ‧ H2. H2O ‧ 22,4 ‧ 4,19 ‧ 250 ‧ 0,362 = 8493 ‧ H2O. Скрытая теплота испарения H2O – (10550 ‧ 4,19) H2O. На основании полученных данных составляется пятое уравнение: 4,19 ‧ (67700 ‧ CO + 68350 ‧ H2) + 9996 ‧ CO2 + 7341 ‧ CO + 7341 ‧ N2 + 7274 ‧ H2 + 8493 ‧ H2O = 1362004 кДж. Составляется система из пяти уравнений: СО + СО2 = 3,658; Н2 + Н2О = 1,11; 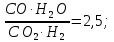 2 СО2 + СО = 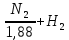 ; ;4,19 ‧ (67700CO + 68350H2) + 9996CO2 + 7341CO + 7341N2 + 7274H2 + 8493H2O = 1362004. Корни данного уравнения: 1) H2 = 1,011; 2) H2O =0.099; 3) CO2 = 0,138; 4) CO = 3,52; 5) N2=5,235 Проверка правильности подстановкой полученных цифр: 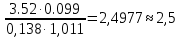 Расчет состава газа из 100 кг длиннопламенного угля Таблица 7 – Состав генераторного газа
Выход влажного газа: Vв.г. = 22,4Vг, (21) где Vг – выход конечного генераторного газа, кг/моль. Vв.г. = 12,29 ‧ 22,4 = 275,3 м3. Выход сухого газа: Vс.г. = (Vг – H2Oг) ‧ 22,4, (22) где H2Oг – содержание влаги в газе, кг/моль. Vс.г. = (12,29 – 1,078) ‧ 22,4 = 251,15 м3. Расход воздуха: 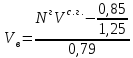 (23) (23)где Nг – содержание азота в газе, %; Vс.г. – выход сухого газа, м3/кг. 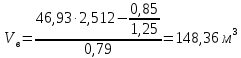 mв = ρ ‧ Vв = 1,29 ‧ 148,36 = 191,38 кг. (24) где ρ – плотность воздуха, ρ = 1,29 кг/м3. Влажность газа: 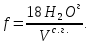 (25) (25) 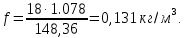 Количество водяного пара: Gв.п. = fVс.г.. (26) Gв.п. = 148,36 ‧ 0,131 = 19,44 кг. Таблица 8 – Плотность газов и их массовая доля
Плотность генераторного газа: 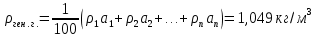 Масса генераторного газа: 263,46 кг. Далее составляем материальный и тепловой баланс процесса, рассчитываемый на 1000 кг исходного сырья, сведенные в таблицу 9 и 10 соответственно. Таблица 9 – Материальный баланс (на 1000 кг угля)
Таблица 10 – Тепловой баланс (на 1000 кг угля)
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
