исправленный курсач 2. Выбор и обоснование источников сырья, энергоресурсов, географической точки строительства
 Скачать 0.51 Mb. Скачать 0.51 Mb.
|
|
3.2.1. Давление С повышением давления увеличивается равновесный выход аммиака и возрастает скорость реакции. Скорость реакции растет так же с уменьшением размеров зерен катализатора. Применение высоких давлений увеличивает скорость процесса синтеза за счет повышения движущей силы процесса ∆P=PN2*PH23 и способствует отделению образовавшегося аммиака от газовой смеси путем его конденсации.[13] 3.2.2. Температура Оптимальный температурный режим процесса определяется общими закономерностями влияния температуры на выход продукта (рис.3.1). 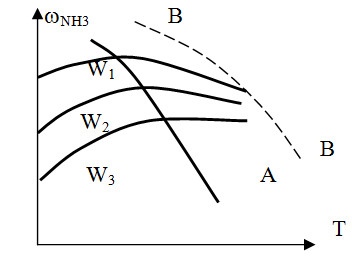 Рисунок 3.1– Зависимость содержания аммиака в газе после синтеза от температуры и объемной скорости газа (W3 > W2 > W1). Для каждого значения объемной скорости газовой смеси W содержание аммиака в ней увеличивается с ростом температуры до определенного предела, отвечающего максимальной скорости процесса и содержанию аммиака в газе. Эта температура будет отвечать наибольшей интенсивности катализатора. Линия А, соединяющая максимумы кривых wNH3 = f(T) для различных значений объемной скорости w, соответствует кривой оптимальных температур. Линия ВВ представляет равновесную кривую. Однако с ростом объемной скорости газа возрастает интенсивность катализатора (рис.3.2). 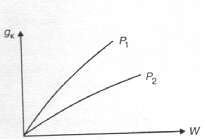 Рисунок 8.8 – Зависимость интенсивности катализатора от объемной скорости при Р1 > P2 Таким образом, увеличение объемной скорости газа до определенного предела положительно сказывается на выходе аммиака. [2] 3.2.3. Примеси Так как присутствие инертных примесей в реакционной смеси равносильно снижению общего давления, то с увеличением содержания метана, аргона, гелия в смеси скорость реакции синтеза уменьшается. 3.2.4. Катализаторы Синтез аммиака с заметной скоростью протекает только в присутствии катализатора. В промышленности нашли применение железные катализаторы, получаемые сплавлением оксидов железа с промоторами и последующим восстановлением оксидов железа. [1] 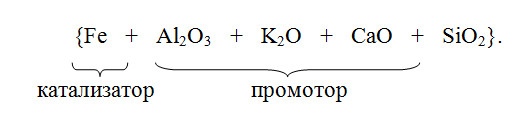 Он дешев, достаточно активен при температуре 450–5000С, менее остальных катализаторов чувствителен к каталитическим ядам. Промоторы в составе контактной массы способствуют созданию высокоразвитой поверхности, препятствуют рекристаллизации катализатора и повышают его активность. Контактную массу готовят сплавлением в атмосфере азота смеси оксидов железа Fe3O4, алюминия Al2O3, калия К2О, кальция СаО и кремния SiO2 или порошков металлических – железа и алюминия – с оксидами кальция и кремния и карбоната калия с последующим измельчением массы до размеров зерен катализатора (5 мм) и восстановлением их водородом в колонне синтеза аммиака. [2] Катализаторы синтеза аммиака необратимо отравляются сернистыми соединениями, хлором, кислородосодержащимися соединениями (H2O, CO, CO2). Они снижают активность катализатора, поэтому сырье для приготовления катализатора, а также азотоводородная смесь должны содержать как можно меньше примесей. 3.2.5. Состав газовой смеси Максимальная скорость реакции в промышленных условиях наблюдается при соотношении H2:N2 близком к 1:3. В промышленных условиях отклонение состава от оптимального соотношения ведет к снижению скорости процесса. Вывод: Термодинамические и кинетические факторы свидетельствуют в пользу проведения процесса при высоких давлениях (увеличивается равновесный выход, повышается скорость синтеза). Таким образом, для достижения более высокой производительности необходимо проводить процесс при высоких давлениях и оптимальном для данного катализатора температурном режиме, при больших объемных скоростях и на возможно более чистом газе. Также для увеличения скорости и выхода аммиака между полками катализатора должен осуществляться ввод свежего холодного синтез-газа (байпас). В современных агрегатах синтеза аммиака большой единичной мощности процесс ведут на плавленых железных катализаторах при температурах 420-500 0С, давлении 25-32 МПа, объемной скорости 15-25 тыс.ч-1. [1] 4. Синтез и анализ ХТС (химическая, структурная, операторная, технологическая схемы) Химическая схема синтеза N2(г) + 3H2(г) ↔ 2NH3(г) +45,9 кДж Условия протекания процесса: 1) Давление – 25 – 32 МПакатализатор – пористое железо с стабилизирующими и промотирующими добавками (Al2O3 и K2O) 2) Температура – 420 – 500 ˚С 3) Катализатор – пористое железо с стабилизирующими и промотирующими добавками(Al2O3 и K2O) Структурная схема 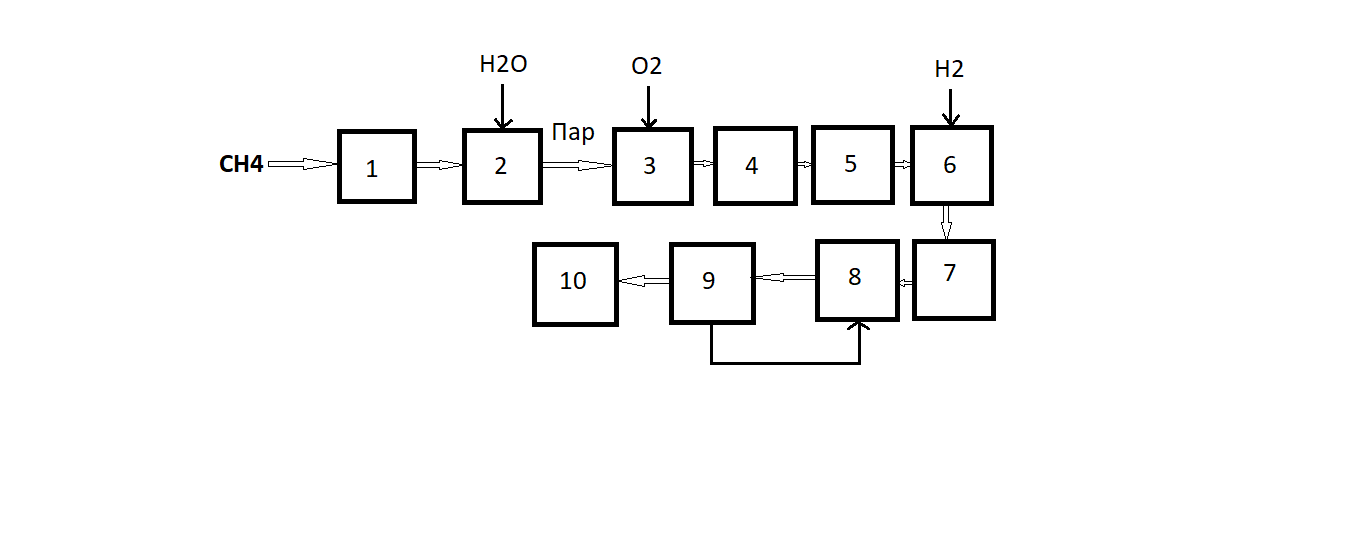 Рис. 6.1 Структурная схема производства аммиака 1- Очистка природного газа от сернистых соединений; 2- Паровая конверсия метана; 3- Воздушная конверсия метана; 4- Конверсия оксида углерода (II); 5- Очистка АВС; 6- Метанирование; 7- Сжатие АВС; 8- Синтез аммиака; 9- Охлаждение аммиака; 10- Сжатие аммиака; Технологическая схема  Рис. 6.2 Технологическая схема блока синтеза аммиака агрегата мощностью 1360 т/сут; 1 – подогреватель газа, 2 – колонна синтеза аммиака, 3 – подогреватель воды, 4 – выносной теплообменник; 5 – циркуляционное колесо компрессора; 6 – сепаратор жидкого аммиака; 7 – блок аппаратов воздушного охлаждения; 8 – конденсационная колонна; 9 – конденсационная колонна продувочных газов; 10 – испаритель жидкого аммиака на линии продувочных газов, 11 – сборник жидкого аммиака, 12 – испаритель жидкого аммиака на линии танковых газов; 13 – сепаратор; 14 – промежуточная дренажная емкость; 15 – испарители жидкого аммиака; 16 – магнитный фильтр ПрГ- природный газ; ДГ — дымовой газ; ПГ — продувочный газ; СГ — свежий газ; ЦГ — циркуляционный газ; ТПГ — смесь танковых и продувочных газов; Свежая азотоводородная смесь после очистки метанированием сжимается в центробежном компрессоре до давления 32 МПа и после охлаждения в воздушном холодильнике (на схеме не показан) поступает в нижнюю часть конденсационной колонны 8 для очистки от остаточных примесей СО2, Н2О и следов масла. Свежий газ барботирует через слой сконденсировавшегося жидкого аммиака, освобождается при этом от водяных паров и следов СО2 и масла, насыщается аммиаком до 3–5% и смешивается с циркуляционным газом. Полученная смесь проходит по трубкам теплообменника конденсационной колонны и направляется в межтрубное пространство выносного теплообменника 4, где нагревается до 185 –195 °С за счет теплоты газа, выходящего из колонны синтеза. Затем циркуляционный газ поступает в колонну синтеза 2. В колонне синтеза газ проходит снизу вверх по кольцевой щели между корпусом колонны и кожухом насадки и поступает в межтрубное пространство внутреннего теплообменника, размещенного в горловине корпуса колонны синтеза. В теплообменнике циркуляционный газ нагревается до температуры начала реакции 400–440 °С за счет теплоты конвертированного газа и затем последовательно проходит четыре слоя катализатора, в результате чего концентрация аммиака в газе повышается до 15%. Пройдя через центральную трубу, при температуре 500–515 °С азотоводородоаммиачная смесь направляется во внутренний теплообменник, где охлаждается до 330°С. Дальнейшее охлаждение газовой смеси до 130 °С осуществляется в трубном пространстве подогревателя питательной воды 3, в трубном пространстве выносного теплообменника 4 до 65 °С за счет холодного циркулирующего газа, идущего по межтрубному пространству, и затем в аппаратах воздушного охлаждения 7 до 40 °С, при этом часть аммиака конденсируется. Жидкий аммиак, сконденсировавшийся при охлаждении, отделяется в сепараторе 6, а затем смесь, содержащая 10–12% NH3, идет на циркуляционное колесо компрессора 5 азотоводородной смеси, где сжимается до 32 МПа. Циркуляционный газ при температуре 50 °C поступает в систему вторичной конденсации, включающую конденсационную колонну 8 и испарители жидкого аммиака 15. В конденсационной колонне газ охлаждается до 18 °С и в испарителях за счет кипения аммиака в межтрубном пространстве до –5 °С. Из трубного пространства испарителей смесь охлажденного циркуляционного газа и сконденсировавшегося аммиака поступает в сепарационную часть конденсационной колонны, где происходит отделение жидкого аммиака от газа и смешение свежей азотоводородной смеси с циркуляционным газом. Далее газовая смесь проходит корзину с фарфоровыми кольцами Рашига, где отделяется от капель жидкого аммиака, поднимается по трубкам теплообменника и направляется в выносной теплообменник 4, а затем в колонну синтеза 2. Жидкий аммиак из первичного сепаратора проходит магнитный фильтр 16, где из него выделяется катализаторная пыль, и смешивается с жидким аммиаком из конденсационной колонны 8. Затем его дросселируют до давления 4 МПа и отводят в сборник жидкого аммиака 11. В результате дросселирования жидкого аммиака до 4 МПа происходит выделение растворенных в нем газов Н2, N2, O2, СН4. Эти газы, называемые танковыми, содержат 16–18% NH3. Поэтому танковые газы направляют в испаритель 12 с целью утилизации аммиака путем его конденсации при –25 °С. Из испарителя танковые газы и сконденсировавшийся аммиак поступают в сепаратор 13 для отделения жидкого аммиака, направляемого в сборник жидкого аммиака 11. Для поддержания в циркуляционном газе постоянного содержания инертных газов, не превышающего 10%, производится продувка газа после первичной конденсации аммиака (после сепаратора 6). Продувочные газы содержат 8–9% NH3, который выделяется при температуре 25–30 °C в конденсационной колонне 9 и испарителе 10 продувочных газов. Смесь танковых и продувочных газов после выделения аммиака используют как топливный газ. [1] Операторная схема 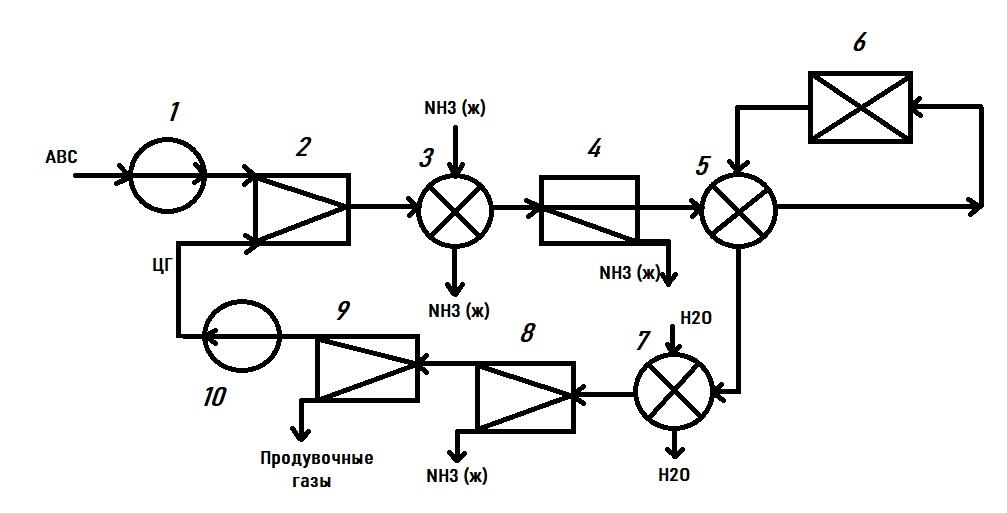 Свежая АВС после очистки метанированием сжимается до давления 32 МПа в операторе 1. В операторе смешения 2 АВС и циркулирующий газ смешиваются и в операторе 3 охлаждаются и очищаются жидким аммиаком. В операторе 4 происходит выделение сконденсировавшегося аммиака. Полученная смесь нагревается в теплообеннике 5 теплотой газа, выходящего из колонны синтеза. В операторе 6 происходит химическое превращение. Азотоводородноаммиачная смесь проходит несколько стадий охлаждения (5, 7), при этом часть аммиака конденсируется и жидкий аммиак отделяется в операторе 8. Газовую фазу разделяют на циркуляционный и продувочные газы в операторе 9. В операторе 10 смесь, содержащая 10-12 % аммиака сжимается до 32 МПа и циркулирующий газ отправляется на рецикл. 5. Выбор и обоснование конструкции основного аппарата 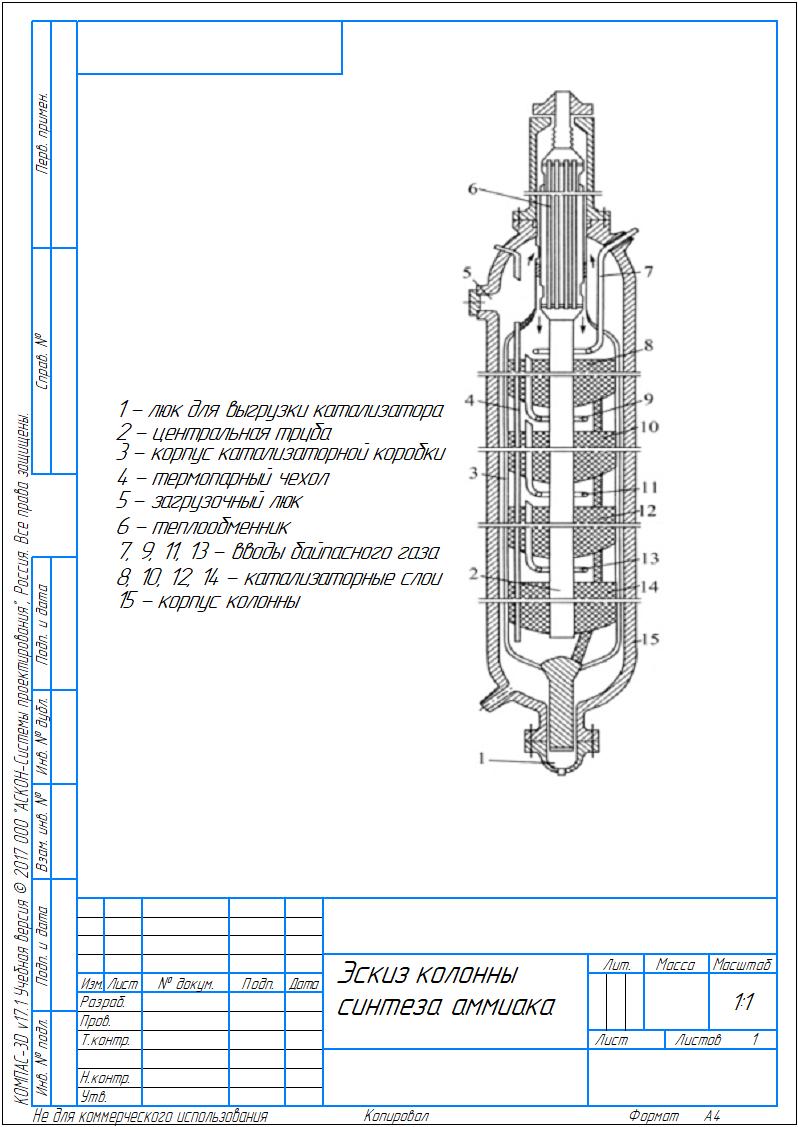 Рис. 6.1 Четырехполочная колонна синтеза аммиака мощностью 1360 т/сут 1 – люк для выгрузки катализатора; 2 – центральная труба; 3 – корпус катализаторной коробки; 4 – термопарный чехол; 5 – загрузочный люк; 6 – теплообменник; 7, 9, 11, 13 – вводы байпасного газа; 8, 10, 12, 14 – катализаторные слои; 15 – корпус колонны В агрегатах мощностью 1360 т/сут получили распространение аксиальные четырехполочные насадки с предварительным теплообменником и трехполочные с выносным теплообменником. На рисунке 6.1 показана четырехполочная колонна с аксиальными насадками. Основной поток газа подается в колонну снизу, проходит по кольцевой щели между корпусом колонны 15 и кожухом катализаторной коробки 3 и поступает в межтрубное пространство теплообменника 6. Здесь синтез-газ нагревается конвертированным газом до 420 – 440°С и проходит последовательно четыре слоя катализатора 8, 10, 12, 14, между которыми подается холодный байпасный газ, через вводы 7, 9, 11, 13. После четвертого слоя катализатора газовая смесь при 500—515 °С поднимается по центральной трубе 2, проходит по трубкам теплообменника 6, охлаждаясь при этом до 320—350 °С, и выходит из колонны. Свежий катализатор загружают в люк 5, отработанный выгружают через люк 1. Для контроля температурного режима служат термопары, опущенные в термопарный чехол 4. Характеристики колонны: Корпус катализаторной коробки изготовлен из хромоникелевомолибденовой стали 10Х18Н12М2Т, теплообменник — из стали 12Х18Н10Т. –давление – 31,5 МПа; –рабочая температура – 300–520°С; –диаметр (внутренний) – 2400 мм; –высота – 32 м; –толщина стенки – 250 мм; –объем катализатора по полкам I–IV соответственно – 7; 8,4; 12,8; 14,7 м3; [1] 6. Расчет материального и энергетического балансов. Определение расходных норм по сырью и энергии. Пути использования вторичных энергоресурсов. Расчеты проводились в программе MicrosoftExcel 6.1 Расчет материального баланса Исходные данные (состав на входе) представлены в таблице 6.1 Таблица 6.1 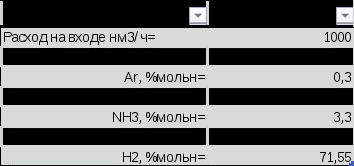 X(N2)=0,18 Балансовые расчеты: Пошло N2 в химическую реакцию = 42,93 нм3/ч По реакции израсходовалось Н2 = 128,79нм3/ч По реакции образовалось NH3 = 85,86нм3/ч  Таблица 6.2 Проверка расчетов по массе представлена в таблице 6.3 Таблица 6.3  6.2 Расчет энергетического баланса В общем виде тепловой баланс для адиабатического процесса в газе с подводом теплоты или отводом теплоты (QТП) рассчитывается по следующей формуле: QТП = Q ФИЗ ВЫХ (Q ФИЗ ВХОД + QХР QПОТЕРЬ) Таким образом, при проведении расчета необходимо определить количество подведенной (отведенной) теплоты. Т(вход)=682 К Т(выхода)=733 К БАЛАНСОВЫЕ РАСЧЕТЫ 1) Перевод V(вход)=1000нм3/ч=0,2778нм3/сек 2)Расчет изобарных объемных теплоемкостей: Ср(входа)= Ср(Ar) * Свх(Аr)/100 + Ср(СH4) * Свх(СH4)/100+Ср(NH3) * Свх(NH3)/100+Ср(N2) * Свх(N2)/100+Ср(Н2) * Свх(Н2)/100=1301,987 Дж/нм3*К 3) Расчет Qвход = V(ВХОД) * Cp(ВХОД) * T(ВХОД)=682*1301,987*0,2778=246673,98Дж/сек 4) Перевод Vвыхода=914,14нм3/ч=0,2539нм3/сек Ср(выхода)=1124,5286Дж/нм3*К 6)Расчет выхода: Qвыхода=1124,5286*733*0,2539=209284,55 Дж/сек 7)Количество ключевого компонента пошедшего в химическую реакцию берется из материального баланса и пересчитывается на моли: Vхр (нм3/ч) / 0,0224 (нм3/моль) / 3600 (сек/ч) = 42,93/0,0224/3600=0,5323 моль/сек 8) Найдем тепловой эффект в химической реакции: dH=-92,38 кДж/моль q=92,38*1000/1=92380 Дж/моль 9) Qхр=Vхр (моль/сек) * ХР (Дж/моль)=92380*0,5323=49173,8 Дж/сек 10) Qрасх(без потерь тепла)=Qвых=209284,55Дж/сек 11)Qпотерь=0,04*209284,55=8371,382 Дж/сек 12) Qрасх=209284,55+8761,6872=217655,932 Дж/сек 13) Qприх=Qвход+Qхр=295847,78 Дж/сек 14) Qотводим=Qприх-Qрасх=295847,78 -217655,932 =78191,848 Дж/сек Таблица 6.5  Реакция синтеза аммиака является экзотермической. Для проведения процесса требуется отвод тепла. |
