Содержательный модуль 1.. Витаминоподобные вещества. Витаминоподобные вещества
 Скачать 161.53 Kb. Скачать 161.53 Kb.
|
|
Содержательный модуль 1. Биохимические основы жизнедеятельности организма 1. Витаминоподобные вещества. Витаминоподобные вещества – это большая группа биологически активных веществ, имеющих некоторые свойства витаминов, но не соответствующих всем параметрам, характерным для витаминов. Иногда такие вещества называют псевдовитаминами. Большинство витаминоподобных веществ синтезируются эндогенно, в организме человека, в достаточных количествах для удовлетворения потребностей организма. Также для отдельных витаминоподобных веществ в настоящее время не удалось определить суточную потребность. К витаминоподобным веществам относятся холин, карнитин, биофавоноиды, липоевая кислота, лецитин, кофермент Q10, инозит, п-аминобензойная кислота (ПАБК), биотин, пангамовая кислота, оротовая кислота, витамин U. Карнитин – витаминоподобное химическое соединение, которое содержится в тканях скелета и сердечной мышцы. Он действует как молекула-носитель при окислении жирных кислот. Организм человека способен синтезировать достаточное количество карнитина, полностью удовлетворяя потребность в нем. Пищевыми источниками карнитина являются мясо и молочные продукты. Холин - это щелочное соединение, первоначально отнесенное к семейству витаминов группы В. Холин синтезируется в организме, но в недостаточном количестве, поэтому он должен также поступать с пищей. Холин является компонентом фосфолипидов, которые образуют структурные элементы клеточных мембран; играет важную роль в нервной функции; участвует в различных метаболических процессах, в том числе транспорте жиров из печени. Ориентировочная суточная потребность в холине составляет 150-1000 мг (в среднем – 500 мг) и, как правило, легко достигается с помощью питания. Холин содержится в зерновых продуктах, яичном желтке, пивных дрожжах и субпродуктах (печень, почки, мозги). Инозит (инозитол) – химическое вещество, представляющее собой шестиатомный спирт. Из всех изомеров биологической активностью обладает только миоинозит (мезо-инозит). Биологическое значение миоинозита пока точно не установлено. В больших количествах у людей он присутствует главным образом как составляющая фосфолипидов.Пищевыми источниками мезоинозита являются печень, пшеничные отруби, орехи, молоко, пивные дрожжи, сладкая кукуруза, овес, цельнозерновые продукты, капуста, изюм, грейпфрут, арахис. Парааминобензойная кислота – один из компонентов фолиевой кислоты (витамин B9). Она синтезируется бактериями в кишечнике. Парааминобензойная кислота оказывает антитиреотоксическое действие, а также участвует в процессах, обеспечивающих пигментацию волос и кожи. Суточная потребность в парааминобензойной кислоте не установлена. В очень больших дозах может вызвать рвоту. Источниками парааминобензойной кислоты в пищевых продуктах являются мясо, яйца, злаки и молоко. Коэнзим Q10 (убихинон) вырабатывается непосредственно в организме человека, а также поступает с пищей. Самая большая концентрация коэнзима Q10 находится в сердечной мышце. Коэнзим Q10 используется клетками организма аэробном (или клеточном) дыхании, а также в качестве эндогенного антиоксиданта. Хорошими источниками CoQ1 в пище являются жирная рыба, растительные масла, зеленый перец, зеленый горошек, зеленая фасоль. Суточная потребность в убихиноне не определена. Лецитины – общепринятое название группы жироподобных веществ, представляющий собой смесь фосфолипидов с триглицеридами небольшим количеством других веществ. Участвуют в образовании клеточных мембран и метаболизме жира. Лецитин вырабатывается в организме человека. Он также содержится в растительных маслах и соевых бобах. Липоевая кислота является коферментом. Она производится в организме в достаточном количестве, дефицита ее у млекопитающих не наблюдается. Липоевая кислота содержится в говяжьем мясе и печени, молоке, бобовых, дрожжах. Биофлавоноиды – растительные полифенолы (рутин, цитрин, кверцетины и пр.), которые совместно с витамином С уменьшают проницаемость и повышают прочность капилляров, стимулируют тканевое дыхание. Биофлавоноиды поступают в организм с фруктами, овощами, ягодами. Биотин – органическая кислота, выполняющая роль кофермента в разнообразных биохимических реакциях в организме. Биотин содержится в субпродуктах (печень, почки), дрожжах, бобовых, цветной капусте и орехах, в шампиньонах. Суточная потребность в биотине не установлена. Пангамовая кислота широко представлена в семенах различных растений.Она обладает липотропными свойствами и может рассматриваться как важный фактор нормализации липидного обмена.Суточная потребность для нее веществе не установлена. Пантгамовой кислотой богаты семена злаковых растений и ядра косточковых плодов. Оротовая кислота в организме используется для синтеза нуклеотидов и нуклеиновых кислот. Содержится в дрожжах, печени, молоке. Витамин U (S-метилметионинсульфоний-хлорид) обладает противоязвенными свойствами. Содержится в капусте, сырых желтках, свекле, зелени петрушки и других зеленых растениях. 2.Общее представление о гормонах. Гормоны — это органические вещества, которые синтезируются в специальных секреторных клетках и органах. Они с током крови доставляются к различным тканям-мишеням, где оказывают регулирующее воздействие на обмен веществ и физиологические функции организма. Сами гормоны не участвуют в метаболических реакциях, а являются их специфическими регуляторами. Под контролем гормонов находятся процессы синтеза белка, активность многих ферментов, проницаемость клеточных мембран для различных энергетических субстратов, коферментов, минеральных веществ. Такое влияние играет важную роль в поддержании постоянства внутренней среды (гомеостаза) в организме при физических нагрузках и других внешних воздействиях, в обеспечении высокой физической работоспособности, в адаптации организма к систематическим физическим нагрузкам. Высокоспециализированные органы или группы клеток, которые осуществляют синтез гормонов (секрета) и выброс (секреция) их непосредственно в кровь, межклеточную жидкость или лимфу, называются железами внутренней секреции. Они не имеют выводящих протоков, поэтому называются эндокринными железами (эндо — "внутрь"). Отдельные железы внутренней секреции анатомически не связаны между собой и находятся на большом расстоянии друг от друга (рис. 45). Однако функционально все они взаимосвязаны и представляют единую эндокринную систему. 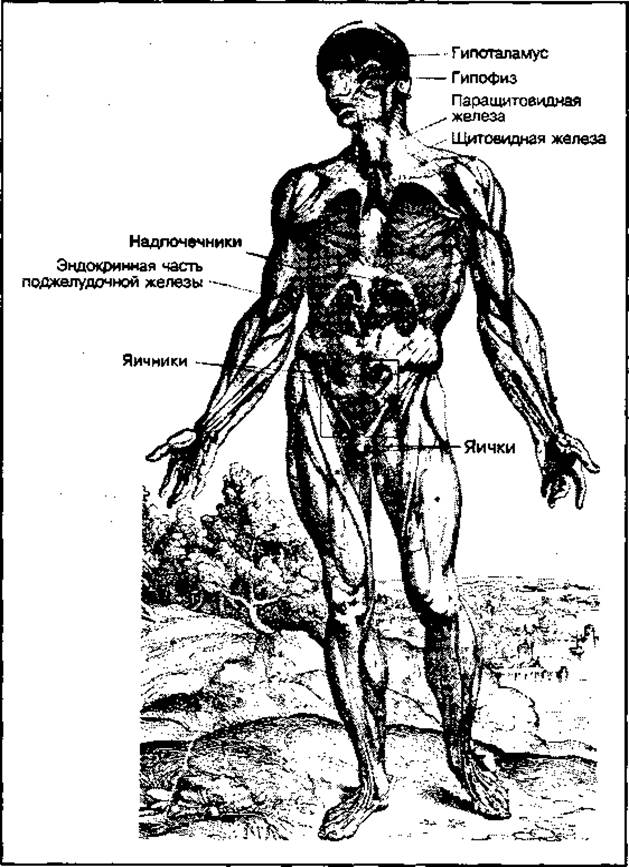 Рис. 45 Основные эндокринные железы человека и их расположение в организме Различают центральные железы (гипоталамус, гипофиз, эпифиз) и периферические (щитовидная, паращитовидная, поджелудочная, надпочечники, половые железы). Центральные железы расположены у основания мозга и напрямую связаны с деятельностью ЦНС. Они выделяют нейрогормоны и гормоны, которые регулируют функции периферических эндокринных желез. Между периферическими железами также существует тесная взаимосвязь. Гормоны одной железы могут усиливать или подавлять секреторную функцию другой железы. Отдельные гормоны, которые образуются в эндокринных железах (инсулин, глюкагон, тироксин), могут синтезироваться и в стенках желудка или кишечника. Регуляторное действие, подобное гормонам, оказывают гуморальные факторы — тканевые гормоны. Тканевые гормоны — это биологически активные вещества, которые синтезируются в различных тканях организма и оказывают местное регулирующее воздействие. Многие из них синтезируются в органах пищеварения и регулируют их деятельность. Это гастрин (стимулирует секрецию желудка), секретин (усиливает секрецию двенадцатиперстной кишки), холецистокинин (усиливает секрецию тонкого кишечника) и др. Такие тканевые гормоны, как гистамин, серотонин, брадикинин, простагландины, влияют на тонус кровеносных сосудов, возбудимость нервной системы. В клетках мозга образуется гамма-аминомасляная кислота (ГАМК), которая регулирует процессы торможения нервной системы и выступает в роли фактора утомления. В гипофизе могут образовываться гормоны эндорфины, которые оказывают обезболивающее действие, а при высоких концентрациях вызывают чувство эйфории подобно наркотическим препаратам. В настоящее время выделено и изучено около 100 гормонов и нейромедиаторов, которые различаются по месту их синтеза, химической структуре и механизмам регуляторного действия. По этим трем критериям чаще всего и классифицируют гормоны. В данном учебнике использована наиболее старая, но удобная классификация гормонов по эндокринным железам, в которых они синтезируются. 3. Регуляция обмена АТФ. Скорость синтеза АТФ зависит от скорости ее использования. Скорость использования АТФ зависит от скорости протекания тех процессов, в которых АТФ является источником энергии (см. рис. 19). Так, при выполнении мышечной работы резко усиливается расщепление АТФ в мышцах. В период восстановления энергия АТФ также интенсивно используется для синтеза белков и других пластических процессов. Образовавшиеся продукты гидролиза АТФ — АДФ, АМФ и пирофосфат — быстро включаются в реакции ресинтеза ее, с тем чтобы восстановить исходный физиологический уровень АТФ. Одним из основных механизмов регуляции обмена АТФ в клетке является величина энергетического заряда клетки, которая определяется соотношением концентраций АТФ, АДФ и АМФ: Обычно концентрация высокоэнергетической АТФ в клетках значительно превышает сумму концентрации АМФ и АДФ. Энергетический баланс системы равен 0,7—0,8. Такое состояние является физиологической нормой и поддерживается метаболическими процессами на постоянном уровне. Это означает, что системы организма функционируют с наименьшей затратой энергии, а скорость образования АТФ равна скорости ее использования. Если энергетический заряд клетки понижается (количество АТФ уменьшается, а АДФ и АМФ — увеличивается), то ускоряются процессы, ведущие к образованию АТФ, и тормозятся процессы ее использования. Если же энергетический заряд системы превышает нормальный уровень и достигает единицы (много АТФ, мало АДФ и АМФ), то процессы синтеза АТФ тормозятся, а процессы ее использования усиливаются. В регуляции постоянства концентрации АТФ в клетке участвует макроэргическое вещество креатинфосфат. При участии фермента креатинфосфокиназы (КФК) креатинфосфат легко передает фосфатную группу на АДФ и способствует восстановлению физиологического уровня АТФ в тканях: 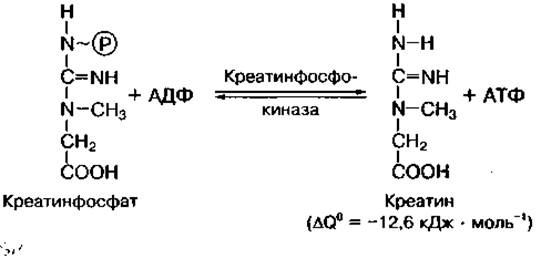 Креатинфосфокиназная реакция обратима. При повышении содержания АТФ в клетках образуется креатинфосфат. Следовательно, креатинфосфат выполняет роль энергетического резерва и энергетического буфера, препятствующего повышению АТФ в клетке. Относительно постоянный уровень АТФ поддерживается до тех пор, пока в тканях не произойдет значительное снижение запасов креатинфосфата. Содержание креатинфосфата в отдельных типах скелетных мышц несколько отличается и составляет в медленносокращающихся мышцах порядка 72—85 ммоль ∙ кг-1 сухой мышечной ткани, в быстросокращающихся — 82—89 ммоль ∙ кг-1. Содержание же АТФ в этих типах мышц примерно одинаковое и составляет около 25 ммоль ∙ кг-1 сухой мышечной ткани. В.А. Саксом и другими авторами обосновано положение о том, что креатинфосфат выполняет в клетках роль "энерготранспортирующего челнока», т. е. переносит энергию, заключенную в макроэргических связях АТФ, от мест образования к местам ее утилизации (см. рис. 17). Связано это с тем, что молекула свободного креатина имеет высокую скорость диффузии, которая почти на порядок выше, чем АТФ. Кроме того, в клетках существуют различные формы фермента креатинфосфокиназы (КФК), которые локализованы на разных ее участках: на внутренней мембране митохондрий, саркоплазматическом ретикулуме, миофибриллах, наружной плазматической мембране, в цитоплазме. Креатинфосфат образуется на внутренних мембранах митохондрий за счет перефосфорилирования свободного креатина и АТФ, которая доставляется из матрикса митохондрий с участием специфического белкового переносчика — аденилаттранслоказы (АТ) и самостоятельно не может перемещаться к местам использования энергии. Часть креатинфосфата образуется в цитоплазме из АТФ в процессе гликолиза. Образовавшийся креатинфосфат легко проникает в цитоплазму и к другим местам его использования. С участием специфических форм креатинфосфокиназы из креатинфосфата образуется АТФ, которая тут же используется либо АТФ-азой миозина, либо Са2+-АТФ-азой саркоплазматического ретикулума или Nа+-К+-АТФ-азой плазматических мембран. Освободившийся креатиннова поступает к митохондриям, где образуется АТФ в процессе окислительного фосфорилирования, и вновь забирает от АТФ макроэргический Фосфат. Благодаря такой функции креатинфосфата в энергообмене предпринимаются попытки использовать медицинские препараты креатинфосфата или креатина для восполнения либо повышения его уровня в организме. Таким образом, соотношение концентраций АТФ, АДФ и АМФ в клетках регулирует скорость обменных процессов, ведущих к накоплению АТФ и ее использованию. Механизмы регуляции синтеза и распада АТФ в настоящее время интенсивно изучаются, поскольку составляют энергетическую основу регуляции скорости сокращения мышц, других АТФ-зависимых процессов. Не исключено, что в скелетных мышцах скорость синтеза АТФ в процессе их работы регулируется ионами кальция, уровень которого изменяется в процессе сокращения—расслабления. Кальций влияет на процесс окислительного фосфорилирования, увеличивая скорость образования АТФ. Некоторые гормоны, например, адреналин, также влияют на этот процесс |
