КАС. Вопрос 1 1 Понятие термодинамической системы
 Скачать 189.82 Kb. Скачать 189.82 Kb.
|
|
ВОПРОС 24 Формула Пуазейля позволяет рассчитать объёмную скорость течения жидкости по известным значениям радиуса трубки r, её длины L, вязкости жидкости η и разности давлений на концах трубки p1 – р2. V 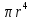 Q=____ =_______(P1-P2) T 8nL Как и можно было ожидать, объёмная скорость прямо пропорциональна разности давлений и обратно пропорциональна вязкости. 8nL/ 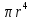 Вопрос №25 Работа, совершаемая сердцем, затрачивается, во-первых, на выталкивание крови в магистральные артериальные сосуды против сил давления и, во-вторых, на придание крови кинетической энергии. Первый компонент работы называется статическим(потенциальным), а второй - кинетическим(динамическим). Статический компонент: Аст=pср*Vc где: р - среднее давление крови в соответствующем магистральном сосуде(аорте - для левого желудочка, легочном артериальном стволе - для правого желудочка); V - систолический(ударный) объём - объём, выбрасываемый каждым из желудочков при одном сокращении. Кинетический компонент: A2=mv2/2=pVy* v2/2 где: p - плотность крови; u - скорость кровотока в магистральном артериальном стволе; Vy - ударный объём сердца В течение одной систолы правый желудочек выбрасывает в аорту ударный объем крови (60-70 мл). На столько же уменьшается и объем желудочка: ΔV ≈ 65х10-6 м3. Полезная работа, совершенная сердечной мышцей за одно сокращение, может быть оценена по формуле: ΔΑ = РсрΔVуд, где ΔVуд - среднее значение ударного объема крови, а Рср - среднее давление, которое создается внутри желудочка. Оно немного выше систолического давления в артерии: Рср ≈ 17 кПа. Отсюда получаем оценку для работы сердечной мышцы за одно сокращение: ΔΑ ≈ 17х103х65х10-6 = 1,1 Дж. Полезная мощность, развиваемая сердечной мышцей во время систолы, Nс = ΔΑ/Ίc, где Tc ≈ 0,3 с - длительность систолы. Отсюда получаем: Nс = 1,1/0,3 = 3,7 Вт. Время одного цикла сердечной деятельности Т ≈ 0,85 с. Средняя мощность за весь цикл равна Nср = 1,1/0,85 = 1,3 Вт. ВОПРОС26 Среди артерий эластического типа важнейшую роль играет грудной отдел аорты. С ним главным образом связана основная функция сосудов этого типа — обеспечение непрерывности кровотока. Источником энергии служит миокард. Его работа имеет два компонента: статический и динамический, причем на долю первого из них (Аст) приходится 98 % всей энергии сократившегося сердца. Аст затрачивается на растяжение стенок артерий (прежде всего, грудного отдела аорты). Накопив энергию во время систолы, аортальная стенка отдает ее крови, когда сердце пребывает в расслабленном состоянии и не поставляет кровь в сосудистое русло. Благодаря упругости артерий эластического типа кровь не останавливается и в диастолу сердца, когда потенциальная энергия растянутой стенки артерии эластического типа преобразуется в кинетическую энергию крови. Механизм функционирования грудного отдела аорты был изучен в прошлом веке физиологом Э. Вебером, в трудах которого он назывался феноменом «Wind- kessel». В отечественной литературе этот немецкий термин переводится как «воздушный колпак». Встретив такой термин, не стоит думать, будто в аорте содержится воздух. Вебер воспользовался технической терминологией, заподозрив аналогию между артериями эластического типа и пожарной помпой, в которой непрерывность струи при ритмичном качании двух рукояток обеспечивается созданием воздушной подушки в стальном резервуаре насоса. Воздух там находится под давлением, создаваемым циклической работой двух людей, попеременно пригибающих рукоятки. Этим давлением в пожарной помпе определяется потенциальная энергия сжатого воздуха, которая преобразуется в кинетическую энергию водяной струи. В стенке аорты потенциальная энергия связана не со сжатием воздуха, а с упругими усилиями, возникающими в растянутых эластических волокнах. Поэтому эффект накопления потенциальной энергии аортальной стенкой во время систолы лучше называть феноменом не «воздушного колпака», а «компрессионной камеры» (этот термин также используется в научной литературе). Биофизические особенности аорты. Под действием крови, выбрасываемой в систолу левым желудочком, происходит растяжение аортальной стенки, обладающей упругими свойствами. Согласно закону Гука, в ней развивается сила упругости: Fynp = -к • х. Оценим значения х и к для аортальной стенки. Существует связь между Fynpy давлением (р), под действием которого сосуд растягивается, и параметрами этого сосуда: Fynp=р»2rl, где г — радиус, I—длина сосуда. При колебаниях давления крови в сосуде изменяется главным образом его просвет, а длина остается практически неизменной. Следовательно, х в уравнении Гука для аорты — не что иное как изменение ее диаметра. При рентгенографии аорты обнаружили, что в систолу ее диаметр увеличивается примерно на 10% относительно своего диастолического значения. Коэффициент упругости (к) определяется преимущественно эластическими волокнами, хотя в аортальной стенке присутствуют наряду с ними коллагеновые волокна. На гистологических препаратах аорты коллагеновые волокна имеют волнистую (гофрированную) форму, обусловленную их свободной (рыхлой) укладкой среди других структур, пребывающих в недеформированном состоянии. Под действием повышения КД в физиологических пределах коллагеновые волокна только распрямляются, но не растягиваются. Деформация сети коллагеновых волокон создает так называемые термокинетические упругие силы, но их величина незначительна вследствие малого значения коэффициента упругости в этом процессе. Высокая упругость коллагеновых волокон, выражением чего является значительный модуль Юнга (108—109 Па), свойственна им при растяжении, а не при распрямлении, при котором возникают термокинетические упругие силы. Иными словами, значительная упругость коллагена проявляется только под действием больших усилий, выходящих за пределы физиологических значений КД. Благодаря коллагеновым волокнам стенки артерий здорового человека не разрушаются даже при 5—10-кратном повышении КД. Следовательно, коллагеновые волокна обеспечивают артериальной стенке не упругость, а жесткость и прочность. Напротив, эластические волокна аортальной стенки растягиваются при обычных колебаниях КД во время систолы сердца. В эластических волокнах возникает сила упругости в соответствии с законом Гука. Коэффициентом пропорциональности между Fynp и величиной растяжения стенки аорты при повышении КД служит модуль Юнга эластических волокон, равный (0,4s* 1,0) 106 Па. Эластическим волокнам аорты в физиологических условиях свойственна экспоненциальная зависимость силы упругости от степени растяжения. При более сильном растяжении устанавливается линейная зависимость, а чрезмерно растянутые эластические волокна разрываются. Сопоставление вклада эластических и коллагеновых волокон в упругие свойства артериальной стенки подтверждает важный принцип биомеханики: анализ механических свойств тканей организма необходимо проводить с учетом реальных сил, действующих на них. Упругость аортальной стенки обусловливает еще одно важное явление — возникновение и распространение пульсовой волны по стенке артерий. Дело в том, что Fynp9 развивающаяся при растяжении аорты, направлена не строго перпендикулярно к оси сосуда (рис. 4.43) и может быть разложена на нормальную и тангенциальную составляющие. Непрерывность кровотока обеспечивается первой из них, тогда как вторая является источником артериального импульса, под которым понимают упругие колебания артериальной стенки. Заметим, что Fn гораздо больше преобладает над JFt, чем показано на рис. 4.43. На создание пульса затрачивается незначительная часть силы упругости растянутой аорты. Пульсовая волна распространяется от места своего возникновения до капилляров, где затухает. Скорость ее распространения (рП) можно рассчитать по формуле: ГЕТ Un “)|2р У где Е — модуль Юнга сосудистой стенки; Ъ — ее толщина; г — радиус сосуда; о — плотность тканей сосудистой стенки. Вопрос 27 Из артерий эластического типа кровь поступает в резистивные сосуды, обладающие гладкомышечными клетками (ГМК), которые способны, сокращаясь, активно изменять просвет сосудов. Тем самым регулируется гемодинамическое сопротивление, от которого, в свою очередь, зависят объемная скорость кровотока в органах, васкуляризируемых этими сосудами, и кровяное давление. Следовательно, резистивные сосуды — важнейшие регуляторы гемодинамики. Типичными представителями артерий мышечного типа являются артериолы большого круга кровообращения. Такое название имеют мелкие артерии диаметром от десятка до сотни микронов с общим структурным признаком — наличием выраженной гладкомышечной оболочки, на долю которой приходится значительная часть общего диаметра сосуда (табл. 4.1). Мощной мышечной оболочкой обусловлено основное функциональное свойство артериол — активный сосудистый тонус, под которым понимают регулируемое тоническое сокращение гладкомышечных клеток сосудистой стенки. Сосудистый тонус создается и поддерживается несколькими механизмами. П е р в ы м из них является возникновение силы упругости при растяжении соединительнотканной наружной оболочки артериолы — tunicae adventitiae (ее называют «сумкой» артериального сосуда, удерживающей его в определенном состоянии и пассивно реагирующей на растяжение кровью созданием силы упругости в соответствии с законом Гука). Второй механизм связан с уникальным свойством ГМК — способностью отвечать на растяжение их кровью генерацией потенциалов действия, инициирующих активное сокращение этих клеток. В ГМК, обладающих автоматией (в спонтанно активных ГМК), третьим механизмом являются их автоматические (спонтанные) сокращения. Три перечисленных процесса создают так называемый базальный сосудистый тонус, для которого характерно относительное постоянство. Вместе с тем сосудистый тонус даже в покое обусловлен не только базальным тонусом, но и сокращениями ГМК под влиянием нервных импульсов, поступающих к ним по вегетативным (главным образом, симпатическим) нервным волокнам. В совокупности с базальным тонусом тонические сокращения ГМК под влиянием управляющих сигналов формируют сосудистый тонус покоя. В сократившейся ГМК модуль Юнга на порядок больше, чем в расслабленной, а увеличение ее жесткости пропорционально повышению внутреннего напряжения при сокращении. Вторая функция артерий мышечного типа — перераспределение крови между органами в зависимости от потребности в ней — обеспечивается работой артериол в качестве «сосудистых кранов». Это меткое образное определение принадлежит И. М. Сеченову. Из уравнения Пуазейля, разрешенного относительно Q.(CM. 4.2.1), прямо следует, что в зависимости от просвета артериол меняется объемная скорость кровотока в органе, которому они принадлежат, причем ее изменения пропорциональны изменениям радиуса этого просвета в четвертой степени. Артериолам принадлежит большая роль в развитии ряда патологических процессов. Гипертоническая болезнь связана с их стойким сужением (спазмом). При гипотонических состояниях сосудистый тонус ослаблен. В капиллярах (обменных кровеносных сосудах) осуществляется обмен веществ между кровью и тканями, ради чего существует вся сердечнососудистая система. Поэтому капилляры зачастую называют центральным (главным) ее элементом. Их характерной особенностью является то, что сосудистая стенка образована одним слоем эндотелия, содержит тонкую базальную мембрану при отсутствии мышечной и адвентициальной оболочек. Диаметр капилляра от 5—7 до 10 мкм, а длина от 0,5 до 1,1 мм, но если все капилляры человека приложить друг к другу конец в конец, то общая длина составит 100 ООО км. Ими можно опоясать Землю по экватору 2,5 раза. Общая площадь обмена через стенки капиллярного русла превышает 1000 м2. В1 мм3 тканей человека содержится в среднем 600 капилляров, но в разных тканях этот показатель неодинаков: в миокарде, головном мозге, почках и печени он достигает 3000, в скелетных мышцах — 300—400 (в тонических даже 100), а в костной и жировой тканях и того меньше. В зависимости от ультраструктурной организации стенки различают три типа капилляров: 1) с непрерывной стенкой, причем эндотелиальные клетки с диаметром пор в плазмолемме 4—5 нм уложены наподобие черепицы — проницаемость стенки таких капилляров наименьшая по сравнению с другими (капилляры с непрерывной стенкой присущи мышцам, легким, жировой ткани); 2) с фенестрированной (окончатой) стенкой — диаметр «окон» в ней достигает 100 нм, что обеспечивает их лучшую проницаемость, например, в почечных капиллярных клубочках и в слизистой оболочке кишки; 3) с прерывистой стенкой — за счет крупных пространств (с линейными размерами более 10 мкм), например между эндотелиальными клетками в капиллярах костного мозга, печеночных и селезеночных синусах, где проницаемость капиллярной стенки наибольшая. Через эндотелиальную стенку капилляра может «протиснуться» даже лейкоцит (рис. 4.42). О механизмах транспорта веществ через стенку капилляра см. 1.4.4. Вены являются емкостными кровеносными сосудами. Благодаря выраженной пластичности (см. 4.1) они могут сильно деформироваться (растягиваться) и вмещать много крови без развития напряжения в сосудистой стенке. При повышении венозного КД на 10 мм рт. ст. вместимость венозного русла большого круга кровообращения увеличивается в 6 раз. Поэтому вены называют резервуаром крови с переменной (регулируемой) емкостью. Ими образованы кровяные депо организма, которые в покое содержат 40—50% всего объема крови (примерно 1,5 л в венозных синусах селезенки, до 1 л в венозных сплетениях кожи и т. д.). Во всех венах большого круга сосредоточено до 80% крови, протекающей по нему. Кровь течет по венам под действием двух сил: «vis a tergo» (действующая сзади) и «vis a fronte» (действующая спереди). Первым термином прежде всего обозначают силу, которая обусловлена механической энергией, сообщенной крови сердцем во время систолы и сохранившейся после кровотока по артериям и капиллярам. Остаточная энергия в венулах большого круга кровообращения составляет в покое не более 13% работы левого желудочка (13% от 0,92 Дж за 1 систолу). Это основной компонент vis a tergo. Дополнительными служат массирующее действие пульсирующих рядом с венами артерий и, в большей степени, сокращения скелетных мышц, сжимающие венозные сосуды и проталкивающие кровь. Такое проталкивание действует в одном направлении (к предсердиям) благодаря наличию в венах клапанов. Движению крови в венах конечностей способствует то обстоятельство, что они образуют с артериями сообщающиеся сосуды. Вторая сила обусловлена присасывающим действием на кровь грудной клетки («дыхательного насоса» и отчасти смещения в сторону желудочков предсердно-желудочковой перегородки в определенную фазу сердечного цикла). КД в правом предсердии называется центральным, венозным давлением (ЦВД). На выдохе оно повышается, а на вдохе понижается. При понижении ЦВД от 0 до -4 мм рт. ст. приток венозной крови в правое предсердие возрастает на 20—30%. Однако дальнейшее снижение ЦВД ухудшает кровоток, поскольку это приводит к спаданию вен. Пределы изменений ЦВД, при которых сердце работает устойчиво, лежат в диапазоне от 0,01—0,05 кПа до 0,1—0,12 кПа. Средняя величина ЦВД у здорового человека в покое от 0,04 до 1,12 кПа. Вопрос28 Среда по отношению к организму выступает как комплекс раздражителей. Раздражителем называют всякий фактор окружающей среды, под действием которого происходят изменения свойств или состояния ткани, органа, целого организма. Такими факторами являются любые отклонения физических, химических и физико-химических параметров среды от тех значений, которые привычны для биологической системы. Разнообразные раздражители принято классифицировать по модальности — по той форме энергии, которая свойственна каждому из них. Встречаются химические, механические, тепловые, осмотические, электрические, световые и другие раздражители. В основу другой классификации раздражителей положен принцип адекватности (соответствия). Все раздражители подразделяются на адекватные и неадекватные по отношению к данной ткани. Адекватным считается стимул, к воздействию которого она приспособилась в ходе эволюции. Адекватность раздражителя для исследуемой ткани проявляется в том, что его пороговая величина значительно ниже, чем у неадекватных раздражителей. Так, ощущение света возникает у человека, когда минимальный поток световой энергии составляет всего 10-17—10-18 Вт. Ощущение вспышки можно вызвать и механическим воздействием на глаз (явление механического фосфена), но для его возникновения необходимы механические стимулы мощностью более 10"4 Вт. Следовательно, разница между механическим (неадекватным) и световым (адекватным) пороговыми раздражителями для органа зрения человека достигает 13—14 порядков. Для механорецепторов, напротив, механический стимул является адекватным, а световой — неадекватным, на который они вообще не реагируют. Значительная разница в чувствительности к адекватным и неадекватным раздражителям свойственна рецепторам всех органов чувств*. Им принадлежит важнейшая роль в получении информации о внешней среде. Именно рецепторы сенсорных систем предназначены в организме для восприятия тех изменений окружающей среды, в реакциях на которые он нуждается. В соответствии с модальностью адекватного раздражителя разнообразные рецепторные аппараты подразделяются на фоторецепторы, механорецепторы, хеморецепторы (химиорецепторы), терморецепторы, осморецепторы и т. п. Фоторецепторы обеспечивают восприятие света. У высших животных они сосредоточены в сетчатой оболочке (сетчатке) глаза. Химиорецепторы воспринимают изменения химических свойств среды. Ого разнообразнее фоторецепторов. К ним относятся обонятельные и вкусовые рецепторы, а также рецепторные аппараты внутренних органов (интероцепторы). Еще более разнообразны механорецепторы. На механические стимулы реагируют слуховые рецепторы, рецепторы органа восприятия гравитации — отолитового аппарата, рецепторы угловых ускорений — рецепторные аппараты полукружных каналов, рецепторы осязания, рецепторы мышц, сухожилий, суставов костей, прессорецепторы (барорецепторы) сердечнососудистой системы и других механорецепторы внутренней среды организма. Терморецепторы воспринимают изменения температуры среды, окружающей их. Они расположены в коже, внутренних органах и промежуточном мозге. Осморецепторы реагируют на изменения осмотического давления, будучи сосредоточены в головном мозге, внутренних органах и тканях организма. Приведенный неполный перечень основных типов рецепторных аппаратов, присутствующих в большом количестве во всех органах и тканях, позволяет сформулировать локализационный принцип классификации рецепторов, согласно которому их подразделяют на экстероцепторы,, обращенные во внешнюю среду, и интероцепторы, информирующие о процессах во внутренней среде организма. Они различаются не только топографически, но и по биофизическим свойствам. У экстероцепторов в большей степени выражена специализация — высокая избирательная чувствительность к адекватным раздражителям. Обладая чрезвычайно высокой чувствительностью к адекватному стимулу, экстероцептор может реагировать и на интенсивные неадекватные раздражители. Однако из-за большой разницы в порогах адекватных и неадекватных стимулов большинство экстероцепторов принято считать мономодальными рецепторными аппаратами, т. е. приспособленными к восприятию агентов одной модальности. Чувствительностью к неадекватным стимулам в этом случае пренебрегают как бесконечно малой величиной. Избирательная чувствительность рецепторов к адекватным раздражителям, а также степень выраженности этого свойства у тех или иных рецепторных аппаратов обусловлены прежде всего их структурными особенностями. Формирование рецепторных структур происходит в ходе преобразования периферического отростка (дендрита) биполярного (или псевдоуниполярного) нейрона и окружающих его тканей. Отросток делится на многочисленные концевые веточки (нервные терминале), открытые воздействию раздражителей (рис. 5.1). Такая организация характерна не только для начального этапа развития рецепторных аппаратов, но и для многих уже сформировавшихся рецепторов. Они называются свободными нервными окончаниями (СНО), поскольку нервные терминали непосредственно контактируют с стимулами. Схема рецепторного акта: I этап — специфическое взаимодействие раздражителя с рецептирующим субстратом рецептора; II этап — образование РП в месте взаимодействия стимула с рецептором (следствие изменения проницаемости плазмолеммы рецептора для ионов); Ш этап — генерация ПД, протекающая по-разному в рецепторных аппаратах разных типов: А — в первично-чувствующих рецепторах, а также в свободных нервных окончаниях и инкапсулированных нервных тельцах ПД возникает вследствие электротонического распространения РП на возбудимые участки плазмолеммы рецепторной клетки; Б — во вторично-чувствующих рецепторах третий этап включает следующие звенья: 1) электротоническое распространение РП по плазмолемме специальной клетки от места взаимодействия рецептора со стимулом к пресинаптической мембране; 2) выделение медиатора пресинаптическими структурами специальной клетки; 3) возникновение ГП на субсинаптической мембране концевой веточки чувствительного нервного волокна; 4) генерация ПД возбудимыми участками постсинаптической мембраны этого волокна, являющегося периферическим отростком чувствительного нейрона. Потенциалы действия, образовавшись в любом из рецепторных аппаратов в той точке афферентного нервного волокна, где оно обладает возбудимостью (т. е. потенциал зависимыми ионными каналами в аксолемме для входящего тока), устремляются без декремента в центральную нервную систему. Вопрос №29 Сигналы одной модальности могут различаться по силе (точнее – по интенсивности). В какой же характеристике потенциалов действия отображаются эти различия? Нетрудно понять, что в соответствии с законом«всё или ничего» все потенциалы действия в данном нервном волокне одинаковы, поэтому величина (амплитуда) и форма ПД не могут служить сигнальными признаками для различения сильных и слабых раздражителей. Эксперименты показали, что от интенсивности раздражителя зависит частота следования потенциалов действия в нервном волокне, отходящем от рецептора. Чем сильнее раздражитель, тем короче интервалы между потенциалами действия, и тем выше частота следования ПД. Серии потенциалов действия, возникающие при воздействии раздражителей большой (А) и малой (Б) интенсивностью Очень важно, что зависимость следования ПД от интенсивности раздражителя почти всегда нелинейная, то есть между частотой интенсивностью нет прямой пропорциональности. Легко понять, что так и должно быть, потому что интенсивность большинства раздражителей может меняться в очень широких пределах. Например, интенсивность самого громкого звука, ещё не повреждающего орган слуха, больше интенсивности самого тихого (порогового) звука в 10-14 раз! Ясно, что частота нервных импульсов (потенциалов действия) не может измениться в такое колоссальное число раз. Между частотой и интенсивностью должна существовать нелинейная функциональная зависимость, при которой интервал частот сжат во много раз по сравнению с интервалом интенсивностей. Такую функцию так и называют – функция сжатия. Легко видеть, что логарифмическая функция – это очень эффективная функция сжатия. Например, если интенсивность раздражителя возрастёт в 10 раз(колоссальное число!), частота ПД увеличится только на 10k единиц . Так как коэффициент k обычно не очень велик, изменение частоты составит десятки, максимум – сотни герц, что очень мало по сравнению с изменением интенсивности. Другое важное свойство логарифмической функции легко получить, если взять производную : dν/dI = k(lgI - lgI0)΄ = k.(1/I) или dν = k(dI/I). Отсюда видно, что абсолютное изменение частоты пропорционально относительному изменению интенсивности. Но именно такое соотношение гарантирует наиболее целесообразную точность восприятия интенсивности: при больших интенсивностях нет надобности оценивать интенсивность с малой абсолютной ошибкой. При оценке интенсивности раздражителя практически значимы не абсолютные, а относительные величины; именно это и обеспечивает логарифмическая функция. Другим вариантом функции сжатия может быть степенная зависимость: то есть опять таки изменение частоты много меньше изменения интенсивности. Надо заметить, что из-за большой сложности биофизических процессов в сенсорных системах никакая простая математическая функция не может в точности отобразить связь частоты нервных импульсов с интенсивностью раздражителя. Особенно большие отклонения наблюдаются при очень малых или при очень больших интенсивностях. Однако, в области средних интенсивностей (которые на практике встречаются чаще всего) логарифмическая или степенная функции достаточно хорошо отображают результаты, получаемые в эксперименте или при клиническом обследовании. Другой способ получения информации об интенсивности раздражителя связан с тем, что почти всегда эта информация передаётся не от одного изолированного рецептора, а от большого их числа по многим волокнам. Порог возбуждения у разных рецепторов различен, поэтому чем больше интенсивность раздражителя, тем больше рецепторов участвует в передаче сигнала, и тем больше клеток в нервных центрах будет возбуждено. Связь между интенсивностью раздражителя и возбуждением нервных центров тоже нелинейная; есть данные, что здесь лучше подходит степенная функция. Однако, этот вопрос пока недостаточно изучен. Кроме интенсивности раздражители одной модальности различаются по качественным признакам. Например, свет от источника может иметь разный цвет; пища может быть разного вкуса и т.п. Одним из способов различения качественных признаков является специализация рецепторных клеток. Например, на поверхности языка находятся четыре типа вкусовых рецепторов, реагирующих соответственно на сладкое, кислое, горькое и солёное. Всё разнообразие вкусовых ощущений возникает в результате различных сочетаний сигналов, поступающих в ЦНС от этих четырёх видоврецепторов. Вопрос №30 |
