Самолечение, доступность
Хорошая растворимость в биожидкостях
Немедицинское применение
Большая поверхность всасывания слизистой
Небрежное хранение в быту
При ХТС-скрининге на вещества основного характера на пластинке не получено окрашенных пятен при детектировании раствором хлорида железа (III). Какие группы лекарственных соединений можно исключить из дальнейшего исследования:
Производные тропана
Производные пиразолона
Производные хинолина
Производные фенотиазина
Производные изохинолина
На какие вещества следует проводить основное исследование, если в условиях ХТС-скрининга получились окрашенные пятна при обработке пластинки реактивом Марки:
Морфин
Пахикарпин
Кодеин
Скополамин
Во внутренних органах эфедрин:
Разрушается быстро
Способен сохраняться в трупе после смерти до 3 недель и более
Может сохраняться в биологическом материале животного происхождения до 2 лет
Данные противоречивы
Противостоит гниению до 3–3,5 месяца
Реактив Миллона имеет следующий состав:
Раствор ацетата ртути в азотистой кислоте
Раствор нитрата серебра в азотной кислоте
Раствор нитрата ртути в серной кислоте
Раствор нитрата ртути в азотной кислоте
Количественное определение салициловой кислоты проводят:
Алкалиметрией
Ацидиметрией
Броматометрией
Йодометрией
Эффектом реакции салициловой кислоты с хлоридом железа является:
Осадок сине-фиолетового цвета
Сине-фиолетовое окрашивание
Сине-зеленое окрашивание
Красно-кирпичное окрашивание
Экстракцию салициловой кислоты хлороформом из кислых растворов проводят:
1 % раствором гидроксида натрия
1 % раствором ацетата натрия
1 % раствором карбоната натрия
Реакция бромирования салициловой кислоты имеет:
Только отрицательное значение
Только положительное значение
Не используется для качественного обнаружения кислоты
В трупном материале барбитураты обнаруживают в течение:
Нескольких часов
Нескольких дней
Нескольких месяцев
Нескольких лет
При целенаправленном исследовании барбитуратов частными методами изолирования являются:
Васильевой
П. Валова
Поповой
Стаса-Отто
Для качественного обнаружения производных фенотиазина используют реактивы:
Эрдмана
Фреде
Манделина
Марки
Количественно производные фенотиазина определяют фотоэлектроколориметрически по реакции с:
Фосфорномолибденовой кислотой
Концентрированной азотной
Хлоридом железа
Концентрированной серной кислотой
При химико-токсикологическом анализе анальгин качественно обнаруживают реакциями с:
Раствором нитрата ртути в азотной кислоте
Раствором KIO3 в кислой среде
Раствором нитрита натрия в серной кислоте
Раствором a – нафтиламина
Раствором резорцина в конц. H2SO4
Эффектом реакции образования нитрозоантипирина является:
Кроваво-красное окрашивание
Зеленый осадок
Сине-фиолетовое окрашивание
Желтое окрашивание
При тяжелой форме отравления производными пиразолона моча окрашивается в:
Лиловый цвет
Красно-бурый цвет
Желто-зеленый цвет
При изолировании производных пиразолона главная их часть экстрагируется хлороформом из:
Кислого раствора
Щелочной раствора
Нейтрального раствора
Фосфорная кислота является продуктом гидролиза:
Карбофоса
Метафоса
Фосфамида
Хлорофоса
Дихлорацетальдегид является продуктом метаболизма:
Фосфамида
Метафоса
Хлорофоса
Дихлофоса
Диметилтиофосфорная кислота образуется в процессе биотрансформации:
Метафоса
Фоксима
Байтекса
Сумитиона
Изолирование хлорофоса возможно:
Перегонкой с водяным паром
Сублимацией в вакууме
Жидкостной экстракцией
Минерализацией
В качестве реактива в реакции Фудживара служит:
Нитропруссид натрия
Пиридин в щелочной среде
Хлорид железа в растворе серной кислоты
Резорцин в растворе натрия карбоната
Реакцией Фудживара качественно обнаруживают:
Кетонную группу в структурах молекул
Гидроксильную группу в структурах молекул
Нитрогруппу в структурах молекул
Атом хлора в структурах молекул
Качественная реакция хлорофоса с ортотолуидином в H2O2 имеет:
Положительное химико-токсикологическое значение
Отрицательное химико-токсикологическое значение
Метафос легко гидролизуется:
В щелочной среде
В кислой среде
Устойчив к действию кислот и щелочей
Впервые ФОС были синтезированы:
Тенаром
Арбузовым
Шееле
Паранитрофенол является продуктом гидролиза:
Карбофоса
Хлорофоса
Метафоса
Тиофоса
Особенностями неорганических пестицидов являются:
Малый расход на единицу обрабатываемой площади
Отсутствие избирательности действия
Высокая дозировка
Стойкость во внешней среде (природе)
Небольшая персистентность и разложение с образованием продуктов, не токсичных для человека и животных
Отличительными особенностями группы ФОС являются:
Небольшая персистентность
Отсутствие избирательности действия
Малый расход на единицу обрабатываемой площади
Отсутствие способности кумулироваться
Высокая дозировка
Стойкость во внешней среде (природе)
При изолировании методами Стаса-Отто или Васильевой хлорофос находится:
В кислом извлечении
В щелочном извлечении
Отличительной реакцией дихлофоса от хлорофоса является реакция:
Фудживара
С ортотолуидином в H2O2 и NaOH
С резорцином в растворе К2СО3
2,4-динитрофенилгидразином
Количественное определение карбофоса методом фотоэлектроколориметрии проводят по реакцию с:
Раствором бромтимолового синего
Диазотированной сульфаниловой кислотой
Спиртовым раствором йодмонохлорида
Раствором сульфата меди
Для определения пестицидов в природных водах, почвах, моче используют:
Перегонку с водяным паром
Сублимацию в вакууме
Жидкостную экстракцию
Твердофазную экстракцию
Для изолирования металлоорганических пестицидов можно использовать методы:
Твердофазную экстракцию
Жидкостную экстракцию
Минерализацию
Сублимацию в вакууме
Перегонку с водяным паром
В зависимости от назначения пестициды делятся на:
Фунгициды
Инсектициды
Зооциды
Фумиганты
Акарициды
Для высоко токсичных пестицидов ЛД50 составляет:
До 50 мг/кг живого веса животного
50—200 мг/кг
200—1000 мг/кг
Выше 1000 мг/кг
При исследовании плазмы крови на активность холинэстеразы желтая окраска индикатора указывает на:
Отсутствие ФОС
Отравление ФОС
При определении активности холинэстеразы окраска индикатора сохраняется, когда:
Ацетилхолин гидролизуется
Ацетилхолин не гидролизуется
Изолирование карбарила из биологического материала производится:
Хлороформом
Эфиром
Этанолом
Бензолом
Фотоэлектрометрию карбарила проводят по реакции с:
Купробромидом натрия
Хлоридом железа
Сульфаниловой кислотой
Нитритом натрия
К пестицидам, ингибирующим ацетилхолинэстеразу, фермента, ответственного за разрушение и прекращение биологической активности медиатора ацетилхолина относят:
Хлорорганические соединения
ФОС
Нитросоединения
Эфиры карбаминовой кислоты
Производные бипиридила
Основным методом изолирования пестицидов является:
Минерализация
Жидкостная экстракция
Твердофазная экстракция
Перегонка с водяным паром
Для мало токсичных пестицидов ЛД50 составляет:
Выше 1000 мг/кг
200—1000 мг/кг
50—200 мг/кг
До 50 мг/кг живого веса животного
Персистентность вещества – это:
Способность выделяться организмом
Способность продолжительно сохраняться во внешней среде
Способность накапливать в живом организме
Способность подвергаться различным неблагоприятным условиям
В гидроксамовой реакции красно-фиолетовое окрашивание указывает на:
На отсутствие сложноэфирной связи
Наличие сложноэфирной связи
Выберите правильную структуру карбарила:
-

|
Бензил
Фенил
α-Нафтил
-Нафтил
|
Выберите правильную химическую структуру ДДТ:
А. 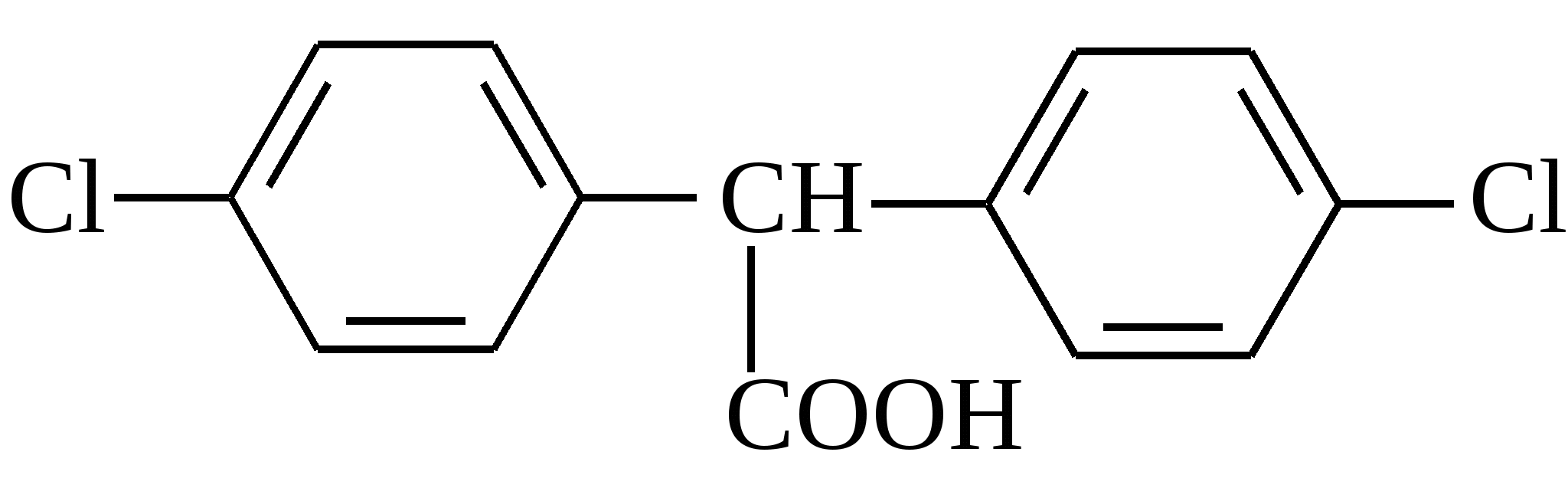 В. В. 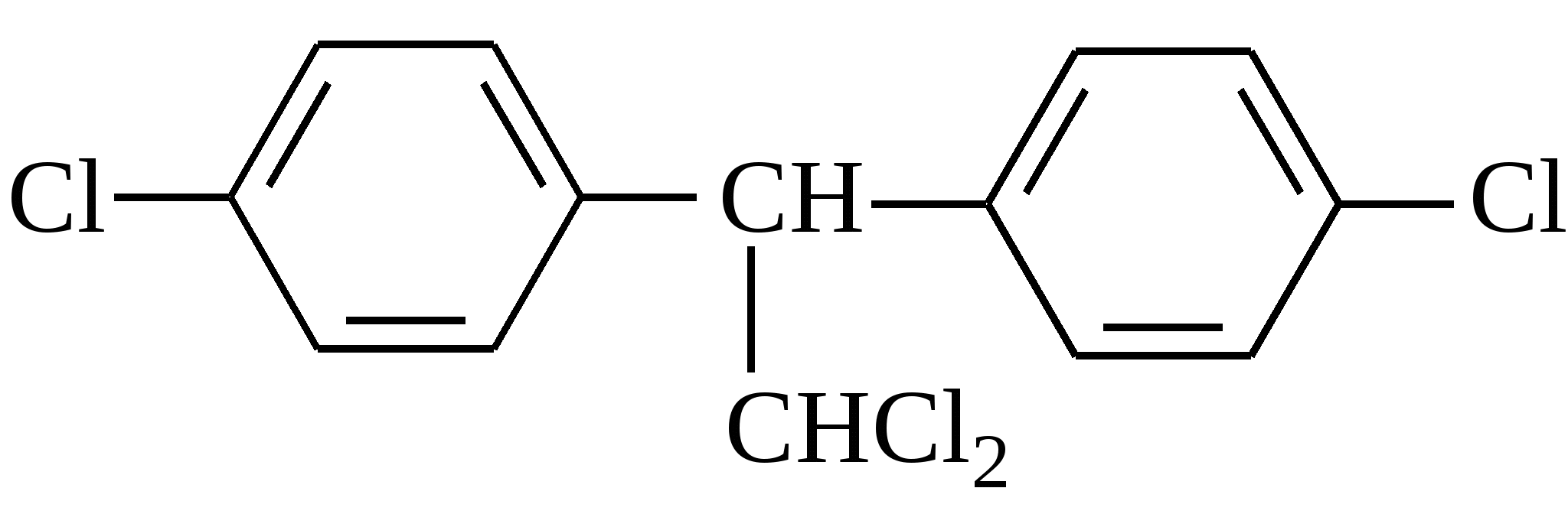
Б. 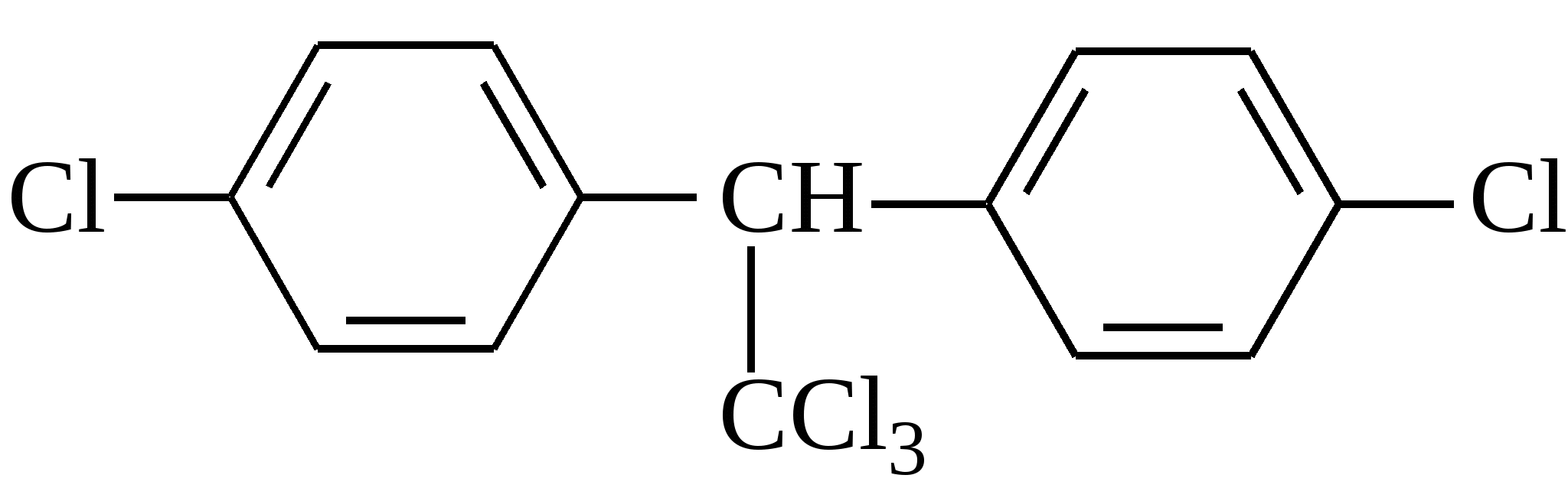 Г. Г. 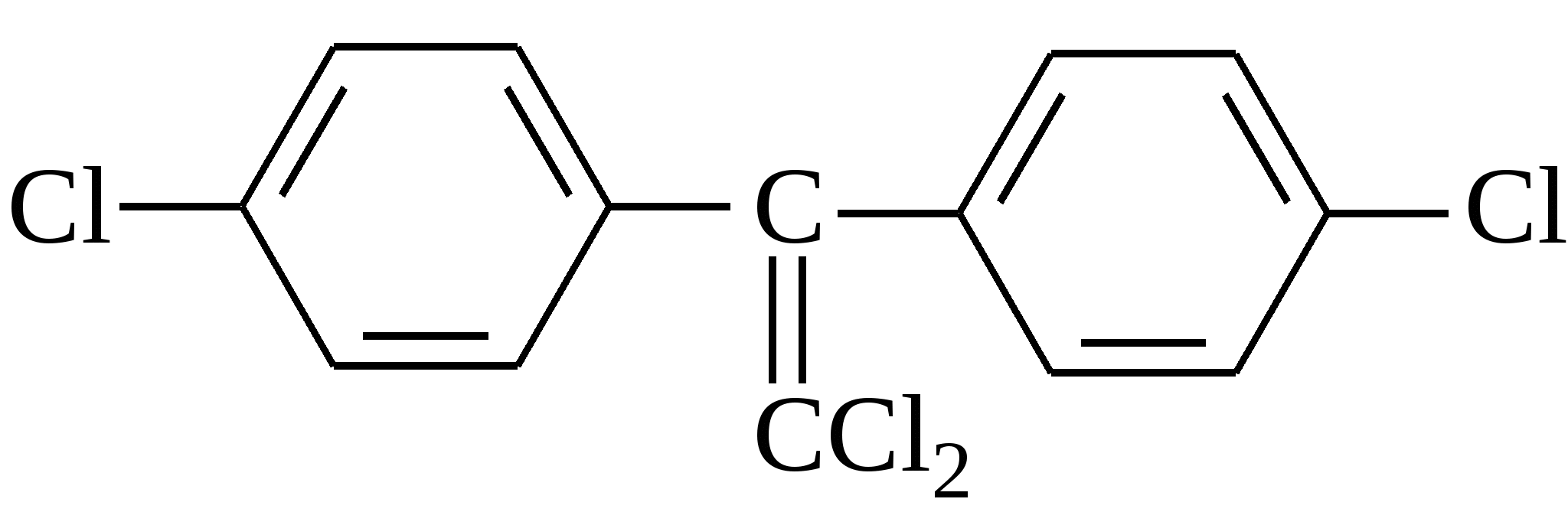
Исходным продуктом для получения ДДТ является:
Дихлорацетальдегид
Хлороформ
Хлораль
Гексахлорцеклогексан
Бензол
Конечным продуктом превращения ДДТ в организме является:
Дихлорфенилдихлорэтилен
Дихлордифенилуксусная кислота
Дихлорфенилоксиуксусная кислота
Дихлорфенилтрихлорэтан
При отравлении пентахлорпропаном основные симптомом отравления является:
Судорожное действие
Наркотическое действие
Раздражающее действие
Поражение паренхиматозных органов
Эффектом реакции нитрования молекулы ДДТ является:
Белый осадок
Сине-фиолетовое окрашивание
Красно-бурое окрашивание
Желто-оранжевое окрашивание
При химико-токсикологическом исследовании изолирование гекасахлорциклогексана проводят:
Экстракцией полярными растворителями
Экстракцией водой в сочетании с диализом
Дистилляцией с водяным паром
Минерализацией
В состав реактива Давидова—Радомского входят:
Метилэтиламин
Диэтаноламина
Гидроксид калия
Нитрат натрия
Метанол
Эффектом реакции гептахлора с реактивом Давидова—Радомского является:
Розовое окрашивание
Желтый осадок
Красно-бурое окрашивание
Фиолетово-сиреневого окрашивание
Качественная реакция гептахлора с реактивом Давидова—Радомского:
Специфична
Неспецифична
По химической структуре ДДТ представляет собой:
4-хлорфенил-2,2,2-трихлорэтан
1,1-ди(4-хлорфенил)-2,2-дихлорэтилен
1,2-ди(4-хлорфенил)-2,2-дихлорэтан
1,1-ди(4-хлорфенил)-2,2,2-трихлорэтан
Для изолирования ДДТ из внутренних органов трупа и выделений человека в качестве растворителя используют:
Хлороформ
Этанол
Эфир
Бензол
Продуктом реакции отщепления хлороводорода от молекулы ДДТ является:
А. 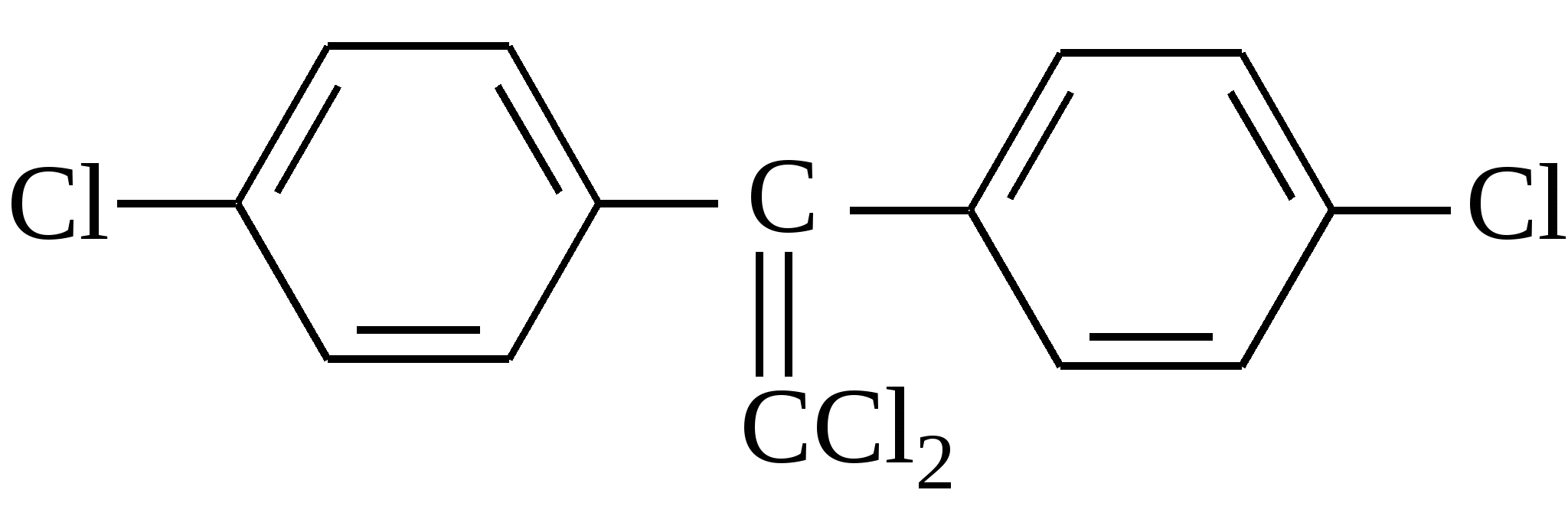 В. В. 
Б. 
При отравлении пропиленхлоридом основным симптомом отравления является:
Раздражающее действие
Наркотическое действие
Судорожное действие
Поражение паренхиматозных органов
Колориметрическое определение ДДТ проводят после реакции:
С этилатом натрия
С нитратом серебра
Нитрования
Гидролиза
Для определения ГХЦГ в крови, моче и каловых массах проводят экстракцию пестицида из объекта исследования:
Эфиром
Спиртом
Бензолом
Хлороформом
Гексаном
При химико-токсикологическом анализе изолирование гептахлора из объектов исследования проводят:
Экстракцией органическим растворителем
Дистилляцией водой с последующим диализом
Дистилляцией с водяным паром
Минерализацией
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-в, 2-в, 3-б, 4-а)
Название метода
|
Назначение метода
|
Стаса-Отто
Васильевой
Крамаренко
Валова
|
Частный для изолирования барбитуратов
Частный для изолирования алкалоидов
Общий для изолирования «нелетучих» ядов
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-в, 2-а, 3-б)
Метод изолирования
|
Экстрагент
|
Частный для алкалоидов
Частный для барбитуратов
Общий для «нелетучих» ядов
|
Подщелоченная вода
Вода, подкисленная щавелевой кислотой
Вода, подкисленная серной кислотой
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-б, 2-а, 3-г)
Метод изолирования
|
Время настаивания с полярным растворителем
|
Водой подкисленной щавелевой кислотой
Водой, подкисленной серной кислотой
Спиртом, подкисленным щавелевой кислотой
|
1 час
2 часа
3 часа
1 сутки
3 суток
|
Установите соответствие. Экстрагирование органическим растворителем на II этапе изолирования (по общим методам): (1-б, 2-в)
Соединения
|
рН среды
|
Барбитураты
Алкалоиды и синтетические азотсодержащие вещества слабоосновного характера
|
7
1-2
10
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-б, 2-а, 3-в)
Реакция обнаружения хинина
|
Эффект реакции
|
С раствором серной кислоты
Образование таллейохина
Образования эритрохинина
|
Ярко-зеленое окрашивание
Голубая флуоресценция
Розовое окрашивание
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-б, 2-в, 3-а)
Алкалоид
|
Растение
|
Пахикарпин
Анабазин
Никотин
|
Табак
Софора толстоплодная
Ежовник безлистный
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-в, 2-а, 3-б)
Алкалоид
|
Растение
|
Атропин
Скополамин
Кокаин
|
Белена
Листья кока
Корень красавки
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-а, 2-г, 3-б, 4-в)
Название реактива для реакций окрашивания
|
Химический состав:
конц.H2SO4, содержащая
|
Марки
Фреде
Манделина
Эрдмана
|
Формальдегид
Ванадиевую кислоту
Азотную кислоту
Модибденовую кислоту
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-б, 2-а, в)
Группы веществ
|
Оптимальный экстрагент на II этапе изолирования
|
Барбитураты
Алкалоиды
|
Хлороформ
Эфир
Дихлорэтан
|
УСТАНОВИТЕ СООТВЕТСТВИЕ (1-а, 2-б, 3-в)
Вещество
|
Эффект реакции с реактивом Марки
|
Морфин
Героин
Наркотин
|
Фиолетовое
Красное → фиолетовое
Фиолетовое → зеленое →желтое
| |
 Скачать 0.68 Mb.
Скачать 0.68 Mb. В.
В. 
 Г.
Г. 
 В.
В. 


