Вопросы к зачету Основы биохимии и молекулярной биологии
 Скачать 5.89 Mb. Скачать 5.89 Mb.
|
1 2 С Рисунок 9.1. Схема строения митохондрии. 9 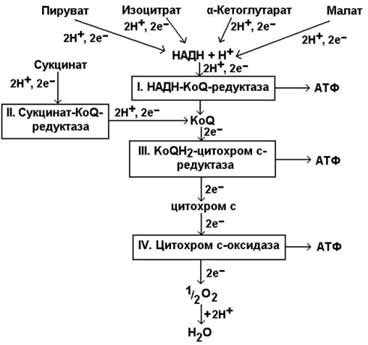 .1.2. Дыхательная цепь – последовательная цепь ферментов, осуществляющая перенос ионов водорода и электронов от окисляемых субстратов к молекулярному кислороду – конечному акцептору водорода. В ходе этих реакций выделение энергии происходит постепенно, небольшими порциями, и она может быть аккумулирована в форме АТФ. Локализация ферментов дыхательной цепи – внутренняя митохондриальная мембрана. .1.2. Дыхательная цепь – последовательная цепь ферментов, осуществляющая перенос ионов водорода и электронов от окисляемых субстратов к молекулярному кислороду – конечному акцептору водорода. В ходе этих реакций выделение энергии происходит постепенно, небольшими порциями, и она может быть аккумулирована в форме АТФ. Локализация ферментов дыхательной цепи – внутренняя митохондриальная мембрана. Дыхательная цепь включает четыре мультиферментных комплекса (рисунок 9.2). Рисунок 9.2. Ферментные комплексы дыхательной цепи (обозначены участки сопряжения окисления и фосфорилирования): I. НАДН-KoQ-редуктаза (содержит промежуточные акцепторы водорода: флавинмононуклеотид и железосерные белки). II. Сукцинат-KoQ-редуктаза (содержит промежуточные акцепторы водорода: ФАД и железосерные белки). III. KoQН2-цитохром с-редуктаза (содержит акцепторы электронов: цитохромы b и с1, железосерные белки). IV. Цитохром с-оксидаза (содержит акцепторы электронов: цитохромы а и а3, ионы меди Cu2+). 9.1.3. В качестве промежуточных переносчиков электронов выступают убихинон (коэнзим Q) и цитохром с. Убихинон (KoQ) – жирорастворимое витаминоподобное вещество, способен легко диффундировать в гидрофобной фазе внутренней мембраны митохондрий. Биологическая роль коэнзима Q – перенос электронов в дыхательной цепи от флавопротеинов (комплексы I и II) к цитохромам (комплекс III). Цитохром с – сложный белок, хромопротеин, простетическая группа которого – гем – содержит железо с переменной валентностью (Fe3+ в окисленной форме и Fe2+ в восстановленной форме). Цитохром с является водорастворимым соединением и располагается на периферии внутренней митохондриальной мембраны в гидрофильной фазе. Биологическая роль цитохрома с – перенос электронов в дыхательной цепи от комплекса III к комплексу IV. 9.1.4. Промежуточные переносчики электронов в дыхательной цепи расположены в соответствии с их окислительно-восстановительными потенциалами. В этой последовательности способность отдавать электроны (окисляться) убывает, а способность присоединять электроны (восстанавливаться) возрастает. Наибольшей способности отдавать электроны обладает НАДН, наибольшей способностью присоединять электроны – молекулярный кислород. На рисунке 9.3 представлено строение реакционноспособного участка некоторых промежуточных переносчиков протонов и электронов в окисленной и восстановленной форме и их взаимопревращение. Р 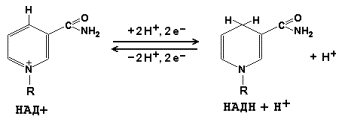 исунок 9.3. Взаимопревращения окисленных и восстановленных форм промежуточных переносчиков электронов и протонов. исунок 9.3. Взаимопревращения окисленных и восстановленных форм промежуточных переносчиков электронов и протонов.9 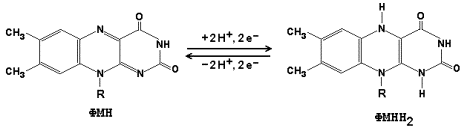 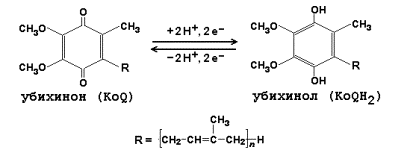 .1.5. Механизм синтеза АТФ описывает хемиосмотическая теория (автор - П. Митчелл). Согласно этой теории, компоненты дыхательной цепи, расположенные во внутренней митохондриальной мембране, в ходе переноса электронов могут «захватывать» протоны из матрикса митохондрий и передавать их в межмембранное пространство. При этом наружная поверхность внутренней мембраны приобретает положительный заряд, а внутренняя – отрицательный, т.е. создаётся градиент концентрации протонов с более кислым значением рН снаружи. Так возникает трансмембранный потенциал (ΔµН+). Существует три участка дыхательной цепи, на которых он образуется. Эти участки соответствуют I, III и IV комплексам цепи переноса электронов (рисунок 9.4). .1.5. Механизм синтеза АТФ описывает хемиосмотическая теория (автор - П. Митчелл). Согласно этой теории, компоненты дыхательной цепи, расположенные во внутренней митохондриальной мембране, в ходе переноса электронов могут «захватывать» протоны из матрикса митохондрий и передавать их в межмембранное пространство. При этом наружная поверхность внутренней мембраны приобретает положительный заряд, а внутренняя – отрицательный, т.е. создаётся градиент концентрации протонов с более кислым значением рН снаружи. Так возникает трансмембранный потенциал (ΔµН+). Существует три участка дыхательной цепи, на которых он образуется. Эти участки соответствуют I, III и IV комплексам цепи переноса электронов (рисунок 9.4).Р 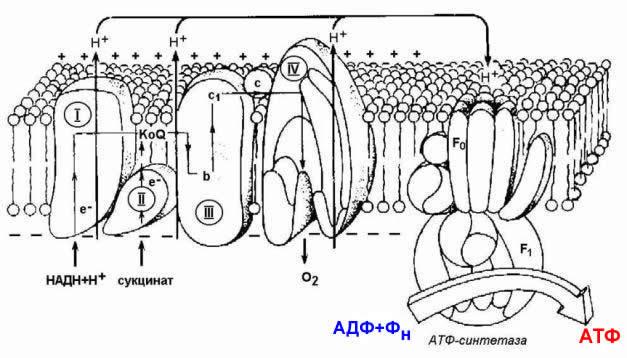 исунок 9.4. Расположение ферментов дыхательной цепи и АТФ-синтетазы во внутренней мембране митохондрий. исунок 9.4. Расположение ферментов дыхательной цепи и АТФ-синтетазы во внутренней мембране митохондрий.Протоны, выведенные в межмембранное пространство за счёт энергии переноса электронов, снова переходят в митохондриальный матрикс. Этот процесс осуществляется ферментом Н+-зависимой АТФ-синтетазой (Н+-АТФ-азой). Фермент состоит из двух частей (см. рисунок 9.4): водорастворимой каталитической части (F1) и погружённого в мембрану протонного канала (F0). Переход ионов Н+ из области с более высокой в область с более низкой их концентрацией сопровождается выделением свободной энергии, за счёт которой синтезируется АТФ. 9.1.6. Энергия, аккумулированная в форме АТФ, используется в организме для обеспечения разнообразных биохимических и физиологических процессов. Запомните основные примеры использования энергии АТФ: 1) синтез сложных химических веществ из более простых (реакции анаболизма); 2) сокращение мышц (механическая работа); 3) образование трансмембранных биопотенциалов; 4) активный транспорт веществ через биологические мембраны. 1 2 |
