Курсовая работа смох. Введение Основные физикохимические свойства
 Скачать 0.71 Mb. Скачать 0.71 Mb.
|

Содержание Введение………………………………………………………………………..…6 1. Основные физико-химические свойства ………..………………………...7 1.1 Физические свойства ……………………………………………………….7 1.2 Химические свойства …………………………………………...…………..9 1.3 Способы получения…………………………………...……………………12 2. Лабораторный синтез орто-аминофенола………………………...…..….13 2.1 Синтез из о-нитрофенолята натрия…………………………………...…13 2.2 Результаты лабораторных методов………………….…………………..15 2.3 Идентификация целевого продукта……………………………………...16 3. Экологический фактор……………………………………………………...17 4. Применение орто-аминофенола..…………………………………………..18 Заключение…………………………………………………………………...…19 Библиографический список………………………………………………..…20 ВведениеВ данной курсовой работе поставлена цель подробно изучить способы получения орто-аминофенола, а также применение некоторых способов синтеза на практике. Важно подойти к этому вопросу более углубленно, потому что орто-аминофенол применяется, например, в медицине в синтезе лекарственных препаратов, используется для окраски меха и волос, а также в качестве проявителя в фотографии. Поэтому мы рассмотрим все теоретические способы получения орто-аминофенола и разберем практический способ получения в лаборатории. Данная работа основана на следующих теоретических данных: - физико-химические характеристики исходных веществ и методы их исследования; - методика проведения синтеза; - обсуждение результатов. Основные физико-химические свойства.Орто-аминофенол (2-Ами́нофено́л, 2-амино-1-оксибензол) — ароматическое органическое соединение, представитель одноатомных фенолов, в молекуле которого один из атомов водорода, находящийся в орто- положении, замещен на аминогруппу. Имеет химическую формулу C6H7NO. 1.1. Физические свойства. Орто-аминофенол (2-Аминофенол) представляет собой белые кристаллы, превращающиеся на воздухе в коричневые, растворим в воде, спирте, эфире, хлороформе. Таблица 1. Физические свойства Орто-аминофенола
1.2. Химические свойства. Орто-аминофенол(2-аминофенол), как и его изомер 4-аминофенол, обладает проявляющими свойствами, но в отличие от 4-аминофенола, не получил широкого распространения. Использовался в составе некоторых мелкозернистых проявителей. Торговое название — урзол жёлтый Брутто-формула (система Хилла): C6H7ON. Формула в виде текста: H2NC6H4OH. Структурная формула представлена на рисунке 2. 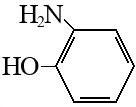 Рисунок 2 – Структурная формула Орто-аминофенола 2-Аминофенол и его изомер 4-аминофенол синтезируются в промышленных масштабах путем восстановления соответствующего нитрофенола водородом в присутствии различных катализаторов. Нитрофенолы также можно восстановить с помощью железа. Соединение имеет внутри- и межмолекулярные водородные связи с участием соседних аминных и гидроксильных групп. В результате 2-аминофенол имеет относительно высокую температуру плавления (174 ° C) по сравнению с другими соединениями аналогичной молекулярной массы (2-метилфенол плавится при 31 ° C). Реакции взаимодействия Взаимодействие фенолов с металлами. 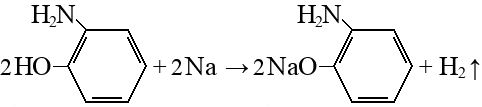 2-орто-аминофенол 2-аминофенолят натрия Взаимодействие с щелочами. 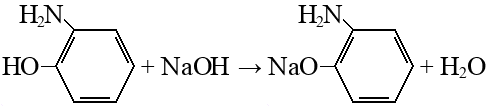 2-орто-аминофенол 2-аминофенолят натрия Получение аммониевых соединений. 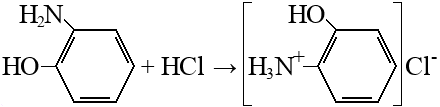 2-орто-аминофенол хлорид (отро-гидроксифенил)аммония Также участвует в реакции горения. Реакция диазотирования. 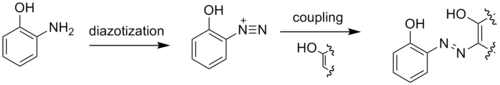  Реакция взаимодействия с железом. 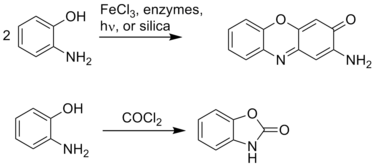 1.3 Способы получения. Существуют 2 промышленных и 1 лабораторный способ получения орто-аминофенола: 2-Аминофенол синтезируется в промышленных масштабах путем восстановления соответствующего нитрофенола водородом в присутствии различных катализаторов. Нитрофенолы также можно восстановить с помощью железа. Синтез из орто-нитрофенолята натрия. 2. Лабораторный синтез орто-аминофенола.2.1. Синтез из орто-нитрофенолята натрия.Сначала 50 г кристаллического сернистого натрия расплавляют в фарфоровой чашке на голом огне. В расплавленную массу при 110—115° С (не выше) постепенно при перемешивании шпателем вносят о-нитрофенолят натрия. Для приготовления о-нитрофенолята натрия 2,9 г чистого едкого натра (или 3,5 г технического) растирают в глубокой фарфоровой ступке и туда же вносят 10 г о-нитрофенола и 5 мл воды. Смесь растирают до образования густой пасты красного-цвета. После внесения всего количества о-нитрофенолята натрия реакционную смесь выдерживают при размешивании в течение 45 мин при 125—130° С. Лабораторная установка получения о-аминофенола 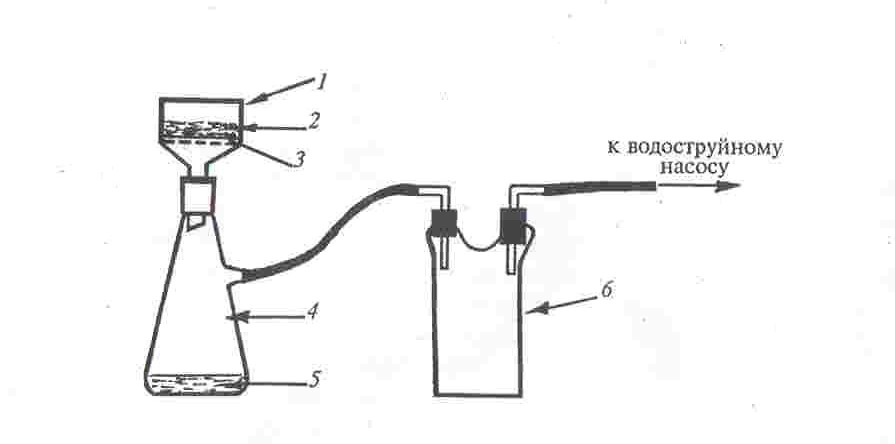 После окончания реакции (конец реакции определяют вливанием капли сплава в воду: полное растворение в воде указывает на конец реакции) нагревание прекращают и сплав выливают в 150 мл воды. Водный раствор фильтруют через складчатый фильтр и в теплый фильтрат (25—30° С) пропускают быстрый ток углекислоты для нейтрализации свободной щелочи и для выделения о-аминофенола. Вскоре начинает выпадать о-аминофенол в виде мелких белых блестящих кристаллов. Пропускание углекислого газа производится под тягой, так как при этом из реакционной смеси выделяется сероводород. Углекислый газ пропускается до тех пор, пока проба жидкости не начнет вспениваться от прибавления к ней небольшого количества раствора бисульфита натрия, необходимого также в среде для того, чтобы воспрепятствовать окислению. Проба с бисульфитом вливается обратно в реакционную массу. После прекращения пропускания углекислоты и охлаждения раствора до комнатной температуры о-аминофенол отсасывают на воронке Бюхнера, промывают 15 мл ледяной воды, к которой прибавлено 2 мл 40%-го раствора бисульфита натрия, затем снова водой (5 мл) и, наконец, этиловым спиртом (5 мл). Кристаллы о-аминофенола отжимают на воронке и высушивают при 100—110° С. Результаты синтеза Выход — 6 г (80%). Тпл чистого о-аминофенола = 174° С. Примечания 1. Весь процесс необходимо закончить в один день. 2. При получении о-нитрофенолята натрия следует надевать очки. 2.2. Результаты лабораторных методов.Был выполнен синтез орто-аминофенол в лабораторных условиях. Первый метод занимает достаточное количество времени и состоит из нескольких стадий, но требует меньшего количества оборудования, чем второй метод. Также в первом методе требуется сравнительно небольшое количество реагентов. Выход по данному методу является средневысоким и составляет 80%. Однако в данном методе необходимо соблюдать условия, такие как необходимость завершения процесса синтеза в один день и наличие очков при синтезе о-нитрофенолята. В итоге был сделан вывод, что метод является выгодным из-за получения большого числа конечного продукта и достаточно меньшей трудоемкости. Однако он требует тщательного контроля за условиями в связи с опасностью используемых реагентов. Было определено, что такой метод подходит для лабораторного синтеза, синтеза органических препаратов, или как синтез промежуточного продукта для препаратов. 2.3 Идентификация целевого продукта. Восстановление нитрозофенолов проводили в течение 50 ч при комнатной температуре при добавлении 3-х-4-х кратного избытка гидразингидрата. Окончание реакции устанавливали по изменению цвета раствора с темно-зеленого на светло-коричневый. Целевые аминофенолы (I-IV) выделяли добавлением твердой углекислоты, выпавшие кристаллы светлобежевого цвета отфильтровывали. Температуры плавления и выходы приведены в таблице. Спектры ЯМР 1 Н регистрировали на приборах Bruker AvanceIII 600 КНЦ СО РАН для растворов соединений в D2O, дейтерохлороформе, дейтероацетоне и дейтеродиметилсульфоксиде с применением ТМС в качестве внутреннего стандарта. ИК-спектры регистрировали с помощью ИК-микроскопа SpecTRA TECH InspectIR на базе ИК Фурьеспектрофотометра Impact 400. Исследуемый образец наносили на позолоченую пластину, раскатывали с помощью роликового ножа, укладывали на столик микроскопа и записывали спектр НПВО. Диапазон волновых чисел 4000–650 см–1, детектор МСТ/А, объектив Si Caplugs, с разрешением 1,928 см–1, количество сканирований 64, ПО OMNIC 5.1 E.S.P. Температуры плавления определяли в открытых капиллярах на приборе ПТП (ТУ 25-11-1144–76). В ЯМР 1 Н спектрах присутствовали все сигналы, подтверждающие строение полученных аминофенолов (I-IV): сигналы алифатических протонов метильной группы кольца в области δ 1,82–2,09 м. д. в виде синглета, триплет метильных (или триплет и квадруплет в случае этильных заместителей) групп сложноэфирного заместителя в области δ 3,35–4,31 (0,74– 1,43) м. д., сигналы ароматических протонов пиридинового заместителя и хим. сдвигом в области δ 7,18– 9,43 м. д., а также видны сигналы протонов аминогруппы в области δ 4,09–4,51 м. д. 3. Экологический фактор. Орто-аминофенол обладает свойствами схожими с N-метил-п-аминофенолом и 2,4-диаминофенолом, токсично воздействуя на кожу. Отмечается, что продукты деструкции биологически разрушаются значительно легче, чем исходные соединения. Скорость окисления зависит от pH среды. Также известно, что настоящие технические условия требуют определения содержания п-аминофенола в воздухе промышленных помещений при санитарном контроле. 4. Применение орто-аминофенола. 2-Аминофенол имеет множество применений. В качестве восстановителя он продается под названиями Atomal и Ortol для проявления черно-белых фотографий. Это полупродукт в синтезе красителей. Он особенно полезен для получения красителей на основе комплексов металлов, диазотированных и связанных с фенолом, нафтолом или другими видами ароматических или резонансных красителей. Металлокомплексные красители с использованием меди или хрома обычно используются для получения матовых цветов. Красители с трехдентатным лигандом полезны, потому что они более стабильны, чем их двух- или монодентатные аналоги. Благодаря смежности амино- и гидроксильных групп 2-аминофенол легко образует гетероциклы. Эти гетероциклы, такие как бензоксазолы, могут быть биологически активными и полезными в фармацевтической промышленности. ЗаключениеВ ходе проделанной работы, был рассмотрены лабораторные и промышленные методы получения орто-аминофенола. Подробно был изучен лабораторный способ синтеза с условиями его проведения. Так как орто-аминофенол мало популярен и применяется в достаточно узких отраслях промышленности и фармацевтической промышленности, известно не так много информации о принятых способах его получения. Существуют экспериментальные способы его синтеза, которые еще не применяются. Орто-аминофенол является промежуточным веществом при получении фармацевтических препаратов и получении красителей, а также при проявлении фотографий. Библиографический списокТимофеев В.С., Серафимов Л.А., Тимошенко А.В. Принципы технологии основного органического и нефтехимического синтеза: учебное пособие. - 3-е изд., перераб. и доп. – М.: Высш. шк. - 2010 - 408 с.; М.: Химия, 1992. – 432 с Практикум по органической химии: Синтез и идентификация органических соединений: учебное пособие для хим. техн. спец. вузов под ред. О.Ф.Гинзбурга, А.А. Петрова. – М.: Высш.шк. 1989. – 318 с Голодников Г.В. Практические работы по органическому синтезу. - Л.: ИЛУ, 1966, стр. 235-236. Синтезы органических препаратов. - Ч. 1.: М., 1949, стр. 82. Синтез перзамещенных аминофенолов, содержащих пиридиновый фрагмент / А. А. Кукушкин [и др.] // Лесной и химический комплексы – проблемы и решения : сб. статей по материалам Всерос. науч.-практ. конф. Красноярск : СибГТУ, 2015. С. 6–7. Получение перзамещенных аминофенолов с бета-пиридиновым фрагментом / А. А. Кукушкин [и др.] // Молодые ученые в решении актуальных проблем науки : Всерос. науч.-практ. конф. студентов, аспирантов и молодых ученых. Красноярск. 2017. Т. 2. Синтез пара-аминофенолов, содержащих альфапиридиновый фрагмент / А. А. Кукушкин [и др.] // Молодые ученые в решении актуальных проблем науки : Всерос. науч.-практ. конф. студентов, аспирантов и молодых ученых. Красноярск. 2017. Т. 2. |

