Контрольная по термодинамике. вариант 01. Задание 1 Расчет параметров и процессов смеси идеальных газов
 Скачать 0.75 Mb. Скачать 0.75 Mb.
|
|
Задание № 1 Расчет параметров и процессов смеси идеальных газов Смесь газов с начальной температурой Т1 = 300 К сжимается от давления p1 = 0,1 МПа до давления p2. Сжатие может происходить по изотерме, по адиабате и по политропе с показателем политропы n. Определить для каждого из трех процессов сжатия конечную температуру Т2 и объем V2 смеси, изменение внутренней энергии U, энтальпии H и энтропии смеси ΔS, а также теплоту Q и работу L. Результаты расчетов занести в таблицу 2 и изобразить процессы сжатия в p-v и T-S – диаграммах. Данные, необходимые для решения задачи, выбрать из таблицы 1. Примечание. Расчет провести, приняв теплоемкость постоянной.
Определим параметры газовой смеси, состав которой задан массовым способом. Выпишем молярные массы компонентов смеси: углекислый газ (СО2) угарный газ (СО) Масса газовой смеси Массовые доли компонентов смеси вычислим по формуле . Газовую постоянную смеси газов определим по формуле где Учитывая, что Кажущуюся молекулярную массу смеси вычислим по формуле По условию задачи теплоемкости компонентов смеси не зависят от температуры. По таблице 3 [4, с. 38] находим мольную изобарную теплоемкость трехатомного газа СО2 и двухатомного газа СO Вычислим массовые изобарные теплоемкости газовой смеси Вычислим массовую изобарную теплоемкость газовой смеси = 951,6 Дж/(кг ∙ К). Из уравнения Майера найдем массовую изохорную теплоемкость газовой смеси Показатель адиабаты газовой смеси Объем газовой смеси в начальном состоянии (точка 1 на рис. 1 и 2) определим из уравнения состояния откуда 1. Рассмотрим изотермический процесс сжатия. Так как Т = const, то Т1 = Т2 = 300 К. Уравнение связи давления и объема газовой смеси в изотермическом процессе имеет вид откуда объем газовой смеси в конечном состоянии Так как в изотермическом процессе Т = const, то изменение внутренней энергии и энтальпии равно нулю, т.е. Изменение энтропии в изотермическом процессе определим по формуле Работу изменения объема в изотермическом процессе определим по формуле  Внешняя работа в изотермическом процессе Знак «–» означает, что внешняя работа затрачивается на сжатие газа. Согласно первому началу термодинамики, количество теплоты 2) Рассмотрим адиабатный процесс сжатия. Уравнение связи температуры и давления в адиабатном процессе имеет вид 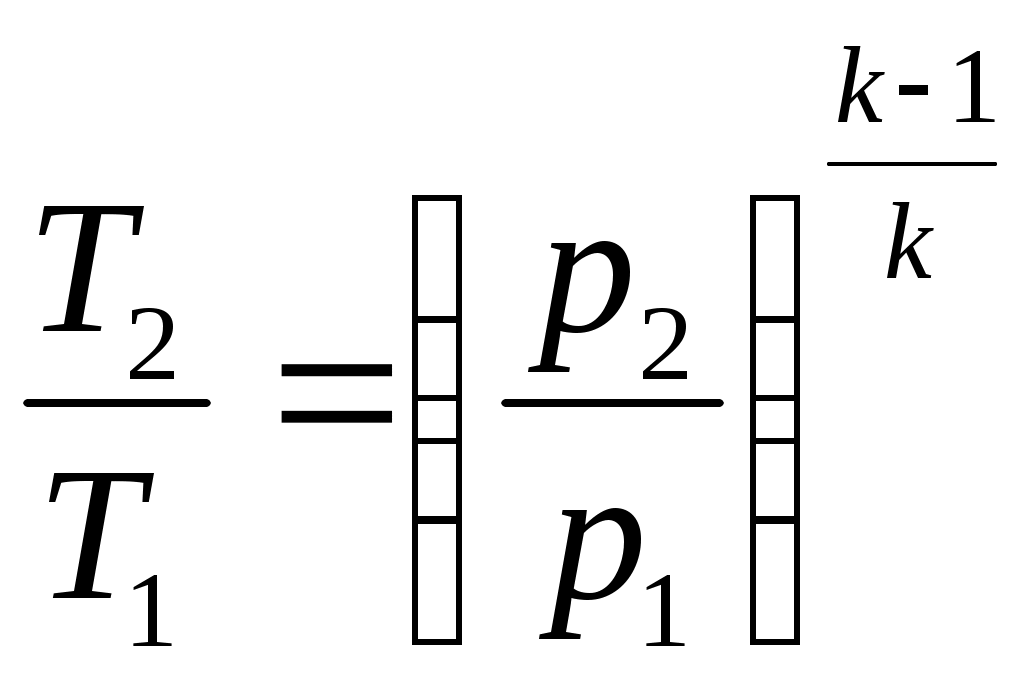 , ,откуда температура газовой смеси в конечном состоянии  . .Уравнение связи давления и объема в адиабатном процессе имеет вид  , ,откуда объем газовой смеси в конечном состоянии  м3. м3.Изменение внутренней энергии Изменение внутренней энтальпии Так как адиабатный процесс протекает без теплообмена с окружающей средой, то количество теплоты в адиабатном процессе Q = 0, изменение энтропии Согласно первому началу термодинамики, количество теплоты откуда работа изменения объема в адиабатном процессе Внешняя работа Знак «–» означает, что внешняя работа затрачивается на сжатие газа. 3) Рассмотрим политропный процесс сжатия. Уравнение связи температуры и давления в политропном процессе имеет вид  , ,откуда температура газовой смеси в конечном состоянии  . .Уравнение связи давления и объема в политропном процессе имеет вид  , ,откуда объем газовой смеси в конечном состоянии  м3. м3.Изменение внутренней энергии Изменение внутренней энтальпии Работа изменения объема в политропном процессе Внешняя работа Удельная теплоемкость политропного процесса Изменение энтропии в политропном процессе Согласно первому началу термодинамики, количество теплоты Результаты расчетов сведем в таблицу 1. Таблица 1
Изображение процессов в pV-и Ts- диаграммах приведено на рис. 1 и 2.  Рис. 1. Изображение процессов сжатия в pV-диаграмме (1 < n < k)  Рис. 2. Изображение процессов сжатия в Ts- диаграмме (1 < n < k) Выводы: 1. Как следует из рис. 1 и результатов расчета, внешняя работа (т.е. работа затрачиваемая на привод компрессора, используемого для сжатия газовой смеси) при одних и тех же начальных параметрах газовой смеси и степени повышения давления p2/p1 будет минимальна в изотермическом процессе (n = 1). C ростом показателя политропы внешняя работа увеличивается. 2. Конечная температура и конечный объем газа увеличиваются с ростом показателя политропы n. 3. В процессе сжатия газовой смеси работа затрачивается. В политропном процессе сжатия (1 < n < k), несмотря на отвод тепла, температура газовой смеси возрастает. Ответ: результаты вычислений сведены в табл. 1. Задание №2. Расчет компрессора. Компрессор, производительностью V1, м3/час, состоящий из m ступеней, сжимает газ от давления р1 до давления р2. Сжатие в ступенях происходит по политропе с показателем n. Промежуточное давление выбрано оптимально, а охлаждение во всех теплообменниках производится до начальной температурыТ1, К. Охлаждающая вода, прокачивающаяся через рубашки цилиндров и теплообменники, нагревается на Δt = 13 °C. Исходные данные для решения задачи приведены в таблице 4. Найти общую мощность, затрачиваемую на сжатие в компрессоре, и расход охлаждающей воды. Сравнить найденную мощность с мощностью, которая затрачивается на сжатие в одноступенчатом компрессоре с процессом с процессом сжатия по политропе с тем же показателем n. Теплоемкость в расчетах считать постоянной. Перед расчетом изобразить принципиальную схему компрессора, а так же процессы сжатия в р-v и Т-s – диаграммах.
Принципиальная схема двухступенчатого компрессора и процессы сжатия вpv- и Ts-диаграммах приведен на рис. 1 и 2. Степень повышения давления в каждой ступени компрессоре будет Давление газа после первой ступени  Рис. 1. Принципиальная схема двухступенчатого компрессора 1 и 2– первая и вторая ступени компрессора, 3 – промежуточный охладитель. Стрелками на схеме показано направление движения охлаждающей воды.  Рис. 2. Процессы сжатия воздуха в двухступенчатом компрессоре Рис. 2. Процессы сжатия воздуха в двухступенчатом компрессоре вpv- и Ts-диаграммах Обозначения: p1, Мощность, затрачиваемая на сжатие газа в одной ступени компрессора,  где Тогда мощность привода двухступенчатого компрессора Теоретическую мощность одноступенчатого компрессора при политропном процессе сжатия определим по формуле 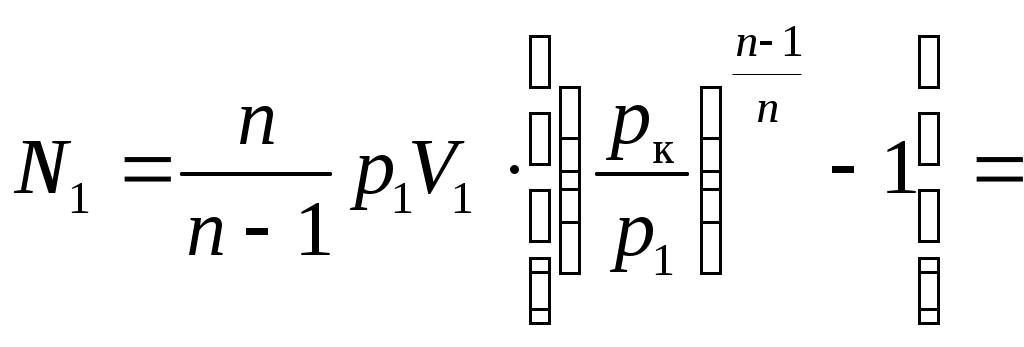  Мощность, затрачиваемая на сжатие газа в одноступенчатом компрессоре, больше мощности, затрачиваемой в двухступенчатом компрессоре, в Таким образом, сжатие в двухступенчатом компрессоре позволяет сократить затраты энергии по сравнению со сжатием в одноступенчатом компрессоре. В многоступенчатом компрессоре теплота отводится в цилиндрах и в промежуточных теплообменниках-холодильниках. Общий расход отведенной теплоты определяется равенством: где Определим газовую постоянную воздуха где Из уравнения состояния определим массовый расход сжимаемого газа Температура воздуха после каждой ступени компрессора: Так как воздух можно считать двухатомным газом, то его показатель адиабаты k= 1,4 . По таблице 3 [4, с. 38] находим мольную теплоемкость двухатомного газа при постоянном давлении Вычислим массовую теплоемкость Используя уравнение Майера, вычислим массовую теплоемкость Массовая теплоемкость политропного процесса Тепловой поток, отводимый в систему охлаждения цилиндров в одной ступени компрессора Охлаждение воздуха в промежуточных охладителях происходит при постоянном давлении, следовательно, тепловой поток, отводимый от воздуха при охлаждении его от температуры Т2 до температуры Т1 в одном промежуточном охладителе, можно определить по формуле Определим суммарный тепловой поток, отводимый в систему охлаждения 3 цилиндров и в 2-ех промежуточных охладителях Расход охлаждающей воды откуда где Выводы: Мощность, затрачиваемая на сжатие газа в одноступенчатом компрессоре, больше мощности, затрачиваемой в двухступенчатом компрессоре, в Таким образом, сжатие в двухступенчатом компрессоре позволяет сократить затраты энергии по сравнению со сжатием в одноступенчатом компрессоре. Ответ: |
