Занятие Система иммунитета Центральные и периферические органы иммунной системы. 2 Иммунопоэз и иммуногенез
 Скачать 2.93 Mb. Скачать 2.93 Mb.
|
|
Приложение 1 Занятие 1. Система иммунитета 1.Центральные и периферические органы иммунной системы. 2 Иммунопоэз и иммуногенез. 3.Роль тимуса в иммунной системе. 4.Понятие о стволовой клетке. 5.Основные клеточные элементы иммунной системы. 6.Стадии развития Т- и В-лимфоцитов. 7.Иммунные процессы в слизистых оболочках. 8.Понятие о дифференцировочных маркерах (CD номенклатура). Анатомия и цитология иммунной системы Органы, клетки и молекулы, осуществляющие обнаружение и удаление чужеродных веществ, составляют иммунную систему, анатомическим синонимом которой является лимфоидная система. Иммунная система (ИС) включает центральные и периферические органы. Органы иммунной системы делятся на центральные, где происходит созревание лимфоцитов и периферические, в которых находятся зрелые лимфоциты. К центральным органам относят красный костный мозг и тимус (вилочковая железа). В центральных органах происходит антигеннезависимая дифференцировка лимфоцитов (иммунопоэз).  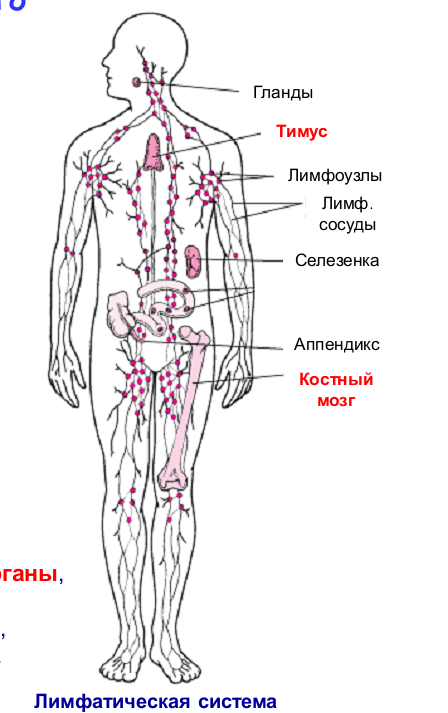 Рис. 1. Лимфоидная система человека Красный костный мозг, расположенный в губчатых костях и эпифизах трубчатых костей, является местом, где формируются все клетки крови (гемопоэз), в том числе и клетки иммунной системы (иммунопоэз). В красном костном мозге присутствуют гемопоэтические стволовые клетки, способные к дифференцировке в различные клеточные элементы, в том числе предшественники миелоидных и лимфоидных клеток. Все клетки ИС за исключением Т-лимфоцитов формируются в красном костном мозге. Здесь происходит селекция и антигеннезависимая дифференцировка В-лимфоцитов. 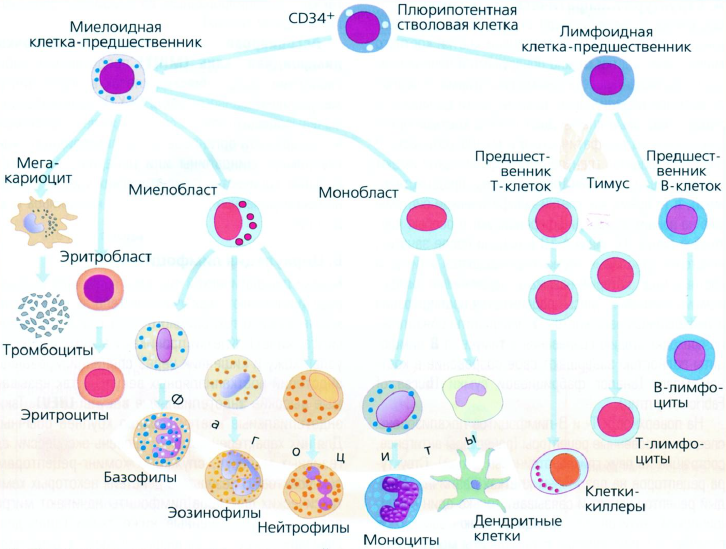 Рис. 2. Схема гемопоэза в красном костном мозге Тимус расположен в переднем верхнем средостении за грудиной. Тимус состоит из двух больших долей, которые фрагментированы на множество долек, разделенных фиброзными перегородками. Эти долькии являются структурными единицами строения тимуса. В каждой дольке четко различимы две гистологические зоны: по периферии — корковая, в центре — медуллярная. Кора содержит большое количество незрелых Т-лимфоцитов (тимоцитов), в медулярной зоне долек имеются плотные образования из скрученных дегенерирующих эпителиальных клеток — тельца Гассаля (тельца вилочковой железы — по новой классификации). Функции тимуса: в тимусе происходит селекция и антигеннезависимая дифференцировка Т-лимфоцитов. Костномозговые клетки-предшественницы Т-лимфоцитов мигрируют в тимус, где созревают, дифференцируются и превращаются в зрелые Т-лимфоциты. Часть созревающих Т-лимфоцитов направлены против собственных антигенов. В период эмбрионального развития в тимусе эти лимфоциты погибают. Тимус вырабатывает ряд гормонов (тимозин, тимопоэтин), которые регулируют дифференцировку и функции зрелых Т-лимфоцитов. Также в процессах селекции и дифференцировки Т-лимфоцитов принимают участие макрофаги, дендритные клетки, эпителиальные клетки. К моменту рождения тимус полностью сформирован. Он густо заселен лимфоцитами в течение всего детства и до момента полового созревания. После пубертатного периода начинается инволюция тимуса, он уменьшается в размерах, сморщивается. Утрата лимфоидных и эпителиальных клеток восполняется развитием жировой ткани. Периферические органы иммунной системы – селезенка, лимфатические узлы, миндалины, аппендикс, лимфоидная ткань, ассоциированная со слизистыми оболочками. В периферических лимфоидных органах происходит антигензависимая дифференцировка лимфоцитов (иммуногенез или иммунный ответ) Лимфоузлы – периферические органы иммунной системы, расположенные по ходу лимфатических сосудов, они задерживают чужеродные антигены, опухолевые клетки и предотвращают их распространение. Строма лимфоузла образована рыхлой соединительной тканью, в его паренхиме различают корковое и мозговое вещество.   В-зона Т-зона 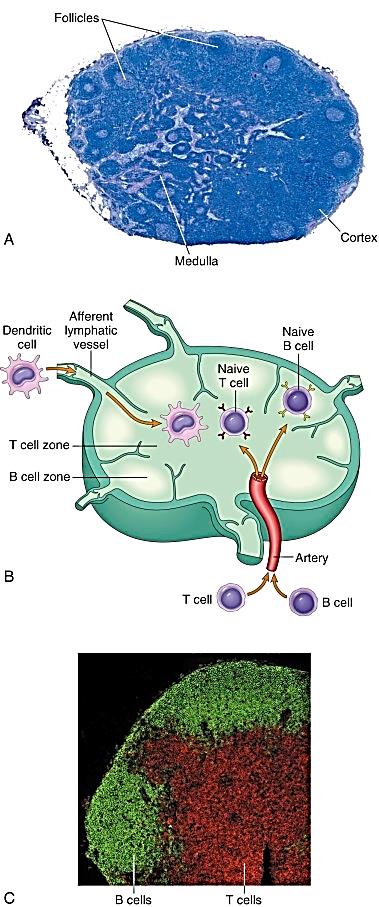 Рис. 3. Строение лимфатического узла Корковое вещество (первичные фолликулы) – В-зависимая зона, здесь происходит пролиферация (размножение) специфических В-лимфоцитов, синтез антител. Т-лимфоциты расположены в паракортикальной – Т-зависимой зоне, являющейся местом образования специфических Т-лимфоцитов. Селезенка – самый крупный лимфоидный орган. Основу селезенки составляет красная пульпа. Лимфоидная ткань селезенки представлена островками белой пульпы, которые разделены на Т- зависимую зону (скопления Т-лимфоцитов вокруг артерий - периартериолярная «муфта»), и В- зависимую зону (область первичного фолликула и герминативного центра). Функции селезенки: Разрушение тромбоцитов, эритроцитов и их фагоцитоз Фильтрация и фагоцитоз микробов Антигензависимая дифференцировка Т- и В- лимфоцитов Антителообразование Задержка и уничтожение антигенов, циркулирующих в крови Обращает на себя внимание преобладание в этом органе В-лимфоцитов над Т-лимфоцитами. Т-клеточный состав селезенки представлен Т-хелперами (CD4+) – 75%, Т- цитотоксическими (CD8+) – 25%. В случае спленэктомии пациенту рекомендована вакцинация от инфекций, вызванных пневмококком, менингококком и гемофильной палочкой.  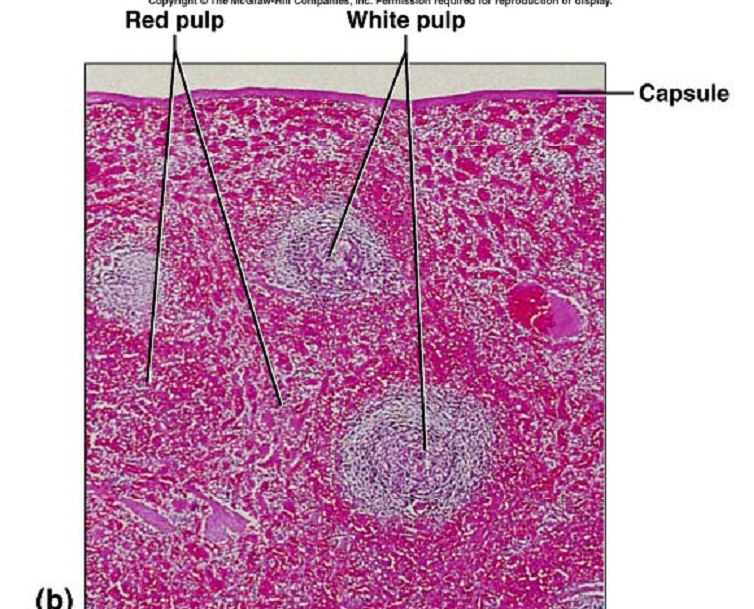 Рис.4. Морфологическое строение селезенки 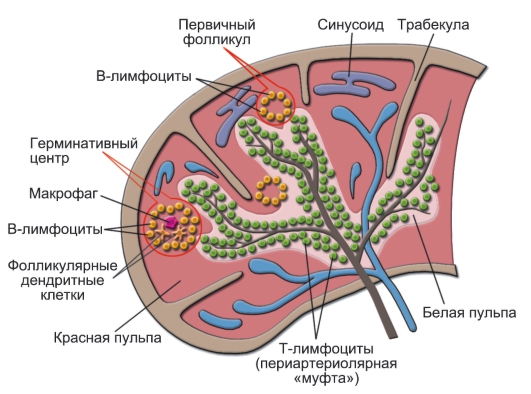 Рис. 5. Строение селезенки человека. Тимусзависимая зона – скопления Т-лимфоцитов вокруг артерий (периартериолярная «муфта»), В-зависимая зона – область первичного фолликула и герминативного центра. . Мукозоассоциированная лимфоидная ткань (МАЛТ) – лимфоидная ткань, ассоциированая со слизистыми оболочками ротовой полости, ЖКТ, респираторного тракта, мочеполовых путей (система местного иммунитета). Состоит из нескольких компонентов: внутриэпителиальные лимфоциты, лимфоциты подслизистого слоя и лимфоидные фолликулы (пейеровы бляшки). Основная функция этих образований: обеспечение иммунного ответа на антигены, проникающие через слизистые покровы и синтез секреторного IgA к этим антигенам. Пейеровы бляшки содержат специализированные М-клетки, транспортирующие антиген с поверхности слизистой в подслизистый слой. Т-клетки находятся в подслизистом слое (lamina propria) и составляют 20-30% пейеровой бляшки, основная масса В-лимфоцитов (50-70%) расположена в В-клеточных фолликулах. 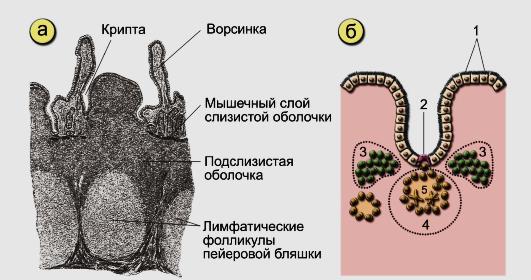 Рис. 6. Пейерова бляшка в стенке кишки: а – общий вид; б – упрощённая схема; 1 - энтероциты (эпителий кишки); 2 – М-клетки; 3 – T-клеточная зона (вокруг артериол); 4 – B-клеточная зона; 5 - фолликул. Основная функция пейеровых бляшек – поддержание иммуногенеза В-лимфоцитов и их дифференцировка в плазматические клетки, синтезирующие IgA. Продукция IgA в слизистой оболочке кишки составляет более 70% общей ежедневной продукции иммуноглобулинов в организме – у взрослого человека около 3 г IgA каждый день. Небные миндалины. Парный лимфоидный орган, расположенный в преддверии глотки. Располагаясь на границе дыхательного и пищеварительного трактов, фильтруют антигены, поступающие с пищей, водой, воздухом. Диффузная (межузелковая) ткань небных миндалин является Т-зависимой, центры размножения лимфоидных узелков являются В-зонами. В небных миндалинах активно синтезируются секреторный IgA, интерферон, в меньшей степени IgM, IgG. Миндалины находятся в функциональной связи с тимусом. Их удаление способствует более ранней инволюции вилочковой железы. Участвуют в формировании мукозального иммунитета. Раннее удаление может способствовать некоторому увеличению респираторных инфекций и аллергических заболеваний. Однако миндалины являются частью глоточного кольца Пирогова-Вальдейера, которое возьмет на себя функции удаленного органа. 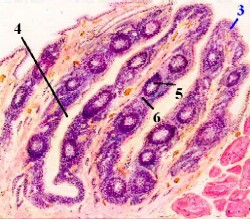 Рис. 7. Строение небных миндалин (3 – крипты, 4 – lamina proptia, 5 – В-зона, 6 – Т-зона) Аппендикс Стенки аппендикса имеют большое количество лимфоидных образований. Т-зависимая зона находится в основании лимфоидных узелков, В-зависимая зона - в области фолликулов. Среди В-лимфоцитов содержится большое количество продуцентов секреторного IgA. Аппендикс регулирует колонизационную резистентность бактерий в кишечнике, определяет оптимальное состояние микрофлоры кишечника. Лимфоциты аппендикса, стимулированные антигенами обитателей кишечника, мигрируют в другие лимфоидные образования, повышая общую устойчивость организма к этим антигенам. 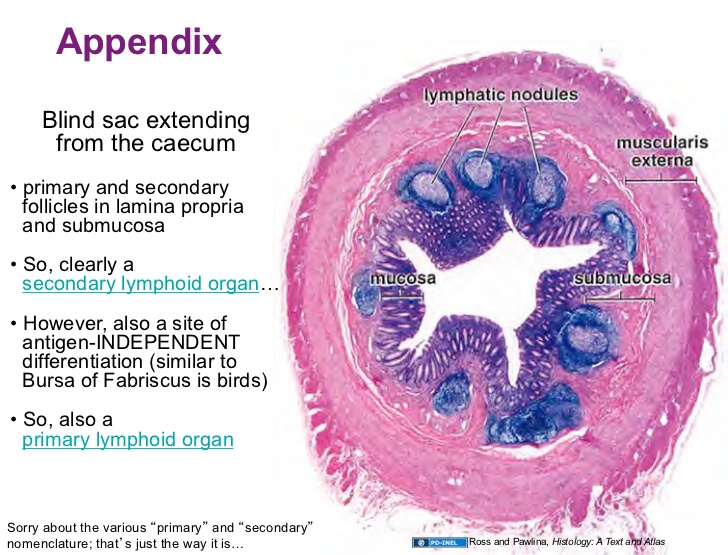 Рис. 8. Строение аппендикса. Т-зависимая зона в основании лимфоидных узелков. В-зависимая зона – область лимфоидных фолликулов. Лимфоидная ткань, ассоциированная с кожей Состоит из клеток Лангерганса, внутриэпителиальных лимфоцитов и периваскулярных лимфоцитов в соединительнотканном слое дермы. Антигены, проникающие через кожу, захватываются клетками Лангерганса и транспортируются в Т-зону регионарного лимфатического узла. Активированные антигеном Т-лимфоциты мигрируют из лимфоузлов через кровь, среди них преобладают Т-хелперы 1 типа, синтезирующие ИЛ-2 и гамма-интерферон. Гамма-интерферон является самым сильным активатором макрофагов. Под действием гамма-интеферона макрофаги, присутствующие в периваскулярном слое дермы, элиминируют антиген. Формируется реакция гиперчувствительности замедленного типа. Основные клеточные элементы иммунной системы Гемопоэтические клетки дают начало большинству клеток ИС. В период эмбриогенеза они созревают в печени, после рождения – в красном костном мозге. Т-лимфоциты дифференцируются в тимусе. Созревание и дифференцировка лимфоцитов происходит под действием цитокинов и межклеточных взаимодействий. К клеткам ИС относятся: Т- и В-лимфоциты; Клетки врожденного иммунитета; Промежуточные клетки, которым свойственны функции обоих групп. Лимфоциты – основные клетки ИС, обеспечивающие развитие адаптивного иммунитета. Лимфоциты – неоднородная популяция клеток, включающая клетки адаптивного иммунитета (Т- и В- лимфоциты и их субпопуляции) и врожденного иммунитета (NK, NKT, B1-лимфоциты). Лимфоциты циркулируют в крови и лимфе, накапливаются в лимфоидных органах, межтканевых пространствах, обладают уникальной способностью проникать через высокий эндотелий венул, не нарушая их целостности. В периферической крови взрослого человека при общем количестве лейкоцитов 4500-9500/мкл абсолютное содержание лимфоцитов составляет 800-1860/мкл. Морфологически лимфоциты представляют собой клетки с крупным ядром, занимающим практически всю или большую часть цитоплазмы. 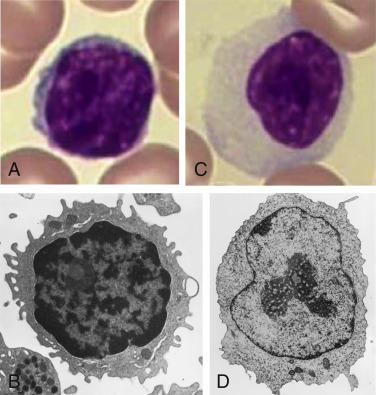  Рис. 9.1. Лимфоцит Т- и В-лимфоциты являются истинными иммунокомпетентными клетками и обладают способностью: высокоизбирательно распознавать антиген с помощью антигенспецифического рецептора TCR и BCR; развивать иммунные реакции, направленные на элиминацию антигена; создавать клоны себе подобных клеток после стимуляции антигеном; формировать иммунную память; развивать иммунную толерантность. Клональный принцип организации Т- и В-лимфоцитов означает, что каждая клетка экспрессирует на своей поверхности уникальный (свой) антигенраспознающий рецептор и предназначена для связывания определенного антигена. В процессе пролиферации клон умножается. Популяция лимфоцитов человека в целом способна распознавать любые антигены. При дифференцировке Т-лимфоцитов в тимусе, а В-лимфоцитов в красном костном мозге образуется не менее 109 вариантов клонов лимфоцитов. Прошедшие первый этап дифференцировки (иммунопоэз) лимфоциты заселяют периферические органы ИС. После встречи с антигеном начинается второй этап дифференцировки – иммуногенез. Т- и В-лимфоциты, имеющие рецептор к данному антигену, начинают делиться. Процесс пролиферации необходим, поскольку клоны специфических Т- и В-лимфоцитов крайне малочисленны и не могут выполнить своих функций, не пройдя нескольких циклов деления. 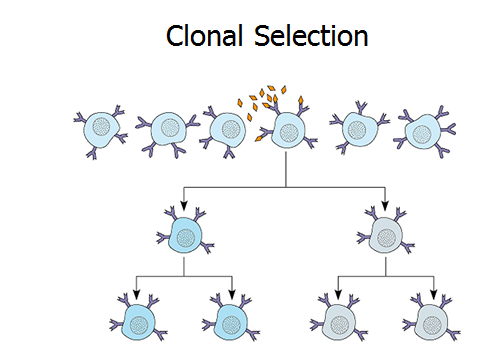 Рис. 9.2. Клональный принцип селекции Т-лимфоцитов В-лимфоциты отвечают за развитие гуморального иммунного ответа, направленного преимущественно на элиминацию внеклеточных инфекционных агентов (гельминты, аллергены, внеклеточные бактерии – стафилококк, стрептококк, кишечная палочка). При связывании специфического антигена с помощью BCR-рецептора В-лимфоциты взаимодействуют с Т-хелперами, пролиферируют, дифференцируются в плазматические клетки и секретируют антитела. Т-лимфоциты – главная популяция клеток в развитии клеточного иммунитета. Среди Т-лимфоцитов выделяют основные субпопуляции: Т-хелперы (Th0, Th1, Th2, Th17, Tfh) регуляторные Т-клетки (Treg, Tr1, Th3) цитотоксические Т-лимфоциты (ЦТЛ) или Т-киллеры Т-хелперы Не обладают непосредственным деструктивным потенциалом. Вырабатывают цитокины и участвуют в формировании клеточного и гуморального иммунного ответа. Т-хелперы 1 типа (Th1) участвуют в формировании Т-клеточного иммунитета. Распознают антиген на мембране антигенпредставляющих клеток (дендритная клетка или макрофаг) в комплексе с молекулой гистосовместимости 2 класса (HLA2), активируются, пролиферируют, синтезируют ИЛ-2 и гама-интерферон (ИФ-γ). Стимулируют размножение Т-киллеров, повышают функциональную активность макрофагов.  Рис. 9.3. Распознавание инфицированной клетки Т-хелпером Т-хелперы 2 типа (Th2) участвуют в формировании гуморального иммунитета. Распознают антиген на мембране антигенпредставляющих клеток (дендритная клетка или В-лимфоцит) в комплексе с молекулой гистосовместимости 2 класса (HLA2), активируются, пролиферируют, синтезируют ИЛ4, ИЛ-5, ИЛ-6, ИЛ-10, ИЛ-13 стимулирует пролиферацию и дифференцировку В-лимфоцитов, а также синтез антител разных классов. Цитотоксические лимфоциты – клетки-киллеры, способные уничтожать собственные клетки, зараженные вирусом, опухолевые клетки, клетки трансплантата. Являются ключевыми в защите организма от внутриклеточных паразитов. С помощью TCR распознают собственные клетки организма, на поверхности которых имеется чужеродный антиген в комплексе с молекулой гистосовместимости 1 класса – HLA1. Цитотоксический эффект обусловлен продукцией перфорина и грамзина, запускающих апоптоз клетки-мишени. 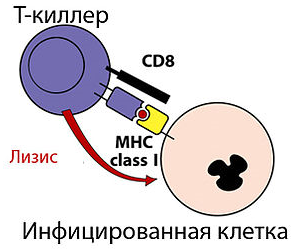 Рис. 9.4. Распознавание инфицированной клетки Т-киллером Регуляторные Т-лимфоциты (Treg) подавляют аутоагрессивные клоны Т-лимфоцитов, способствуют формированию толерантности к пищевым антигенам и микробам-комменсалам. Tr1, Th3 выполняют супрессивную функцию, подавляя активность Т-киллеров в исходе иммунного ответа. Клетки врожденного иммунитета Моноциты – крупные одноядерные лейкоциты диаметром 18-20 мкм с эксцентрично расположенным ядром и азурофильной зернистостью в цитоплазме. Имеют овальную форму, крупное бобовидное ядро. В норме составляют 3-11% (450/мкл) от общего числа лейкоцитов крови. Помимо крови присутствуют в лимфатических узлах, селезенке, красном костном мозге. Образуются в красном костном мозге. Способны к миграции за пределы кровеносного русла. Обладают выраженной фагоцитарной функцией, поглощают крупные частицы и клетки, не погибают после фагоцитирования. Синтезируют цитокины. Моноциты являются не окончательно созревшими клетками. Они циркулируют в крови 2-3 дня, затем выходят в окружающие ткани, где превращаются в тканевые макрофаги. 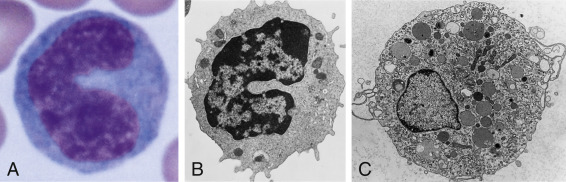 Рис. 9.5. Моноцит Макрофаги – крупные полиморфные клетки с ядром небольшого размера округлой, бобовидной или неправильной формы. Цитоплазма базофильна, богата лизосомами, фагосомами. Макрофаги располагаются во всех тканях и органах: в рыхлой соединительной ткани (гистиоциты), костной (остеокласты), нервной ткани (микроглия), печени (клетки Купфера), легких (альвеолярные макрофаги), коже, селезенке, лимфатических узлах. Обладают выраженной способностью к фагоцитозу. Поглощают и уничтожают внедрившиеся микроорганизмы, поврежденные, дегенерированые, вирусинфицированные и опухолевые клетки. Могут оказывать цитотоксическое действие на клетки, выделяя свободные радикалы кислорода. Способны не только фагоцитировать, но и презентировать антиген Т-лимфоцитам. Вырабатывая хемотаксические факторы и цитокины, оказывают регуляторное действие на клетки ИС. Срок жизни в тканях – 120 дней. Макрофаги активируются под действием множества сигнальных молекул, вызывающих их дифференцировку в различные функциональные типы. Классически активированные макрофаги (М1-фенотип) – формирующийся при действии внутриклеточных микробов и\или IFN-γ. Их основные функции – фагоцитоз внутриклеточных паразитов (вирусы, микобактерии) и синтез провоспалительных цитокинов. Альтернативно активированные макрофаги (M2-фенотип) – мигрируют в зоны инвазии гельминтами, скапливаются в локусах фиброза, в заживающих ранах кожи и неопластических образованиях, участвуют в регенерации тканей, аллергических реакциях, секретируют противовоспалительные цитокины. Также выделяют две основные разновидности макрофагов — резидентные и воспалительные. Резидентные макрофаги возникают в результате спонтанной (плановой) миграции моноцитов из кровотока в ткани, не связанной с воспалением. Они выполняют преимущественно гомеостатические и регуляторные функции, участвуя в разрушении старых клеток и регуляции иммунных и воспалительных процессов, а также выступают в роли антигенпрезентирующих клеток. Резидентные макрофаги обладают более длительным сроком жизни (годы по сравнению с неделями для воспалительных макрофагов). Воспалительные макрофаги образуются в процессе экстренной миграции в очаги воспаления. Воспалительные макрофаги обладают высокой фагоцитарной и бактерицидной активностью, выделяют ряд цитокинов и других гуморальных веществ, важных для формирования воспаления и реализации иммунной защиты. Эти свойства позволяют воспалительным макрофагам играть роль эффекторных клеток воспаления и врожденного иммунитета, участвуют в репарации тканей.  Фагоцитоз или презентация АГ 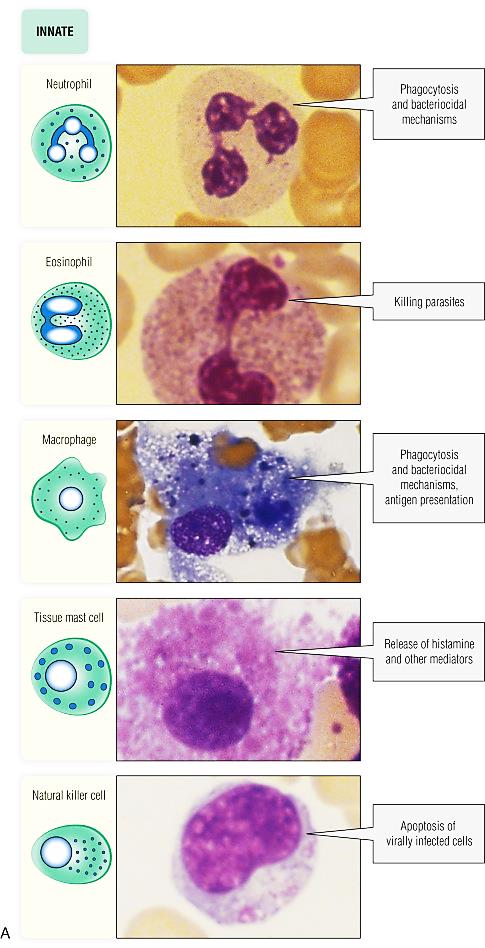 Рис. 9.6. Макрофаг Дендритные клетки – антигенпрезентирующие клетки. Могут быть лимфоидного и миелоидного происхождения. Распределены по всему организму, наиболее многочисленны в коже и слизистых оболочках (входные ворота для антигенов), а также в органах иммунной системы (место презентации антигенов). К антигенпредставляющим относят ретикулярные клетки, интердигитирующие клетки, клетки Лангерганса. Обладают подвижностью, могут переноситься с током лимфы и крови. Клетки Лангерганса локализуются в коже. Они захватывают антиген, перерабатывают его и мигрируют в ближайший лимфоузел для презентации его Т-лимфоцитам. Ретикулярные клетки располагаются в В-зависимых зонах лимфоузлов и селезенки и представляют антиген В-лимфоцитам, интердигитирующие клетки – в Т-зависимых зонах лимфоузлов, селезенки, миндалин и представляют антиген Т-лимфоцитам..  Фагоцитоз, продукция цитокинов, презентация АГ 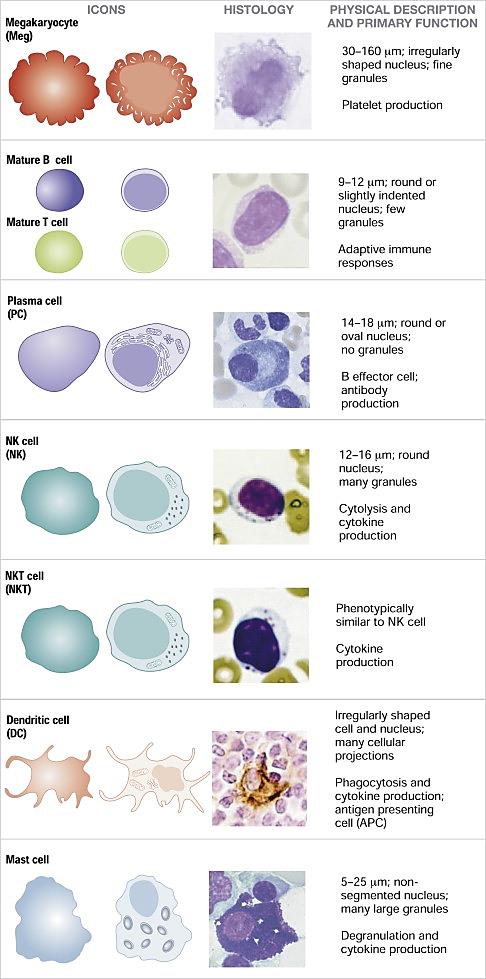 Рис. 9.7. Дендритная клетка Нейтрофилы образуются из миелоидного ростка кроветворения и относятся к группе гранулоцитов. Составляют самую многочисленную популяцию клеток крови, 65-75% (3000-7000/мкл). Короткоживущие клетки, срок жизни 3-4 дня. Первыми мигрируют в очаг воспаления и преобладают там в первые 24 ч. Обладают мощным биоагрессиным потенциалом, способностью фагоцитировать и перевариваривать микробы. Являются первой линией защиты против бактерий и грибов.  Фагоцитоз или внеклеточный бактерицидный механизм  Рис. 9.8. Нейтрофил Эозинофилы – разновидность гранулоцитов. Их доля от общего числа лейкоцитов 2-5%. Зрелые эозинофилы несколько часов циркулируют в крови, а затем выселяются в ткани, где живут несколько суток. Способны к фагоцитозу и внеклеточному цитолизу. Обладают цитотоксической активностью в отношении простейших и гельминтов, играют важную роль в защите организма от паразитарных инвазий. Крупные размеры гельминтов не позволяют переваривать их внутриклеточно, поэтому эозинофилы, содержащие большое количество гранул (эозинофильный катионный белок, пероксидаза, кислая фосфатаза) умерщвляют объект. Кроме того эозинофилы участвуют в аллергических реакциях (гиперчувствительность немедленного типа, поздняя стадия).  Киллинг паразитов  Рис. 9.9. Эозинофил Базофилы. Составляют 1% от общего числа лейкоцитов. Мигрируя в ткани, становятся тучными клетками. Несут на своей поверхности рецептор к IgE, принимают участие в аллергических реакциях (гипречувствительность немедленного типа). Гранулы этих клеток содержат биологически активные вещества (гистамин, гепарин, серотонин, дофамин, ферменты (протеазы, пероксидазы), хемотаксические факторы нейтрофилов, эозинофилов.  Участие в аллергических реакцияхнемедленного типа 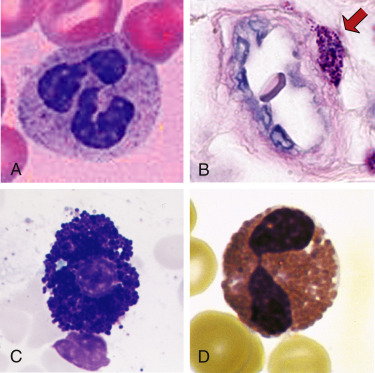 Рис. 9.10. Базофил NK-клетки (естественные, натуральные киллеры, CD16, CD56). Большие зернистые лимфоциты. Основные клетки неспецифического иммунобиологического надзора. Обладают противовирусной и противоопухолевой активностью. Распознавать клетки-мишени им позволяет система рецепторов, определяющих плотность молекул MHC (HLA). Цитотоксический эффект обусловлен продукцией перфорина и грамзина, запускающих апоптоз клетки-мишени.  Апоптоз инфицированной или опухолевой клетки 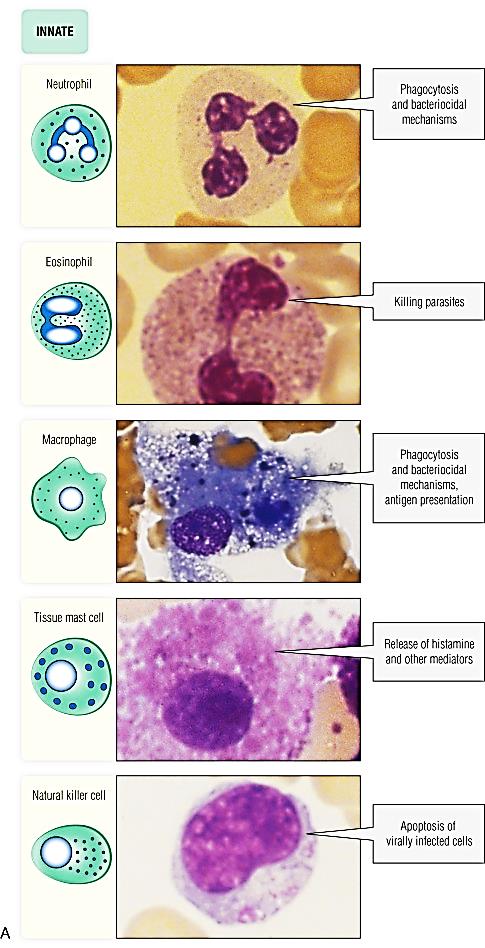 Рис. 9.11. Базофил Промежуточные клетки γδТ-лимфоциты способны элиминировать отдельные антигены (токсоплазмы, микобактерии) без предварительной сенсибилизации. Вырабатывают цитокины, осуществляют иммунорегуляторные функции. В1-лимфоциты синтезируют спонтанно, без предварительной активации естественные антитела (IgМ), которые обладают низкой специфичностью и способны перекрестно свзязывать многие антигены. NKТ-клетки имеют рецепторы, как NK-клеток, так и Т-лимфоцитов. Осуществляют регуляторную функцию, синтезируя цитокины. Понятие о дифференцировочных маркерах (CD номенклатура) Под световым микроскопом все лимфоциты выглядят одинаково, однако их можно отличить по антигенам клеточной поверхности и функциям. Антигены клеточной поверхности обозначают CD - молекулами и выявляют с помощью моноклональных антител, меченых флюоресцентными красителями. Номера СD1, СD2, СDЗ и т.д. до СD130 обозначают отдельные поверхностные молекулы. Набор антигенов клеточной поверхности зависит от типа клеток. В соответствии с общепринятой в мире СD-кластерной классификацией маркером всех Т-лимфоцитов считают CD3, маркером Т-хелперов CD4, маркером Т-киллеров/цитотоксических CD8 и т.д. |
