Тема 24. Ароматические амины. Ароматические амины
 Скачать 0.53 Mb. Скачать 0.53 Mb.
|
|
АРОМАТИЧЕСКИЕ АМИНЫ Ароматическими аминами называют производные ароматических углеводородов, в которых один или несколько атомов водорода бензольного кольца замещены на аминогруппы (NH2). Ароматические амины можно также рассматривать как производные аммиака, в молекуле которого один или несколько атомов водорода замещены ароматическими радикалами. Как и в алифатическом (жирном) ряду, ароматические амины могут быть первичными, вторичными и третичными. В зависимости от того, какие радикалы (только ароматические или ароматические и алифатические) связаны с атомом азота, различают чисто ароматические и жирноароматические. Аминогруппа может быть непосредственно связана с ядром или находиться в боковой цепи. Анилин является родоначальником класса ароматических аминов, в которых аминогруппа непосредственно связана с бензольным кольцом: 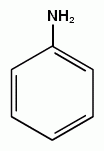 анилин (фениламин, аминобензол) Номенклатура ароматических аминов Для названия ароматических аминов обычно используют тривиальную номенклатуру. Например, анилин, толуидин. По систематической (заместительной) номенклатуре названия аминов образуют из названий радикалов с добавлением окончания –амин или приставки амино- и названия соответствующего углеводорода: 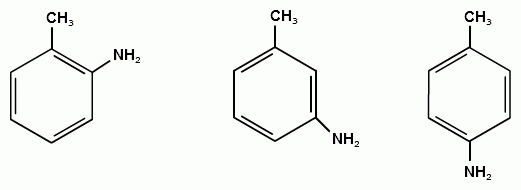 Тривиальная: орто-толуидин мета-толуидин пара-толуидин Заместительная: орто-толиламин мета-толиламин пара-толиламин орто-аминотолуол мета-аминотолуол пара-аминотоуол (2-аминотоуол) (3-аминотолуол) ( 4-аминотолуол) В ароматическом кольце может быть две и более аминогрупп. Названия соединений с двумя аминогруппами (диамины) образуют из названия двухвалентного углеродного остатка и окончания –диамин или приставки диамино- и названия соответствующего углеводорода: 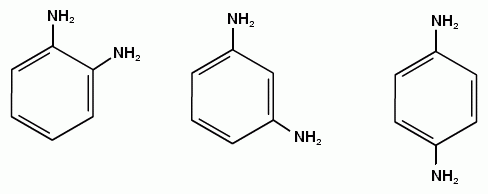 о-фенилендиамин м-фенилендиамин п-фенилендиамин о-диаминобензол м-диаминобензод п-диаминобензол (1,2-диаминобензол) (1,3-диаминобензол) (1,4-диаминобензол) В зависимости от числа радикалов, связанных с атомом азота, различают также вторичные и третичные ароматические амины. Названия вторичных и третичных аминов чаще всего образуют по принципам рациональной номенклатуры, перечисляя имеющиеся в соединении радикалы и добавляя окончание –амин: 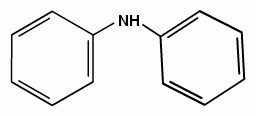 дифениламин (вторичный амин) 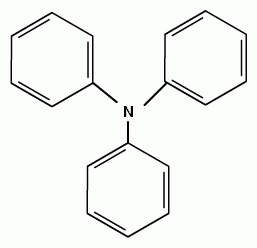 трифениламин (третичный амин) Если в молекуле амина с атомом азота связаны одновременно и ароматические и алифатические радикалы, то такие амины называют жирноароматическими. В случае жирноароматических аминов за основу названия берется слово «анилин» и, чтобы показать, что радикал расположен у атома азота, а не в бензольном кольце, перед названием радикала ставится буква N: 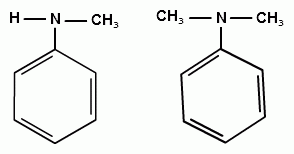 N-метиланилин N,N-диметиланилин Рациональная: метилфениламин диметилфениламин Заместительная: N-метиламинобензол N,N-диметиламинобензол Амины с аминогруппой в боковой цепи: 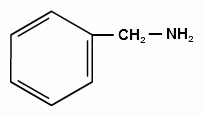 бензиламин α-аминотолуол Ароматические амины с аминогруппой в боковой цепи обладают свойствами алифатических аминов. Изомерия ароматических аминов 1) изомерия по положению алкильного радикала: 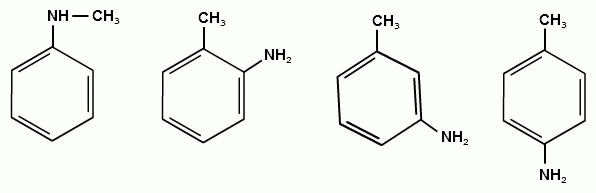 N-метиланилин о-толуидин м-толуидин п-толуидин 2) изомерия по положению аминогруппы: 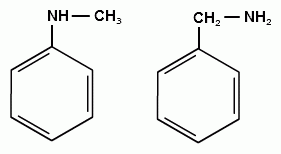 N-метиланилин бензиламин Способы получения ароматических аминов Способы получения первичных аминов 1. Прямое аминирование бензольного кольца Прямое аминирование бензольного кольца аммиаком протекает в крайне жестких условиях на сложных катализаторах (соли молибдена, вольфрама или хрома и оксиды никеля или меди) при температуре 4000С: 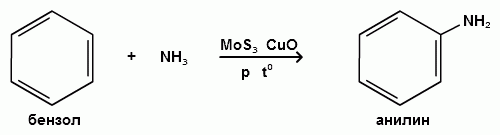 2. Восстановление нитробензола Восстановление нитробензола – основной способ получения анилина. 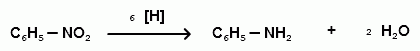 Таким путем Зинин Н.Н. (1842 г.) впервые получил анилин действием сульфида аммония на нитробензол. В качестве восстановителей могут быть использованы железо и соляная или серная кислоты, олово и соляная кислота, сероводород и сульфиды щелочных металлов, гидросульфиты и, наконец, восстановление можно вести каталитическими или электрохимическими методами. В зависимости от условий реакции (рН-среды и типа восстановителя) восстановление приводит к получению различных промежуточных продуктов, которые могут быть использованы в органическом синтезе. Более подробно восстановление нитробензола было рассмотрено при обсуждении химических свойств ароматических нитросоединений. 3. Аммонолиз арилгалогенидов В последнее время ароматические амины получают из галогенопроизводных ароматического ряда и аммиака: Ar-Cl + 2 NH3 → Ar-NH2 + NH4Cl Вследствие малой подвижности атома галогена, связанного с ароматическим ядром, реакцию замещения проводят или в очень жестких условиях, или усиливают подвижность галогена введением в бензольное кольцо электроноакцепторных заместителей. При очень жестких условиях (высокие температуры и давление и в присутствии катализаторов – меди и ее соединений) атом галогена может замещаться на амино-группу по механизму отщепления-присоединения (кине-механизм): 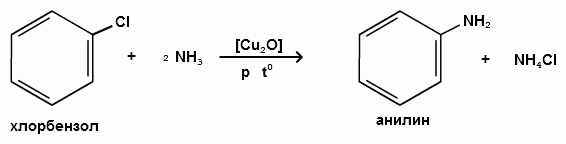 Электроноакцепторные группы (-NO2, -SO3H), находящиеся в орто- и пара-положениях бензольного кольца по отношению к заместителю, увеличивают подвижность галогена и реакция протекает по механизму SN2аром (присоединение-отщепление): 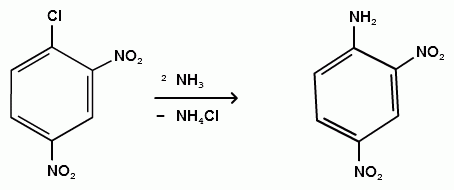 2,4-динитрохлорбензол 2,4-динитроаналин 4. Реакция Гофмана Реакция превращения амидов карбоновых кислот в первичные ароматические амины с отщеплением СО2 происходит в присутствии гипогалогенитов щелочных металлов при нагревании до 40-800С: 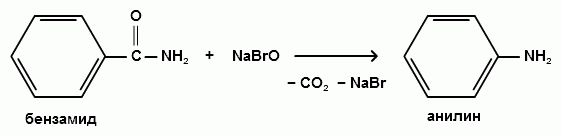 Способы получения вторичных аминов Вторичные жирноароматические амины (Ar-NH-R) получают следующими способами: 1) Алкилирование первичных ароматических аминов Вторичные жирноароматические амины получают алкилированием первичных ароматических аминов спиртами или алкилгалогенидами: 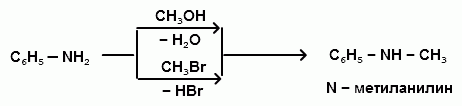 2) Гидрирование оснований Шиффа 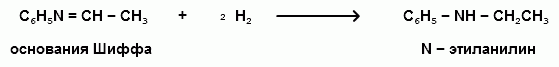 Вторичные ароматические амины (Ar2NH) получают следующими способами: 1) Нагревание первичных ароматических аминов с их солями  2) Взаимодействие ариламинов с арилгалогенидами 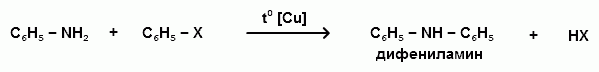 Способы получения третичных аминов Третичные жирноароматические и ароматические амины часто получают алкилированием или арилированием первичных или вторичных ароматических аминов. 1) Алкилирование первичных ароматических аминов 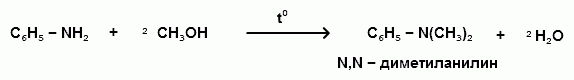 2) Арилирование вторичных ароматических аминов 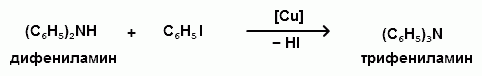 Физические свойства ароматических аминов Ароматические амины – высококипящие жидкости или кристаллические вещества с характерным неприятным запахом; являются токсичными веществами. Низшие ароматические амины плохо растворимы в воде. Накопление алкильных и фенильных радикалов делает эти соединения нерастворимыми в воде. С увеличением числа аминогрупп растворимость в воде повышается. Ароматические амины хорошо растворяются в спиртах и эфирах. Ароматические амины очень легко окисляются кислородом воздуха и поэтому, являясь в чистом виде бесцветными веществами, часто окрашены продуктами окисления. Электронное строение ароматических аминов В молекуле анилина за счет большей ЭО атома азота электронная плотность по системе σ-связей смещена в сторону гетероатома, т.е. имеет место –I –эффект. Однако ЭО азота (3,0) ненамного превышает ЭО атома углерода в sp2-гибриди-зации (2,8). Поэтому –I –эффект атома азота небольшой. Свободная электронная пара атома азота в молекуле анилина находится в сопряжении с π-электронами бензольного кольца, т.е. имеет место +М-эффект (р-π-сопряжение). При этом +М-эффект довольно большой, что связано с близкими значениями атомных радиусов атомов азота и углерода и эффективным перекрыванием электронных облаков этих атомов. Таким образом, положительный мезомерный эффект будет в значительной степени преобладать над отрицательным индуктивным эффектом: +М > -I 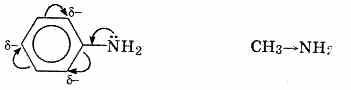 Электронное строение анилина можно представить в виде следующих граничных (или резонансных) структур: 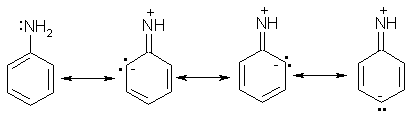  Эти структурные формулы показывают, что: 1) электронная пара азота втягивается в бензолное кольцо, при этом на атоме азота появляется частичный положительный заряд (δ+) и основные свойства аминогруппы уменьшаются. 2) в бензольном кольце, напротив, электронная плотность увеличивается, причем наиболее сильно в орто- и пара-положениях по отношению к аминогруппе. Поэтому атака электрофильных реагентов происходит в орто- и пара-положения. Аминогруппа является ориентантом 1 рода. Химические свойства ароматических аминов Ароматические амины вступают в химические превращения как с участием аминогруппы, так и ароматического кольца. 1. Кислотно-основные свойства аминов 1) Основные свойства аминов Ароматические амины, обладая основными свойствами, реагируют с сильными кислотами, образуя соли аминов: 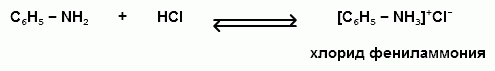 Соли аминов называют заменяя слово –амин на –аммоний, и перед названием указывают название аниона (хлорид, сульфат, нитрат). Под действием более сильных оснований ароматические амины вытесняются из их солей: Ароматические амины имеют менее выраженный основный характер, чем алифатические. Уменьшение основности анилина по сравнению с алифатическими аминами объясняется взаимодействием неподеленной пары электронов азота с электронами ароматического ядра - их сопряжением. Сопряжение уменьшает способность неподеленной электронной пары присоединять протон. Расположив амины по мере снижения основности, получим следующий ряд: Alk-NH2 > NH3 > C6H5N(Alk)2 > C6H5NHAlk > C6H5NH2 > (C6H5)2NH > (C6H5)3N Таким образом, алкилирование аминогруппы в ароматических аминах увеличивает основность, а введение в молекулу второго или третьего ароматического кольца приводит к ослаблению основных свойств (трифениламин почти совсем не обладает основными свойствами). Введение в ароматическое кольцо различных заместителей оказывает значительное влияние на основные свойства ароматических аминов. Электроноакцепторные заместители (-NO2, –CN, –COOH) усиливают сопряжение атома азота с бензольным кольцом и уменьшают основные свойства аминов. Электронодонорные заместители (Alk, -OCH3) приводят к увеличению электронной плотности на атоме азота и, следовательно, к усилению основных свойств. 2) Кислотные свойства Кислотные свойства у ароматических аминов выражены сильнее, чем у алифатических. Это связано со снижением электронной плотности на атоме азота за счет р,π-сопряжения, приводящего к увеличению поляризации связи N-H. Однако, кислотные свойства ароматических аминов очень слабы, и водород может замещаться лишь при действии щелочных металлов и амидов: 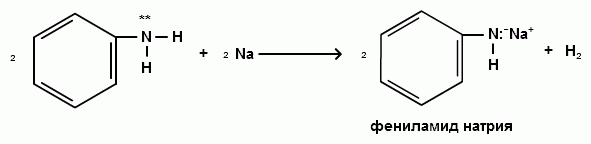 2. Реакции аминов как нуклеофильных реагентов Хотя нуклеофильные свойства у ароматических аминов выражена слабее, чем у алифатических (за счет сопряжения свободной электронной пары с бензольным кольцом), для них характерны реакции алкилирования и ацилирования, взаимодействие с альдегидами и кетонами, реакции с азотистой кислотой. 1. Алкилирование ароматических аминов Атомы водорода в аминогруппе ароматических аминов могут быть замещены на алкильные радикалы. В качестве алкилирующих агентов используют галогеналканы, спирты, диалкилсульфаты. Реакция алкилирования приводит к получению вторичных и третичных аминов. Реакция протекает по механизму нуклеофильного замещения (SN). В качестве нуклеофила выступает молекула ароматического амина, которая за счет свободной электронной пары атома азота атакует атом углерода с частичным положительным зарядом (δ+). В зависимости от строения галогеналкана (спирта) может реализовываться SN1 или SN2 механизм: 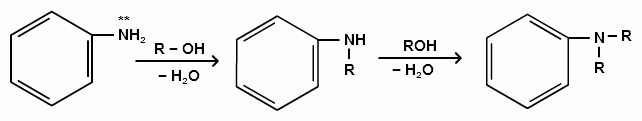 Ди- и трифениламины – плохие нуклеофилы, поэтому реакции алкилирования происходят с ними с трудом. 2. Ацилирование ароматических аминов Атомы водорода в аминогруппе первичных и вторичных аминов могут быть замещены на ацильные радикалы (RCO-). Ароматические амины ацилируются не только ангидридами и хлорангидридами карбоновых кислот, но и карбоновыми кислотами. В результате реакции ароматические амины превращаются в амиды соответствующих карбоновых кислот. Ацильные производные анилина называют анилидами. Реакция протекает по механизму нуклеофильного замещения (SN). Нуклеофилом является ароматический амин, который атакует карбонильный атом углерода с частичным положительным зарядом (δ+). 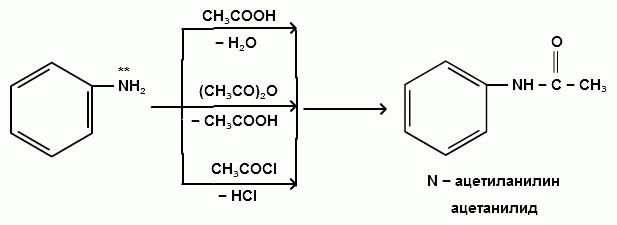 Реакция ацилирования имеет большое значение. Она используется для защиты аминогруппы от нежелательных воздействий, для уменьшения ориентирующего влияния аминогруппы при проведении некоторых реакций. Амиды карбоновых кислот могут легко гидролизоваться как в кислой, так и в щелочной среде, поэтому после проведения необходимых реакций ацильная «защита» легко снимается и образуется свободная аминогруппа. 3. Реакции с альдегидами и кетонами Первичные ароматические амины легко вступают в реакции с ароматическими альдегидами и кетонами с образованием азометинов (основания Шиффа). При их образовании в качестве нуклеофила выступает ароматический амин. Первая стадия – реакция нуклеофильного присоединения по карбонильной группе (АN), на второй стадии следует отщепление молекулы воды: 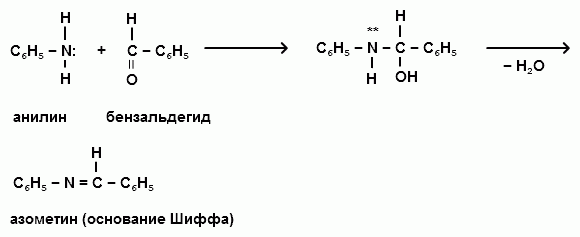 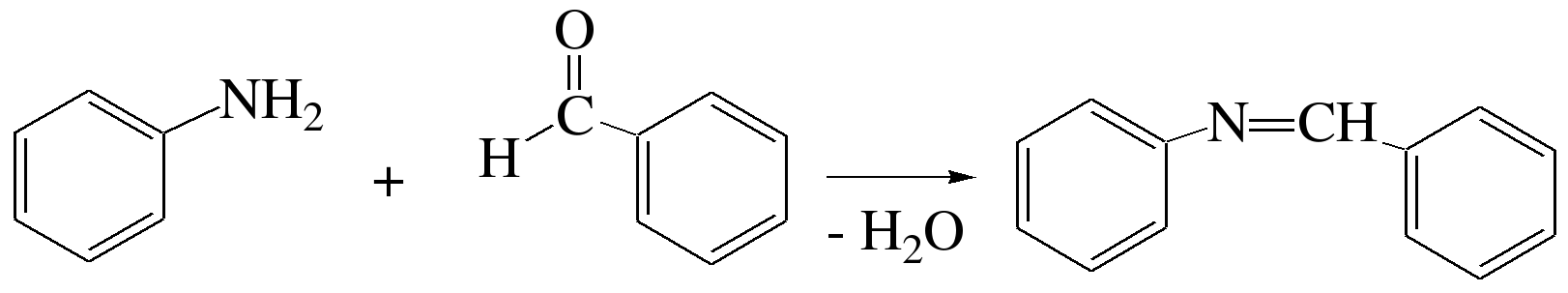 Шиффовы основания легко гидролизуются в кислой среде с образованием исходных веществ (анилина и бензальдегида):  Простейшие шиффовы основания бесцветны, более сложные окрашены и относятся к классу азометиновых красителей. Для крашения тканей эти красителе не нашли широкого применения в связи с легкостью гидролиза связи C=N в кислой среде. Однако они широко используются в цветной фотографии, для крашения пластмасс и в полиграфии. 4. Реакции аминов с азотистой кислотой Первичные ароматические амины с азотистой кислотой при 0 – 5°С образуют соли диазония: 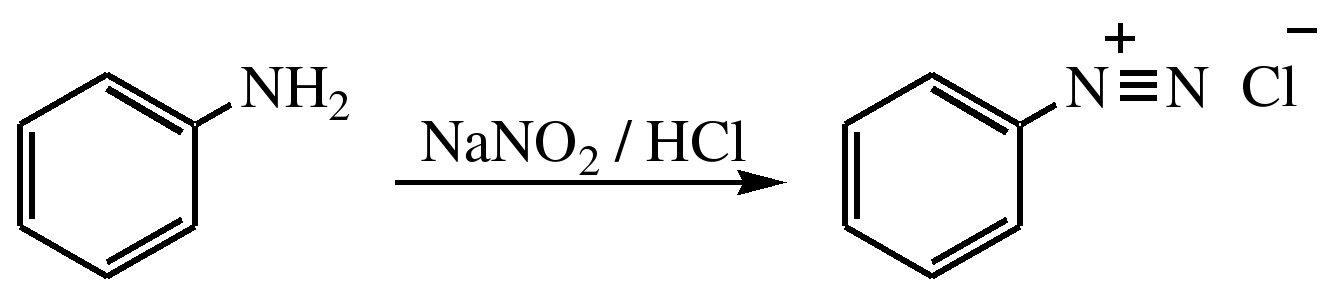 хлорид фенилдиазония Вторичные амины при взаимодействии с азотистой кислотой образуют N-нитрозо-N-метиланилины: 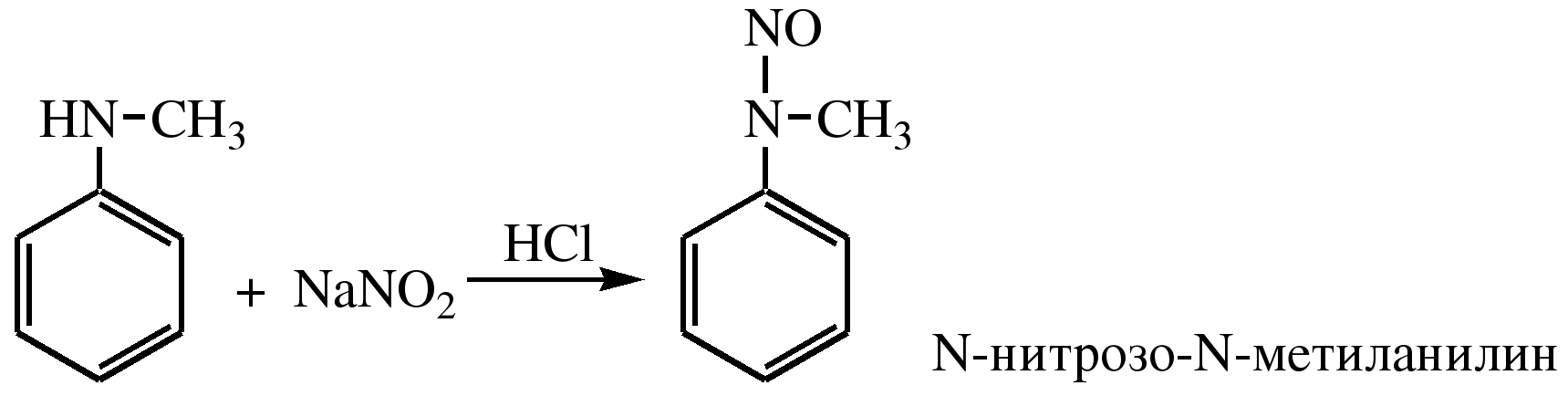 Третичные амины с азотистой кислотой вступают в реакцию электрофильного замещения: 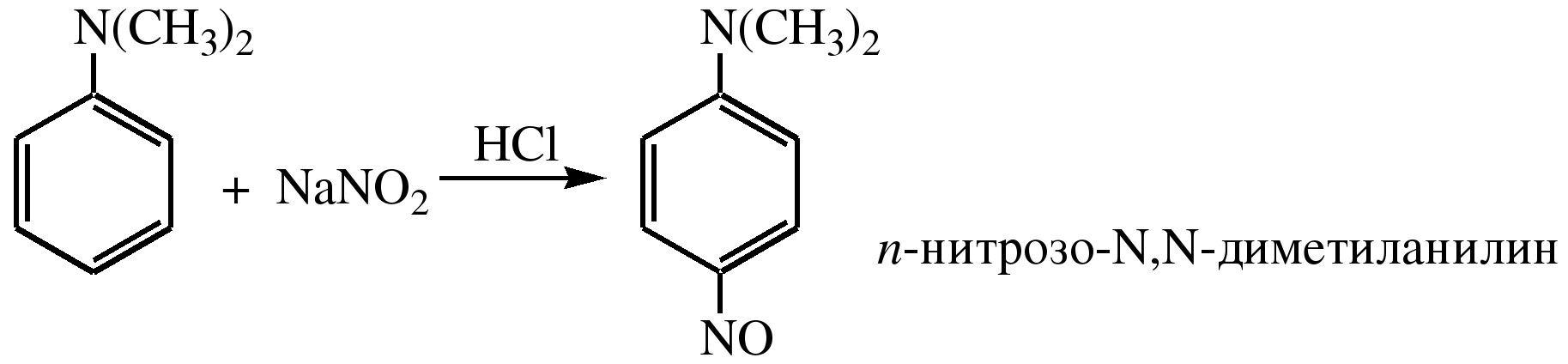 5. Окисление ароматических аминов Ароматические амины в отличие от аминов алифатического ряда легко окисляются, вследствие чего при хранении они обычно приобретают окраску. Первичные ароматические амины окисляются пероксисерной кислотой (H2SO5) до нитрозосоединений, в то время как окисление перманганатом калия (KMnO4) или пероксидом водородом (Н2О2) приводит к нитропроизводным аренов: 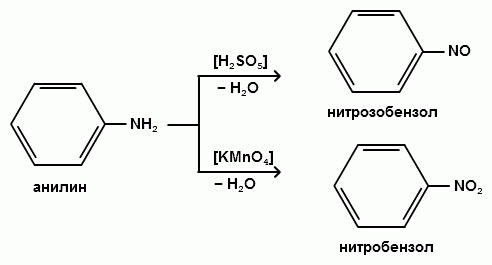 Окисление анилина хромовой кислотой, диоксидом марганца (1У) и серной кислотой приводит к образованию бензохинона-1,4: 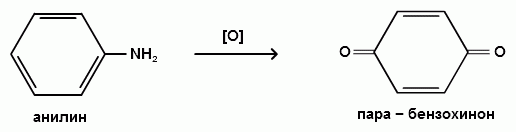 3. Реакции электрофильного замещения в бензольном кольце 1. Реакция галогенирования В ароматических аминах аминогруппа облегчает замещение в орто- и пара-положениях бензольного кольца. Поэтому галогенирование анилина происходит быстро и в отсутствие катализаторов, причем замещаются сразу три атома водорода бензольного кольца, и выпадает белый осадок 2,4,6-триброманилина: 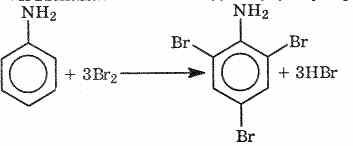 Эта реакция бромной водой используется как качественная реакция на анилин. 2. Реакция сульфирования Взаимодействие серной кислоты с анилином на холоду приводит к гидросульфату анилиния. Реакция в кольцо не происходит из-за образования сильно акцепторной дезактивирующей аммонийной группы. Незначительное нагревание гидросульфата анилиния приводит к фенилсульфаминовой кислоте, которая при длительном нагревании при 200о превращается в пара-аминобензолсульфониевую (сульфаниловую) кислоту. 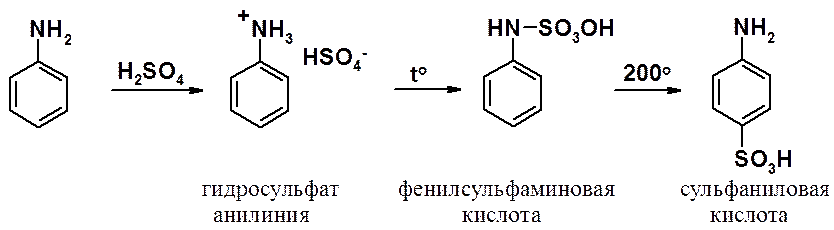 |
