|
|
2 коллоквиум по БХ. Катаболтм(дисеималяция)
Билет 1
1) Катаболтм(дисеималяция) - расщепление крупных молекул до более простых вещест в результате окислительных процессов или процессов гидролиза и фосфоролиза, сопровождающееся разрывов ковалентных связей и высвобождением энергии.
Примеры: гликолиз, гликогенолиз, окисление жирных кислот.
Анаболизм(ассимилящия) — синтез сложных органических соединений из простых молекул в результате восстановительных процессов (как правило), сопровождающийся образованием связей между малыми молекулами в процессе синтеза более высокомолекулярных соединений и осуществляющийся с затратой энергии. Примеры: глюконеогенез, синтез жирных кислот, фотосинтез у растений.
. , '
Отличительный признак
|
Катаболизм
|
Анаболизм
|
1. Энергия
|
Высвобождается (эюергонический процесс)
|
Затрачивается (эндергонический процесс)
|
2. Характер процесса
|
Окислительный
|
Восстановительный
|
3. Локализация в клетке (компартм ентация метаболических процессов)
|
Цитоплазма, митохондрии, лизосомы
|
Цитоплазма клетки, рибосомы, ЭПС КГ; ядро
|
4. Обратимость реакций
|
Практически необратимы
|
В основном обратимы
|
Также процессы катаболизма и анаболизма различаются по механизмам регуляции. Уровни взаимосвязи между ката- и анаболизмом.
На уровне источников углерода (субстратов).
Продукты катаболизма - исходные субстраты для продуктов анаболизма. Важнейшие метаболиты, на уровне которых происходит пересечение метаболических путей: глюкозо-6-фосфат, пируват, ацетил-КоА.
На уровне восстановленных эквивалентов.
В процессе катаболизма происходит восстановление кофермента, который затем используется для анаболических процессов. КАДФН основной донор электронов в восстановительных реакциях биосинтеза. НАДН и ФАДН2 основные акцепторы и переносчики электронов при окислении ''топливных молекул". .
3)Катаболизм основных пищевых веществ сопровождается высвобождением энергии, которая может аккумулироваться в фоще АТФ. При анаболических процессах происходит потребление АТФ с образованием АДФ и неорганического фой|йш, используемых в реакциях диссимиляции для нового синтеза АТФ.
2) ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА
Осуществляется при участии набора ферментов, объединенных в пируватдегидроге- назный комплекс (ПВДГК). Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами)
Е1 — пируватдекарбоксилаза. Коферментом является активная форма витамина В1, тиамина — ТПФ (тиаминпирофосфат).
Е2 — дигидролипоилацетилтрансфераза. Коферментом является витаминоподобное вещество — липоевая кислота (липоил), которая может временно превращаться в дигидроли- поил, присоединив 2 атома водорода. Липоил может также переносить ацетильные остатки.
С этим ферментом также работает активная форма пантотеновой кислоты — КоА-SH, которая принимает ацетильный остаток от липоевой кислоты.
Ез — дигидролипоилдегидрогеназа. Коферментом является ФАД — активная форма витамина В2, рибофлавина. С работой этого фермента связан также кофермент НАД+ — активная форма витамина РР, никотиновой кислоты.
Суммарно: СН3-СО- СООН * НS-КоА + НАД+ ------ПДГК------ СО2+СНз- CO-SKoA + НАДН*Н+
Основными поставщиками восстановленных субстратов являются центральные метаболические пути — окислительное декарбоксилирование пировиноградной кислоты и цикл лимонной кислоты. Они локализованы в матриксе митохондрий, в ходе этих процессов происходят реакции декарбоксилирования (большая часть всей углекислоты, образующейся в клетках, образуется именно здесь). 3) 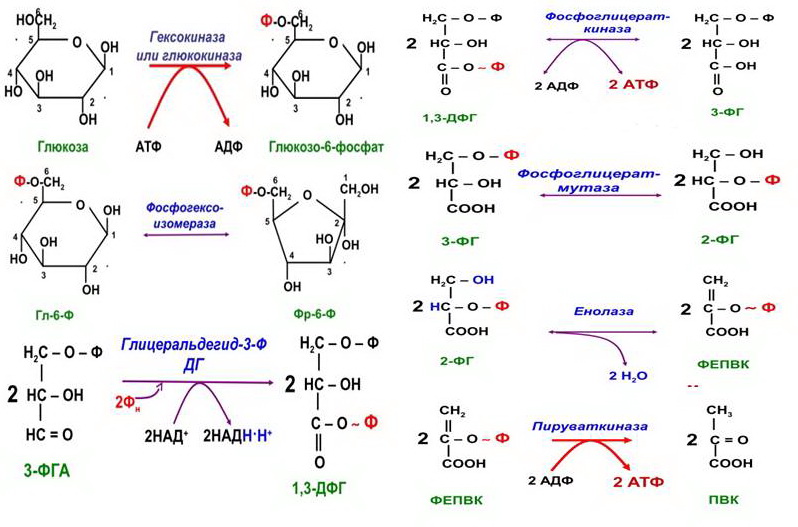 4) СИНТЕЗ ГЛИКОГЕНА (ГЛИКОГЕНЕЗ) Гликогенез- синтез гликогена, осущ-ся почти во всех клетках, но в больших кол-вах он образ и накапл в печени и мыш тканях Общее содержание гликогена в организме взрослого человека около 450 г (в печени — до 150 г, в мышцах — около 300 г). Более интенсивно гликогенез осуществляется в печени. Гликогенсинтаза — ключевой фермент процесса — катализирует присоединение глюкозы к молекуле гликогена с образованием а-1,4-гликозидных связей. Биологическая роль: запасание глюкозы, предотвращение осмотического повреждения клетки.  Включение одной молекулы глюкозы в синтезирующуюся молекулу гликогена требует затраты энергии двух молекул АТФ. 5) Гипоэнергетические состояния возникают в организме вследствие дефицита АТФ в клетках. Причины их следующие:
алиментарные (голодание, гиповитаминозы РР, В2);
г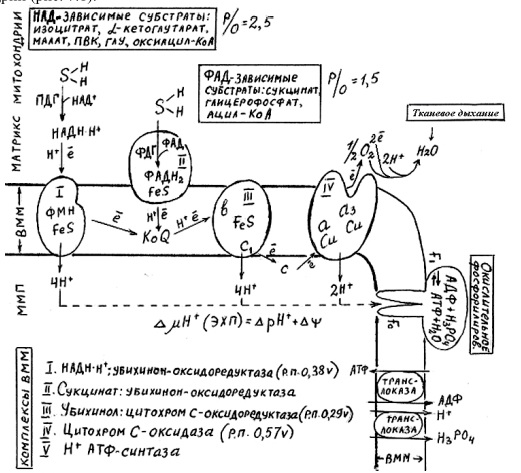 ипоксические (нарушения доставки 02 в клетки); ипоксические (нарушения доставки 02 в клетки);
митохондриальные (действие ингибиторов и разобщителей).
6) все верно
Билет 2
1) путь окисления — оксигеназный- не дает клетке энергии, кислород включается в субстрат с образованием новой гидроксильной или карбоксильной группы. Этот путь происходит в основном в мембранах эндоплазматического ретикулума (микросомах). Путем микросомного окисления осуществляется альфа- и w-окисление жирных кислот, синтез ненасыщенных жирных кислот, стероидов. Таким путем обезвреживаются ксенобиотики, т. е. чужеродные для организма вещества (лекарства, ядохимикаты, косметические препараты).
Ферменты, осуществляющие такое окисление, называются оксигеназами. Различают диоксигеназы, которые включают в молекулу субстрата два атома молекулы кислорода. Более распространены в клетках монооксигеназы (гидроксилазы). Они катализируют реакции, при которых в молекулу субстрата включается один атом из молекулы кислорода, второй же атом кислорода восстанавливается при этом до воды. Монооксигеназные системы представляют собой короткие цепи переноса электронов и протонов, источником которых служит чаще всего восстановленный НАДФ+, реже НАД+ или аскорбиновая кислота. Активатором кислорода при этом является цитохром Р450 — одноцепочечный хро- мопротеин с молекулярной массой 50 кДа. Примерная схема монооксигеназной цепи представлена на рисунке 7.4.
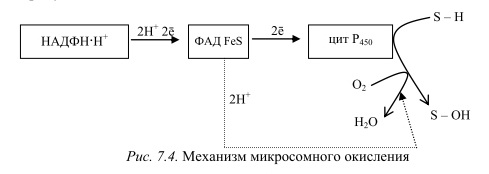
Смысл такого процесса заключается в том, что ксенобиотики, которые обычно гидрофобны, гидроксилируясь, становятся более гидрофильными, что способствует их обезвреживанию и выведению из организма с желчью или мочой. С участием микросомных систем осуществляется также биосинтез стероидов, желчных кислот, витамина Д3.
2)
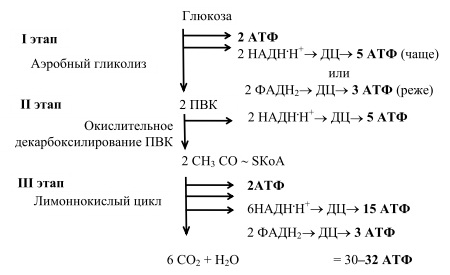
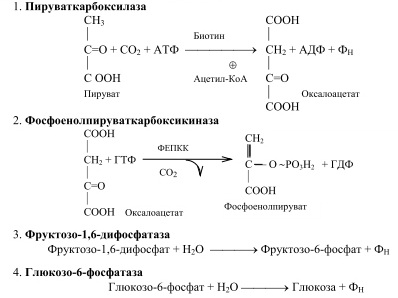
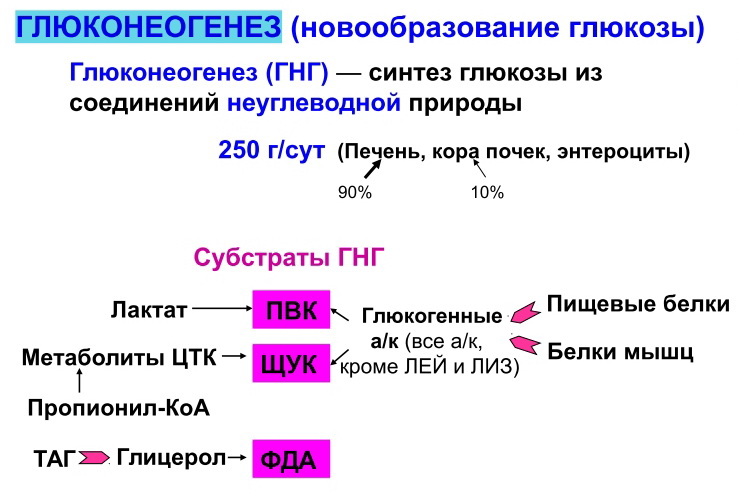
3) Регуляция глюконеогенеза. Глюконеогенез стимулируется в условиях гипогликемии при низком уровне инсулина и преобладании его антагонистов (глюкагона, катехоламинов, глюкокортикоидов).
Регуляция активности ключевых ферментов:
фруктозо-1,6-дифосфатаза по аллостерическому механизму активируется АТФ, ингибируется фруктозо-2,6-дифосфатом и АМФ;
пируваткарбоксилаза активируется CH3CO -SK0A (аллостерический активатор).
Регуляция количества ключевых ферментов: глюкокортикоиды и глюкагон индуцируют синтез ключевых ферментов, а инсулин — репрессирует.
Регуляция количества субстрата: количество субстратов глюконеогенеза увеличивается под действием глюкокортикоидов (катаболическое действие на белки мышечной и лимфоидной ткани, на жировую ткань), а также глюкагона (катаболическое действие на жировую ткань).
Биологическая роль глюконеогенеза:
Поддержание уровня глюкозы в крови.
Возвращение лактата в метаболический фонд углеводов.
Предотвращение лактатного ацидоза, то есть в ходе глюконеогенеза лактат крови превращается в глюкозу.
4)
5) В процессе аэробного ок-я глюкозы образ НАД\ФАД-зависимые субстраты, которые передают протоны и электроны на комплексы ДЦ. Электроны транспортируются по этим комплексам к кислороду, а протоны выходят в межмембр пространство в 1,3,4 комплексах ДЦ. Эти пункты – пункты сопряжения или фосфорилирования. Они создают электрохим потенц, энергия которого используется 4-ым комплексом ВММ для синтеза АТФ

6) все верно
Билет 3
1) Механизмы образования АТФ в клетках животных и растений:
Фотосинтетическое фосфорилирование - синтез АТФ у растений за счёт квантов солнечной энергии.
Окислительно фосфорилирование - синтез АТФ за счёт энергии, выделяющейся при окислении водорода субстрата кислородом с участием дыхательной цепи. Основной способ синтеза АТФ для большинства клеток.
Субстратное фосфорилирование - синтез АТФ за счёт энергии гидролиза макроэргической связи субстрата (пример: фосфоглицераткиназная и пируватк иназная реакции анаэробного гликолиза).
Для митохондрий характерно ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ.
Окислительное фосфорилирование - синтез АТФ за счёт энергии, выделяющейся при окислении водорода органических субстратов кислородом с участием дыхательной цепи.
Основные положения хемиоемотической теории Митчелла:
Энергия, выделяющаяся при транспорте электронов I, ill и IV комплексами дыхательной цепи, используется для перекачивания протонов в межмембранное пространство, генерируя градиент рН.
Обратныйы поток протонов по протонным каналам АТФ-синтазы в матрикс обеспечивает энергией головку АТФ-синтазы для синтеза АТФ.
2) Катаболическая функция цикла Кребса:
конечный путь окисления большинства органических веществ;
основной источник запасания энергии в клетке в форме АТФ.
До образования ЩУК образуется один НАДН*Н+ => 2,5 моль АТФ.
Фумарат состоит из 4 атомов углерода С. за один цикл Кребса происходит два декарбоксилирования, данное вещество проходит дополнительно два полных цикла Кребса. Т.к за один цикл выделяется 10 моль АТФ, а у нас 2 оборота цикла, значит выделяется 20 моль АТФ. И в сумме получится 20+2,5 =22,5 моль АТФ.
3) 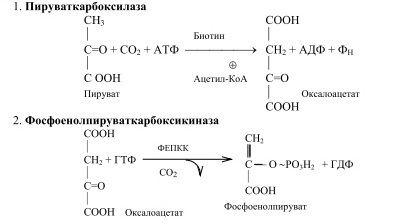 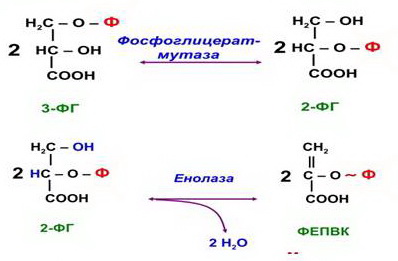
К
райние 2 – общие с р-циями гликолиза
4) Значение окислительного этапа:
Главный поставщик рибозо-5-фосфата для биосинтеза мононуклеотидов (АМФ, ГМФ, УМФ, ЦМФ, ТМФ и др.), которые в свою очередь необходимы для синтеза нуклеиновых кислот (дНк, РНК) и коферментов (НАД+, НАДФ+, ФАД, КоА^Н).
Основной источник НАДФНН+ в клетках. ПФП на 50 % обеспечивает потребности клетки в НАДФНН+.
НАДФНН+ в клетках используется:
в реакциях биосинтеза веществ как восстановитель:
синтез жирных кислот;
биосинтез холестерола, стероидных гормонов, желчных кислот;
синтез заменимых аминокислот (НАДФН-Н+ как кофермент глутаматдегидрогена- зы в реакциях восстановительного аминирования а-кетоглутаровой кислоты);в глюкуроновом пути и др.
в обезвреживании веществ: в реакциях гидроксилирования различных ксенобиотиков, лекарственных веществ, этанола и других веществ, которые осуществляются с участием микросомной цитР450-зависимой системы окисления;
как антиоксидант: используется на восстановление окисленного глутатиона. Глута- тион — важный антиоксидант клеток;
в фагоцитозе: генерирование активных форм кислорода. Фагоциты с использованием НАДФНН+ генерируют супероксидные анион-радикалы, выполняющие основную роль в разрушении поглощённых бактериальных клеток. При недостаточной продукции НАДФНН+ в условиях нарушения ПФП отмечается хроническое течение инфекционных заболеваний.
5) во-первых, ингибиторы дыхательной цепи - это яды, которые блокируют перенос электронов через I, II, III, IV комплексы. Ротенон и барбитураты блокируют I комплекс, малонат — II, антимицин А — III, цианиды, угарный газ блокируют перенос электронов на кислород, осуществляемый IV комплексом дыхательной цепи.
Во-вторых, ингибиторы окислительного фосфорилирования (олигомицин), закрывающие протонный канал V комплекса.
6) все верно
Билет 4
1) Окисли́тельное фосфорили́рование — метаболический путь, при котором энергия, образовавшаяся при окислении питательных веществ, запасается в митохондриях клеток в виде ATФ
Основные постулаты теории:
внутренняя митохондриальная мембрана (ВММ) непроницаема для ионов, в частности для Н+ и ОН ;
за счет энергии транспорта электронов через I, III и IV комплексы дыхательной цепи из матрикса выкачиваются протоны;
возникающий на мембране электрохимический потенциал (ЭХП) и есть промежуточная форма запасания энергии;
возвращение (транслокация) протонов в матрикс митохондрии через протонный канал V комплекса за счет ЭХП является движущей силой синтеза АТФ.
2) ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА
Осуществляется при участии набора ферментов, объединенных в пируватдегидроге- назный комплекс (ПВДГК). Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами)
Е1 — пируватдекарбоксилаза. Коферментом является активная форма витамина В1, тиамина — ТПФ (тиаминпирофосфат).
Е2 — дигидролипоилацетилтрансфераза. Коферментом является витаминоподобное вещество — липоевая кислота (липоил), которая может временно превращаться в дигидроли- поил, присоединив 2 атома водорода. Липоил может также переносить ацетильные остатки.
С этим ферментом также работает активная форма пантотеновой кислоты — КоА-SH, которая принимает ацетильный остаток от липоевой кислоты.
Ез — дигидролипоилдегидрогеназа. Коферментом является ФАД — активная форма витамина В2, рибофлавина. С работой этого фермента связан также кофермент НАД+ — активная форма витамина РР, никотиновой кислоты.
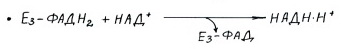
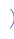 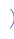
НАДФ+: Никотинамид-рибоза-фосфат

Аденин-рибоза-фосфат
фосфат
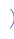
ФАД: Изоаллоксазин-рибитол-фосфат
Аденин-рибоза-фосфат
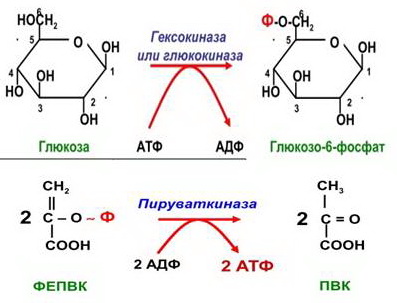
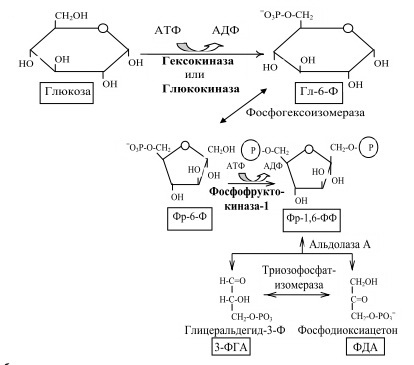
3) Ключевые ферменты гликолиза:
Гексокиназа — это регуляторный фермент гликолиза во внепеченочных клетках. Гексокиназа аллостерически ингибируется глюкозо-6-фосфатом. Глюкокиназа — регуля- торный фермент гликолиза в гепатоцитах. Синтез глюкокиназы индуцируется инсулином.
Фосфофруктокиназа-1. Это главный ключевой фермент, катализирует реакцию, лимитирующую скорость всего процесса (наиболее медленная реакция). Синтез фермента индуцируется инсулином. Аллостерические активаторы — фруктозо-2,6-дифосфат, АМФ, АДФ. Уровень фруктозо-2,6-дифосфата увеличивается под действием инсулина и понижается под действием глюкагона. Аллостерические ингибиторы — АТФ, цитрат.
Пируваткиназа. Фермент активен в нефосфорилированной форме. Глюкагон (в ге- патоцитах) и адреналин (в миоцитах) стимулируют фосфорилирование фермента, а значит инактивируют фермент. Инсулин, наоборот, стимулирует дефосфорилирование фермента, а значит активирует фермент. Аллостерический активатор — фруктозо-1,6-дифосфат. Алло- стерический ингибитор — АТФ, ацетил-КоА. Синтез фермента индуцирует инсулин.
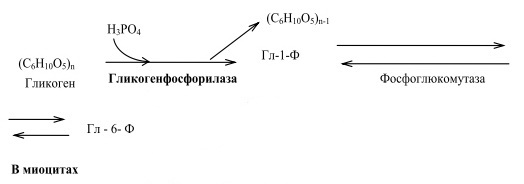
4) Основной механизм гликогенолиза — фосфоролиз (расщепление а-1,4-гликозидных связей с участием фосфорной кислоты и гли- когенфосфорилазы)
Гликолиз — это сложный ферментативный процесс расщепления глюкозы до двух молекул пирувата (аэробный гликолиз) или двух молекул лактата (анаэробный гликолиз, протекающий без потребления кислорода).
5)
Коэффициент фосфорилирования – количество молекул неорганического фосфата, которое включается в АТФ в расчете на 1 атом О2
При окислении НАД-зависимых субстратов в ММП выбрасывается 10 протонов (см. схему комплексов дыхательной цепи). Следовательно, в таком случае может быть синтезировано 2,5 моль АТФ (10:4), т. е. коэффициент фосфорилирования Р/О = 2,5.
6) нет, да, нет
Билет 5
1) Метаболизм — совокупность химических реакций, протекающих в клетках организма с момента поступления пищевых веществ в организм до образования конечных продуктов обмена.
Функции метаболизма:
снабжение клеток химической энергией;
превращение молекул пищи в строительные блоки;
сборка из этих блоков компонентов клетки (белки, липиды, нуклеиновые кислоты);
синтез и разрушение специфических биологических молекул.
Метаболический путь — последовательность химических превращений конкретного вещества в клетке:
Циклический метаболический путь - замкнутая последовательность химических превращений, проиводящая в итоге к регенерации исходного вещества. Примеры: цикл лимонной кислоты, орнитиновый цикл мочеобразования Кребса.
Линейный метаболический путь - линейная последовательность химических реакций. Примеры: гликолиз, пентозофоефатный путь.
Ферменты (фермент), которые определяют скорость всего процесса в целом, называются ключевыми, катализируют необратимые реакции, имеют четвертичную структуру и легко регулируются,обычно располагаются либо в начале метаболических путей, либо в местах ключевых разветвлений. Примером может служить фосфофруктокиназа-1, ацетил-КоА- карбоксил аза, пируваткарбоксилаза, протеи нкиназа.
2) Катаболическая функция цикла Кребса:
конечный путь окисления большинства органических веществ;
основной источник запасания энергии в клетке в форме АТФ.
От сукцинил КоА до ЩУК образуется: 1 АТФ; 1 НАДФ*Н+; 1ФАДН2; Т.к. Р/0= 2,5, а 1НАДН*Н= 1*2,5=2,5 моль АТФ
Т.к. р/о= 1,5, а 1ФАДН2- 1+2,5+1,5=5 моль АТФ М 2,5+1,5- 5 мольАТФ.
Он состоит из 4 атомов С, за один цикл Кребса происходит 2 декарбоксилирования, то сукцинил КоА проходит ещё дополнительно два полных Цикла. Т.к за один цикл выделяется 10 моль АТФ, а у нас 2 оборота цикла, значит выделяется 20 моль АТФ. В сумме 20+5=25 моль.
4)
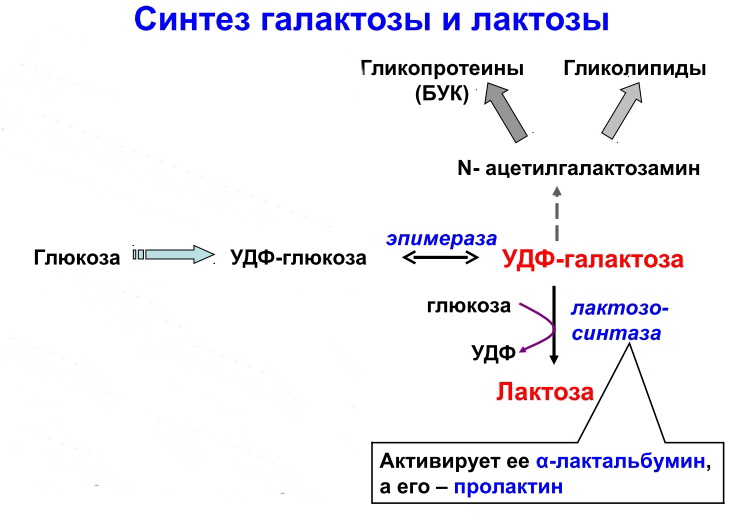
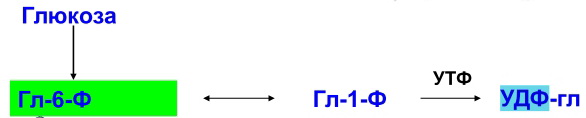 Используется в гликолизе и в глюкуроновом обмене углеводов. Используется в гликолизе и в глюкуроновом обмене углеводов.
В гепатоцитах УДФ-глюкуроновая кислота используется на процессы обезвреживания (реакции конъюгации с билирубином, продуктами гниения белков, лекарствами и др.).
В фибробластах УДФ-глюкуроновая кислота используется на синтез гетерополи- сахаридов (гиалуроновая кислота, хондроитинсульфат, дерматансульфат, гепарин).
3)
5)
V комплекс внутренней мембраны митохондрий — фермент, осуществляющий реакцию синтеза АТФ и называемым протонной АТФ-синтазой .Этот ферментативный комплекс состоит из двух частей: Fо (о — олигомицин), который встроен в мембрану, пронизывает ее насквозь и представляет собой протонный канал, и F1. Последний по форме напоминает шляпку гриба или дверную ручку и обращен в матрикс митохондрии. В изолированном виде F1 не может синтезировать АТФ, но может проводить ее гидролиз до АДФ и фосфата.
6) нет, нет, нет
Р-ции глюкоза->сорбитол->фруктоза - необтатимы
Билет 6
1) Адениловая система
система адениловых нуклеотидов, которая включает в себя АТФ, АДФ, АМФ,
неорганический фосфат й ионы Mg2+.
Роль адениловой системы:
Играет центральную роль в энергообмене всех клеток;
Благодаря неустой чивостипАТФ энергия ее концевой фосфоан гидрид ной связи АТФ может использоваться на синтез фосфорилйрованных метаболитов, имеющих свободную энергию гидролиза меньше, чем АТФ. Обратное превращение АДФ в АТФ требует энергии.
Основные процессы, использующие энергию гидролиза АТФ: 1)С и нтез разл ичных веществ.
2) Активный транспорт (транспорт веществ через мембрану против градиента их концентраций). 30 % от общего количества расходуемого АТФ приходится на Na\ К-АТФазу.
2) ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА
пируватдегидрогеназный комплекс (ПВДГК) - Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами)
С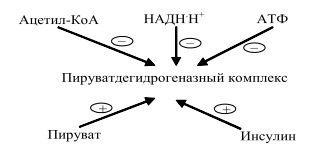
уммарно: СН3-СО- СООН * НS-КоА + НАД+ ------ПДГК------ СО2+СНз- CO-SKoA + НАДН*Н+
Окислительное декарбоксилирование ПВК даст 1 моль НАДФ*1Г(а т.к. Р/0=2,5, в процессе окислительного фосфорилирования образуется 2,5 моль АТФ).
Образуется ещё 1 моль CH3CO-SKoA, он вступает в ЦТК, там образуется 1 ФАДН2; 3 НАДН*Н+ и 1 моль АТФ.
3 НАДН*Н+ дадут в окислительном фосфор ил ировании 7,5 моль АТФ, 1 ФАДН2 - 1,5 моль АТФ, В сумме: 1,5+7,5+1+2,5=12,5 моль АТФ.
5)
Место того или иного переносчика в дыхательной цепи определяется величиной редокс-потенциала. Все реакции в дыхательной цепи направлены по термодинамической лестнице от компонента с самым отрицательным редокс-потенциалом (НАДН-Н+) к кислороду, имеющему самый положительный редокс-потенциал.
Редокс-потенциал (Е0) численно равен ЭДС в вольтах, возникающей между растворами окислителя и восстановителя (концентрации 1М, рН = 7,0, температура 25 °С). Чем отрицательнее редокс-потенциал системы, тем выше ее способность отдавать электроны (восстановители). Чем положительнее редокс-потенциал, тем выше способность вещества присоединять электроны (окислители).
Реакция синтеза АТФ, которую проводит V комплекс, носит название окислительного фосфорилирования и описывается уравнением:
АДФ + Н3РО4 = АТФ + H2O
промежуточные макроэргические соединения служат посредником между процессом тканевого дыхания и окислительным фосфорилированием.
6) да, да – общее да
3)
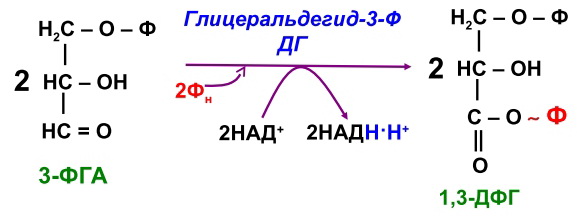 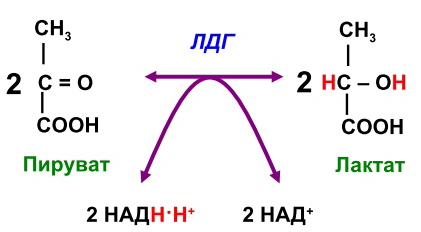
4)
 
Билет 7
1)
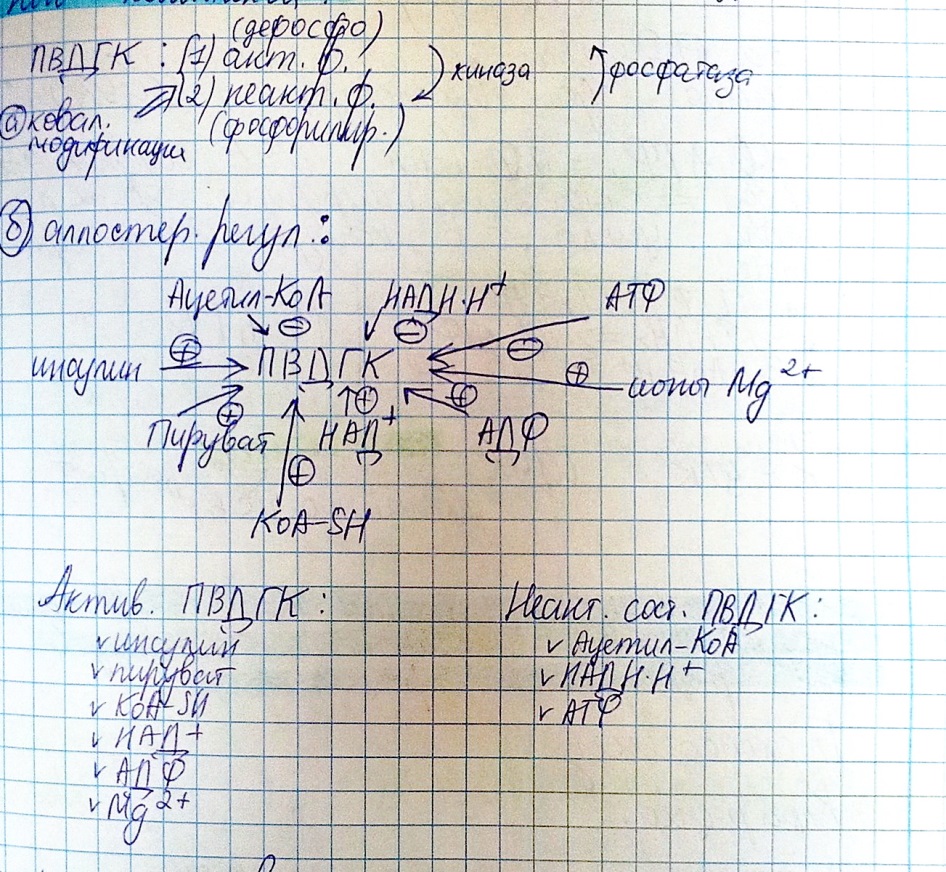
2)
Катаболическая функция цикла Кребса:
конечный путь окисления большинства органических веществ;
основной источник запасания энергии в клетке в форме АТФ.
В 4 фермент коферменты ТПФ (B1) амидлилоевой к-ты,HS-KoA (В3), ФАД (В2), НАД+(В5(РР)
В 6 ферменте кофермент ФАД (В2)
Образуется три Н АДН*Н+; один ФАДН2; и один АТФ в ходе субстратного формирования.
При окислении НАД- зависимых коэффициент фосфорилирования (Р/0)=2,5 => три НАДН*Н4 дадут 7,5 моль АТФ. Р/О при окислении ФАД Н — зависимых субстратах = 1,5 => 1 моль ФАДН2 даст 1,5 моль АТФ. В сумме 1 + 1,5+7,5=10 моль АТФ
Оксалоацетат - это ЩУК(от ЩУК до ЩУК).
3)
4)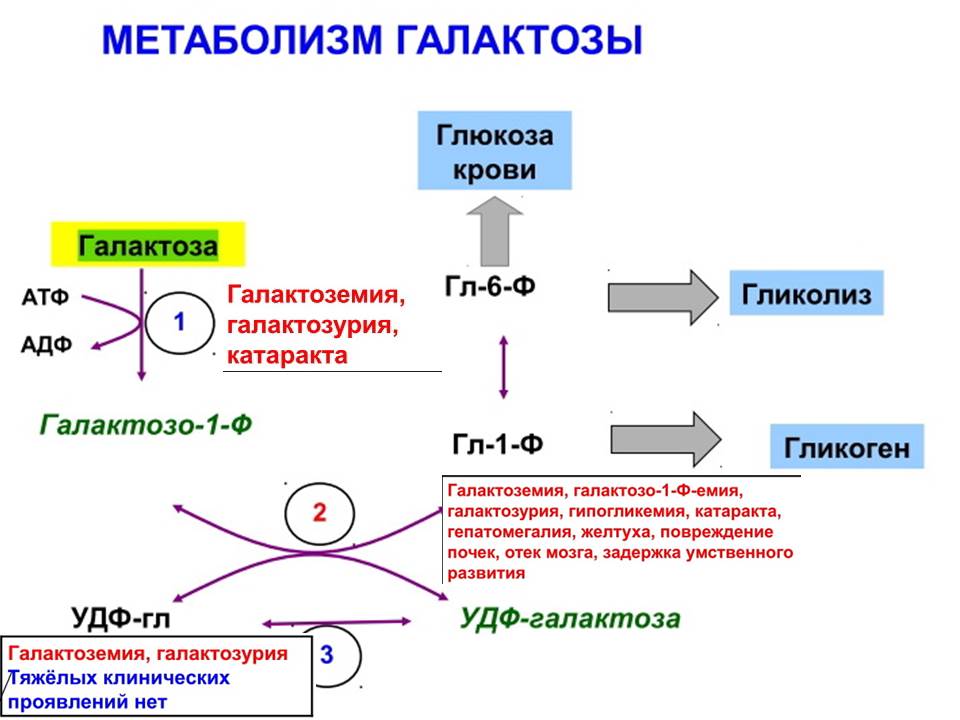
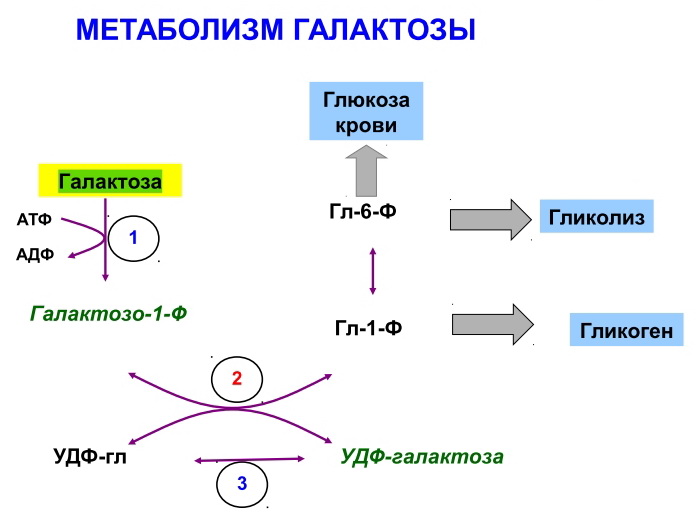
1- галактокиназа
2- галакто-1-фосфатурадилтрансфераза
3- эпимераза
Диагностика
Определение активности 2 :
в эритроцитах(постнатально)
в клетках амниотической жидкости (пренатально)
Лечение:Запрет молока и молочных продуктов
5)Коэффициент фосфорилирования – количество молекул неорганического фосфата, которое включается в АТФ в расчете на 1 атом О2
При окислении ФАД-зависимых субстратов в ММП выбрасывается 6 протонов в III и IV пунктах сопряжения. В таком случае может быть синтезировано 1,5 моль АТФ (6:4), т. е. коэффициент фосфорилирования Р/О = 1,5.
6) часть1-неверно. Вместо гипоглюкоземии нужно гипогликемии
Билет 8
1) Окислительно фосфорилирование - синтез АТФ за счёт энергии, выделяющейся при окислении водорода субстрата кислородом с участием дыхательной цепи. Основной способ синтеза АТФ для большинства клеток.
Субстратное фосфорилирование - синтез АТФ за счёт энергии гидролиза макроэргической связи субстрата (пример: фосфоглицераткиназная и пируватк иназная реакции анаэробного гликолиза).
Для митохондрий характерно ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ.
Окислительное фосфорилирование - синтез АТФ за счёт энергии, выделяющейся при окислении водорода органических субстратов кислородом с участием дыхательной цепи.
2)
Вит. И активные формы: ТПФ(акт. ф-ма вит В1), КоА-SH(акт. ф-ма пантотеновой кислоты(В5)), ФАД(акт. ф-ма В2), НАД+( акт. ф-ма вит РР)
3)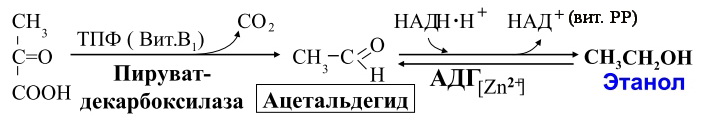
4)
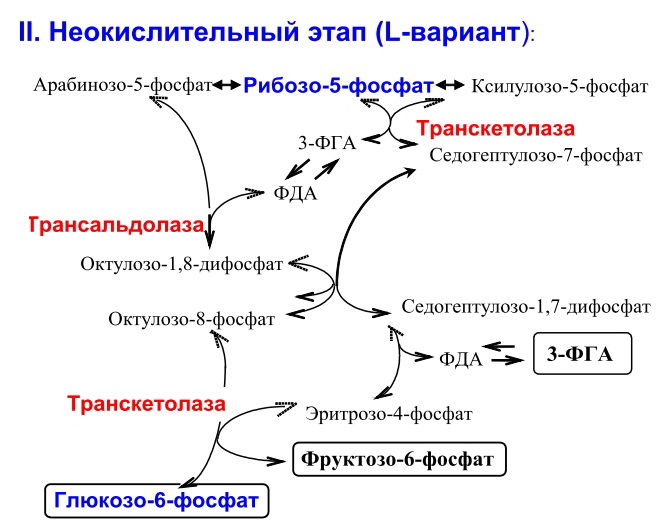
Все реакции обратимы
Транскетолазная (перенос 2С-фрагментов), кофермент - ТПФ (вит. В1)
Трансальдолазная (перенос ЗС-фрагментов)
|
|
|
 Скачать 3.5 Mb.
Скачать 3.5 Mb.


 ипоксические (нарушения доставки 02 в клетки);
ипоксические (нарушения доставки 02 в клетки);










 Используется в гликолизе и в глюкуроновом обмене углеводов.
Используется в гликолизе и в глюкуроновом обмене углеводов.









