ацетальдегид расчет. Проект узла синтеза ацетальдегида из этилена в присутствии хлористого палладия
 Скачать 156.51 Kb. Скачать 156.51 Kb.
|
|
Министерство образования и науки Российской Федерации федеральное государственное автономное образовательное учреждение высшего образования «НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» Отделение химической инженерии Направление 18.03.01 «Химическая технология» Профиль «Химическая технология органических веществ» БАКАЛАВРСКАЯ РАБОТА
Студент
Руководитель
ДОПУСТИТЬ К ЗАЩИТЕ:
Томск – 2020 г. Оглавление3 Расчет и аналитика 2 3.1 Материальный расчет 2 3.2 Расчет основных расходных коэффициентов 14 3.3 Тепловой расчет аппарата 16 3.3.1 Тепловой расчет реактора РТ1 16 3.3.2 Тепловой расчет колонны КЛ1 18 3.4. Технологический расчет аппарата 21 3.4.1 Технологический расчет аппарата РТ1 21 3.4.2 Технологический расчет реактора РТ2 22 3.4.3 Технологический расчет колонны КЛ1 23 3.5. Гидравлический расчет аппарата 25 3.6 Механический расчет 27 3.6.1 Расчет диаметра штуцеров 28 3.6.2 Расчет втулки фланца 28 3.7 Подбор вспомогательного оборудования 31 3 Расчет и аналитика3.1 Материальный расчетИсходные данные: Годовая производительность установки по ацетальдегиду 90000 т; Годовой фонд рабочего времени 8000 ч; Состав технического этилена, [φi(xi),%] : - этилен–99,90; - этан–0,10; Степень конверсии этилена 0,98. Доля этилена, расходуемого на образование продуктов окисления, [φi(xi), %]: - ацетальдегид–93; - уксусная кислота–1; - диоксид углерода–2,5; - щавелевая кислота–0,6; - кротоновый альдегид–0,3; - высокомолекулярные и полимерные продукты–0,9; - этилхлорид–0,08; - монохлорацетальдегид–1,03; - дихлормеацетальдегид–0,3; - трихлорацетальдегид–0,15; - трихлорметан–0,07; - дихлорметан–0,07. Потери, (%): - ацетальдегида на стадии ректификации–2,0; - этилена на стадии синтеза–2,1; Объемная доля кислорода в отработанном воздухе - 0,04 В расчетах используем схему потоков стадии синтеза (рисунок 7.1). 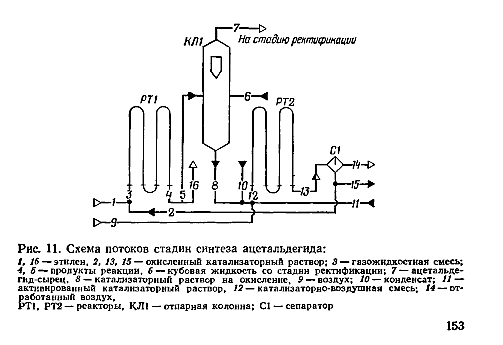 Рисунок 7.1 – Схема потоков стадий синтеза 1, 16 – этилен, 2, 13, 15 – окисленный катализаторный раствор, 3 – газожидкостная смесь, 4, 5 – продукты реакции, 6 – кубовая жидкость со стадии ректификации, 7 – ацетальдегид-сырец, 8 – катализаторный раствор на окисление, 9 – воздух, 10 – конденсат, 11 – активированный катализаторный раствор, 12 – катализаторно-воздушная смесь, 14 – отработанный воздух. РТ1 , РТ2 – реакторы, КЛ1 – отпарная колонна, С1 – сепаратор Часовая производительность установки по ацетальдегиду: П ч= (П год/ Тэф) ∙1000 (1) где Пгод - производительность в год, кг/ч; Тэф - время эффективное, ч; Пч= (90000/8000)∙1000 = 11250 кг/ч или 11250/44 = 255,681 кмоль/ч. С учетом 2 % потерь на стадии ректификации необходимо получить ацетальдегида на стадии синтеза: 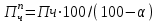 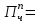 255,681∙100/(100-2) = 260,899 кмоль/ч или 11479,5 кг/ч. 255,681∙100/(100-2) = 260,899 кмоль/ч или 11479,5 кг/ч.Расходуется этилена на получение ацетальдегила: 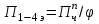 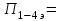 260,899/0,93 = 280,537 кмоль/ч. 260,899/0,93 = 280,537 кмоль/ч.Расходуется этилена с учетом степени конверсии: 280,537/0,98 = 286,262 кмоль/ч. Содержание этилена в продуктах реакции: 286,262 -280,537 = 5,725 кмоль/ч. Расходуется этилена с учетом потерь на стадии синтеза: 286,262∙100/(100,0 – 2,1) =292,402 кмоль/ч или 292,402∙28 = 8187,3 кг/ч. Потери этилена (поток 16): 292,402 – 286,262 = 6,141 кмоль/ч или 171,9 кг/ч. Расходуется технического этилена: 292,402/0,999 = 292,694 кмоль/ч. Количество этана, содержащегося в техническом этилене: 292,402 – 292,694 = 0,292 кмоль/ч или 8,8 кг/ч. Выполняем материальный расчет системы из двух реакторов (условно принимаем, что окисление этилена происходит воздухом и хлороводородом). По основной реакции 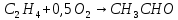 (3.1) (3.1)расходуется: этилена: 260,899 кмоль/ч или 7305,1 кг/ч; кислорода: 0,5∙260,899 = 130,45 кмоль/ч или 4174,38 кг/ч; Образуется ацетальдегида: 260,899 кмоль/ч или 11479,5 кг/ч. По реакции 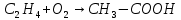 (3.2) (3.2)расходуется: этилена: 0,01 ∙ 280,537 = 2,805 кмоль/ч или 78,48 кг/ч; кислорода: 2,805 кмоль/ч или 95,6 кг/ч. Образуется: уксусной кислоты: 2,805 кмоль/ч или 168,3 кг/ч. По реакции 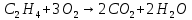 (3.3) (3.3)расходуется: этилена: 0,025 ∙ 280,537 = 7,013 кмоль/ч или 196,3 кг/ч; кислорода: 3∙7,013 = 21,039 кмоль/ч или 673,2 кг/ч. Образуется: диоксида углерода: 2∙7,013 = 14,026 кмоль/ч или 617,0 кг/ч; водяного пара: 14,026 кмоль/ч или 252,5 кг/ч. По реакции 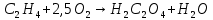 (3.4) (3.4)расходуется: этилена: 0,006 ∙ 280,537 = 1,683 кмоль/ч или 47,2 кг/ч; кислорода: 2,5∙1,683 = 4,208 кмоль/ч или 134,6 кг/ч. Образуется: щавелевой кислоты: 1,683 кмоль/ч или 151,56 кг/ч; водяного пар: 1,683 кмоль/ч или 30,2 кг/ч. По реакции 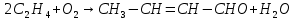 (3.5) (3.5)расходуется: этилена: 0,003 ∙ 280,537 = 0,842 кмоль/ч или 23,6 кг/ч; кислорода: 0,5∙0,842 = 0,421 кмоль/ч или 13,5 кг/ч. Образуется: кротонового альдегида: 0,421 кмоль/ч или 29,5 кг/ч; водяного пара: 0,421 кмоль/ч или 7,5 кг/ч. По реакции 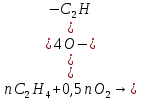 (3.6) (3.6)расходуется: этилена: 0,009 ∙ 280,537 = 2,525 кмоль/ч или 70,7 кг/ч; кислорода: 0,5∙2,525 = 1,263 кмоль/ч или 40,5 кг/ч. Образуется: высокомолекулярных и полимерных продуктов (массовых расход определяем по сумме расходов этилена и кислорода): 2,525 кмоль/ч или 111,2 кг/ч. По реакции 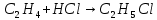 (3.7) (3.7)расходуется: этилена: 0,0008 ∙ 280,537 = 0,225 кмоль/ч или 6,3 кг/ч; хлороводорода: 0,225 кмоль/ч или 8,1 кг/ч. Образуется: этилхлорида: 0,225 кмоль/ч или 14,5 кг/ч. По реакции 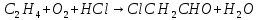 (3.8) (3.8)расходуется: этилена: 0,0103 ∙ 280,537 = 2,889 кмоль/ч или 80,8 кг/ч; кислорода: 2,889 кмоль/ч или 92,5 кг/ч; хлороводорода: 2,889 кмоль/ч или 105,5 кг/ч. Образуется: монохлорацетальдегида: 2,889 кмоль/ч или 226,6 кг/ч; водяного пара: 2,889 кмоль/ч или 52,0 кг/ч. По реакции 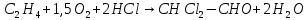 (3.9) (3.9)расходуется: этилена: 0,003 ∙ 280,537 = 0,842 кмоль/ч или 23,6 кг/ч; кислорода: 1,5∙0,842 =0,702 кмоль/ч или 40,5 кг/ч; хлороводорода: 2∙0,842 = 0,936 кмоль/ч или 59,8 кг/ч. Образуется: дихлорацетальдегида: 0,842 кмоль/ч или 95,2 кг/ч; водяного пару: 1,684 кмоль/ч или 30,2 кг/ч. По реакции 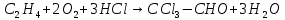 (3.10) (3.10)расходуется: этилена: 0,0015 ∙ 280,537 = 0,421 кмоль/ч или 11,7 кг/ч; кислорода: 2∙0,421 =0,468 кмоль/ч или 26,8 кг/ч; хлороводорода: 3∙0,421 = 0,702 кмоль/ч или 46,1 кг/ч. Образуется: трихлорацетальдегида: 0,421 кмоль/ч или 62,1 кг/ч; водяного пару: 1,263 кмоль/ч или 22,6 кг/ч. По реакции 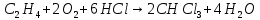 (3.11) (3.11)расходуется: этилена: 0,0007 ∙ 280,537 = 0,196 кмоль/ч или 5,6 кг/ч; кислорода: 2∙0,196=0,392 кмоль/ч или 12,4 кг/ч; хлороводорода: 6∙0,196= 1,177 кмоль/ч или 43,0 кг/ч. Образуется: трихлорметана: 0,392 кмоль/ч или 46,8 кг/ч; водяного пару: 4∙0,196 = 0,784 кмоль/ч или 14,0 кг/ч. По реакции 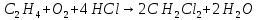 (3.12) (3.12)расходуется: этилена: 0,0007 ∙ 280,537 = 0,196 кмоль/ч или 5,6 кг/ч; кислорода: 0,196 кмоль/ч или 6,3 кг/ч; хлороводорода: 4∙0,196= 0,784 кмоль/ч или 28,6 кг/ч. Образуется: дихлорметана: 2∙0,196 = 0,392 кмоль/ч или 33,3 кг/ч; водяного пару: 0,392 кмоль/ч или 7,0 кг/ч. Всего расходуется кислорода по реакциям 3.1 - 3.6,3.8 – 3.12: 130,450 + 2,804 + 21,038 + 4,208 + 0,421 + 1,264 + 2,889 + 1,264 + 0,842 + 0,392 + 0,196 = 165,769 кмоль/ч или 5304,6 кг/ч. Всего расходуется хлороводорода: 0,225 + 2,889 + 1,685 + 1,264 + 1,178 + 0,785 = 8,024 кмоль/ч или 292,8 кг/ч. Всего образуется водяного пара: 14,026 + 1,683 + 0,421 + 2,889 + 1,264 + 1,685 + 0,785 + 0,392 = 23,144 кмоль/ч или 416,5 кг/ч. Расход воздуха на окисление находим из уравнения 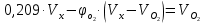 (3.13) (3.13)где 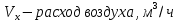 ; ;0,209 – объемная доля кислорода в воздухе, доли ед.; 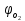 - - 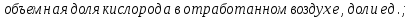 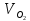 - расход кислорода на окисление этилена, - расход кислорода на окисление этилена, 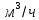 . .Расход кислорода на окисление этилена: 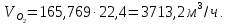 Расход воздуха: 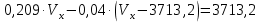 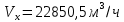 . .Рассчитываем состав воздуха: кислород: 0,209∙22850,5 = 4775,8 м3/ч или 213,203 кмоль/ч или 6822,5 кг/ч. азот: 22850,5-4775,8 = 18074,7 м3/ч или 806,906 кмоль/ч или 22593,4 кг/ч. Содержится кислорода в продуктах реакции: 213,203 – 165,769 = 47,434 кмоль/ч или 1517,9 кг/ч. Количество отработанного воздуха (поток 2): 47,434+806,906 = 854,339 кмоль/ч или 24111,0 кг/ч. Составляем таблицу 8 материального баланса стадии синтеза. Таблица 8 – Материальный баланс стадии синтеза
Так как в действительности в реакторе РТ1 окисление этилена осуществляется катализаторным раствором, допускаем, что расход последнего равен расходу кислорода и хлороводорода на образование продуктов реакции. Определяем расход катализаторного раствора: 11479,5/6,0 = 1913,4 м3/ч, где 11479,5 – производительность установки по ацетальдегиду, кг/ч; 6,0 – производительность катализаторного раствора по ацетальдегиду, кг/м3 катализаторного раствора. Принимаем, что плотность катализаторного раствора равна 1100 кг/м3, тогда его расход составит 1913,4∙1100 = 2104574 кг/ч. Рассчитываем состав катализаторного раствора:
Допускают, что количество катализаторного раствора на выходе из реактора уменьшиться за счет прореагировавших воды и хлороводорода: 2104574 – ( 292,8 + 5304,6) = 2098976,5 кг/ч, где 5304 – расход кислорода на образование продуктов реакции, кг/ч. Составляем таблицу материального баланса по реактору РТ1. Таблица 9 - Материальный баланс реактора РТ1
Рассчитываем материальный баланс отпорной колонны. В колонну КЛ1 поступает реакционная смесь с катализаторным раствором из реактора РТ1 для отделения ацетальдегида и побочных продуктов от катализаторного раствора. Таблица 10 - Материальный баланс отпарной колонны
Для поддержания постоянной концентрации катализаторного раствора в колонну подают постоянное количество кубовой жидкости со стадии ректификации (1,8 – 2,0 т на одну тонну ацетальдегида, температура 84 - 94ºС). Принимают, что в газовую фазу переходит 95,7% ацетальдегида и все компоненты, кроме щавелевой кислоты и катализаторного раствора. Количество ацетальдегида, переходящего в газовую фазу: 11479,5∙0,957 = 10985,9 кг/ч Расходуется кубовой жидкости из отделения ректификации: 1,9∙11479,5 = 21811,1 кг/ч. Выполняем материальный расчет реактора РТ2. Таблица 11 – Материальный баланс реактора РТ2.
Расход воздуха по таблице 8: 29415,4 кг/ч. Расход катализаторного раствора, поступающего на окисление таблице 3.3: 2098976,9 кг. Расход конденсата: 0,2∙11479,5 = 2295,9 кг/ч. где 0,2 – удельный расход конденсата, тонн на одну тону ацетальдегида. Расход активированного катализаторного раствора: 1,85∙11479,5 = 21237,075 кг/ч. где 1,85 – удельный расход катализаторного раствора, тонн на одну тонну ацетальдегида. Рассчитывают количество катализаторного раствора, подаваемого на активацию: (29415,9 + 2098976,9 + 2295,9 + 21237,075) – (2104574,4 + 24111,0) = 23885,41 кг/ч. где 2104574,4 – расход катализаторного раствора в реактор РТ1, кг/ч; 24111,0 – количество отработанного воздуха, кг/ч. Потери катализаторного раствора при активации: 100 – (21237,075/24111)∙100 = 11,1%, что соответствует оптимальному технологическому режиму. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
