вариант 3 ОГЭ. Решение. В предложениях 1 и 5 о свинце говорится как о химическом элементе, а в остальных как о простом веществе
 Скачать 355.05 Kb. Скачать 355.05 Kb.
|
|
1. Задание 1 № 5844 Выберите два высказывания, в которых говорится о свинце как о химическом элементе: 1) В алхимии свинец ассоциировался с планетой Сатурн 2) Свинец — металл серебристо-серого цвета с синеватым оттенком 3) Свинец очень ковкий и легко плавится 4) Свинец используется для защиты пациентов от излучения рентгеновских аппаратов 5) Свинец относится к группе тяжёлых металлов Запишите в поле ответа номера выбранных высказываний. Решение. В предложениях 1 и 5 о свинце говорится как о химическом элементе, а в остальных — как о простом веществе. Ответ: 15. Ответ: 15|51 2. Задание 2 № 11003 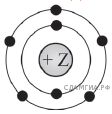 На приведённом рисунке изображена модель атома химического элемента. Запишите в поле ответа номер периода и номер группы, в которых расположен химический элемент, модель которого изображена на рисунке. (Для записи ответа используйте арабские цифры.) На приведённом рисунке изображена модель атома химического элемента. Запишите в поле ответа номер периода и номер группы, в которых расположен химический элемент, модель которого изображена на рисунке. (Для записи ответа используйте арабские цифры.)Решение. Число заполняемых электронных оболочек соответствует номеру периода химического элемента, то есть элемент, о котором идёт речь в условии задания, расположен во втором периоде. А количество валентных электронов указывает на то, что элемент расположен в VA группе. Ответ: 25. Ответ: 25 3. Задание 3 № 10736 Расположите химические элементы – 1) галлий 2) кислород 3) фосфор в порядке уменьшения радиуса атома. Запишите номера выбранных элементов в соответствующем порядке. Решение. Радиус атома уменьшается при движении снизу вверх по группе и слева направо по периоду. Поэтому последовательность элементов в порядке уменьшения радиуса атома следующая: галлий — фосфор — кислород. Ответ: 132. Ответ: 132 4. Задание 4 № 10767 Установите соответствие между формулой соединения и степенью окисления иода в этом соединении: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Решение. Степень окисления кислорода в подавляющем большинстве соединений равна −2, галогенов −1, водорода и щелочных металлов +1 (но водород в гидридах имеет степень окисления −1), щёлочноземельных металлов +2. Молекула электронейтральна, поэтому количество «+» равно количеству «−». Определим степени окисления элементов: А. Б. В. Ответ: 432. Ответ: 432 5. Задание 5 № 10831 Из предложенного перечня выберите два вещества с ионной химической связью: 1) 2) 3) 4) 5) Решение. Ковалентная неполярная связь образуется в молекулах между атомами одного элемента-неметалла. Металлическая связь присуща металлам. Ковалентная полярная связь присутствует в молекулах между атомами разных неметаллов. Ионная — между атомами металлов и неметаллов. А водородная присутствует между молекулами соединений, содержащих атом водорода, связанный с атомом с высокой электроотрицательностью Установим соответствие: 1. ковалентная полярная; 2. ковалентная полярная; 3. ионная; 4. ковалентная полярная; 5. ионная. Ответ: 35. Ответ: 35|53 6. Задание 6 № 5868 Какие два утверждения верны для характеристики как неона, так и криптона? 1) Электроны в атоме расположены на четырёх электронных слоях 2) Число нейтронов в ядре атома (наиболее распространённого изотопа) химического элемента равно 12 3) Число протонов в ядре атома химического элемента равно 20 4) Химический элемент относится к инертным газам 5) Соответствующее простое вещество существует в виде одноатомного газа Запишите в поле ответа номера выбранных утверждений. Решение. 1. Неон расположен во втором периоде Периодической системы Д. И. Менделеева и имеет 2 заселённых электронных слоя, а криптон — в четвёртом периоде и имеет 4 заселённых электронных слоя; 2. Число нейтронов в ядре изотопа неона-20 равно 10, а криптона-84 — 48; 3. Число протонов в ядре неона равно 10, а криптона — 36; 4. И неон, и криптон расположены в VIIIA группе Периодической системы Д. И. Менделеева и относятся к инертным газам; 5. Неон и криптон имеют завершённую валентную оболочку и их простые вещества представляют собой одноатомные газы. Ответ: 45. Ответ: 45|54 7. Задание 7 № 3593 Об азоте как о простом веществе сказано в следующем предложении. 1) Растениям нужен азот для построения молекул белков. 2) Молекула аммиака состоит из атомов азота и водорода. 3) С минеральными удобрениями азот вносится в почву. 4) Азотом наполняют электролампы. Решение. Только в утверждении № 4 об азоте говорится как о простом веществе. Правильный ответ указан под номером 4. Ответ: 4 8. Задание 8 № 10891 Из предложенного перечня выберите два вещества, которые не реагируют с водой: 1) оксид калия 2) оксид алюминия 3) оксид кремния(IV) 4) оксид кальция 5) оксид серы(IV) Решение. С водой не будут реагировать нерастворимые оксид кремния(IV) и оксид алюминия. Ответ: 23. Ответ: 23|32 9. Задание 9 № 934 Установите соответствие между реагирующими веществами и продуктами(-ом) их взаимодействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Решение. А. Б. В. Ответ: 524. Ответ: 524 10. Задание 10 № 129 Установите соответствие между формулой вещества и реагентами, с которыми это вещество может взаимодействовать.
Решение. Фосфор не будет реагировать с угарным газом, сульфатом натрия, гидроксидом меди(II). Правильный вариант ответа №3. Оксид железа(III) не будет реагировать с сульфатом натрия, кальцием и кислородом, цинком и гидроксидом меди. Правильный вариант ответа №1. Разбавленная серная кислота не будет реагировать с азотной кислотой, угарным газом, сульфатом натрия, кислородом. Правильный вариант ответа №4. Ответ: 314 11. Задание 11 № 1225 В уравнении реакции разложения нитрата меди(II) отношение коэффициента при 1) 1 2) 2 3) 4 4) 8 Решение. Ответ: 3 12. Задание 12 № 1264 Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Решение. A) Аммиак - бесцветный газ с резким запахом Б) Оксид азота (IV) бурый газ с неприятным запахом В) Углекислый газ - бесцветный газ без запаха Ответ: 421 13. Задание 13 № 6558 Какие две записи соответствуют процессу электролитической диссоциации? 1) 2) 3) 4) 5) Решение. Электролитическая диссоциация — процесс распада электролита на ионы при его растворении или плавлении. Ответ: 25. Ответ: 25|52 14. Задание 14 № 6775 Сокращённому ионному уравнению соответствуют две левые части схемы уравнения химической реакции 1) 2) 3) 4) 5) 6) Решение. Этому ионному уравнению соответствует реакция между растворимой солью цинка и растворимым основанием/ Ответ: 14. Ответ: 14|41 15. Задание 15 № 5902 Установите соответствие между схемой процесса и веществом-восстановителем в нём, происходящего в окислительно-восстановительной реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Решение. Восстановитель — это вещество, в состав которого входят атомы, отдающие электроны в результате химической реакции, следовательно, повышающие свою степень окисления. Определяем степень окисления каждого элемента и определяем в каком соединении элемент повышает свою степень окисления. А. Сера в сероводороде была -2, стала 0; Б. Алюминий был 0, стал +3; В. Сера в оксиде серы(IV) была +4, стала +6. Ответ: 134. Ответ: 134 16. Задание 16 № 10912 Из перечисленных суждений о влиянии антропогенных факторов на окружающую среду выберите одно или несколько верных. 1) Все опыты, связанные с выделением газов, надо проводить только в вытяжном шкафу. 2) При нагревании растворов необходимо направлять отверстие пробирки или колбы в сторону от лица и от соседей. 3) Вещества, находящиеся в лаборатории, запрещается пробовать на вкус, даже если они в обыденной жизни употребляются в пищу (например, хлорид натрия). 4) При попадании кислоты на кожу поражённое место надо промыть большим количеством раствора щёлочи. Запишите в поле ответа номер(а) верных суждений. Решение. 1. Нет, например, опыты с участием угольной кислоты в вытяжном шкафу проводить не обязательно. 2. Да, во избежание попадания содержимого пробирки или колбы на лицо экспериментатора или соседей при нагревании отверстия пробирки или колбы нужно направлять от лица и от соседей. 3. Да, потому что вещества используемые в химической лаборатории могут содержать примеси, токсичные для человека. 4. Нет, поражённое место надо промыть большим количеством воды и раствором гидрокарбоната натрия. Ответ: 23. Ответ: 23|32 17. Задание 17 № 855 Установите соответствие между двумя солями и реактивом, с помощью которого можно различить эти соли.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Решение. Соли аммония реагируют со щелочами (давая аммиак, который легко определить по запаху), а хлорид натрия нет. Растворимые галогениды с разными анионами легко можно различить по реакции с нитратом серебра — с фторидами она не идет, а бромид серебра светло-желтый. Карбонаты растворяются в сильных кислотах с выделением углекислого газа, а сульфаты нет. Ответ: 134 18. Задание 18 № 10952 Вычислите в процентах массовую долю кислорода в сульфате алюминия. Запишите число с точностью до целых. Сульфат алюминия — химическое соединение Решение. Формула сульфата алюминия: Ответ: 56. Ответ: 56 19. Задание 19 № 10988 Какая масса (в граммах) алюминия содержится в 20 г сульфата алюминия? Ответ запишите с точностью до десятых. Решение. Молярная масса сульфата алюминия Ответ: 3,2. Ответ: 3,2 20. Задание 20 № 1217 Используя метод электронного баланса, составьте уравнение реакции по схеме: Определите окислитель и восстановитель. Решение. 1) Составим электронный баланс: 2) Определим коэффициенты и составим уравнение реакции: 3) Укажем окислитель и восстановитель: окислитель — 21. Задание 21 № 438 Дана схема превращений: Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции. Решение. Написаны уравнения реакций, соответствующие схеме превращений: 1) 2) 3) Составлено сокращенное ионное уравнение 4) Комментарий Решу ЕГЭ: Растворение гидроксида алюминия в щёлочи с образованием тетрагидроксоалюмината натрия и его последующее термическое разложение допустимо. 22. Задание 22 № 87 Вычислите объём газа (н. у.), который выделится при действии избытка сульфида железа(II) на 490 г 10%-ного раствора серной кислоты. Решение. 1) Составим уравнение реакции: 2) Рассчитаем массу и количество вещества серной кислоты, содержащейся в растворе: 3) Определим объём сероводорода: по уравнению реакции Ответ: 11,2 л. 23. Задание 23 № 5956 Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства металлического цинка, и укажите признаки их протекания. Дан металлический цинк, а также набор следующих реактивов: водные растворы аммиака, гидроксида натрия, сульфата магния, соляной кислоты и нитрата калия. Решение. Элементы ответа: Составлены уравнения двух реакций, характеризующих химические свойства цинка, и указаны признаки их протекания: 1. 2. 24. Задание 24 № 6063 Подготовьте лабораторное оборудование, необходимое для проведения эксперимента. Проведите химические реакции между цинком и выбранными веществами в соответствии с составленными уравнениями реакции, соблюдая правила техники безопасности, приведённые в инструкции к заданию. Опишите изменения, происходящие с веществами в ходе проведённых реакций. Решение. Реакция 1: Цинк как металл, стоящий левее водорода в электрохимическом ряду активности металлов, реагирует с кислотами с образованием соответствующей соли и водорода. Наблюдается выделение бесцветного газа без запаха, издающего при поджигании хлопок. Реакция 2: Цинк как амфотерный металл реагирует с водными растворами щелочей с образованием комплексных соединений и выделением водорода. Наблюдается растворение цинка и выделение бесцветного газа без запаха, издающего при поджигании хлопок. |
