Задачи. Задача 26 Как влияет катализатор на величину энергии активации реакции и на равновесие
 Скачать 17.41 Kb. Скачать 17.41 Kb.
|
|
Задача №26 Как влияет катализатор на величину энергии активации реакции и на равновесие? Катализатор уменьшает энергию активации, изменяя механизм реакции, – она протекает через новые стадии, каждая из которых характеризуется невысокой энергией активации. Введение катализатора в равновесную систему не изменяет положение химического равновесия, так как катализатор в одинаковой мере увеличивает скорость прямой и обратной реакций. Однако роль катализаторов при проведении обратимых реакций очень высока. При низких температурах в силу малых скоростей прямой и обратной реакций, равновесие часто устанавливается очень медленно. Поэтому приходится ждать долгое время, чтобы добиться получения необходимых количеств продуктов реакции. Повышение температуры для этой цели не всегда приемлемо. Если реакция экзотермична, то равновесие сместится в сторону исходных веществ. Применение же катализатора позволяет ускорить наступление равновесия, не повышая температуры, и получить необходимые продукты реакции в нужном количестве. Задача №29 Имеют ли отношение фотохимические реакции к механизму действия зрительного анализатора? Ответ обоснуйте. Имеют отношение. Под воздействием световых лучей в фоторецепторах происходит распад зрительных пигментов (фотохимическая реакция) В результате выделяется энергия (возникает потенциал действия). Эта энергия передается на ганглиозные клетки (удаление помех, усиливает слабые контакты, воспринимает движение предметов). Отсюда нервный импульс переходит на нервные волокна, которые собираются со всей сетчатки в зрительный нерв (слепое пятно). Зрительные нервы перекрещиваются, и информация поступает в затылочные доли головного мозга, где происходит формирование зрительного образа. Задача №34 Какие теории катализа вам известны? Каковы основные положения этих теорий? Для объяснения механизма каталитических реакций были предложены три группы теорий: геометрические, электронные и химическая. В геометрических теориях основное внимание обращено на соответствие между геометрической конфигурацией атомов активных центров катализатора и атомов той части реагирующих молекул, которая ответственна за связывание с катализатором. Электронные теории исходят из представления, что хемосорбция обусловливается электронным взаимодействием, связанным с переносом заряда, т.е. эти теории связывают каталитическую активность с электронными свойствами катализатора. Химическая теория рассматривает катализатор как химическое соединение с характерными свойствами, которое образует химические связи с реагентами, в результате чего формируется нестабильный переходный комплекс. После распада комплекса с высвобождением продуктов катализатор возвращается в исходное состояние. Последняя теория считается сейчас наиболее адекватной. Для понимания механизма гомогенного катализа предложена теория промежуточных соединений. Сущность этой теории заключается в том, что если медленно протекающую реакцию А + В = АВ вести в присутствии катализатора К, то катализатор вступает в химическое взаимодействие с одним из исходных веществ, образуя непрочное промежуточное соединение: А + К = АК. Реакция протекает быстро, т.е. энергия активации этого процесса мала. Затем промежуточное соединение АК взаимодействует с другим исходным веществом, при этом катализатор освобождается: АК + В = АВ + К. Энергия активации этого процесса также мала, а поэтому реакция протекает с достаточной скоростью. Некоторые реакции могут катализироваться кислотами и основаниями. Согласно протонной теории кислот и оснований кислота – это соединение, способное отщеплять протон, основание – вещество, способное присоединять протон. В ходе катализа происходит перераспределение электронов в молекуле субстрата, возникают промежуточные соединения с повышенной активностью (карбониевые ионы, карбоанионы, полярные комплексы). При этом снижается энергия активации и ускоряется реакция. В основе объяснения механизма гетерогенного катализа лежит адсорбционная теория катализа. Согласно этой теории, молекулы реагирующих веществ адсорбируются поверхностью катализатора, ее так называемыми активными центрами. В результате на поверхности катализатора создается повышенная концентрация этих веществ; это отчасти также приводит к ускорению реакции. Но главной причиной возрастания скорости реакции является снижение энергии активации вследствие образования поверхностных промежуточных соединений. Известны также две теории ферментативного катализа (осуществляется при контакте субстрата с ферментом): - теория Фишера – фермент взаимодействует с субстратом по принципу полного пространственного и топографического соответствия (как ключ к замку); - гипотеза Кошленда – основана на принципе комплементарного взаимодействия фермента при контакте с субстратом (индукция соответствия). Также есть электронная теория катализа – она рассматривает структуру электронных уровней в твердых телах, энергию отрыва электрона от поверхности и другие параметры. Эти параметры зависят не от свойств отдельного атома, а от свойств всего твердого тела. Задача №65 Появление изотопов азота появляется при атомных взрывах. Один из таких изотопов имеет период полураспада 9,93 ч. Какая часть данного изотопа распадается через сутки после начала процесса? (0,81) Закон радиоактивного распада: 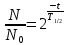 N0 – число радиоактивных ядер в начальный момент времени; N – число нераспавшихся ядер в момент времени t. 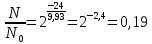 – доля нераспавшихся ядер. – доля нераспавшихся ядер. Доля распавшихся ядер: 1-0,19=0,81. Ответ: 0,81 Задача №80 Для определения срока годности порошка папаверина гидрохлорида проведено исследование по методике «ускоренного старения» и получены следующие результаты:
Определите срок годности порошка (время разложения 10% вещества) при температуре хранения 20 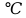 (1,22 года). (1,22 года).Сперва необходимо найти константу скорости разложения порошка папаверина гидрохлорида: 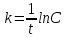 где t – время, сут (среднее значение из таблицы – 5 сут); C – концентрация (среднее значение из таблицы), равное отношению при соответствующих температурах. При 50 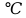 среднее значение: 99,52 среднее значение: 99,52При 80 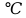 среднее значение: 99,06 среднее значение: 99,06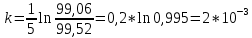 ч-1 ч-1Далее находим срок годности порошка: m=m0*e(-kt) m=0,9*m0, k=2*10-3, 0,9=e-2*10(-3)t ln(0,9)=-2*10-3t t=-0,0046/(-2*10-3t)=10687,2 ч=1,22 г. Ответ: 1,22 г. |
