Ответы по инфекционным болезням. ОТВЕТЫ - ИНФЕКЦИИ 3. 1. Аденовирусная инфекция, этиология, эпидемиология, патогенез, клиника, диагностика, лечение, профилактика
 Скачать 2.27 Mb. Скачать 2.27 Mb.
|
|
Схемы применения антибактериальных препаратов для терапии бубонной чумы 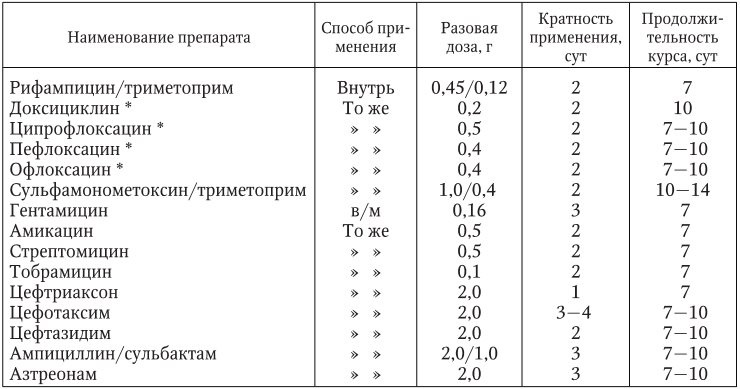 ** Выпускаются растворимые формы препаратов для парентерального введения. Таблица 14 Схемы применения антибактериальных препаратов для лечения легочной и септической форм чумы 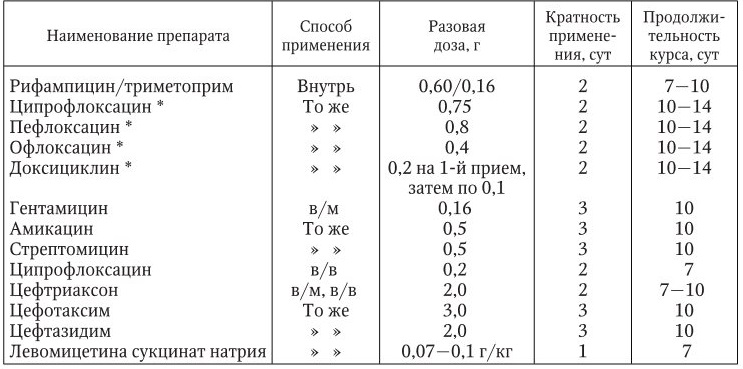 * Существуют инъекционные формы препаратов, предназначенные для внутривенного введения, с которых можно начинать лечение (2–3 дня с уменьшением дозы) с последующим переходом на прием внутрь (ступенчатая терапия). Таблица 15 Схемы применения комбинаций антибактериальных препаратов при лечении больных легочной и септической формами чумы 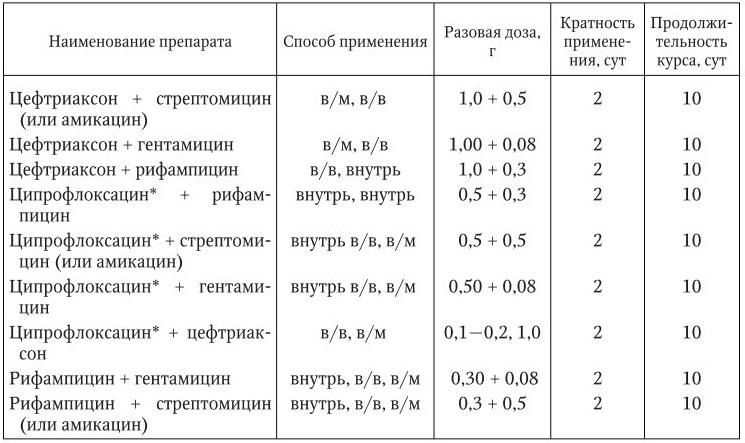 * Ципрофлоксацин можно заменить на офлоксацин (разовая доза – 0,2 г) или пефлоксацин (разовая доза – 0,4 г). Лечение больных можно начинать с внутривенного введения препаратов с последующим переходом на внутримышечные инъекции и прием внутрь (ступенчатая терапия). Нельзя назначать детям до 15 лет. Для повышения эффективности антибиотикотерапии и целенаправленного действия на чумных микробов используют определение чувствительности возбудителей чумы к антибиотикам. Наряду с антибактериальным лечением проводят дезинтоксикационную патогенетическую терапию, включающую введение дезинтоксикационных жидкостей, мочегонных средств (при задержке жидкости в организме), глюкокортикостероидов, сосудистых и дыхательных аналептиков, сердечных гликозидов, витаминов. По окончании терапии через 2 – 6 дней обязательно производят трехкратный бактериологический контроль пунктата из бубонов, мокроты, слизи из дыхательных путей и каловых масс. Выписка больных из стационара производится при полном клиническом выздоровлении и отрицательных результатах бактериологического контроля. Профилактика. В системе профилактики чумы основное и определяющее значение имеет эпидемиологический надзор, составной частью которого является слежение за эпизоотическим состоянием в природных очагах инфекции. Профилактика включает следующие мероприятия: – предупреждение заболеваний людей и возникновения вспышек в природных очагах; – предупреждение инфицирования лиц, работающих с зараженным или подозрительным на зараженность чумой материалом; – предупреждение завоза чумы на территорию страны из‑за рубежа; – профилактическая вакцинация групп риска. Меры по предупреждению заражения людей чумой в энзоотичных районах, лиц, работающих с больными особо опасными инфекциями или их возбудителями, а также по предупреждению выноса инфекции за пределы очагов в другие районы страны осуществляются противочумными и другими учреждениями здравоохранения. Лица, подозрительные на заболевание чумой, должны быть немедленно изолированы и госпитализированы. В очаге инфекции вводится карантин. Подвергшиеся риску заражения подлежат изоляции и наблюдению в течение 6 дней (срок инкубационного периода), а также экстренной профилактике (превентивному лечению). Утверждена схема экстренной профилактики (табл. 16). Таблица 16 Схемы применения антибактериальных препаратов при экстренной профилактике чумы 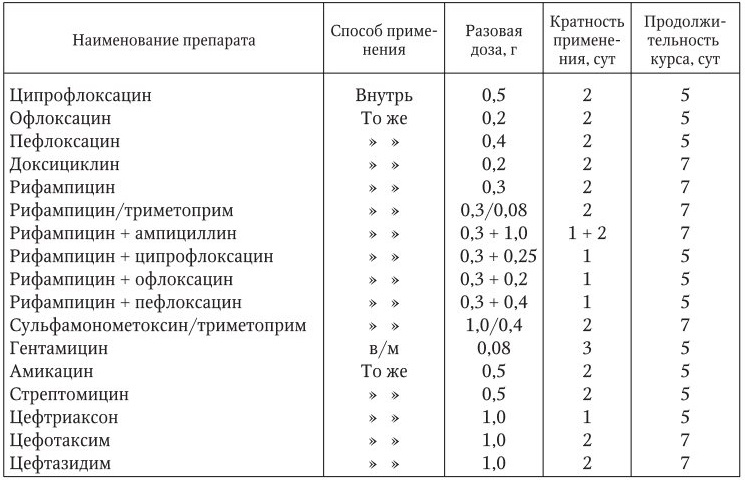 Работа в госпиталях для больных чумой проводится в специальных защитных костюмах с соблюдением строгого порядка надевания и снятия защитного костюма. В очагах чумы по эпидемическим показаниям в первую очередь проводится профилактическая вакцинация контингентов высокого риска заражения (пастухи, охотники, геологи, работники противочумных учреждений). Показанием к проведению на территории природных очагов чумы вакцинопрофилактики являются эпизоотические или эпидемические проявления. В зависимости от конкретной эпизоотической или эпидемической обстановки вакцинацию проводят на строго определенной территории. Руководители противочумных учреждений определяют необходимость вакцинопрофилактики всего населения или отдельных групп, подверженных повышенному риску заражения. Они определяют сроки вакцинации с учетом сезонов активизации эпизоотической активности очага, сроков охотопромысла на носителей возбудителя чумы и других моментов. Решение о проведении вакцинопрофилактики принимает санитарно‑противоэпидемическая комиссия. Ревакцинацию проводят через 12 мес. после первой прививки, в особо тяжелых эпидемических условиях – через 6 мес. Ревакцинация населения отменяется по прекращении эпизоотии, угрожаемых контингентов – спустя один год после прекращения эпизоотии. Основным методом вакцинации является накожный. Целесообразно использовать безыгольный инъектор БИ‑3М (с противоинфекционным протектором). В случае необходимости проведения массовой специфической профилактики населения для защиты от легочной чумы с воздушно‑капельным механизмом передачи возбудителя целесообразно использовать ингаляционный метод согласно нормативным документам. С этой целью применяется живая вакцина, приготовленная из штамма EV чумных бактерий. Вакцину применяют накожно или внутрикожно. После вакцинации создается относительный иммунитет продолжительностью до 6 мес. Заболеваемость в результате вакцинации снижается, но случаи чумы среди привитых возможны. 77.Эндемический или крысиный сыпной тиф, Этиология. Эпидемиология. Патогенез. Клиника. Диагностика. Лечение. Профилактика. Эндемический сыпной тиф (Rickettsiosis endemica murina ) (син.: блошиный сыпной тиф, средиземноморский крысиный риккетсиоз, маньчжурский эндемический тиф, индийский тиф, корабельный тиф) – острое заболевание, обусловленное риккетсиями Музера, характеризуется высокой лихорадкой и распространенной розеолезно папулезной сыпью. Этиология. Возбудитель – R. typhi (mooseri ) – по своим морфобиологическим, биологическим и антигенным свойствам очень близок к риккетсиям Провачека. Они отличаются видоспецифическим термолабильным антигеном, который определяет их серологическую дифференциацию. Эпидемиология. Эндемический сыпной тиф – зооноз, его резервуаром являются мелкие дикие грызуны (серые крысы, черные крысы и мыши) и их эктопаразиты – блохи и гамазовые клещи. Переносят риккетсий крысиные блохи – Xenopsylla cheopis , выделяющие риккетсии с испражнениями, могут служить переносчиками и человеческие блохи (Pulex irritans ), и крысиный клещ (Bdelonyssus bacoti ), способный к трансовариальной передаче R. mooseri. Человек заражается алиментарным путем через продукты, загрязненные мочой больных грызунов, а также при втирании в поврежденную кожу и слизистые оболочки инфицированных риккетсиями фекалий переносчиков или аэрогенно – при вдыхании воздуха со взвешенным инфицированным материалом. От человека к человеку R. mooseri не передаются. Эндемический сыпной тиф чаще встречается в портовых городах и регионах, где имеется большое количество грызунов – резервуар возбудителя. Заболевание наиболее распространено в прибрежных городах Северной и Южной Америки, Индии, Австралии, в виде спорадических случаев регистрировалось в бассейнах Черного, Балтийского и Каспийского морей. В России эндемический сыпной тиф не регистрируется. Патогенез и патологоанатомическая картина . Сходные по антигенной структуре и биологическим свойствам возбудители эпидемического и эндемического сыпного тифа определяют общие черты патогенеза этих двух родственных заболеваний, но вызванный риккетсиями Музера патологический процесс идет менее выражено. Так как эндемический сыпной тиф имеет благоприятный исход, патологоанатомическая картина изучена недостаточно. После перенесенного эндемического сыпного тифа развивается стойкий гомологичный иммунитет, выявляются антитела не только к риккетсиям Музера, но и к риккетсиям Провачека, однако их титр на порядок ниже. Клиническая картина. Инкубационный период колеблется от 5 до 15 дней. Начало заболевания, как правило, острое. Клиническая картина болезни во многом схожа с таковой при эпидемическом сыпном тифе, но по тяжести ближе не к классическому его варианту, а к болезни Брилля. Лихорадка у больных, не находящихся на антибиотикотерапии, имеет продолжительность 8 – 12 сут, хотя возможны варианты укороченной лихорадки до 3 дней или удлиненной до 3 нед. Температурная реакция постоянного или ремиттирующего типа. Лихорадка сопровождается головной болью, снижением аппетита, астенией, миалгиями. На 4 – 7 й день болезни у 3/4 больных появляется обильная розеолезная или розеолезно папулезная сыпь, локализующаяся на груди, животе, конечностях, в том числе на ладонной и подошвенной поверхностях и на лице. Сыпь исчезает через 7 – 10 дней, не оставляя следа. В клинической картине редко встречаются такие проявления поражения нервной системы, как status typhosis , бред, менингеальные явления. Как правило, печень и селезенка не увеличены. При анализе крови сначала определяется лейкопения, затем – лейкоцитоз с лимфоцитозом. Осложнений и рецидивов заболевания не наблюдается, прогноз благоприятный. Диагностика. Заболевание диагностируется на основании оценки клинической картины, эпидемиологических и лабораторных данных. Обязательна верификация диагноза серологическими методами (РСК и РНГА) с антигенами из R. typhi и R. prowazekii . Только отчетливое преобладание титра антител в реакции с антигеном из R. typhi (mooseri ) по сравнению с антигеном из R. prowazekii позволяет разграничить эти заболевания. Дифференцировать в первую очередь необходимо с легкими и средней тяжести формами эпидемического сыпного тифа. Лечение во многом аналогично терапии больных эпидемическим сыпным тифом. Применяют тетрациклин по 0,2 г 4 раза в сутки или левомицетин в течение 4 – 5 дней. Профилактика. Так как больной эндемическим сыпным тифом не опасен для окружающих, он, как правило, обязательной госпитализации не подлежит. Профилактика направлена на уничтожение источников инфекции путем дератизации и дезинсекции, на охрану пищевых продуктов от загрязнения выделениями грызунов. Специфической профилактики нет. 78.Энтеровирусная инфекция. Этиология. Эпидемиология, патогенез, патологическая анатомия, клиника, диагностика, лечение, профилактика. Энтеровирусный гастроэнтерит – острое вирусное заболевание, вызываемое энтеровирусами, входящими в семейство Picornaviridae , род Picornaviruses . Этиология. Возбудители энтеровирусного гастроэнтерита – группа кишечных вирусов (размножаются в кишке и выделяются из организма с фекалиями) рода Enterovirus , семейства Picornaviridae (pico – маленький). Род энтеровирусов объединяет полиовирусы (3 серовара), которые являются возбудителями полиомиелита, вирусы Коксаки А (24 серовара), Коксаки В (6 сероваров) и ECHO (34 серовара), а также 5 энтеровирусов человека (табл. 40). Наиболее доказана этиологическая роль вирусов Коксаки А 18, 20, 21, 22, 24 и ECHO 11, 14, 18. Вспышки энтеровирусного гастроэнтерита чаще бывают локальными. Вирионы энтеровирусов имеют размер 15 – 35 нм, относятся к группе РНК содержащих вирусов. Они устойчивы в окружающей среде, резистентны к низким температурам, устойчивы к замораживанию и оттаиванию (в фекалиях при низкой температуре сохраняют жизнеспособность более полугода). Также устойчивы к 70 % раствору этанола, 5 % раствору лизола. В сточных водах, мелких водоемах могут сохраняться до 1,5 – 2 мес. Вирусы чувствительны к высушиванию, при комнатной температуре сохраняются до 15 сут. При температуре 33 – 35 °C погибают в течение 3 ч, при температуре 50 – 55 °C – в течение нескольких минут и мгновенно при кипячении и автоклавировании. Быстро погибают под воздействием дезинфицирующих средств. Эпидемиология. Источник инфекции – больной человек и вирусоносители, число последних чрезвычайно велико, особенно среди детей дошкольного возраста. Во внешнюю среду возбудители поступают с фекалиями и носоглоточным секретом, обеспечивая широкое инфицирование воды, предметов домашнего обихода, продуктов питания и др. Основной механизм передачи возбудителя – фекально оральный, а пути передачи – водный и алиментарный. Хотя наиболее интенсивно вирус выделяется в первые дни болезни, но в ряде случаев энтеровирусы могут выделяться в течение нескольких месяцев. Факторами передачи чаще становятся вода, овощи, реже молоко и другие пищевые продукты. Заражение возможно при купании в водоемах, контаминированных энтеровирусами. Вирус может передаваться через грязные руки, игрушки. Не исключен воздушно капельный путь передачи и трансплацентарная передача энтеровирусов от больной матери плоду. Восприимчивость высокая. Часто наблюдаются групповые заболевания в детских учреждениях, возможны семейные вспышки. Бессимптомное вирусоносительство встречается часто у детей младшего возраста. После перенесенной энтеровирусной инфекции вырабатывается стойкий типоспецифический иммунитет. Энтеровирусная инфекция распространена повсеместно. Во всех странах мира встречаются спорадические случаи болезни, вспышки и эпидемии энтеровирусной инфекции. Миграции людей, широкое распространение туризма приводят к распространению в коллективах новых штаммов энтеровирусов, к которым у людей нет иммунитета. Клиническая картина включает в себя синдром интоксикации, сопровождающийся внезапным повышением температуры тела до 38 – 39 оС, и синдром гастроэнтерита (несильные боли в животе, тошнота, рвота, нечастый, но обильный водянистый стул без патологических примесей, нередко со зловонным запахом и зеленоватого цвета, обычно не чаще 4 – 6 раз в сутки). При пальпации живота определяются небольшое вздутие, урчание. У 1/3 больных увеличивается печень. Течение в подавляющем большинстве случаев нетяжелое, общая продолжительность заболевания 1 – 3 дня. Прогноз в большинстве случаев благоприятный. Энтеровирусная инфекция часто протекает без кишечных проявлений в форме серозных менингитов, энцефалитов, миокардитов и миокардиодистрофий, эпидемической миалгии, герпангины и др. Диагностика. Диагноз острых кишечных инфекций вирусной природы базируется на клинической картине заболевания (особенно важно сочетание синдрома гастроэнтерита и поражения верхних дыхательных путей), учете эпидемиологических данных и исключении бактериальной природы заболевания. Лабораторно диагноз подтверждается обнаружением энтеровирусов в испражнениях методами ПЦР, ИФА, иммунофлуоресценции. Лечение. Лечение больных вирусной диареей принципиально не отличается от комплексной терапии больных другими острыми кишечными инфекциями, в частности ротавирусной инфекции. Профилактика. Проводят дезинфекционные мероприятия – заключительную и текущую дезинфекцию препаратами, обладающими вирулицидной активностью. Для организации текущей дезинфекции экспозицию препаратов увеличивают в 2 раза. При необходимости вводится гиперхлорирование питьевой воды, подаваемой населению, в учреждениях (детских, ЛПУ) устанавливается питьевой режим с обязательным кипячением воды или раздачей бутилированной воды. При эпидемических вспышках вводится усиление надзора за системой водоснабжения, организацией питания, содержанием территории, соблюдением режима детских организованных коллективов и лечебно профилактических учреждений. Одним из методов экстренной профилактики энтеровирусной инфекции является применение аттенуированной оральной полиомиелитной вакцины. Принцип ее действия основан на быстром (2 – 3 дня) заселении кишечника у детей в возрасте от одного года до 14 лет вакцинным полиовирусом и, как следствие, вытеснении из циркуляции других энтеровирусов. Вакцинация по эпидемическим показаниям проводится однократно, независимо от ранее проведенных профилактических прививок против полиомиелита. 79. Эпидемический возвратный тиф. Этиология. Эпидемиология, патогенез, клиника, диагностика, лечение, профилактика. Тиф возвратный вшивый (Typhus recurrens ) (син.: вшивый возвратный тиф, эпидемический (вшивый) возвратный тиф; возвратная лихорадка, возвратный спирохетоз) – острое инфекционное заболевание, вызываемое спирохетами с трансмиссивным механизмом передачи возбудителя, характеризуется острым началом, приступообразной лихорадкой, общей интоксикацией, увеличением печени и селезенки. В настоящее время в нашей стране не регистрируется. Этиология. Возбудителем является спирохета Borrelia recurrentis Obermeieri , она относится к семейству Treponemataceae , роду Borrelia , имеет длину 20 – 40 мкм, толщину 0,3 – 0,4 мкм и извитое тело с 5 – 6 завитками. Боррелии способны к поступательным, вращательным и сгибательным движениям, грамотрицательны, хорошо окрашиваются анилиновыми красителями. Боррелии патогенны для белых мышей, крыс, обезьян. Растут на питательных средах, содержащих асцитическую жидкость или сыворотку и кусочки тканей, и на развивающихся куриных эмбрионах, строгие аэробы. Чувствительны к пенициллину, антибиотикам тетрациклиновой группы, левомицетину, эритромицину. Эпидемиология. Тиф возвратный эпидемический – антропонозная трансмиссивная инфекция, единственный источник и резервуар возбудителя – больной человек. Переносчиками служат платяные вши (головные и лобковые большого эпидемиологического значения не имеют), которые могут передавать инфекцию через 5 дней после заражения и сохраняют способность заражать в течение 4 нед. Предполагается участие носителей спирохет в поддержании популяции возбудителя. Заражение человека возвратным эпидемическим тифом происходит в результате втирания в кожу гемолимфы раздавленных вшей при расчесывании места укуса насекомого. Возможно заражение вследствие попадания гемолимфы вшей на слизистые оболочки. Патогенез. После проникновения в организм спирохеты интенсивно размножаются в клетках системы мононуклеарных фагоцитов. Затем спирохеты поступают в кровь, возникают спирохетемия и токсемия, определяющие начало клинических проявлений болезни. Под воздействием антител образуются агрегаты из спирохет, нагруженных тромбоцитами, которые задерживаются в капиллярах и вызывают расстройство микроциркуляции во внутренних органах. Тяжесть состояния больного и повреждений органов и тканей зависит от количества циркулирующих спирохет. Может развиться тромбогеморрагический синдром. В ответ на инфекцию в организме синтезируются антитела, под влиянием которых основная масса спирохет погибает, наступает период апирексии. Но небольшое количество спирохет нового антигенного варианта сохраняется в крови или в тканях. Этот антигенный вариант образуется спонтанно при генетических мутациях. Спирохеты нового антигенного варианта размножаются и примерно через 7 дней количество достигает уровня, достаточного для развития нового приступа. Морфологические изменения наиболее четко выражены в селезенке, печени, костном мозге. Селезенка значительно увеличена, капсула ее уплотнена, часто с разрывами и фибринозными наложениями. Пульпа селезенки переполнена кровью, в ней определяются многочисленные милиарные некрозы, а иногда и инфаркты. В очагах некроза обнаруживаются спирохеты. Печень увеличена, в ее паренхиме обнаруживаются некротические очаги, мелкие очаги некроза имеются и в костном мозге. В почках отмечается картина паренхиматозного нефрита с поражением эпителиальных клеток извитых канальцев. В миокарде, эндокарде и нервных узлах сердечной мышцы выявляются дистрофические изменения, возможно развитие очагов некроза. В динамике инфекционного процесса формируется иммунитет против нескольких рас спирохет, происходит их элиминация и наступает клиническое выздоровление. Клиническая картина. Инкубационный период колеблется от 3 до 14 дней (чаще 7 – 8 дней). В клинической картине заболевания характерно чередование лихорадочных приступов с периодами апирексии. Болезнь может протекать в легкой, средней тяжести и тяжелой формах. Приступ заболевания чаще начинается остро, обычно в первую половину дня. У больного появляется озноб, иногда потрясающий, сменяющийся затем ощущением жара, головная боль. Температура тела уже в 1 й день болезни поднимается до 39 °C и выше, достигая максимума на 2 – 3 й день болезни. Больные жалуются на боли в мышцах, особенно нижних конечностей, резкую слабость, тошноту, нередко появляется рвота. Характерен внешний вид больного: кожа лица гиперемирована, склеры инъецированы. В дальнейшем гиперемия лица сменяется его бледностью, что обусловлено анемией. Иногда появляются высыпания на коже в виде розеол, петехий, крупнопятнистых элементов. При обследовании выявляются выраженная тахикардия, понижение артериального давления, глухость сердечных тонов. Частота пульса достигает 140 – 150 уд./мин. Выявляется увеличенная печень, нередко развивается желтуха. У больных отсутствует аппетит; может быть тошнота, рвота, понос. Язык сухой, покрыт белым или желтоватым налетом. За счет увеличения селезенки в первые дни болезни возможны тупые боли в левом подреберье. Болезненность селезенки выражена на высоте приступа и обусловлена переполнением ее кровью; продолжительная болезненность может быть вызвана развитием периспленита или (иногда) инфаркта. Первый приступ продолжается чаще всего 5 – 8 дней, после чего следует безлихорадочный период длительностью 7 – 14 дней; за ним возникают новые приступы с безлихорадочными интервалами. Всего бывает не более пяти лихорадочных приступов, причем каждый последующий приступ короче предыдущего, а период апирексии, наоборот, продолжительнее. К концу каждого приступа в течение 4 – 6 ч происходит критическое снижение температуры с обильным потоотделением. Иногда падению температуры предшествует предкритический ее подъем с ухудшением общего состояния больного, усилением болей и тахикардии. При первом лихорадочном приступе температурная кривая всегда постоянного типа, при повторных приступах она может быть постоянной, ремиттирующей и неправильной. У 10 – 15 % больных на высоте приступа появляются менингеальные симптомы. Гемограмма характеризуется нейтрофильным лейкоцитозом со сдвигом формулы влево, анэозинофилией и тромбоцитопенией. При анализе в моче обнаруживаются повышенное содержание белка, выщелоченные эритроциты, лейкоциты, небольшое количество гиалиновых цилиндров. Во время приступов выявляется олигурия с высокой (а после кризиса – полиурия с низкой) относительной плотностью мочи. Осложнения. При возвратном тифе в качестве осложнения в основном выступают менингиты, ириты, иридоциклиты, увеиты, разрыв селезенки, синовииты. Прогноз при эпидемическом сыпном тифе благоприятный, при своевременном лечении летальность не превышает 1 %, до введения в практику антибиотиков летальность достигала 30 % и выше. Диагностика. Диагноз возвратного эпидемического тифа устанавливают по данным клинической картины: острое начало, лихорадка, критическое падение температуры тела с обильным потоотделением в конце приступа, раннее и значительное увеличение селезенки, увеличение печени, выраженный общетоксический синдром, появление рецидивов лихорадки у больных из эпидемического очага инфекции. Дифференциальный диагноз проводят с малярией, гриппом, лептоспирозом, брюшным и сыпным тифами, эндемическим возвратным тифом, крупозной пневмонией, сепсисом. Лабораторная диагностика включает обнаружение спирохет в толстой капле и мазках крови, взятых на высоте лихорадочной реакции, окрашенных по Романовскому – Гимза. Лечение. Больные подлежат обязательной госпитализации в инфекционный стационар. Назначают пенициллин (500 000 ЕД через 4 ч в течение 5 – 7 дней), левомицетин (по 0,5 г через 6 ч в течение 5 – 7 дней), ампициллин (по 1 г через 6 ч в течение 7 дней), тетрациклиновые препараты (по 0,3 – 0,4 г через 6 ч в течение 5 – 7 дней). С учетом степени тяжести болезни применяют инфузионную дезинтоксикационную и симптоматическую терапию, проводят лечение осложнений. Разрыв селезенки требует срочного оперативного лечения. Диспансеризация. Реконвалесцентов выписывают не ранее 15 дней после последнего приступа. После выписки за ними ведется медицинское наблюдение с термометрией в течение 2 нед. Профилактика. Во время эпидемий осуществляется выявление и госпитализация всех лихорадящих больных. Контактные лица подвергаются санитарной обработке, и за ними устанавливается медицинское наблюдение с ежедневной термометрией в течение 25 дней после госпитализации. В целях ликвидации педикулеза в очагах инфекции по эпидемическим показаниям обязательно проводится санитарная обработка всего населения. |
