1. Количественный анализ бывает
 Скачать 1.01 Mb. Скачать 1.01 Mb.
|
|
Порог коагуляции – наименьшая концентрация электролита, достаточная для того, чтобы вызвать коагуляцию золя.
Коагуляцию вызывают различные факторы: механическое воздействие, изменение температуры (кипячение и вымораживание), излуче-ние, посторонние вещества, особенно электролиты, время (старение), концентрация дисперсной фазы. http://vmede.org/sait/?id=Obwaja_himija_jolina_2012&menu=Obwaja_himija_jolina_2012&page=16
Белки — это биополимеры, мономерами которых являются аминокислоты.Аминокислоты представляют собой низкомолекулярные органические соединения, содержащие карбоксильную (-СООН) и аминную (-NH2) группы, которые связаны с одним и тем же атомом углерода. К атому углерода присоединяется боковая цепь — какой-либо радикал, придающий каждой аминокислоте определенные свойства. Липи́ды (от греч. λίπος, lípos — жир) — обширная группа природных органических соединений, включающая жиры и жироподобные вещества. Молекулы простых липидов состоят из спирта и жирных кислот, сложных — из спирта, высокомолекулярных жирных кислот и других компонентов. Содержатся во всех живых клетках Углеводы — органические соединения, состоящие из углерода, водорода и кислорода. Различают простые углеводы, или моносахариды, например глюкоза, и сложные, или полисахариды, которые делятся на низшие, содержащие немного остатков простых углеводов, например дисахариды, и высшие, имеющие очень большие молекулы из многих остатков простых углеводов. В животных организмах содержание углеводов составляет около 2% сухой массы. http://www.polnaja-jenciklopedija.ru/biologiya/uglevody.html
Белки́ (протеи́ны, полипепти́ды[1]) — высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединённых в цепочку пептидной связью . В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Функции белков в клетках живых организмов более разнообразны, чем функции других биополимеров — полисахаридов и ДНК. Так, белки-ферменты катализируют протекание биохимических реакций и играют важную роль в обмене веществ. Некоторые белки выполняют структурную или механическую функцию, образуя цитоскелет, поддерживающий форму клеток. Также белки играют ключевую роль в сигнальных системах клеток, при иммунном ответе и в клеточном цикле.Белки обладают свойством амфотерности, то есть в зависимости от условий проявляют как кислотные, так и осно́вные свойства. Белки различаются по степени растворимости в воде. Водорастворимые белки называются альбуминами, к ним относятся белки крови и молока. К нерастворимым, или склеропротеинам, относятся, например, кератин. Денатурацией белка называют любые изменения в его биологической активности и/или физико-химических свойствах, связанные с потерей четвертичной, третичной или вторичной структуры (см. раздел «Структура белка»). Как правило, белки достаточно стабильны в тех условиях (температура, pH и др.), в которых они в норме функционируют в организме[9]. Резкое изменение этих условий приводит к денатурации белка. https://ru.wikipedia.org/wiki/%C1%E5%EB%EA%E8#.D0.A4.D0.B8.D0.B7.D0.B8.D0.BA.D0.BE-.D1.85.D0.B8.D0.BC.D0.B8.D1.87.D0.B5.D1.81.D0.BA.D0.B8.D0.B5_.D1.81.D0.B2.D0.BE.D0.B9.D1.81.D1.82.D0.B2.D0.B0
Углеводы – очень широко распространённый в живой природе класс органических молекул. В зависимости от состава и строения они могут выполнять две главные функции:
Химическое определение углеводов
Следовательно, углеводы – это бифункциональные молекулы, а именно:
Классификация углеводов По сложности молекулы углеводов делят на три группы:
Пространственная или стереоизомерия моносахаридов Асимметрическим называется атом углерода, который соединён с четырьмя разными атомами или группами атомов Все моносахариды, за исключением диоксиацетона, содержат асимметрические атомы углерода. Конфигурация таких атомов в пространстве может быть различной и, в результате, моносахариды могут существовать в двух изомерных формах. Разберём образование таких изомеров на примере самой простой молекулы углевода – глицеринового альдегида. Пространственная конфигурация глицеринового альдегида 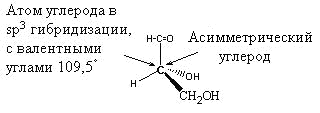 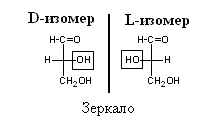 2 изомерные молекулы глицеринового альдегида, являющиеся зеркальным отражением друг друга D-изомеры – гидроксил асимметрического углерода расположен справа от вертикальной цепи; L-изомеры – гидроксил расположен слева от вертикальной цепи 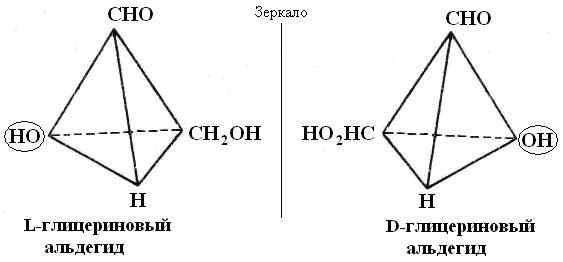 Рис. 2-2. Стереоизомеры глицеринового альдегида Кольчато-цепная таутомерия. Явление мутаротации Моносахариды представляют собой кристаллы, очень хорошо растворимые в воде. В кристаллической форме они находятся в виде кольца, чаще всего – β-аномера, наиболее термодинамически выгодной формы. При растворении β-кольцо раскрывается, превращаясь в цепную структуру, затем опять образуется кольцо, причём не только β-форма, но и α-форма. В течение некоторого времени между всеми тремя структурами устанавливается равновесие. После установления равновесия в растворе будут присутствовать цепная форма моносахарида (очень немного), β-аномер и α-аномер. Эти три изомера, находящиеся в равновесии, называют таутомерами, а само явление установления равновесия между ними – кольчато-цепной таутомерией. В приведённом ниже примере использована молекула глюкозы. 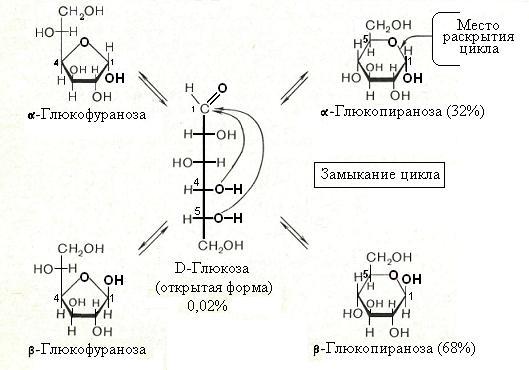 Рис. 2-9. Кольчато-цепная таутомерия глюкозы При образовании равновесной таутомерной смеси могут возникать кольцевые формы, различающиеся также размерами цикла (пиранозы и фуранозы). Взаимный переход различных кольцевых структур возможен только через промежуточную, открытую, оксо-форму моносахарида. В свежеприготовленных растворах моносахаридов кольчато-цепную таутомерию можно наблюдать по явлению мутаротации. Оно заключается в том, что во время установления равновесия между всеми таутомерными формами, происходит изменение угла вращения плоскости поляризации света. Это изменение объясняется тем, что у каждой таутомерной формы угол вращения плоскости поляризации – свой. После установления равновесия угол поворота становится постоянным.
Химические свойства моносахаридов Реакционная способность углеводов-моносахаридов определяется наличием в их молекуле нескольких реакционных центров.
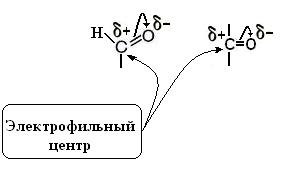 Этот центр присутствует только в цепной, развёрнутой форме моносахаридов Для электрофильного центра характерны реакции нуклеофильногоприсоединения Примеры реакций нуклеофильного присоединения:
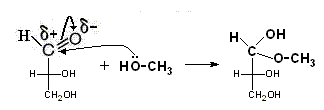
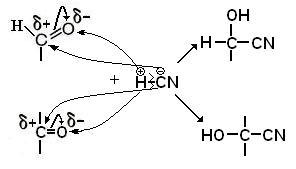
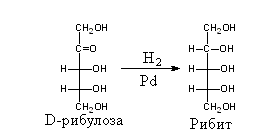
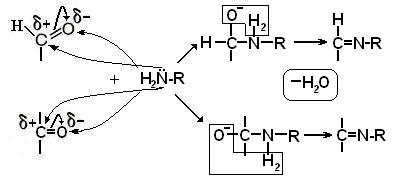
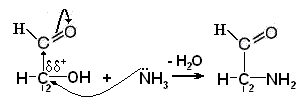 Электрофильный центр у С2 более слабый, чем центр у карбонильного углерода. С ним может реагировать только такой сильный нуклеофил, как азот в аммиаке Аминосахара – производные моносахаридов, имеющие большое значение при образовании гетерополисахаридов
Реакции по спиртовым гидроксилам могут проходить с любой формой моносахаридов – и с развёрнутой цепью, и с циклической молекулой. Примеры реакций по спиртовым гидроксилам
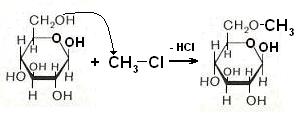 Реакция получения простых эфиров может проходить по любому из спиртовых гидроксилов
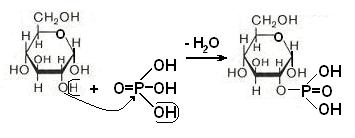 Фосфорно-кислые эфиры моносахаридов – производные, участвующие в метаболизме углеводов в живых клетках
В альдозах-моносахаридах есть две химические группы, способные окисляться. Первая – это альдегидная группа, которая может окислиться такими слабыми окислителями как бромная вода, реактив Толленса (аммиачный раствор оксида серебра), гидроксид меди (II) или холодный водный раствор перманганата калия. 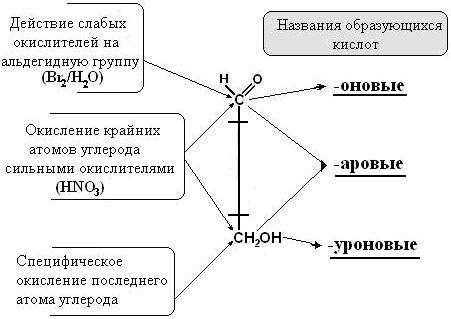 Глюконовая кислота используется для получения растворимой формы кальция Глюкуроновая кислота образуется в клетках печени из глюкозы, участвует в процессах обезвреживания Рис. 2-10. Схема окисления моносахаридов альдоз Вторая группа – это концевой спиртовый гидроксил, который можно окислить более сильными окислителями. При этом сначала надо защитить от окисления альдегидную группу. Третий вариант окисления наблюдается при действии сильного окислителя (например, азотной кислоты) на обе окисляемые группы. Образующиеся при окислении кислоты различаются по названиям. У каждого типа кислоты в названии своё окончание (см. рис. 2-10). Моносахариды кетозы не окисляются слабыми окислителями (бромная вода и другие), и это их отличает от альдоз.
В результате этих реакций могут образовываться различные гликозиды (О-, N-, или S-гликозиды). Реакция лежит в основе образования всех сложных углеводов. Пример образования О-гликозида D-фруктозы. Реакция идёт в присутствии кислого катализатора. 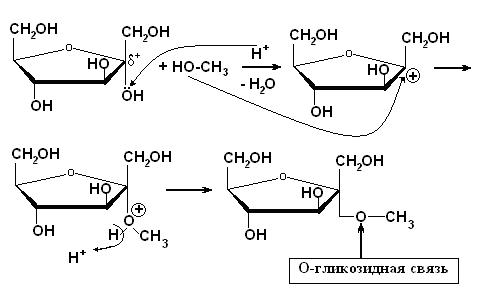 Свойства гликозидов.
Изображение кольцевых форм моносахаридов по правилам Хеуорса.
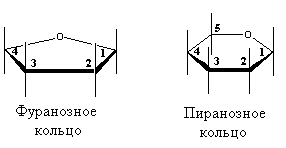
На примере рибозы: 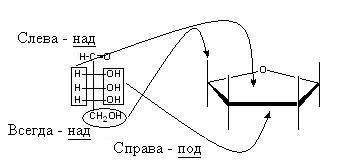 Рис. 2-7. Иллюстрация правил Хеуорса
Таким образом, молекула глюкозы, изображенная в форме Хеуорса, будет выглядеть так: 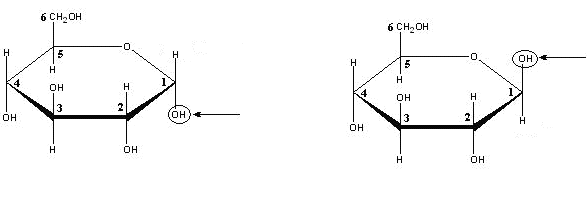 β-аномер α-аномер Рис. 2-8. D-Глюкоза-пираноза
Все дисахариды можно разделить по способности окисляться, восстанавливая окислитель, на восстанавливающие и не восстанавливающие. Восстанавливающие дисахариды Целлобиоза – дисахаридный фрагмент цепей целлюлозы. В свободном виде не встречается. Состоит из 2-х остатков β-глюкозы Мальтоза – солодовый сахар – фрагмент молекулы крахмала. Содержится в солоде – продукте расщепления зерна. Состоит из 2-х остатков α-глюкозы Лактоза – молочный сахар – основной углевод любого молока. Состоит из остатка β-галактозы и остатка α-глюкозы 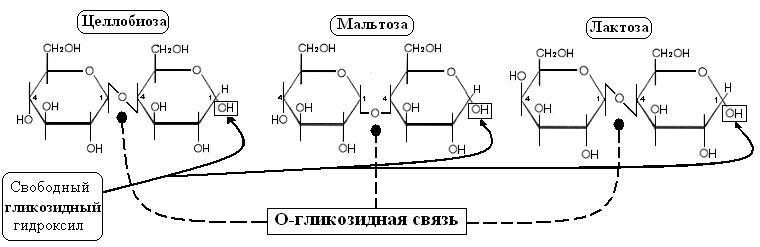 По месту свободного гликозидного гидроксила кольца могут раскрываться. Поэтому эти дисахариды обладают восстанавливающими свойствами В названии связи указывают конфигурацию гликозидного гидроксила (α или β) и номера атомов, образующих эту связь Целлобиоза Мальтоза Лактоза β-1,4 α-1,4 β-1,4 Невосстанавливающие дисахариды Сахароза – свекловичный или тростниковый сахар – основной углевод растительных клеток. Состоит из остатка α-глюкозы и остатка β-фруктозы 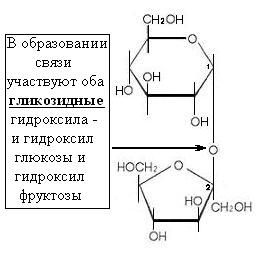 Сахароза не обладает восстанавливающими свойствами, потому что кольца не могут разворачиваться (нет свободных гликозидных гидроксилов) Связь – α-1, β-2-О-гликозидная Свойства дисахаридов
28.Крахмал (С6Н10О5)n – резервное питательное вещество растений – содержится в семенах, клубнях, корнях, листьях. Например, в картофеле – 12–24% крахмала, а в зернах кукурузы – 57–72%. Крахмал представляет собой смесь двух полисахаридов, различающихся строением цепи молекулы, – амилозы и амилопектина. В большинстве растений крахмал состоит из 20–25% амилозы и 75–80% амилопектина. Полный гидролиз крахмала (как амилозы, так и амилопектина) приводит к D-глюкозе. При мягких условиях можно выделить промежуточные продукты гидролиза – декстрины – полисахариды (С6Н10О5)m с меньшей молекулярной массой, чем крахмал (m < n), олигосахариды, а также дисахарид мальтозу. 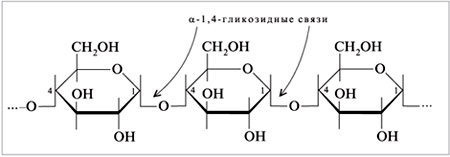 Гликоген (животный крахмал) образуется в печени и мышцах животных и играет важную роль в обмене углеводов в животных организмах. Гликоген – белый аморфный порошок, растворяется в воде с образованием коллоидных растворов, при гидролизе дает мальтозу и D-глюкозу. Подобно амилопектину, гликоген является нелинейным полимером D-глюкозы с -1,4- и -1,6-гликозидными связями. Каждая ветвь содержит 12–18 звеньев глюкозы. Однако гликоген имеет меньшую молекулярную массу и еще более разветвленное строение (примерно 100 ответвлений в молекуле), чем амилопектин. Общее содержание гликогена в организме взрослого хорошо питающегося человека примерно 350 г, которые в равных долях распределены между печенью и мускулами. Гликоген образует энергетический резерв, который может быть быстро мобилизован при необходимости восполнить внезапный недостаток глюкозы.Только гликоген, запасённый в клетках печени (гепатоциты) может быть переработан в глюкозу для питания всего организма. 29.Протеогликаны и гликопротеины: определение, структура, свойства , функции в организме. ПРОТЕОГЛИКАНЫ - углевод-белковые компоненты животных тканей, в к-рых полисахаридные цепи ковалентно связаны с белком, занимающим в молекуле центр. положение. Структура протеогликанов: 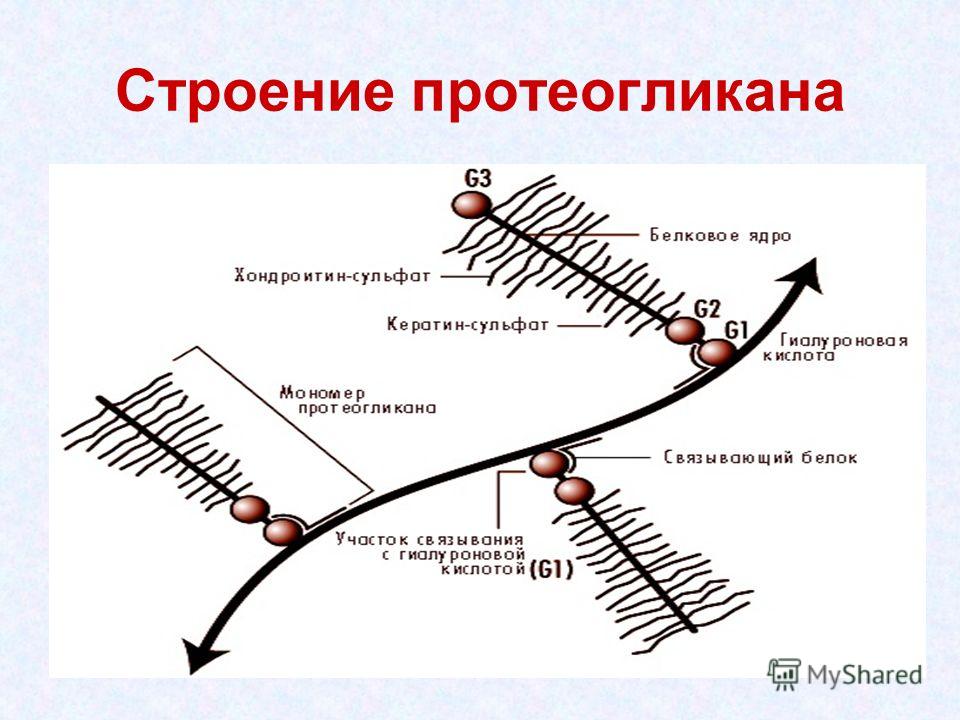 Функции в организме: они являются структурными компонентами межклеточного матрикса; • протеогликаны и гликозаминогликаны специфически взаимодействуют с коллагеном, эластином, фибронектином, ламинином и другими белками межклеточного матрикса; • все протеогликаны и гликозаминогликаны, являясь полианионами, могут присоединять, кроме воды, большие количества катионов (Na+, K+, Са2+) и таким образом участвовать в формировании тургора различных тканей; • протеогликаны и гликозаминогликаны играют роль молекулярного сита в межклеточном матриксе, они препятствуют распространению патогенных микроорганизмов; • гиалуроновая кислота и протеогликаны выполняют рессорную функцию в суставных хрящах; • гепарансульфатсодержащие протеогликаны способствуют созданию фильтрационного барьера в почках; • кератансульфаты и дерматансульфаты обеспечивают прозрачность роговицы; • гепарин - антикоагулянт; • гепарансульфаты - компоненты плазматических мембран клеток, где они могут функционировать как рецепторы и участвовать в клеточной адгезии и межклеточных взаимодействиях. Они также выступают компонентами синаптических и других пузырьков. • Гликопротеи́ны — это сложные белки, в которых белковая (пептидная) часть молекулы ковалентно соединена с одной или несколькими группами гетероолигосахаридов. Кроме гликопротеинов существуют также протеогликаны и гликозаминогликаны. • Функции в организме: Транспортная функция, Каталитическая функция, Структурно-механическая функция, защитная функция 30. Отличие глюкозы и фруктозы. Фруктоза - в отличие от глюкозы, служащей универсальным источником энергии, почти никакие клетки человеческого организма (кроме сперматозоидов) не могут использовать фруктозу. Фруктоза поступает в печень, где превращается или в жирные кислоты (приводя к ожирению, а также к повышению уровня триглицеридов, что повышает риск атеросклероза) , или в глюкозу (в виде отдельных молекул или гликогена) . Однако превращение фруктозы в глюкозу — сложный многоступенчатый процесс, и способность печени перерабатывать глюкозу ограничена. Глюко́за (от греч. glykys — сладкий) (виноградный сахар) , углевод из группы моносахаридов. Хорошо растворима в воде, имеет сладкий вкус. В значительных количествах содержится в плодах винограда, меде. Входит в состав сахарозы, лактозы; образует крахмал и гликоген, а также целлюлозу. Глюкоза — один из ключевых продуктов обмена веществ, обеспечивающий живые клетки энергией (в процессах дыхания, гликолиза, брожения) , исходный продукт биосинтеза многих веществ. У человека и животных постоянный уровень глюкозы в крови (ок. 100 мг%) поддерживается путем синтеза и распада гликогена. В организме человека и животных глюкоза является основным и наиболее универсальным источником калорийной энергии для обеспечения метаболических процессов, «единой энергетической валютой» организма. Способностью усваивать глюкозу обладают все клетки организма животных. В то же время, способностью использовать другие источники энергии — например, свободные жирные кислоты и глицерин, фруктозу или молочную кислоту — обладают не все клетки организма, а лишь некоторые их типы.(http://otvet.mail.ru/question/25527030) Глюкоза принадлежит к классу альдегидоспиртов — соединений, содержащих гидроксильные и альдегидные группы. В молекуле глюкозы пять гидроксильных групп и одна альдегидная. Наличие этих группы в глюкозе можно доказать с помощью реакции "серебряного зеркала". Формулу глюкозы обычно приводят в сокращённом виде: 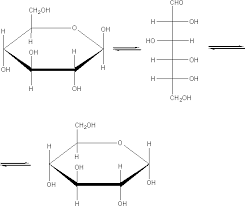 Глюкоза (а также любой другой из семи изомерных ей сахаров) может существовать в виде двух изомеров, молекулы которых являются зеркальным отображением друг-друга. Наличие глюкозы в каком-либо растворе можно проверить с помощью растворимой соли меди: В щелочной среде соли меди (II-валентной) образуют с глюкозой ярко окрашенные комплексы (рисунок слева 1). При нагревании эти комплексы разрушаются: глюкоза восстанавливает медь до жёлтого гидроксида меди (I-валентной) CuОН, который превращается в красный оксид Сu2О (рисунки слева 2 и 3). Фруктоза Фруктоза (фруктовый сахар) изомерна глюкозе, но в отличие от неё относится к кетоспиртам — соединениям, содержащим кетоновые и карбонильные группы 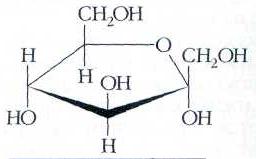 альфа-фруктоза альфа-фруктоза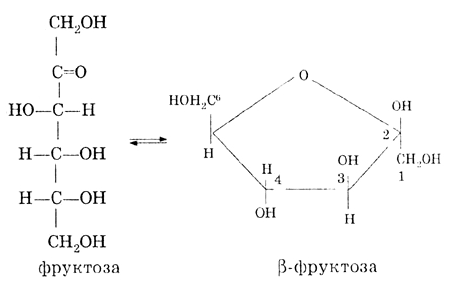 В щелочной среде её молекулы способны изомеризоваться в глюкозу, поэтому водные растворы фруктозы восстанавливают гидроксид меди (II-валентной) и оксид серебра Ag2O (реакция «серебряного зеркала»). Фруктоза — самый сладкий из сахаров. Она содержится в мёде (около 40%), нектаре цветов, клеточном соке некоторых растений.( http://www.kristallikov.net/page45.html) 31. Липиды в заависимости от способности к гидролизу разделяют на омыляемые и неомыляемые. Омыляемые липиды при гидролизе образуют 2 компонента: спирты и карбоновые кислоты Простые: Жиры и Воски Сложные: фосфолипиды, сфинголипиды и гликолипиды. Жиры: глицерин+3 высшие прямоцепочечные карбоновые кислоты) 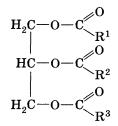 Растительные жиры содержать остатки непредельных(ненасыщенных) карбоновых кислот, а животные- предельных(насыщенных). Насыщенные: Пальмитиновая(С15Н31СООН) и стеариновая(С17Н35СООН) Ненасыщенные: Олеиновая(С17Н33СООН), Линолевая(С17Н31СООН), Линоленовая(С17Н29СООН) Основная реакция- гидролиз(в частности щелочной гидролиз-омыление) Воски. Природные воски- сложные смеси эфиров одноатомных первичных высших прямоцепочных алифатических спиртов и высших прямоцепочечных насыщенных и ненасыщенных высших карбоновых кислот . Причем и кислоты и спирты содежрат четное число углеводов.Нерастворимы в воде. Подразделяются на растительные и животные. Животный воск- воск в черепной полости кашалота(спермацет) состоящий главным образом из мирицилпальмитата и цетилпальмитата. Овечью шерст покрывает ланлолин. Фосфолипиды: 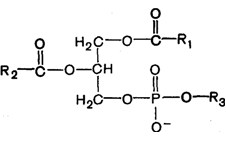 Природные фосфолипиды : фосфатидилхолин(лецитин), фосфатидилэтаноламин (кефалин), фосфатидилсерин, фосфатидилнозит. Составляют основу липидного бислоя биомембран. Сфинголипиды-структурные аналоги фосфолипидов, содержащие вместо глицерина сфингозин 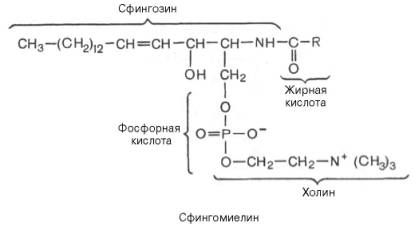 Наиболее распространенные –церамиды и сфингомиелины Гликолипиды-сложные липиды, образующиеся в результате соединения липидов с углеводами. Включают углеводные остатки глюкозы, галактозы и олигосахаридов, присоединенные к гидроксилу при С-1 церамидов. Входят в состав миелиновой оболочки нервных волокон, регулируют рост клеток. 32.Неомыляемые липиды - выполняют роль низкомолекулярных биорегуляторов. Включают: Стероиды, жирорастворимые витамины и простагландины. Стероиды. В основе-стеран- конденсированный четырехциклический остов 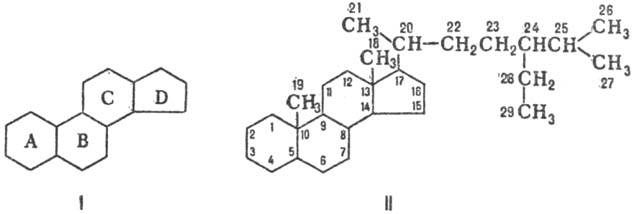 К стероидам относятся многочисленные вещества гормональный природы: Холестерин(или холестерол), являющийся предшественником всех стероидных гормонов, включая мужские андростерон и более активный тестостерон и женские эстрадиол и прогестерон Жирорастворимые витамины. Витамины группы D, E, K, Q Простагландины. Впервые обнаружены в семенной жидкости баранов. Названиеполучили как продукты предстательной железы(простаты) 33. Строение холестерина, функции в организме. Холестерин — органическое соединение, природный жирный (липофильный) спирт, его молекулярная формула — С27Н46О. Холестерин имеет сложное гетероциклическое стероидное ядро. Углеродный скелет холестерина состоит из четырех колец: три кольца содержат по 6 атомов углерода и одно — 5 атомов. От него отходит длинная боковая цепь. Нерастворим в воде, но может образовывать с ней коллоидные растворы, растворим в жирах и органических растворителях. В чистом виде холестерол представляет собой мягкое белое вещество (жирные на ощупь жемчужные кристаллы в виде игл) без запаха и вкуса. Холестерин присутствует только в животных организмах, в растениях его нет. В организме человека холестерин содержится в печени, спинном и головном мозге, надпочечниках, половых железах, жировой ткани; входит в состав оболочек почти всех клеток. Без холестерина невозможна нормальная работа жизненно важных органов и систем нашего организма. Он входит в состав клеточных мембран, обеспечивая их прочность и регулируя их проницаемость, а также оказывая влияние на активность мембранных ферментов. Следующая функция холестерина заключается в его участии в метаболических процессах, производстве желчных кислот, необходимых для эмульгации и абсорбции жиров в тонком кишечнике, и различных стероидных гормонов, в том числе половых. При непосредственном участии холестерина происходит выработка в организме витамина D (который играет ключевую роль в обмене кальция и фосфора), гормонов надпочечников (кортизола, кортизона, альдостерона), женских половых гормонов (эстрогенов и прогестерона),мужского полового гормона тестостерона. Кроме того, холестерин необходим для нормальной деятельности мозга. Согласно последним научным данным, холестерин напрямую влияет на интеллектуальные способности человека, так как принимает участие в образовании нейронами головного мозга новых синапсов, обеспечивающих реактивные свойства нервной ткани. 34. Сфинголипиды: строение, свойства. Отдельные представители Сфинголипиды — это класс липидов, относящихся к производным алифатических аминоспиртов. Онииграют важную роль передаче клеточного сигнала и в клеточном распознавании. Особенно богатасфинголипидами нервная ткань. |

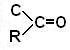 – кетонная
– кетонная