ксенобиология. ответы. экзамен. 1. Масштабы и причины химического загрязнения. Классификация загрязнений
 Скачать 1.55 Mb. Скачать 1.55 Mb.
|
|
17.Общие закономерности. Адсорбция. Изотермы Ленмюра. Зависимость доза-эффект. Многие ксенобиотики действуют на поверхность клетки, адсорбируясь на клеточной мембране. Играет роль в познании механизмов как прямых и опосредованных мембранотропных эффектов, и вызываемых ими реакций. Площадь поверхности белков, содержащихся в 1 см3 сыворотки крови человека - 100м2.с другой стороны физ хим характеристики веществ после их адсорбции на молекулярной плёнке отличаются. Адсорбция - это обратимое концентрирование на поверхности и определяется суммой всех химических связей, образующихся между молекулами или молекул с поверхностью. Особенности поверхности: 1)на ней создаются 100% концентраций веществ. 2) содержание не насыщенных валентностей, которые в твёрдом веществе затрачивает на связывание друг с другом соответствующих его атомов. На молекулу действуют силы, стремящиеся возвратить её в раствор. Мера способности возврата в среду - растворимость (мера способности десорбироваться). Виды адсорбции на поверхности : неспецифическая - для веществ амфифильной природы (пав), имеют концентрацию гидрофильных групп, связанных с относительно большими гидрофобными остатками (занимает любую поверхность); специфическая - гидрофильные вещества, стремятся разместиться на поверхности комплементарного характера. (притяжение аниона к полярно заряженному участку поверхности, катиона - к отрицательно заряженным). 1918 год Лэнгмюр вывел уравнение, позволяющее получить количественные характеристики адсорбции. Основные предположения: 1)энергия адсорбции постоянна и не зависит от степени заполнения поверхности. 2)адсорбция происходит на локальных центрах, и адсорбированные молекулы между собой не взаимодействуют. 3)максимально возможная адсорбция соответствует полному заполнению монослоя. Г=Гmax*С/Ксд+С. Г - число молей вещества, адсорбированного на поверхности, выражается в виде функции равновесной концентрации вещества в растворе. Ксд - константа сорбции - десорбции. С - концентрация ксенобиотика в растворе. Гmax - число молей растворенного вещества, адсорбированного на поверхности адсорбента с образованием полностью заполненного монослоя. Изотерма Лэнгмюра в линейной форме е/Г= 1/Гmax + Ксд/Гmax+C.  Уравнение показывает, что адсорбент насыщается при высоких значениях С, т.е.при образовании монослоя. Наблюдается явление, когда эффект от последнего удвоения становится менее ощутимым, кривая является гиперболой. Типы кривых: 1)L-кривые, нормальные изотермы Лэнгмюра, характеризует адсорбцию молекул, ориентированных на поверхности горизонтально. Чем > вещества адсорбировано, тем > затрудняется дальнейшая адсорбция. 2) S-кривые, соответствующие вертикальной ориентации молекул относительно поверхности. На начальном участке - сигмоидной кривой, чем > вещества уже адсорбировано, легче идёт дальнейшая адсорбция - кооперативный эффект. 3) Н-кривые, случаи с высокой степенью сродства; начальные концентрации велики, когда вещество образуется в виде мицелл, при адсорбции ионов с высокой степень сродства и способствующих обмену с ионами, обладающими < степенью сродства. Ещё есть С-кривые, когда молекула быстрее оказывается в адсорбенте, чем растворитель. 18.Основные этапы: связывание молекул эффектора мемранактивными структурами и «пострецепторное» развитие реакции; условия доступа и взаимодействия эффектора с активными центрами, стехиометрия и кооперативность связывания. Анализ развития мембранотропных эффектов должен опираться на совокупность модельных представлений, отражающих течение двух основных этапов : 1) связывание молекул эффектора с некими центрами сродства (рецепторами), инициирующими процесс, т.е. важные процессы доступа эффектора к мембраноактивным центрам. 2)последующее развитие реакции (биологического ответа). Предполагается, что образование комплекса лиганд- мембраноактивный центр происходит при отсутствии диффузионных ограничений стехиометрией 1:1 (один лиганд на один рецептор) и независимости мест связывания друг от друга (образование комплекса с одним из мембраноактивных центров не влияет на взаимодействие остальных активных центров с молекулами лиганда), реакция связывания лиганда А с местом связывания записывается так: 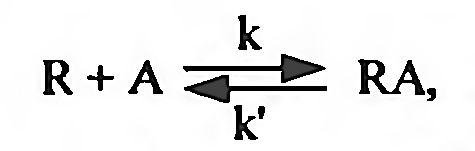 A-лиганд, R - рецептор, k-константа скорости реакции. При локализации рецепторов прямо на поверхности мембраны равенство для скорости изменения концентрации комплексов (Z) лиганд- рецептор во времени и в условиях: Q концентрация место связывания, C- концентрация эффектора. dZ/dt(приращение функции во времени =k(Q-Z) C-k'Z. Такая ситуация реализуется при избытке лиганда С»Q. При состоянии равновесия dZ/dt=0 Zравн =QC/K+C. K- отношение обратной скорости реакции к прямой К=k'/k. Таким образом образование комплексов будет описываться уравнением 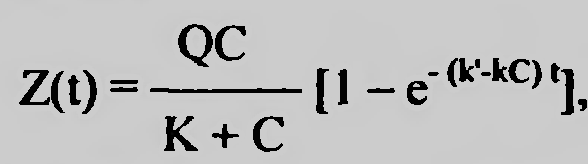 Хорошо используется в фармакологии. разрушения комплекса можно увидеть на графике зависимости количества связывания комплексов к количеству мест связывания (Z/Q) к концентрации лиганда С. 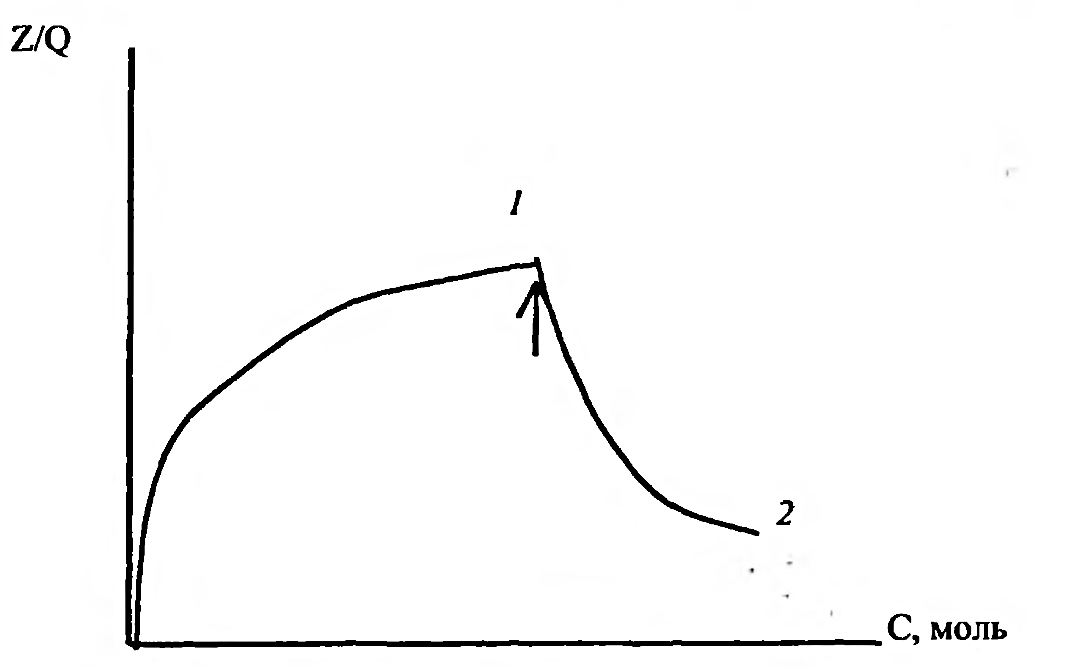 1)связывание лиганда с мембраноактивным центром. Чем больше лиганда, тем больше мест связывания и больше концентрация. 2) Диссоциация комплексов между лигандом и рецептором, ↑- момент удаления лиганда. При локализации рецепторов внутри мембраны процесс образования комплексов рецептор- эффектор будет развиваться немного иначе. 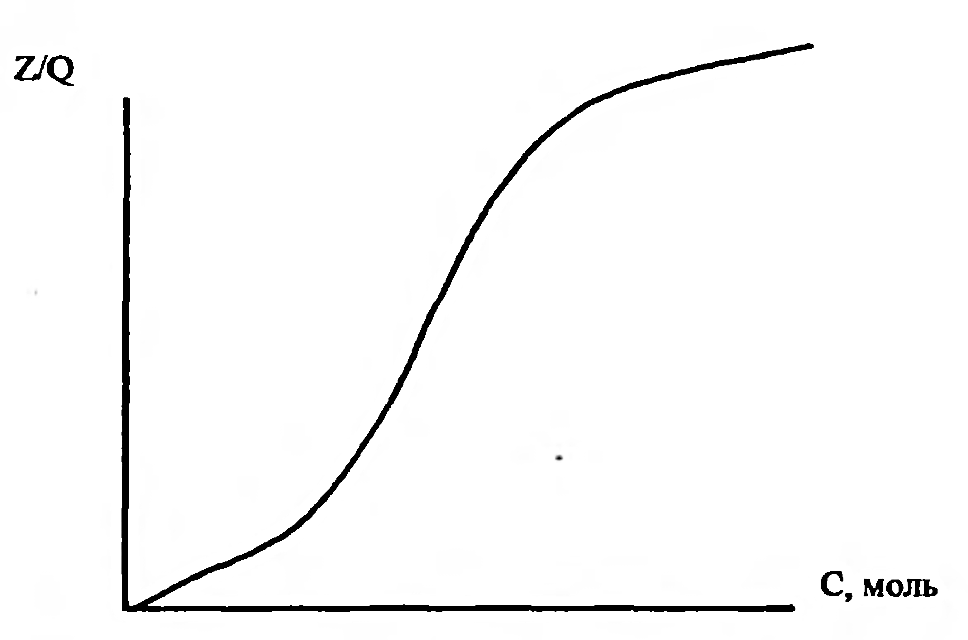 19.Модель «биофазы». Биофаза это comportament, который содержит рецепторы, находящиеся в контакте со средой. По Фортгофу биофаза находится в непосредственном контакте с компонентом, являющимся источником эффектора. Выход эффектора из биофазы в прочие компартаменты рассматривается как реакция первого порядка; стехиометрия связывания эффектора с активным центром в этом случае принимается равной 1:1. Можно допустить существование комплексов лиганд- рецептор типа RAn с любыми стехиометрическими компонентами (многовалентные места или рецепторы, обладающие комплексами RAn путём последующего присоединение лиганда) . RA1+A=RA2. RАn-1+A>RA2. Если присоединение каждой последующей молекулы лиганда не зависит от количества ранее связавшихся с активным центром молекул, то процесс подчиняется классическому уравнению по расчёту комплексов рецептор- лиганд. В противном случае эффекты называются кооперативными. Различают положительную кооперативность (1) - это присоединение каждой последующей молекулы облегчается вследствие посадки предыдущий (гемоглобин). Отрицательная кооперативность (2) - это присоединение каждой последующей молекулы затрудняется в следствии посадки предыдущей. Способы обнаружения кооперативности (этапы): 1) препарат рецепторов насыщенный радиоактивными лигандом переносят в среды, содержащие высокую концентрацию немеченого лиганда и без лиганда измеряют скорость диссоциации меченых комплексов. 2) расчёт констант связывания лиганда препаратом рецепторов при высоких и низких концентрациях. 3)анализ характера отличий концентрационной зависимости количества связывающего лиганда от классического уравнения. 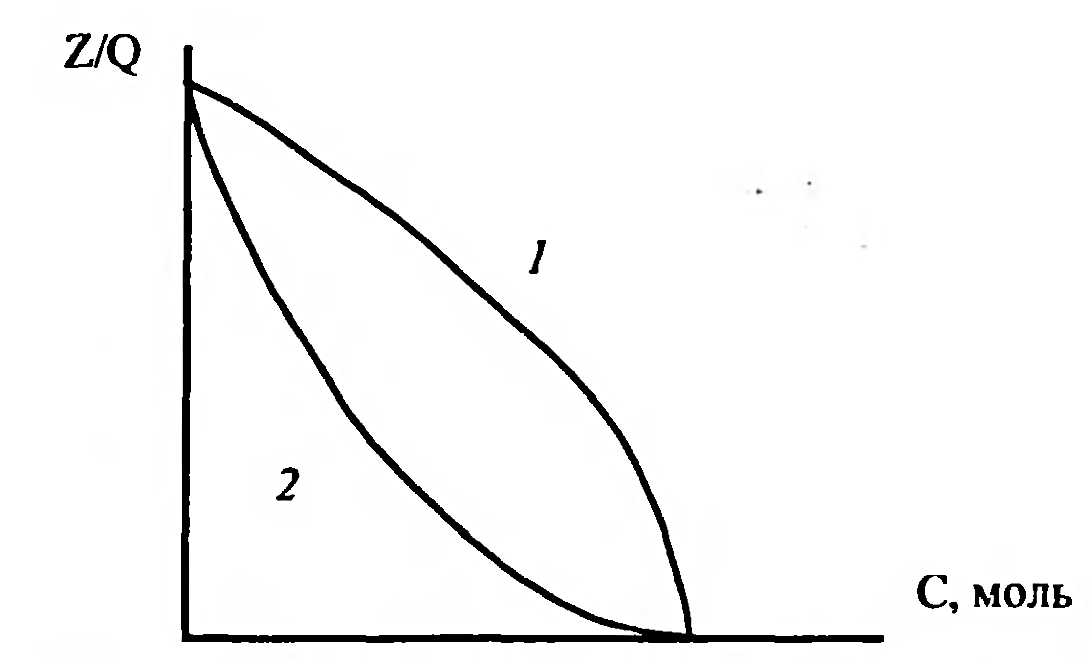 20.Многоканальная система передачи сигнала. ро=f(z). Развитие реакции биологического ответа на хим раздражитель обычно рассматривается как функция количества образованных компонентов. По Кларку регистрируемая реакция ро является функцией количества центров связывания занятых молекулой эффектором. При малых концентрациях эффектора реакция пропорциональна количеству занятых рецепторов - линейная зависимость. Представление кинетики биологической реакции в виде Ро=f[z(c, t)] представляет собой то, что биологическая реакция является функцией числа образующихся комплексов и верна только в тех случаях, когда показатели времени процессов развивающаяся после образования комплексов рецептор - эффектор существенно меньше, чем время достижения равновесного значения Z. 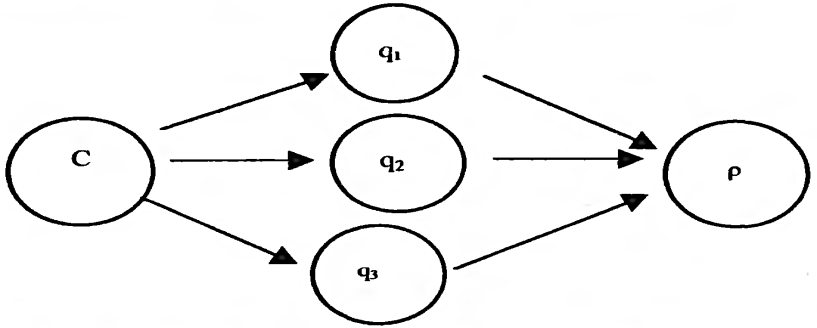 По мере увеличения примененной концентрации ксенобиотика появляются эффекты иных каналов связи, сигналы которых очевидно могут отличаться по знаку (вход отдельных каналов м.б.+ стимулируют реакцию и - угнетает). Возможно два случая: 1)лиганд взаимодействует с мембран активными центрами одного типа, а разветвление характера действия происходит на последующих стадиях. 2)лиганд взаидействует с центрами разных типов, каждый из которых инициирует процесс различающийся по конечному эффекту на регистрируемую реакцию. Т.о.возможно взаимодействие вещества с несколькими типами рецепторов : может происходить не только со специфическими рецепторами, но и с другими центрами связывания, что отразится на развитии регистрируемой реакции. 21.Особенности мембранотропных эффектов и развитие реакции на действие ПАВ. Основные закономерности и механизмы, лежащие в основе этих явлений. При обработке клеток поэтапно увеличивающейся концентрацией детергента ПАВ выявлены четыре различные стадии: первая стадия - (связывание) при низких концентрациях молекулы и детергенты вещества с поверхностной активностью связываются с мембранами посредством внедрения во внешнюю среду липидного бислоя без существенного изменения его структуры. Вторая стадия (лизис мембраны) - при повышении концентрации детергента происходит дестабилизация мембраны, то есть встраивание ПАВ в мембрану, образование пор, деформация пор в виде связанных каналов или в виде выемок на поверхности мембраны. 3 стадия (диссоциация мембраны) при ещё больших концентрациях происходит фазовый переход, мембрана распадается на смесь мицелл, содержащих комплексы детергент- липид, детергент - липид- протеин. 4 стадия (высвобождение частиц белков) при последующем увеличении концентрации пав отношение липид- белок уменьшается, то есть происходит полное разделение фракций белков и липидов. Мембрана обладает выраженной селективностью по отношению к различным веществам. Многие коэффициенты проницаемости могут различаться на порядки. Нарушение этой упорядоченности, наступающее при внедрении в мембрану уже сравнительно незначительных количеств детергентов немедленно сказываются на селективности. ПАВ мало: большая часть связывающихся с мембраной молекул «разрыхляет» удаленные друг от друга участки мембраны и каждая из них действу ет как бы независимо. ПАВ много: молекулы располагаются плотнее, так что присутст вие одной из них усиливает разрушающий эффект другой. 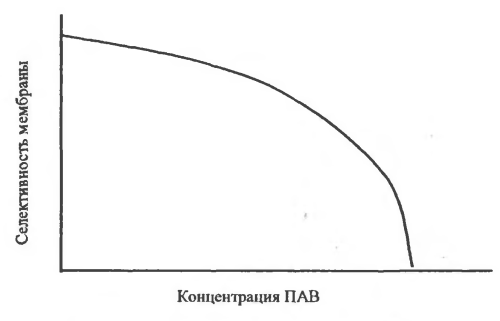 22.Типы антагонизмов: конкурентный, химический, бесконкурентный, смешанный, функциональный, физический. Антагонизм - это ослабевание или подавление биологического эффекта при совместной деятельности по сравнению с влиянием отдельных агентов. Классы антагонистов: химические (через нейтрализацию) - взаимодействие антагониста агонистом, происходит инактивация последнего. А+В>Е, Кв=Са×Св/Се. Является конкурентным взаимодействием, снижается константа диссоциации комплекса из-за конкуренции за связь с агонистом. Конкурентный антагонизм – антагонист взаимодействует с сайтами как и агонист, но не вызывают биологические реакции. Выражение Гаддума: Zа= QCa/Ca+(1+Cв/Кв)Ка. Q-количество мест связывания. Са, Св - концентрация эффектора. Ка и Кв - константы диссоциации агониста и антагониста. Неконкурентный антагонизм - аналогичен аллостерическому эффекту при ферментативном катализе. Взаимодействие не конкурентного антагониста с рецептором не приводит к независимому биологическому эффекту, а снижает эффект при образовании комплекса агонист - рецептор. Антагонист, приводящий к уменьшению внутренней активности агониста или обобщённо к изменению форм зависимости p(Z) - метакоидный. Метаффиноидный - антагонизм, при котором занятие антагонистом не конкурентного центра вызывает некоторые изменения рецептора агониста, приводит к снижению его сродства к агонисту. Функциональный - взаимодействие двух агентов с независимыми рецепторными системами вызывают противоположное влияние в одной и той же эффекторной системе. Физический - вызывается противоположным физическим действием эффектов, активируемых независимые рецептор - эффектор системы. Бесконкуретный - инактивация комплекса агонист - рецептор лигандом, не способным образовывать комплекс с рецептором, не занятым агонистом. Снижается количество рецепторов, способных образовать эффективный комплекс с агонистом, снижается константа диссоциации комплекса. Возможно лишь когда агонист и антагонист обладает средством и различной функциональной группой рецептора. Смешанный антагонизм - общая схема взаимодействия агониста А и антагониста В с рецепторами, допускающую комплексообразование рецепторов с обоими лигандами, а также образование тройного комплекса. Он формально эквивалентен действию смеси конкурентного и бесконкурентного антагонистов в равных концентрациях. Выражение для концентраций комплексов (Za). Zn=QCa/(1+Cв/Кв2)Са+(1+Св/Кв1)Ка1. 23.Механизмы взаимодействия аганистов и антагонистов с мембранными структурами. Примеры антагонизма и синергизма разных ксенобиотиков. Аддитивность - это отсутствие влияния одного ксенобиотика на характер другого, то есть биологическая реакция является суммой эффектов вызываемых каждым веществом. Синергизм - это усиление биологических ответов при совместной деятельности ксенобиотиков по сравнению с эффектом вызываемым каждым веществом в отдельности. Антагонизм - это ослабевание или подавление биологического эффекта при совместной деятельности по сравнению с влиянием отдельных агентов. Химический антагонизм, или антагонизм через нейтрализацию, проявляется при непосредственном взаимодействии антагониста с аго нистом, приводящим к инактивации последнего. Конкурентный антагонизм проявляется обычно в тех случаях, ко гда антагонист взаимодействует с теми же сайтами, что и агонист, но в отличие от последнего антагонист не вызывает биологической реакции. 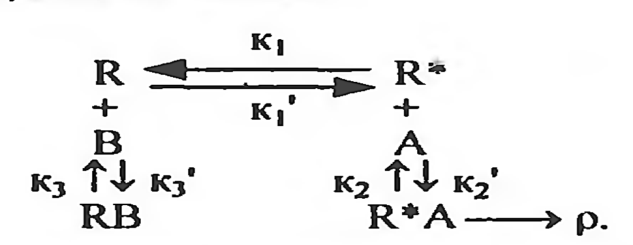 Неконкурентный антагонизм реализуется по механизму, аналогич ному аллостерическим эффектам при ферментативном катализе. Взаи модействие неконкурентного антагониста с собственными рецептора ми не приводит к независимому биологическому эффекту, а снижает эффект при образовании комплекса агонист-рецептор. Функциональный ан тагонизм характеризуется взаимодействием двух агентов (агонист и ан тагонист) с независимыми рецепторными системами, причем вызывает ся противоположное влияние в одной и той же эффекторной системе. Физический антагонизм вызывается противоположным физиологиче ским действием эффекторов, активирующих полностью независимые рецептор-эффекторные системы. 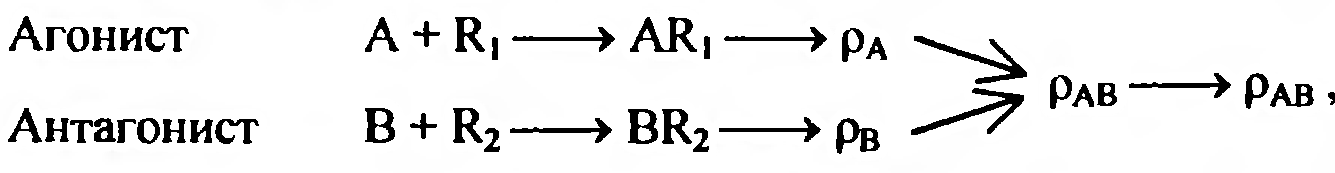 Бесконкурентный антагонизм предполагает инактивацию ком плекса агонист-рецептор лигандом, не способным образовывать ком плекс с рецептором, не занятым агонистом. Бесконкурентный антаго низм, таким образом, предполагает наличие двух процессов. Бесконкурентный антагонист в равной мере снижает количество рецепторов, способных образовывать эффективный комплекс с агони стом (т. е. в отсутствие резерва рецепторов уменьшает максимально достижимую реакцию), и снижает константу диссоциации этого ком плекса (т. е. увеличивает сродство агониста к рецепторам, оказывая действие, противоположное конкурентному антагонизму). Взаимодействие бесконкурентного антагониста с агонист- рецепторным комплексом представляется возможным лишь в том слу чае, когда агонист и антагонист обладают сродством к различным функциональным группам рецептора. 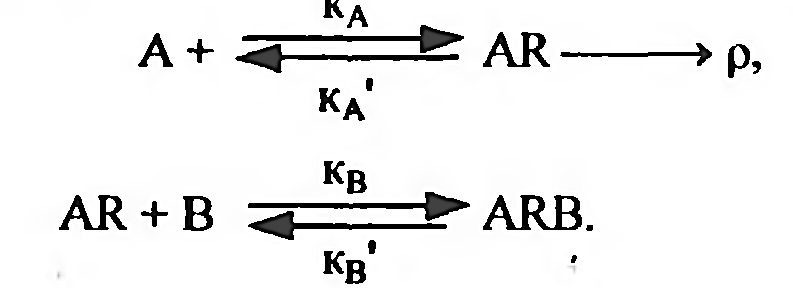 Смешанный антагонизм представляет собой более общую схему взаимодействия агониста А и антагониста В с рецепторами, допус кающую комплексообразование рецепторов с обоими лигандами, а также образование тройного комплекса. 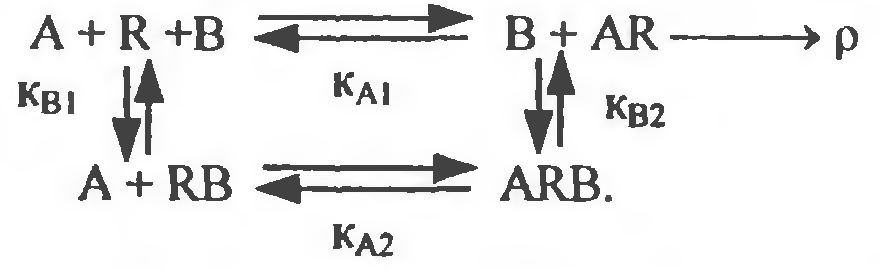 24.Механизмы транспорта: пассивная и облегченная диффузия, активный перенос, редокс-цепи, пиноцитоз и фагоцитоз. Физиологическая активность ксенобиотиков в значительной степени зависит от способности взаимодействовать с клеточными мембранами и проникать внутрь клетки. Выдерживают следующие формы прохождения ксенобиотиков через мембрану: 1)пассивная диффузия 2)облегченная диффузия - без затраты АТФ. 3)активный транспорт веществ, выполняемый молекулярными машинами (АТФазы) иди редокс цепями (дыхательная цепь ферментов). 4)активный транспорт, осуществляемый за счёт сопряжения термодинамических (электрохим) градиентов. При пассивной диффузии ксенобиотики проходят через мембрану в результате случайного молекулярного движения, и величина потока линейно зависит от концентрации и коэффициента проницаемости мембраны для данного вещества. Не полярные вещества сравнительно легко проникают в клетки ( гидрофобные группы способствуют увеличению проникающей способности, полярные - её уменьшению). Пассивный перенос - это движение вещества по градиенту эхп без затраты энергии, т.е.движущей силы пассивного транспорта веществ служит градиент эхп. При облегчённой диффузии происходит соединение вещества со специфическим переносчиком и образуется комплекс вещество - переносчик и дифундирует внутри молекулы о наружной поверхности к внутренней, где комплекс не диссоциирует с высвобождением вещества внутрь клетки, переносчик дифундирует назад к наружной поверхности. Такая диффузия происходит по градиенту концентрации без затраты энергии и относится к пассивному транспорту. Глюкоза и некоторые другие моносахариды с такими же размерами молекул хорошо проникают в клетку. Отличие между облегченной и простой диффузией: 1)при простой поток вещества пропорционален внешней концентрации и всё время возрастает с увеличением последней. При облегчённой диффузии кривая, описывающая поток веществ через мембранц стремится к насыщению при концентрациях обеспечивающих связывание всех молекул переносчиков. 2)наличие специфических переносчиков, взаимодействующих с веществами определённого строения обуславливает резко выраженную зависимость проникающей способности вещества от его хим структуры и от простой конформации молекул. 3)Облегчённая диффузия в отличие от простой может ингибироваться некоторыми соединениями, которые блокируют переносчики. Активный транспорт веществ осущ с затратами энергии и идёт против градиента эхп. Различают первый и второй (сопряженный) активный транспорт. Первичный активный транспорт - трансмембранный векторный перенос веществ осущ непосредственно в ходе реакции энергии преобразованной в АТФазных системах или ОВЦ, т.е. использование энергии либо АТФ, либо ОВР. Он подразделяется на: а) электротранспорт - первый активный перенос веществ через мембрануво время АТФазной или ОВР - циях., сопровождаемых генерацией электропотенциала. б) электронейтральный активный транспорт - первый активный перенос веществ во время АТФазной или ОВР не сопровождающихся генерацией электропотенциала (стехиометрия 1:1). Вторичный активный транспорт совершается, когда в качестве энергетических источников используется градиенты эхп др ионов. Стадии активного транспорта: 1) активация - носитель в результате хим реакции, протекающей с поглощением метаболической энергии видоизменяется, т.о., что он приобретает сильное сродство к подлежащему переносу молекуле и присоединяет её к себе ; 2)переориентация - образовавшийся комплекс носителя с этой молекулой проходит через мембрану, 3)релаксация - в результате двух хим реакций благодаря уменьшению сродства носителя в транспортируемой молекуле она высвобождается и выделяется внутрь. При переносе веществ через мембраны принимают участие редокс цепи мембран. Т.е. ОВР (дыхательные цепи, монооксигеназная система). Исходным звеном редокс цепей выступают восстановительные пиридин нуклеотиды, а конечным акцептором является О2. К субстратам, которые могут с той или иной эффаувностью использоваться в редокс цепях м.б.глицерофосфат, лактат, оксибутират. По данному механизму транспортируется галактоза, арабиноза, гл-6-ф, глюконат, глюкуронат (большинство природных АК за исключением глутамина, аргинина, метионина, аргинина). Белки, полинуклеотиды, полисахариды, твердые частицы в большинстве клеток проходят в обоих направлениях через плазматические мембраны. При переносе макромолекул или твердых частиц происходит инвагинация мембраны с последующим образованием пузырьков везикул. Пути реализации: экзо и эндоцитоз. Каждый пузырек сливается только со специфичными мембранными структурами., что гарантирует правильный перенос макромолекул и их распределение между внеклеточным пространством и внутренностью клетки. Оба процесса представляют собой локальные ответные реакции плазматической мембраны и находящейся под ней цитоплазмы. Этапы пиноцитоза: 1)адсорбция на мембране молекул вещества 2)инвагинация мембраны - образование пиноцитозного пузырька и отрыв его от мембраны с затратой АТФ. 3)миграция пузырька внутрь протопласта, органеллы или наружу. 4)растворение мембраны пузырька под воздействием фермента или просто её разрыв. |
