ксенобиология. ответы. экзамен. 1. Масштабы и причины химического загрязнения. Классификация загрязнений
 Скачать 1.55 Mb. Скачать 1.55 Mb.
|
|
33.Особенности ферментов, участвующих в реакциях окисления. Особое место принадлежит микросомным монооксигеназам (на долю их приходится большая часть детоксикации чужеродных веществ в организмах). Оксигеназа (монооксигеназа) - это фермент, катализирующий ре акцию элементарного кислорода с некоторым субстратом, в процессе которой один из атомов кислорода входит в состав субстрата, тогда как второй атом кислорода реагирует с другим акцептором, чаще всего водородом, образуя воду. Окисление спиртов и альдегидов осуществляется алкогольдегидрогеназой, альдегидоксидазами и др. ферментами. Ферменты дегидрогеназы удаляют водород: образуются все более полярные вещества, которые способны диссоции ровать с образованием отрицательно заряженных ионов. Гидроксилирование кольцевых систем (алициклические кольце вые структуры гидроксилируются легче, чем ароматические, в этом заключается причина высокой токсичности бензола, ферменты – оксигеназы. Ароматизация алициклических соединений - происходит в случае окисления некоторых циклогексанкарбоновых кислот (с четным чис лом СН2-групп в боковой цепи) с участием митохондрий до бензойной кислоты. При реакциях окисления с участием фермента эпоксидазы обра зуется эпоксидное кольцо (реакция эпоксидации) Биологическое окисление, катализируемое системами микросомальных ферментов, включает широкий круг реакций, но все они могут быть сведены к одному общему механизму, а именно к гидроксилированию 34.Факторы, влияющие на метаболизм ксенобиотиков. Чужеродные соединения обычно метаболизируются несколькими различными путями, образуя множество метаболитов. Скорость, с которой протекает каждая из этих реакций, и их относительная важность зависят от многих факторов, в результате чего происходят изменения в картине метаболизма и возникают различия в токсичности. Факторы по происхождению могут быть: генетическими, физиологическими, связанными с условиями окружающей среды. К генетическим факторам относятся видовые различия и различия внутри одного вида. К физиологическим факторам, которые влияют на метаболизм, относятся возраст, пол, состояние питания, заболевания и т. д. К факторам окружающей среды можно отнести стресс из-за неблагоприятных условий, облучение ионизирующей радиацией, свет, ОВП и т. д., наличие других ксенобиотиков. К генетическим факторам относятся видовые различия и различия внутри одного вида. К физиологическим факторам, которые влияют на метаболизм, относятся возраст, пол, состояние питания, заболевания и т. д. К факторам окружающей среды можно отнести стресс из-за неблагоприятных условий, облучение ионизирующей радиацией, свет, ОВП и т. д., наличие других ксенобиотиков. Чужеродные соединения: Активирование микросомальных ферментов ксенобиотиками у многих видов (человек, крысы, мыши, кролики, собаки) в различных тканях (печень, почки, легкие, кишечник) может рассматриваться как регуляторный механизм метаболизма ксенобиотиков. Ксенобиотики оказывают стимулирующий эффект путем увеличения количества микросомальных ферментов (вследствие увеличения поверхности мембраны, скорости синтеза ферментов и в ряде случаев уменьшения скорости их распада). Для соединений, стимулирующих микросомальные ферменты, характерна высокая растворимость в липидах и медленная скорость метаболизма. 35.Особенности метаболизма ксенобиотиков у различных ксенобиотиков. Различия между организмами в их реакции на действие ксенобиоти ков могут быть очень существенными и обусловлены разной способно стью метаболизировать эти вещества. В пределах одного вида уровень микросомной активности зависит от пола организма и стадии его развития. В разных органах - печени, кишечнике, легких и т. д. - активность также различна. Однако существует и особенность в трансформации чужеродных со единений микроорганизмами. В микробиологической трансформации ксенобиотиков различаются процессы метаболизма и кометаболизма. Метаболизм - превращение соединения до конечного продукта реакции, который не участвует в трансформации. Кометаболизм - это изменение структуры молекулы ксенобиотика, катализируемое ферментами микроорганизмов, которые выросли на субстратах или их метаболитах. Во многих случаях в метаболизм сложных органических веществ вовлекается не одна, а несколько ферментативных систем микроорганизмов (политрансформация). Важно, что генетическая способность некоторых штаммов бактерий разрушать тот или иной ксенобиотик зависит от наличия в клетках плазмид. Бактерии - окислительные ферменты – диоксигеназы (внедряют два атома кислорода в субстрат). Высшие наземные и водные растения - пероксидазы, каталаза и полифенолоксидазы (активаторы кислорода и его восстановления). Трансформация органических веществ: у растений - образование глюкозида (гликозилтрансферазы в присутствии в качестве кофактора уридиндифосфатглюкозы); у животных - образование глюкоуронида или этерифицированного сульфата. 36.Металлы в живых системах и их биоцидные эффекты. О метаболизме чужеродных неорганических в-х известно мало по сравнению с органическими. В тканях обычно присутствуют в исследуемых количествах многие Ме, хотя их биологическая функция, если таковая имеется, не всегда известна. Тем не менее в настоящее время уже известны реакции трансформации отдельных не органических соединений происходящих в живых организмах. Известно, что многие Ме способны образовывать с органическими в - ми хелатные соединения и другие комплексы. При распаде хелатобразованного комплекса составляющие его агенты окажутся ксенобиотиком для определённых организмов. Живые организмы нуждаются в катионах Ме, обеспечивающих протекание многих жизненно важных процессов: 1- тяжелые Ме (Co, Cu, Fe, Mn, Mo, Zn, и в меньших количествах Ni, свинец) 2- легкие Ме встречаются в большом количестве ( Са, Мg, K, Na). Токсическое действие чужеродных Ме обусловлено антагонистом катионов. Н- р свинец известный нейротоксин поэтому вытясняет Са из некоторых отделов нервной системы и препятствует выделению нейромедиаторов. Остеомиелит- онтогонист кадмия и кальция. Синергическое действие Ме. 37.Двухфазность реакции на действие тяжелых металлов. Реакция (ρ) организма на тяжелые металлы является двухфазной: 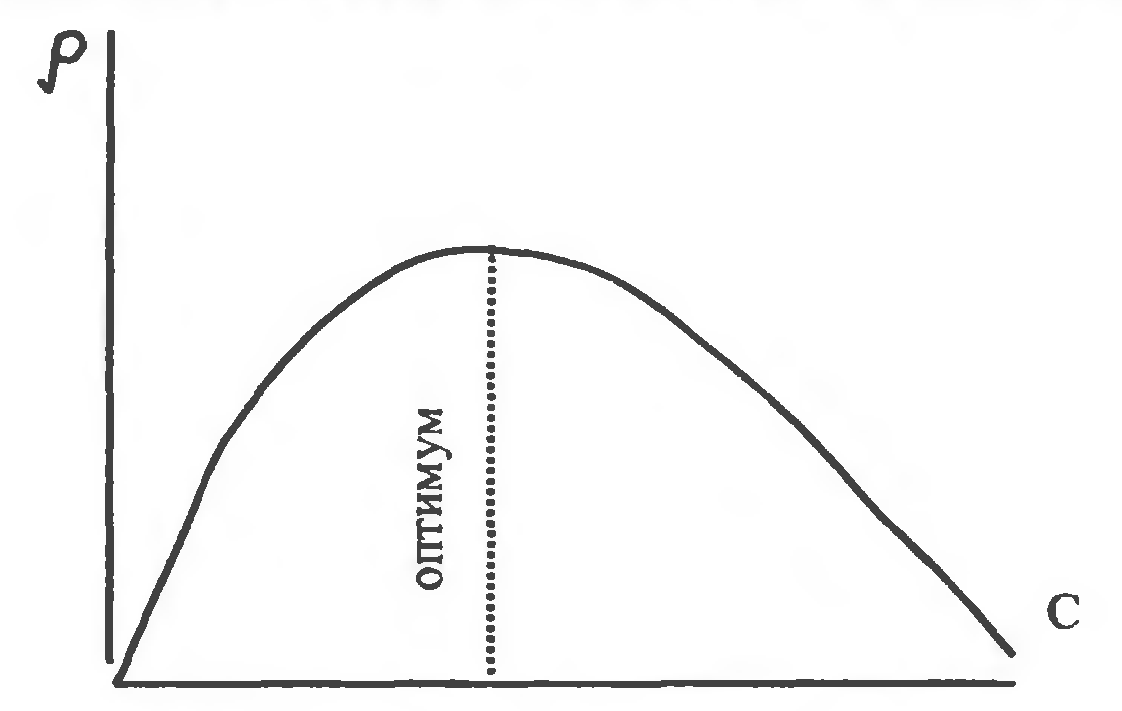 1 фаза: мало Ме в организме- тяжелый ущерб, множество ферментов которые могут функционировать в присутствии тяжелых Ме, теряют свою активность. 2 фаза: много Ме- токсическое действие избыточного количества(катионы блокируют всё в организм-батарейка в желудке). 38.Хелатообразование и снижение токсических эффектов. Множество в-в ( лигандов) способно связываться с Ме с образованием хелатных соединений (если обыкновенное комплексообразование, то стехиометрия его больше чем 1:1). Образование хелатных связей атомами азота и кислорода происходит в тех случаях, когда при этом получаются 5- и 6- членные циклы( 5членные более устойчивы). При участии серы в данных процессах наиболее устойчивы 4- членные циклы. Константа устойчивости - это мера оценки прочности связи и характеризует равновесие между лигандами и ионом Ме (закон действующих масс). 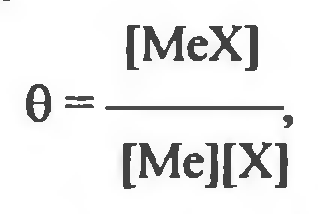 Константу устойчивости обычно определяют потенциометрическим титрованием лиганда в присутствии или отсутствии Ме и обработкой математических рез-в. Понятие "лиганд" относится к молекулам органических соединений, находится в соответствующей форме способной связать катион Ме ( этилендиамин, щавелевая к- та, глицин, могут служить лигандом как в ионизирующей форме, так и в виде моно- и дианионов). Ме по своему сродству к большинству хелатирующих агентов распределяются примерно в следующем порядке ( от наибольшего сродства с наименьшему): Fe, Hg, Cu, Al, Ni, Pb, Ca, Zn, Fe, Cd, Mn, Mg, Ca, Li, Na, K. Повышение сродста ( хелатмрующим) агентом является следствие уменьшения ионного радиуса и увеличение валентность Ме. Хелатобразование зависит от степени ионизации хелатобразующих агентов, в-ва обладающие меньшим сродством к Ме способны образовывать значительно больше анионов. Большинство Ме легче соединяются с лигандами содержащими кислород чем серу. Но Сu, As, Hg, лучше связываются с серой. Ме могут изменять избирательность органического лиганда: 1- влияя на распределение электронов в лиганде; 2- повышая реакционную способность активного центра лиганда; 3- вызывая изменение конформации лиганда; 4- обеспечивая возможность присоединения или отрыва электрона; 5- увеличивая липофильность лиганда и его способность проникать в клетку. 39.Количественные аспекты связывания металлов лигандами. Константа устойчивости - это мера оценки прочности связи и характеризует равновесие между лигандами и ионом Ме (закон действующих масс). 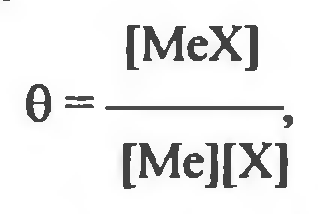 Константу устойчивости обычно определяют потенциометрическим титрованием лиганда в присутствии или отсутствии Ме и обработкой математических рез-в. Вкратце метод заключается в следующем: кислотная группа возможного хелатообразующего агента титруется щелочью, причем значение pH регистрируется после добавления каждой десятой доли эквивалента. Затем титруется смесь (1:1) исследуемого вещества и соли (например, перхлората или нитрата меди). Если образования комплекса не происходит, то новая кривая последовательно воспроизводит индивидуальные кривые обоих компонентов. Если же комплекс образовался, то катионы водорода, выделившиеся в процессе хелатообразования, сдвигают кривую в сторону более низких значений pH. Вещества в форме солей с кислотами, не имеющие кислотного характера, можно титровать щелочью. 40.Перспективы применения хелатообразующих соединений. Наличие двухфазной реакции организма на Ме свидетельствует о существовании 2х разных механизмов действия хелатирующих агентов в биологической системе: 1) удаление Ме из клетки или «маскировка» их в клетке в виде комплексов. 2) накопление в клетке Ме в большем количестве, чем в обычных условиях. Дальнейшее подразделение зависит от того является ли исследуемый Ме жизненно важным или токсичным для организма. Механизм 1. Бол-во хелатирующих агентов получили распространение в качестве антидотов, предназначенных "для маскировки" и удаления из организма токсических в-в или Ме случайно попавших в организм ( хелатобр- е димеркапролом при отравлениях золотом, ртутью, мышьяком). Для того, чтобы антидот смог проникнуть в клетку небольших количествах и быстро выводится из организма его молекулы должны: 1- содержать полярные группы, легко ионизирующиеся ( ОН, СООН, SH, NH2) , которые должны проникнуть в избытке чтобы по меньшей мере одна из них оставалась свободной после насыщения антидотов Ме; 2- хелатные комплексы не должны проникать в клетку из кровотока; 3- легко выводится почками. Лишь в редких случаях сам агент связывающий Ме оказывается токсичным для организма. Однако маскировка может приводить и к негативным результатам (синильная кислота). Механизм 2(накопление). Обусловлен переводом в-ва из одной формы в другую и облегчает поступление ксенобиотиков в организм. Сущность механизма связана с определением: кооперативный эффект и эффект распределения. Кооперативный эффект - явление возростания химической активности ксенобиотика, вследствии хелатобраз-я (соли Fe обладают некоторой каталазной и пероксидазной активностью возрастающей во много раз при включении железа в парфириновое ядро связанное со специфическим белком). Токсическим действием обычно обладают Ме способные изменять валентность (Fe, Cu) . Кооперативный эф-т чаще всего проявляется тех случаях, когда прибавляется не достаточное количество комплексообраз- го агента, т е образуется не насыщенный комплекс. Эффект распределения: ни один хелатирующий агент не активен в биологической среде, если константы устойчивости его компонентов по меньшей мере не столь же высоки как у комплексов обычных АК. При поиске новых хелатир-х агентов необходимо знать место их биологического действия (внутри и вне клетки). Если молекула должна проникнуть внутрь клетки, то в нее необходимо включить липофильные группы. Для этого используют а то в углерода, атомы галогенов (лучше йод или бром), водорода и серы, а азот и кислород придают молекуле полярность(их лучше использовать, чтобы хелат был вне клетки). Контроль можно проводить по величине коэффициента распределения в системе масло-вода. Очень небольшое изменение в хим структуре молекулы ксенобиотиков могут вызывать значительные сдвиги в величинах коэффициентов распределения. Увеличить способность проникать вещества в клетки можно путем повышения коэффициента распределения и используя лиганды сходные с природными субстратами (АК, углеводами). Современная проблема поиска хелатов связаны с одной стороны с вопросами детоксикации и обезвреживанием ткани поврежденных химическими, токсическими или радиоактивными Ме, и с другой стороны необходимостью предупреждения хелатобраз-я как, например, в случаи кариеса зубов, преждевременного старения из-за потери кальция из костной ткани. 41.Примеры биотрансформации неорганических соединений (неорганическая ртуть, цианиды, арсенаты и др.). Реакций биотрансформации неорганических ксенобиотиков: Реакции восстановления атомов с переменной валентностью: трансформация арсенатов As5+ в арсениты с As3+, селенатов с Se6+ в селениты Se4+, хлоратов CI+6 в хлориты С+4 - токсичность вещества возрастает. Реакции метилирования для превращения металлов в металлорганические соединения.   Реакции конъюгации: неорганический цианид обезвреживается в живых организмах конъюгацией с серой, в результате которой образуется тиоцианит:  Процесс катализирует роданаза, находящийся в митохондриях печени различных видов животных и растений. Донорами серы служат тиосульфаты, тиосульфонаты, полисульфиды. Путь биотрансформации сернистого газа (SO2). Первая стадия - окисление в сульфиты (SO32-) и сульфаты (SO42-) происходит в клеточной стенке при участии пероксидазы, затем происходит включение в фотосинтетический метаболизм серы. Аденозинфосфосульфат (АФS) - первый продукт в реакции взаимодействия SO42- с АТФ. Активированный сульфат (фосфо-АФБ) связывается с серосодержащим переносчиком белковой природы (CS) и образуется комплекс C-SO3, который восстанавливается до сульфида (CS-SH) при участии света через ферродоксин. При переносе на о-ацетилсерин (AS) образуется цистеин и метионин. В случае высокого содержания сульфаты аккумулируются в виде глутатиона. Если восстанавливающая сила превышает имеющиеся в наличии источники углерода, сера, соединяясь с водородом, образует дисульфид (H2S), который теряется в результате газового обмена. Эффективность реакций детоксикации ограничена: при продолжительном поглощении SO2 и увеличении кислотности буферная способность цитоплазмы становится недостаточной, уровень сульфитов в хлоропластах увеличивается, и SО2 занимает места связывания СО2 на рибулозодифосфаткарбоксилазе. В результате этого происходит ингибирование вторичных процессов фотосинтеза и разрушение третичной структуры ферментов. 42.Коэффициенты накопления ксенобиотиков. Организмы, обитающие в окружающей среде, содержащей относительно низкую концентрацию какого-либо вещества, мо гут накапливать его в своих тканях до концентраций, на не сколько порядков больших, чем в среде обитания. Способность живых организмов накапливать различные элементы даже при очень низком их содержании в среде называется биоаккумулирова нием. Способность организмов к накоплению веществ характери зуется коэффициент накопления (N): содержание (концентрация) вещества в организме N = –––––––––––––––––––––––––––––––––––––––––––––––––––––. содержание (концентрация) вещества в окружающей среде Явление биоаккумуляции ксенобиотиков было обнаружено при изучении накопле ния пестицидов, в частности хлорсодержащих углеводородов. В больших количествах идет накопление организмами ПХБ (полихлорбифенилы). Обладая низкой скоростью разложения в окружающей среде (период полураспада около 5 лет), ПХБ поступают в пищевые цепи и в значительных количествах аккумулируются в живых организмах. Включение ПХБ в трофические цепи может привести к поступлению в организм человека с продуктами питания боль ших количеств этих токсикантов. Накопительные свойства растений используются для: для поиска полезных ископаемых (так называемые фитогеохимические ме тоды); выделения биогеохимических провинций на основании анализа золы растений-концентраторов; контроля радиоактивности вод Мирового океана (радиоальгологический анализ). 43. Одно- и многокомпартментные системы. Важно вычислить разовую дозу и период полувыведения: Введение в ор ганизм разовой дозы вещества; Появление определенного количества этого вещества в тканях; Экскреция этого вещества осуществляется с определенной скоро стью. Например, была изучена скорость выведения ДЦТ из организма человека (концен трационная зависимость ДДТ в жировой ткани): 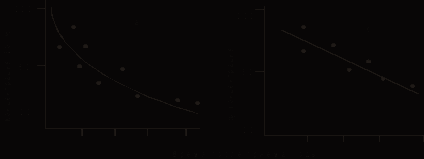 Наклон прямой опреде ляет константу скорости реакции. Период полувыведения - 3,7 года. Максимальное содержание вещества (А ср) можно рассчитать по формуле: l,44 t1/2 Qof Аср = –––––––––––––– τ где t1/2 – пе риодом полувыведения вещества, Qo – массой ежедневной дозы, f – часть этой дозы, которая поглощается организмом, τ – интер вал между введением доз. Максимальная концентрация вещества в тканях зависит: от размера дозы (повышается при ее увеличении) и от периода по лувыведения или скорости выведения. Вещества с большим пе риодом полувыведения соответственно накапливаются в больших концентрациях. Другим важным фактором является время, не обходимое для достижения состояния равновесия. Многокомпартментные системы (многоячеистые). Каждая ткань животного – ткань почек, печени, сердца, мозга, жировые отложения – рассматривает ся как ячейка. После того как вещество попадает в организм, оно начинает перемещаться с током крови. Каждая ячейка характеризуется своим размером, содержанием жира, скоростью тока крови, коэффициентом распределения, определяющим способность вещества перемещаться из крови в ткань. Соответствие таких моделей реальным системам необходимо подтверждать экспериментальными данными. В рамках разработанной модели можно про вести анализ взаимного влияния различных переменных и про гнозировать те ситуации, которые невозможно воспроизвести экспериментально. |
