ксенобиология. ответы. экзамен. 1. Масштабы и причины химического загрязнения. Классификация загрязнений
 Скачать 1.55 Mb. Скачать 1.55 Mb.
|
|
25.Структурное строение отдельных транспортных систем биологических мемран (канал, переносчик, помпа). Проницаемость мембраны для некоторых малых молекул оказывается более высокой, чем это можно было бы ожидать на основании данных об их растворимости в липидах: глицерин, мочевина, заряженные частицы. Молекулы проходят через особые участки мембраны, так называемые поры (каналы). Канал - это две макромолекулы, образующие в мембране пору через бислой липидов. В поле есть узкий селективный фильтр вблизи наружной поверхности мембраны и воротное устройство вблизи внутренней поверхности мембраны. Пространство между селективным фильтром и воротами называют тунеллем. Сенсор напряжения, расположенный в липидном слое управляет открытием ворот под влиянием внутри молекулярного поля. Расширенные части канала у наружной и внутренней мембран образуют устья. Через ионные каналы осуществляется не только транспорт веществ, они непосредственно участвуют в передаче сигнала возбудимым клеткам (генерация потенциала действия). Хемовозбудимые (рецепторы ацетилхолина, глутамата) электровозбудимые (натриевые, калиевые, хлорные) каналы. Схема транспорта веществ с участием подвижного (а) и фиксированного (б) переносчиков – облегченная диффузия. 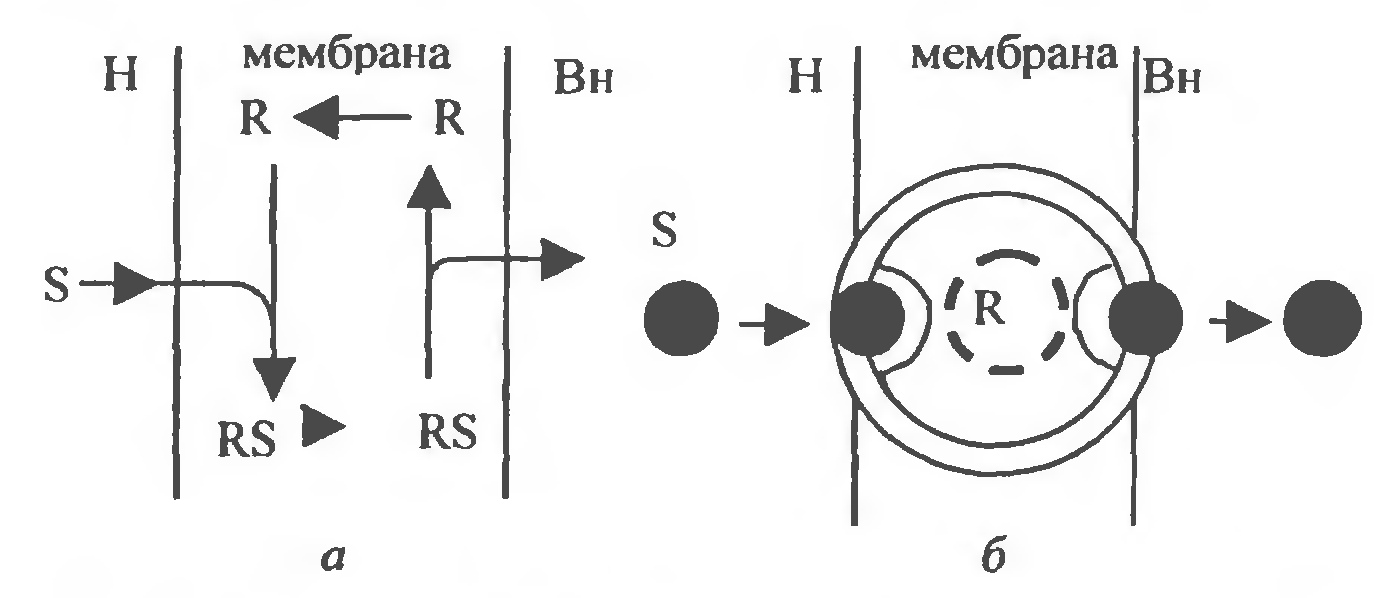 Регулировать перенос веществ возможно используя ионофоры. Ионофоры - это небольшие гидрофобные молекулы, которые растворяются в липидных бислоях и повышают их проницаемость для ионов. Боль шинство ионофоров синтезируется микроорганизмами (антибиотики – грамицин А) и широко приме няются для повышения проницаемости мембран по отношению к опре деленным ионам. Классификация ионофоров: подвижные пере носчики ионов и каналообразующие ионофоры. Механизм действия: действуют, экранируя заряд транспортируемого иона так, чтобы послед ний мог пройти гидрофобную внутреннюю область липидного бислоя, т.е. позволяют ионам двигаться по электрохимическим градиентам. 26.Проницаемость мембран к различным веществам. Коэффициенты проницаемости и распределения. Количественный параметр проникновения веществ в клетку - коэффициенты проницаемости (закон Фика) : чем выше липофильность вещества, тем выше коэффициент распределения. 1/А+dS/dt=-DKp Cн-Св/дельтаХ. D-коэффициент диффузии, А-площадь поверхности, Сн, Св-концентрация снаружи и внутри, Кр-коэффициент распределения представляющий отношение концентрации растворенного вещества в мембране к концентрации вне мембраны, дельтаХ - расстояние, преодолеваемое соединением при прохождении через мембрану. D=dKp/dx- коэффициент проницаемости. Кр=С2/С1. С1-водная фаза, С2-не водная (масло, липид). Не учтены взаимодействия в системе: между молекулами растворенного вещества или между растворенным веществом и растворителем. ЭХП (мю) характеризуется свободной энергией некоторого вещества и другие виды потенциальной энергии являются относительной величиной.  В случаях переноса не заряженных частиц. Система в состоянии равновесия, когда электрохи мический потенциал вещества одинаков по обеим сторонам мембраны: 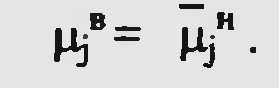 Процесс переноса веществ через мембраны с помощью переносчика описывается в рамках кинетики Михаэлиса- Ментен. Состояние насыщения описывается уравнением: 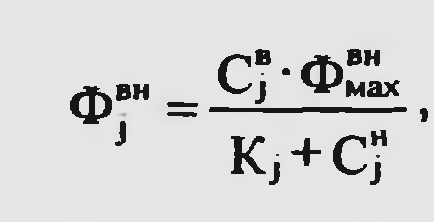 27.Влияние ксенобиотиков на барьерно-траспортные свойства мембраны и физ хим характеристики цитоплазмы. Физико-химические изме нения в цитоплазме являются ведущими в процессах жизне деятельности клетки. Вязкость. Вяз кость – свойство, присущее жидкостям, обладающим внутрен ней структурой. Основное вещество цитоплазмы – цитозоль содер жит систему микрофиламентов. Крупные молекулы – белки и РНК – образуют коллоидный раствор, который может быть золем (невязким) или гелем (вязким). Взаимодействие гидратированных ионов ксенобиотиков с за ряженными белковыми молекулами цитоплазмы может вызы вать переходы золя в гель и обратно. Она служит хорошим показателем физиологического состояния клеток, уровня их жизнедеятельности. В структурной вязкости находит отраже ние реакция живых организмов на изменение внешних усло вий (температура, освещение и др.) и, конечно, на химические агенты. Движение цитоплазмы. Скорость движения цитоплазмы (СДЦ) варьируется от не скольких микрометров в секунду до десятков и зависит от усло вий окружающей среды (свет, температур, рН) и от присутствия ксенобиотиков. Индуцируемое химическими агентами движение цитоплаз мы получило название хемодинеза. Заметное влияние на СДЦ оказывают ксенобиотики, подавляющие обмен веществ у жи вых организмов. Изоэлектрическая точка цитоплазмы (ИЭТ). Значение рН, при котором белок имеет минимальный элек трический заряд, принято называть ИЭТ. В растворе с рН, рав ном ИЭТ, белок не движется ни к одному из полюсов, тогда как в кислой среде он перемещается к катоду, а в щелочной – к аноду. Различные ксенобиотики, имеющие кислотные или щелоч ные свойства, способны сдвигать величину рН в ту или иную сторону и тем самым изменять ИЭТ цитоплазмы. Влияние ксенобиотиков на проницаемость мембран. (антибиотики - бактериальные мембраны). Химические соединения: вызывают структур ные перестройки в мембранах, могут изменять условия для диффузии других соединений как через гидрофобные липидные участки, так и через гидрофильные поры (каналы), способны воздейство вать на переносчики, могут влиять на транспорт соединений, которые переносятся через биологические мембраны, могут ингибировать активный перенос соединениями, нарушающими сопряжение ме жду транспортной системой и источником энергии. 28.Пути поступления и выведения ксенобиотиков. Основные пути поступления токсических ксенобиотиков (про мышленных ядов, пестицидов) в организм человека - это органы ды хания и кожа, а также пищеварительный тракт: до 70 % человек получает с пищей, 20 % - из воздуха, 10 %-с водой. Через слизистую оболочку дыхательных путей поступают ксено биотики, находящиеся в газо- и парообразном состоянии, в виде аэро золей и пыли. Через кожу проникают преимущественно липофильные вещества, находящиеся в жидком или газообразном состоянии при непосредст венном контакте. Проникновение ксенобиотиков через слизистую оболочку пищева рительного тракта наблюдается при аварийных ситуациях в результате заглатывания распыленных в воздухе токсических аэрозолей, при применении отравляющих веществ, при поступлении отравленных пищи и воды и т. д. Экскреция ксенобиотиков и их метаболитов через различные выде лительные системы - заключительный этап в процессе поступления и трансформации. Экскреция осуществляется через почки, легкие, кожу, кишечник, слюнные, потовые, слезные, сальные железы, а также мо лочные железы при лактации. Почечная экскреция ксенобиотиков - основной путь удаления из организма ксенобиотиков и продуктов их биотрансформации. В основе почечной экскреции лежат следующие биологические процессы: клу бочковая фильтрация, канальцевая секреция, канальцевая реабсорбция. Экскреция ксенобиотиков легкими. Через легкие удаляются в ос новном летучие и газообразные вещества, например ингаляционные наркотики и их метаболиты, промышленные газы, а также продукты печеночной биотрансформации многих токсических веществ, в том числе хлорированных углеводородов, этанола и т. д. Экскреция ксенобиотиков печенью. Выделение метаболитов или конъюгатов из гепатоцитов происходит главным образом через систему желчных ходов или после обратного всасывания в синусоиды — через почки. Интенсивность желч ной экскреции зависит также от соотношений между константами свя зывания ксенобиотиков с белками гепатоцитов и плазмой крови. Выделение через молочные железы - в период лактации. 29.Общая схема процесса биотрансформации. Общая картина превращения ксенобиотиков в высших организмах представляется следующей:  Окислительные, восстановительные и гидролитические процессы называют реакциями функциональными или преконъюгационными, а реакции синтеза - конъюгационными. Общей тенденцией является превращение экзогенного вещества в более полярную форму и последующее связывание образовавшегося производного с высокополярным фрагментом, который облегчает вы деление ненужных организму веществ посредством имеющихся у него соответствующих функций. 30.Основные реакции метаболизма ксенобиотиков: окисление, восстановление, гидролиз, дегалогенирование, конъюгация. Наиболее широко в живых организмах представлены ферменты и ферментативные системы, катализирующие процессы окисления, вос становления, гидролиза ксенобиотиков и синтеза метаболитов, содер жащих эндогенные соединения. Наиболее активной системой в мета болических превращениях являются микросомные ферменты. Реакции, участвующие в путях биотрансформации чужеродных веществ разделяют на 4 класса: реакции окисления; реакции восстановления; реакции деградации (гидролиза); ре акции конъюгации. Реакции окисления. Особое место принадлежит микросомным монооксигеназам (детоксикация чужеродных веществ в организмах). Оксигеназа (монооксигеназа) - это фермент, катализирующий ре акцию элементарного кислорода с некоторым субстратом, в процессе которой один из атомов кислорода входит в состав субстрата, тогда как второй атом кислорода реагирует с другим акцептором, чаще всего водородом, образуя воду: Окисление спиртов и альдегидовосуществляется алкогольдегидрогеназой, альдегидоксидазами и др. ферментами. 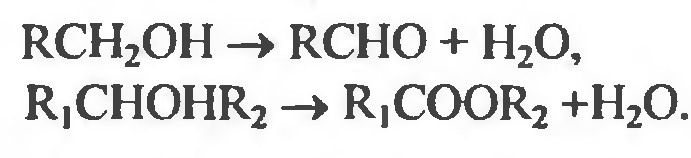  Окисление аминов (получается канцероген – диэтилнитрозамин):   Окисление ароматических аминов:  Гидроксилирование кольцевых систем(алициклические кольце вые структуры гидроксилируются легче, чем ароматические, в этом заключается причина высокой токсичности бензола, ферменты – оксигеназы):  Окислительное дезалкилирование О- и N-атомов: необходим кислород и монооксигеназами (динитроанилины, фенилмочевина, симметричные триазины, фосфорорганические соединения, алкиламины). ВЫВОД: при окислительной биотрансформа ции ксенобиотиков нередко получаются более токсичные или канцеро генные соединения. Реакции восстановления. Менее обычны, чем реакции окисления. Альдегиды и кетоны могут восстанавливаться в спирты под действием алкогольдегидрогеназ (ацетон может входить в цикл аэробного метаболизма через ацетоацетат и ацетил-КоА):  Восстановление нитро- и азогрупп(нитробензол, паранитробензойная кисло та и хлорамфеникол):  Восстановление N-оксидов (катализируется N-оксиредуктазами). Гидролиз. Сложные чужеродные вещества могут гидролизоваться рядом гидролитических ферментов (гидролаз), находящихся в печени и плазме крови. Гидролиз эфиров карбоновых кислот: Эстеразы классифицируют по группам веществ, на которые они воздействуют, и по их отношению к ингибиторам: а) арилэстеразы гидролизуют ароматические эфиры; б) карбоксилэстеразы гидролизуют преимущественно алифатиче ские эфиры; участвуют в метаболизме многочисленных фосфорорганических инсектицидов; в) холинэстергидролазы действуют наиболее эффективно на эфиры холина; г) ацетилэстеразы подобны ферментам, указанным в первой группе, однако они по-другому реагируют на воздействие ингибиторов. Гидролиз амидов, гидразидов и нитрилов. Фосфорорганические вещества гидролизуются с помощью фер ментов, атакующих эфирные связи или действующих на ангидриды кислот (фторгидролаза, β-глюкуронидаза и сульфатаза). Реакции конъюгации. К конъюгационным относятся процессы био синтеза, в результате которых из ксенобиотиков или их метаболитов и эндогенных продуктов образуются сложные вещества. Схематически реакцию конъюгации можно представить в следую щем виде: RX+эндогенное соединение (донорное вещество) – (над стрелкой - фермент) – конъюгат. Реакции конъюгации катализируются ферментами - трансферазами, переносящими заместитель в другое соединение. Реакции конъюгации считаются высо коэффективными путями снижения токсичности некоторых ксенобио тиков. Ацетат конъюгируется при участии ацетил-КоА с некоторыми ароматическими аминами и сульфонамидами (ацетил-трансферазами): Глицин. Конъюгация глицина с бензойной кислотой - одна из первых изученных реакций биотрансформа ции  Глутатионовая конъюгация (нафталин, антацен, фенантрен)  Алкилирование с участием метионина и этионина (метилированиея пиридина, пирогаллола; сульфиты, селениты, теллуриты ). Орнитин и аргинин (бензойная кислота). Рибоза и глюкоза (гликолизирование ксенобиотиков). Глюкуроновая кислота (образова ние глюкуронидов) - детоксикация спиртов, фенолов, карбокислот, аминов, гидроксиламинов, карбамидов, сульфонамидов и тиолов (уридиндифосфатглюкуронозилтрансфераза УДФГТ).  Сульфатная конъюгация (сульфатирование: фенолы, спирты, ароматические амины, гидроксиламины, некоторые стероиды - сульфат-аденилтрансферазы, аденилсульфаткиназы).  Конъюгирование является обезвре живанием вещества лишь для данного организма. Дегалогенирование. Формально реакции дегалогенирования хлор содержащих ксенобиотиков могут относиться к описанным выше преконъюгационным классам реакций, но экологическая важность этих процессов требует к себе более внимательного отношения. Проблемы дегалогенирования освещены на примерах ДДТ, и т. д. Виды реакций дегалогенирования: гидролитические, восстановительные, окислительные. Гидролитическое дегалогенирование изучено у хлорированных алифатических кислот. Восстановительное дегалогенирование - это реакция замещения атома галоида на водород. Окислительное дегалогенирование: а) дегидрогалогенирование; б) окислительное дегалогенирование с образованием двойной связи; в) дегалогенирова ние - гидроксилирование с участием молекулярного кислорода. 31.Принципы функционирования ферментативных систем. Ферменты — белковые молекулы, выполняющие функцию биологических катализаторов. Специфичность — наиболее важное свойство ферментов, определяющее биологическую значимость этих молекул. Различают субстратную и каталитическую специфичности фермента, определяемые строением активного центра. Субстратная специфичность: способность каждого фермента взаимодействовать лишь с одним или несколькими определёнными субстратами (абсолютная, групповая и стерео). Абсолютная субстратная специфичность. Активный центр ферментов, обладающих абсолютной субстратной специфичностью, комплементарен только одному субстрату. Следует отметить, что таких ферментов в живых организмах мало. Групповая субстратная специфичность. Большинство ферментов катализирует однотипные реакции с небольшим количеством (группой) структурно похожих субстратов. Большинство протеолитических ферментов, осуществляющих гидролиз белков, имеет групповую субстратную специфичность, гидролизуя пептидные связи, образованные разными аминокислотами. Стереоспецифичность. При наличии у субстрата нескольких стерео-изомеров фермент проявляет абсолютную специфичность к одному из них. Каталитическая специфичность. Фермент катализирует превращение присоединённого субстрата по одному из возможных путей его превращения. Это свойство обеспечивается строением каталитического участка активного центра фермента и называется каталитической специфичностью, или специфичностью пути превращения субстрата. Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы (коферментах) и/или в ионах металлов (кофакторах). Белковая часть получила название «апофермент», который в отсутствие кофермента не обладает каталитической активностью. Кофермент с белковой молекулой (апоферментом) формируют молекулу холофермента, обладающую каталитической активностью. 32.Характеристика ферментов, катализирующих метаболизм ксенобиотиков. Метаболические превращения ксенобиотиков можно классифицировать с учетом природы ферментов: Окисление микросомалъными ферментами: гидроксилирование ациклических, ароматических и алициклических соединений, эпоксидирование, дезапкилирование, дезаминирование и сульфирование. Восстановление микросомальными ферментами: восстановление нитро- и азосоединений. Немикросомное окисление: дезаминирование, окисление спиртов и альдегидов, ароматизация алициклических соединений. Немикросомное восстановление: восстановление альдегидов и кетонов. Гидролиз: гидролиз сложных эфиров и амидов с участием микросомальных и немикросомальных ферментов. Прочие реакции: сюда относятся дегидроксилирование катехолов и гидроксамовых кислот, дегалогенирование, разрыв кольца, образова ние кольца, восстановление ненасыщенных соединений, восстановле ние дисульфидов в тиолы, окислительное расщепление мышьякови стых соединений в арсеноксиды и т. д.Основная тенденция метаболических процессов в организмах выс ших животных заключается в снижении сложности молекулы, введе нии в нее при необходимости полярных заместителей и в дальнейшем повышении растворимости в воде посредством сопряжения (конъюгирования) еще до вывода из организма с последующей секрецией. |
