КОЛЛОКВИУМ 2. 1. Предмет, задачи, методы генетики. История развития генетики. Роль отечественных ученых (Н. К. Кольцов, А. С. Серебровский, С. С. Четвериков) в развитии генетики
 Скачать 408 Kb. Скачать 408 Kb.
|
|
26.Болезни человека с наследственной предрасположенностью, механизмы их возникновения и проявления. Примеры. Эта группа болезней отличается от генных болезней тем, что для своего проявления нуждается в действии факторов внешней среды. Среди них также различают моногенные, при которых наследственная предрасположенность обусловлена одним патологически измененным геном, и полигенные. Последние определяются многими генами, которые в нормальном состоянии, но при определенном взаимодействии между собой и с факторами среды создают предрасположение к появлению заболевания. Они называются мультифакториальными заболеваниями (МФЗ). Заболевания моногенные с наследственным предрасположением относительно немногочисленны. К ним применим метод менделевского генетического анализа. Учитывая важную роль среды в их проявлении, они рассматриваются как наследственно обусловленные патологические реакции на действие различных внешних факторов (лекарственных препаратов, пищевых добавок, физических и биологических агентов), в основе которых лежит наследственная недостаточность некоторых ферментов. К таким реакциям могут быть отнесены наследственно обусловленная непереносимость сульфаниламидных препаратов, проявляющаяся в гемолизе эритроцитов, повышении температуры при применении общих анестезирующих средств. Наряду с химическими агентами у людей отмечается наследуемая патологическая реакция на физические факторы (тепло, холод, солнечный свет) и факторы биологической природы (вирусные, бактериальные, грибковые инфекции, вакцины). Иногда отмечается наследственная устойчивость к действию биологических агентов. Например гетерозиготы HbA HbS устойчивы к заражению возбудителем тропической малярии. К болезням с наследственной предрасположенностью, обусловленной многими генетическими и средовыми факторами, относятся такие заболевания, как псориаз, сахарный диабет, шизофрения. Этим заболеваниям присущ семейный характер, и участие наследственных факторов в их возникновении не вызывает сомнений. Однако генетическая природа предрасположенности к ним пока не расшифрована. Нередко предрасположенность к ряду заболеваний наблюдается у людей с определенным сочетанием различных генов. Так, у людей со II (А) группой крови чаще наблюдается рак желудка и кишечника, матки, яичников и молочной железы, а также пернициозная анемия, сахарный диабет, ишемическая болезнь сердца, холецистит, желчно-каменная болезнь, ревматизм. У людей с I (0) группой крови чаще встречается язвенная болезнь желудка и двенадцатиперстной кишки. Установление с помощью различных методов генетических исследований точного диагноза заболевания, выяснение роли наследственности и среды в его развитии, определение типа наследования в случае наследственных болезней дают возможность врачу разрабатывать методы лечения и профилактики появления этих заболеваний в следующих поколениях. ^ Другие особенности: 1.Мало различается риск рождения больного ребенка для потомства и сибсов пробанда. Например, расщелина губ и неба составляет для обоих категорий 4% 2.Конкордантность МБ не достигает 100%. как при моногенных, но выше чем показатель дизиготных У МБ 21-63%. Если этот показатель в 4 раза выше. чем у дизиготных –модель полигенного наследования предпочтительнее 3.Риск рождения ребенка с мультифакториальным заболеванием прямо пропорционален тяжести порока: 4.Риск МП для родственников первой степени родства значительно превышает популяционный и выше аналогичного 2 и 3 степени родства. Шизофрения риск для 1 –9-13, а для 2 –3% 5.Риск зависит от числа больных в семье % :чем больше больных. тем больше риск. Например, анэнцефалия после рождения одного больного –2-5%, а после третьего - уже 15-20% 6. Влияние пола Вывих бедра чаще встречается у девочек. Если пробанд женского пола, то для братьев риск =1%. а для сестер –5%. Если пробанд мужского пола, то для братьев-5%. а для сестер –7%. т. е. порог проявления для чаще поражаемого пола ниже, чем для реже поражаемого. 27.Генеалогический метод изучения генетики человека. Особенности наследования признаков в родословных с аутосомно-доминантным, аутосомно-рецессивным, Х-сцепленным и У-сцепленным типах наследования. В основе этого метода лежит составление и анализ родословных. Родословные человека составлялись на протяжении многих столетий в отношении царствующих семейств в Европе и Азии. Как метод изучения генетики человека генеалогический метод стали применять только с начала XX столетия, когда выяснилось, что анализ родословных, в которых прослеживается передача из поколения в поколение какого-то признака (заболевания), может заменить собой фактически неприменимый в отношении человека гибридологический метод. При составлении родословных исходным является человек — пробанд, родословную которого изучают. Обычно это или больной, или носитель определенного признака, наследование которого необходимо изучить. С помощью генеалогического метода может быть установлена наследственная обусловленность изучаемого признака, а также тип его наследования (аутосомно-доминантный, аутосомно-рецессивный, X-сцепленный доминантный или рецессивный, Y-сцепленный). При анализе родословных по нескольким признакам может быть выявлен сцепленный характер их наследования, что используют при составлении хромосомных карт. Этот метод позволяет изучать интенсивность мутационного процесса, оценить экспрессивность и пенетрантность аллеля. Он широко используется в медико-генетическом консультировании для прогнозирования потомства. Однако необходимо отметить, что генеалогический анализ существенно осложняется при малодетности семей. Родословные при аутосомно-доминантном наследовании. - равная вероятность встречаемости данного признака как у мужчин, так и у женщин. Это обусловлено одинаковой двойной дозой генов, расположенных в аутосомах у всех представителей вида и получаемых от обоих родителей, и зависимостью развивающегося признака от характера взаимодействия аллельных генов. При доминировании признака в потомстве родительской пары, где хотя бы один родитель является его носителем, он проявляется с большей или меньшей вероятностью в зависимости от генетической конституции родителей (рис. 6.25). 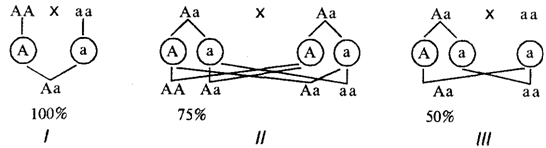 Если анализируется признак, не влияющий на жизнеспособность организма, то носители доминантного признака могут быть как гомо-, так и гетерозиготами. В случае доминантного наследования какого-то патологического признака (заболевания) гомозиготы, как правило, нежизнеспособны, а носители этого признака — гетерозиготы. Таким образом, при аутосомно-доминантном наследовании признак может встречаться в равной мере у мужчин и у женщин и прослеживается при достаточном по численности потомстве в каждом поколении по вертикали. Анализируя родословные, необходимо помнить о возможности неполного пенетрирования доминантного аллеля, обусловленной взаимодействием генов или факторами среды. Показатель пенетрантности может быть вычислен как отношение фактического числа носителей признака к числу ожидаемых носителей этого признака в данной семье. Необходимо также помнить, что некоторые заболевания проявляются не сразу с момента рождения ребенка. Многие болезни, наследуемые по доминантному типу, развиваются лишь в определенном возрасте. Так, хорея Гентингтона клинически проявляется к 35—40 годам, поздно проявляется и поликистоз почек. Поэтому при прогнозировании подобных заболеваний в расчет не принимаются братья и сестры, не достигшие критического возраста. Родословные при аутосомно-рецессивном наследовании. Рецессивные признаки проявляются фенотипически лишь у гомозигот по рецессивным аллелям. Эти признаки, как правило, обнаруживаются у потомков фенотипически нормальных родителей — носителей рецессивных аллелей. Вероятность появления рецессивного потомства в этом случае равна 25%. Если один из родителей имеет рецессивный признак, то вероятность проявления его в потомстве будет зависеть от генотипа другого родителя. У рецессивных родителей все потомство унаследует соответствующий рецессивный признак. Для родословных при аутосомно-рецессивном типе наследования характерно, что признак проявляется далеко не в каждом поколении. Чаще всего рецессивное потомство появляется у родителей с доминантным признаком, причем вероятность появления такого потомства возрастает в близкородственных браках, где оба родителя могут являться носителями одного и того же рецессивного аллеля, полученного от общего предка. Родословные при доминантном Х-сцепленном наследовании признака. Гены, расположенные в Х-хромосоме и не имеющие аллелей в Y-хромосоме, представлены в генотипах мужчин и женщин в разных дозах. Женщина получает две свои Х-хромосомы и соответствующие гены как от отца, так и от матери, а мужчина наследует свою единственную Х-хромосому только от матери. Развитие соответствующего признака у мужчин определяется единственным аллелем, присутствующим в его генотипе, а у женщин он является результатом взаимодействия двух аллельных генов. В связи с этим признаки, наследуемые по Х-сцепленному типу, встречаются в популяции с разной вероятностью у мужского и женского пола. При доминантном Х-сцепленном наследовании признак чаще встречается у женщин в связи с большей возможностью получения ими соответствующего аллеля либо от отца, либо от матери. Мужчины могут наследовать этот признак только от матери. Женщины с доминантным признаком передают его в равной степени дочерям и сыновьям, а мужчины — только дочерям. Сыновья никогда не наследуют от отцов доминантного Х-сцепленного признака. Примером такого типа наследования служит описанная в 1925 г. родословная с фолликулярным кератозом —кожным заболеванием, сопровождающимся потерей ресниц, бровей, волос на голове (рис. 6.30). Характерным является более тяжелое течение заболевания у гемизиготных мужчин, чем у женщин, которые чаще всего являются гетерозиготами. При некоторых заболеваниях наблюдается гибель мужчин-гемизигот на ранних стадиях онтогенеза. Тогда в родословных среди пораженных должны быть только женщины, в потомстве которых отношение пораженных дочерей, здоровых дочерей и здоровых сыновей равно 1:1:1. Мужские доминантные гемизиготы, не погибающие на очень ранних стадиях развития, обнаруживаются в самопроизвольных абортах или среди мертворожденных. Такими особенностями наследования у человека характеризуется пигментный дерматоз. Родословные при рецессивном Х-сцепленном наследовании признаков. Характерной особенностью родословных при данном типе наследования является преимущественное проявление признака у гемизиготных мужчин, которые наследуют его от матерей с доминантным фенотипом, являющихся носительницами рецессивного аллеля. Как правило, признак наследуется мужчинами через поколение от деда по материнской линии к внуку. У женщин он проявляется лишь в гомозиготном состоянии, вероятность чего возрастает при близкородственных браках. Наиболее известным примером рецессивного Х-сцепленного наследования является гемофилия. Другим примером наследования по данному типу является дальтонизм — определенная форма нарушения цветоощущения. Родословные при Y-сцепленном наследовании. Наличие Y-хромосомы только у представителей мужского пола объясняет особенности Y-сцепленного, или голандриче-ского, наследования признака, который обнаруживается лишь у мужчин и передается по мужской линии из поколения в поколение от отца к сыну. Одним из признаков, Y-сцепленное наследование которого у человека все еще обсуждается, является гипертрихоз ушной раковины, или наличие волос на внешнем крае ушной раковины. Предполагают, что в коротком плече Y-хромосомы кроме этого гена находятся гены, определяющие мужской пол. В 1955 г. у мыши описан определяемый Y-хромосомой трансплантационный антиген, названный HY. Возможно, он является одним из факторов половой дифференцировки мужских гонад, клетки которых имеют рецепторы, связывающие этот антиген. Связанный с рецептором антиген активизирует развитие гонады по мужскому типу (см. разд. 3.6.5.2; 6.1.2). Этот антиген в процессе эволюции остался почти неизменным и встречается в организме многих видов животных, в том числе и человека. Таким образом, наследование способности к развитию гонад по мужскому типу определяется голандрическим геном, расположенным в Y-хромосоме (рис. 6.32). Сущность генеалогического метода. -установление наследственной этиологии заболевания - установление типа наследования - установление локализации гена в хромосоме - дифференциация болезней генетической этиологии с близкими к ним ненаследственми формами - дифференциация наследственных заболеваний, несходных по гены наследования. 28.Близнецовый метод изучения генетики человека, возможности метода. Определение соотносительной роли наследственности и среды в развитии признаков и патологических состояний человека. Рождение близнецов – довольно редкое явление. В европейских странах 1-1,2% всех родов – близнецы, в Восточной Европе РФ 1,5%, в Нигерии 4%, в Японии 0,7% у европеоидов – 0,7% у негроидов – 1,1% у монголоидов – 0,2% Эти различия касаются дизиготных близнецов. Зависит от возраста матери (чем старше, тем больше вероятность рождения близнецов), искусственное оплодотворение. Монозиготные близнецы – редкое явление, не зависит от возраста, расы, географического положения и условий жизни. Имеют большое значение для анализа т. к. очень похожи. Близнецовый метод позволяет установить, в какой мере признак зависит от генов и в какой – от внешней среды (т. к. организм взаимодействует с окружающей средой). Используются понятия: конкордантность и дискордантность. Близнецовые методы часто используются для исследования туберкулеза, сахарного диабета, шизофрении, эпилепсии и других болезней и отклонений. Этот метод заключается в изучении закономерностей наследования признаков в парах одно - и двуяйцевых близнецов. Он предложен в 1875 г. Гальтоном первоначально для оценки роли наследственности и среды в развитии психических свойств человека. В настоящее время этот метод широко применяют в изучении наследственности и изменчивости у человека для определения соотносительной роли наследственности и среды в формировании различных признаков, как нормальных, так и патологических. Он позволяет выявить наследственный характер признака, определить пенетрантность аллеля, оценить эффективность действия на организм некоторых внешних факторов (лекарственных препаратов, обучения, воспитания). Суть метода заключается в сравнении проявления признака в разных группах близнецов при учете сходства или различия их генотипов. Монозиготные близнецы, развивающиеся из одной оплодотворенной яйцеклетки, генетически идентичны, так как имеют 100% общих генов. Поэтому среди монозиготных близнецов наблюдается высокий процент конкордантных пар, в которых признак развивается у обоих близнецов. Сравнение монозиготных близнецов, воспитывающихся в разных условиях постэмбрионального периода, позволяет выявить признаки, в формировании которых существенная роль принадлежит факторам среды. По этим признакам между близнецами наблюдается дискордантность, т. е. различия. Напротив, сохранение сходства между близнецами, несмотря на различия условий их существования, свидетельствует о наследственной обусловленности признака. Трудности близнецового метода связаны, во-первых, с относительно низкой частотой рождения близнецов в популяции (1:86—1:88), что осложняет подбор достаточного количества пар с данным признаком; во-вторых, с идентификацией монозиготности близнецов, что имеет большое значение для получения достоверных выводов. Для идентификации монозиготности близнецов применяют ряд методов. 1. Полисимптомный метод сравнения близнецов по многим морфологическим признакам (пигментации глаз, волос, кожи, форме волос и особенностям волосяного покрова на голове и теле, форме ушей, носа, губ, ногтей, тела, пальцевым узорам). 2. Методы, основанные на иммунологической идентичности близнецов по эритроцитарным антигенам (системы АВО, MN, резусу), по сывороточным белкам (γ-глобулину). 3. Наиболее достоверный критерий монозиготности предоставляет трансплантационный тест с применением перекрестной пересадки кожи близнецов. Несмотря на трудоемкость близнецового метода и возможность ошибок при определении монозиготности близнецов, высокая объективность выводов делает его одним из широко применяемых методов генетических исследований у человека. 29.Молекулярно-генетические методы исследований генетики человека. Эти методы позволяют анализировать фрагменты ДНК, находить и изолировать отдельные гены и их сегменты и устанавливать в них последовательность нуклеотидов. Для выявления специфических фрагментов ДНК используется метод блот-гибридизации по Саузерну. Эта методика состоит из следующих этапов: 1) после окончания электрофореза гели помещают в щелочной раствор для денатурации фрагментов ДНК — получают одноцепочечные ДНК; 2) одноцепочечные ДНК вымывают из геля на нитроцеллюлозный или нейлоновый фильтры перпендикулярным поверхности геля током буфера; одноцепочечные фрагменты ДНК фиксируют на фильтре; 3) для визуального выявления нужных фрагментов проводят гибридизацию исследуемого образца со специфическим по нуклеотид-ной последовательности меченным радиоактивно или флюоресцентной меткой олигонуклеотидным синтетическим зондом; радиоактивно меченные участки выявляют путем экспонирования фильтра с рентгеновской пленкой (ауторадиография); флюоресцентные метки выявляют в люминесцентном микроскопе. Этот метод позволяет обнаружить единственный ген среди десятков тысяч. Гомологичные последовательности можно идентифицировать как полностью, так и частично. Различные модификации этого метода позволяют в клинике анализировать очень малые количества ДНК, взятые у больного. 30.Цитогенетический метод изучения генетики человека. Денверская и Парижская классификация хромосом. Возможности идентификации хромосом человека Цитогенетический метод основан на микроскопическом изучении хромосом в клетках человека. Его стали широко применять в исследованиях генетики человека с 1956 г., когда шведские ученые Дж. Тийо и А. Леван, предложив новую методику изучения хромосом, установили, что в кариотипе человека 46, а не 48 хромосом, как считали ранее. Современный этап в применении цитогенетического метода связан с разработанным в 1969 г. Т. Касперсоном методом дифференциального окрашивания хромосом, который расширил - возможности цитогенетического анализа, позволив точно идентифицировать хромосомы по характеру распределения в них окрашиваемых сегментов (см. разд. 3.5.2.3). Применение цитогенетического метода позволяет не только изучать нормальную морфологию хромосом и кариотипа в целом, определять генетический пол организма, но, главное, диагностировать различные хромосомные болезни, связанные с изменением числа хромосом или с нарушением их структуры. Кроме того, этот метод позволяет изучать процессы мутагенеза на уровне хромосом и кариотипа. Применение его в медико-генетическом консультировании для целей пренатальной диагностики хромосомных болезней дает возможность путем своевременного прерывания беременности предупредить появление потомства с грубыми нарушениями развития. Материалом для цитогенетических исследований служат клетки человека, получаемые из разных тканей,—лимфоциты периферической крови, клетки костного мозга, фибробласты, клетки опухолей и эмбриональных тканей и др. Непременным требованием для изучения хромосом является наличие делящихся клеток. Непосредственное получение таких клеток из организма затруднено, поэтому чаще используют легкодоступный материал, каковым являются лимфоциты периферической крови. В норме эти клетки не делятся, однако специальная обработка их культуры фитогемагглютинином возвращает их в митотический цикл. Накопление делящихся клеток в стадии метафазы, когда хромосомы максимально спирализованы и хорошо видны в микроскоп, достигается обработкой культуры колхицином или колцемидом, разрушающим веретено деления и препятствующим расхождению хроматид. Микроскопирование мазков, приготовленных из культуры таких клеток, позволяет визуально наблюдать хромосомы. Фотографирование метафазных пластинок и последующая обработка фотографий с составлением кариограмм, в которых хромосомы выстроены парами и распределены по группам, позволяют установить общее число хромосом и обнаружить изменения их количества и структуры в отдельных парах В качестве экспресс-метода, выявляющего изменение числа половых хромосом, используют метод определения полового хроматина в неделящихся клетках слизистой оболочки щеки. Половой хроматин, или тельце Барра, образуется в клетках женского организма одной из двух Х-хромосом. Оно выглядит как интенсивно окрашенная глыбка, расположенная у ядерной оболочки (см. рис. 3.77). При увеличении количества Х-хромосом в кариотипе организма в его клетках образуются тельца Барра в количестве на единицу меньше числа Х-хромосом. При уменьшении числа Х-хромосом (моносомия X) тельце Барра отсутствует. В мужском кариотипе Y-хромосома может быть обнаружена по более интенсивной по сравнению с другими хромосомами люминесценции при обработке их акрихинипритом и изучении в ультрафиолетовом свете. Хромосомы бывают: -метацентрические -субметацентрические -акроцентрические. . Общее число хромосом в гаплоидном наборе равно.23. Все хромосомы пронумерованы и распределены по классам. Из них к классу А относятся хромосомы 1, 2;3; к классу В хромосомы 4, 5; к классу С - хромосомы 6, 7,8, 9,10,11, 12; к классу D - хромосомы 1З 14,15; к классу Е-хромосомы 16,17, 18; к классу F-хромосомы 19,20; к классу G- хромосомы 21, 22. Перечисленные хромосомы называются аутосомы, они имеются и у мужчин, и у женщин. В диплоидном наборе (2п=46) каждая аутосома представлена двумя гомологами. Двадцать третья хромосома является половой хромосомой она может быть представлена или X или Y-хромосомой. Половые хромосомы у женщин, представлены двумя Х-хромосомами, а у мужчин одной Х-хромосомой и одной Y-хромосомой. Изменение кариотипа, как правило, связано с развитием генетических заболевании (см. ниже). Благодаря культивированию клеток человека in vitro можно быстро подучить достаточно большой материал для приготовления препаратов. Для кариотипирования обычно используют кратковременную культуру лейкоцитов периферической крови (рис. 7)-Цитогенетические методы используются и для описания интерфазных клеток. Например, по наличию или отсутствию полового хроматина (телец Барра, представляющих собой инактивированные Х-хромосомы) можно не только определять пол индивидов, но и выявлять некоторые генетические заболевания, связанные с изменением числа X-хромосом (см. ниже). Группы хромосом А-1-3 большие метацентрические Б - 4-5 большие субметацентрические С-6-12 средние субметацентрические d - 13-15- акроцентрические е-16-18 короткие метацентрические f-19-20 мелкие метацентрические g - 21-22 маленькие акроцентрические 23- половые. Согласно Парижской классификации хромосомы разделены на группы по их размерам и форме, а также линейной дифференцировке. В настоящее время используются дифференциальные методы окрашивания метафазных хромосом с избирательным выявлением их отдельных фрагментов. Топография окрашиваемых участков по длине хромосомы зависит от локализации определенных фракций ДНК, например сателлитной, распределения участков структурного гетерохроматина и ряда других факторов. Применяют 4 основных метода дифференциальной окраски: Q, G, R и С. Все они выявляют закономерную линейную неоднородность фрагментов по длине метафазных хромосом. Характер окрашивания специфичен для каждой негомологичной хромосомы, что дает их точную идентификацию (рис. 19). Постоянство локализации окрашиваемых фрагментов позволяет составить «химические» карты хромосом. Сопоставление этих карт с генетическими используется для расшифровки функционально-генетических особенностей различных районов хромосом. На основе избирательной окраски в 1971 году в Париже были разработаны карты линейной дифференцированности хромосом человека и предложена система их обозначения. Латинскими буквами р и q обозначаются соответственно короткое и длинное плечо хромосомы. От центромеры к теломере по имеющимся отчетливым морфологическим указателям (маркерам) в каждом плече выделяют районы, обозначаемые арабскими цифрами. В пределах районов идентифицируют сегменты — регулярные участки, отличающиеся по интенсификации окраски. Они также обозначаются арабскими цифрами. Так, символ 1р22 означает 2-й сегмент 2-го района короткого плеча хромосомы 1. Так для Х-хромосомы человека известны 96 локусов, некоторые из которых картированы. Имеются «пучки» сцепленных генов, концентрирующихся вокруг локусов цветовой слепоты, группы крови Xq и др. (рис.19). Классификация и номенклатура равномерно окрашенных хромосом человека впервые были приняты на международном совещании в 1960 году в г. Денвере, в дальнейшем несколько измененные и дополненные (Лондон, 1963 и Чикаго, 1966). Согласно Денверовской классификации все хромосомы человека разделены на 7 групп, расположенных в порядке уменьшения их длины и с учетом центриольного индекса (отношение длины короткого плеча к длине всей хромосомы, выраженное в процентах). Группы обозначаются буквами английского алфавита от А до G. Все пары хромосом принято нумеровать арабскими цифрами. Характеристика групп представлена в табл. 4. Предложенная классификация позволяла четко различать хромосомы, принадлежащие к различным группам. С 1960 года начинается бурное развитие клинической цитогенетики: в 1959 году Дж. Лежен открыл хромосомную природу синдрома Дауна; К. Форд, П. Джекобс и Дж. Стронг описали особенности кариотипа при синдромах Клайнфельтера и Тернера; в начале 70-х гг. была открыта хромосомная природа синдромов Эдвардса, Патау, синдрома «кошачьего крика»; описана хромосомная нестабильность при ряде наследственных синдромов и злокачественных заболеваниях. Вместе с тем применение метода получения равномерно окрашенных хромосом оказалось недостаточно эффективным для идентификации хромосом. Недостатком денверской классификации является то, что разграничение гомологичных пар внутри группы хромосом встречает зачастую непреодолимые трудности. Идиограммы - систематизированного кариотипа. В 1960 году была предложена Денверская международная классификация хромосом, где хромосомы классифицированы по величине и расположению центромеры. В кариотипе соматической клетки человека различают 22 пары аутосом и пару половых хромосом. Набор хромосом в соматических клетках называют диплоидным, а в половых клетках - гаплоидным (он равен половине набора аутосом). В идиограмме кариотипа человека хромосомы делят на 7 групп, в зависимости от их размеров и формы. 1 - 1-3 крупные метацентрические. 2 - 4-5 крупные субметацентрические. 3 - 6-12 и Х-хромосома средние метацентрические. 4 - 13-15 средние акроцентрические. 5 - 16-18 относительно малые мета-субметацентрические. 6 - 19-20 малые метацентрические. 7 - 21-22 и Y-хромосома наиболее малые акроцентрические. |
