|
|
Шпаргалки акрипол. Акрипол вопросы-1. 2. Классификация водорастворимых полимеров, примеры. Классификация
Ценность метода – быстрота и возможность работать с очень малыми количествами полимера (несколько мг). Метод оказывается очень полезным при подборе систем осадитель-растворитель для препаративного фракционирования, при определении пределов растворимости сополимеров, для качественной оценки ММР полимеров при изучении механизма полимеризации и т.д.
Ультрацентрифугирование
Он является единственным методом, позволяющим непосредственно получить кривые распределения по молекулярным весам.
Однако этот метод очень сложен по конструктивному оформлению и требует выполнения ряда условий: свойства раствора должны оставаться постоянными иногда в течение нескольких суток, а растворитель и полимер должны обладать разными плотностями, растворитель должен иметь низкую вязкость, а полимер — растворяться при комнатной температуре.
Гель-проникающая хроматография
Этот метод объединяет в себе непрерывное фракционирование образца с анализом фракций.
Непременное условие ГПХ – полное отсутствие адсорбции.
Ограничения
1. Метод ГПХ – это относительный метод определения молекулярных масс. Следовательно, для определения ММР полимера необходимо знать калибровочную зависимость lgМ=f(Vr). В современных приборах эта задача решается путем использования детектора многоуглового рассеяния света, позволяющего определять в ходе анализа ГПХ абсолютную средневесовую молекулярную массу полимера. Можно также использовать вискозиметрический детектор и рассчитывать ММР по универсальной калибровочной зависимости Бенуа. Такой подход применим и для разветвленных макромолекул.
2. В применении метода ГПХ для анализа сополимеров, особенно композиционно-неоднородных, т.е. представляющих собой набор макромолекул разного состава. Для анализа таких продуктов желательно использовать высокоэффективную жидкостную хроматографию (ВЭЖХ), однако в этом случае требуется дополнительный трудоемкий поиск элюирующих систем.
Несмотря на указанные недостатки, метод ГПХ стал доступным, легким, простым и широко используемым методом определения ММР полимеров.
Удерживаемый объем: 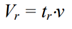
где 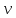 – объемная скорость протекания растворителя через колонку (мл/мин); – объемная скорость протекания растворителя через колонку (мл/мин);
t – время удерживания.
Метод светорассеяния – один из основных количественных методов исследования полимеров в растворе, который, не требуя специальной калибровки, позволяет напрямую определять молекулярную массу и радиус инерции макромолекул, а также дает возможность оценивать термодинамические параметры межмолекулярного взаимодействия. Метод основан на классической теории Рэлея – рассеяние света малыми частицами в газах. Интенсивность падающего света уменьшается экспоненциально:
I/I0=exp(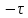 x) x)
где I0 и I – интенсивности падающего света и прошедшего через среду толщиной x, 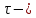 мутность среды, характеризующая долю пучка света, рассеянного во всех направлениях при прохождении через среду толщиной 1 см. мутность среды, характеризующая долю пучка света, рассеянного во всех направлениях при прохождении через среду толщиной 1 см.
Можно применить только для определения молекулярного веса сравнительно низкомолекулярных полимеров.
Осмометрический метод
Для определения молекулярного веса полимера следует изменить осмотическое давление растворов при нескольких концентрациях и экстраполировать полученную прямую к нулевой концентрации. Осмометрическим методом можно измерять молекулярный вес от 104 до 106Да. Зависимость приведенного осмотического давления от концентрации для разбавленных растворов полимеров выражена уравнением: 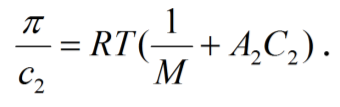
Статический метод состоит в том, что измеряется равновесная разность уровней в осмометре. Статический метод обычно не рекомендуется для определения молекулярной массы полимеров, которые могут структурироваться.
Динамический метод основан на измерении скорости проникновения растворителя через мембрану в зависимости от приложенного давления. Основным достоинством динамического метода является быстрота измерений.
Криоскопический и эбулиоскопический методы
Криоскопия основана на измерении понижения температуры замерзания раствора исследуемого вещества по сравнению с чистым растворителем. А эбулиоскопия на повышении температуры кипения.
Коэффициенты пропорциональности К и Е в этих формулах называют криоскопической и эбуллиоскопической константами. Они равны понижению температуры замерзания и повышению температуры кипения при единичной моляльности раствора. Константы К и Е является константами растворителей и приведены в справочниках физико-химических величин.
Зависимость ∆T/C от С представляет собой прямую, отсекающую на оси координат отрезок, равный K/Mn, тангенс угла которой характеризует второй вириальный коэффициент. Так криоскопический и эбулиоскопический методы определения Mn применяется для полимеров с молекулярной массой от 103 до 5∙104.
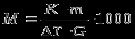
М — молекулярная масса растворённого вещества;
К — эбулиоскопическая или криоскопическая константа;
m — масса растворённого вещества;
G — масса растворителя;
Вискозиметрический метод
Измерение вязкости жидкостей производят чаще всего в капиллярных вискозиметрах, и оно основано на уравнении Пуазейля, которое, в свою очередь, выведено из закона Ньютона. При исследовании разбавленных растворов полимеров определяют относительную вязкость, при условии, что плотности разбавленного раствора (ρ) и чистого растворителя (ρ0) практически совпадают.
Для вязкости разбавленного раствора непроницаемых, сплошных, невзаимодействующих частиц справедлива формула Эйнштейна. Обычно применяемая размерность этой величины дл/г (децилитры на грамм) соответствует концентрации раствора, выраженной в г/100 мл.
Уравнение Марка—Куна—Хаувинка. Это уравнение справедливо для широкого круга полимерных веществ и является основным уравнением вискозиметрии разбавленных растворов полимеров.
Константы К и a находят, представив в логарифмической форме уравнение Марка—Куна—Хаувинка. Постоянная K=10–2–10–5 зависит от температуры, природы полимера и растворителя. В общем случае постоянная a изменяется в пределах: 0≤a≤2.
Если значение α близко к единице, то по [η] находится средневесовой молекулярный вес полидисперсного полимера. Однако, если α ≠1, то значение молекулярного веса, определенное по [η], лежит между средневесовым и среднечисловым молекулярными массами и называется «средневязкостным молекулярным весом».
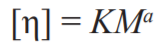
13. Свойства растворов полимеров. Полиэлектролитный эффект сущность.
Ряд свойств растворов полимеров в значительной степени зависит от их концентрации. В связи с этим различают разбавленные и концентрированные растворы, а также полиэлектролиты.
Разбавленными называют растворы, в которых макромолекулы находятся друг от друга на расстояниях, превышающих их собственные геометрические размеры.
Концентрированными называют растворы, в которых макромолекулы растворенного полимера взаимодействуют друг с другом.
Полиэлектролиты – это полимеры, макромолекулы которых содержат функциональные группы, способные к электролитической диссоциации. В зависимости от природы ионогенных групп полиэлектролиты, как и низкомолекулярные электролиты, могут быть сильными и слабыми кислотами, основаниями, солями.
Разбавленные растворы
Осмотическое давление растворов полимеров
Осмотическое давление характеризует с одной стороны число растворенных частиц, а с другой – степень взаимодействия частиц растворителя и растворенного вещества.
Осмотическое давление идеального раствора подчиняется уравнению:
π = сRT или π/с = RT
Растворы полимеров в большинстве случаев не являются идеальными, и их осмотическое давление подчиняется иному уравнению, в котором концентрационная зависимость разложена в ряд Тейлора: π = RT (A1c + A2c2 + A3c3 + ···)
Для разбавленных растворов полимеров (обычно 0.5 – 1%) величина с мала и можно ограничиться первыми двумя членами ряда: π/с = RT(A1 + A2c)
Вязкость растворов полимеров
Вязкость растворов полимеров на много порядков превосходит вязкость растворов низкомолекулярных соединений; это относится даже к сильно разбавленным растворам (менее 1%). Это связано с большими размерами макромолекул, перемещение которых в растворе идет намного труднее, чем «обычных» малых молекул. Для растворов полимеров определяют относительную вязкость:
удельную вязкость:
приведенную вязкость:
характеристическую вязкость:
Зависимость характеристической вязкости от молекулярной массы выражается уравнением Куна-Марка-Хаувинка:
[η] = КМα
Что касается «протекаемости», то здесь возможны два варианта:
«Свободно протекаемый» клубок
«Непротекаемый клубок».
Концентрированные растворы полимеров – это растворы, в которых, в отличие от разбавленных растворов, проявляется заметное взаимодействие между растворенными макромолекулами. Можно считать, что в этих растворах макромолекулы как бы сцеплены в отдельных местах, и в растворе образуется пространственная сетка зацеплений. Свойства концентрированных растворов начинают проявляться для жесткоцепных полимеров уже при концентрациях менее 1%, для гибкоцепных – при концентрациях порядка 5%.
Существование сетки зацеплений приводит к тому, что вязкость концентрированных растворов намного выше вязкости разбавленных; вязкость растворов растет намного быстрее, чем концентрация. Если представить зависимость вязкости от концентрации как η
сn, то для разбавленных растворов n= 1, а для концентрированных n= 10-20.
Растворы полиэлектролитов
Особыми свойствами обладают растворы специфических полимеров – полиэлектролитов. Это – полимеры, в макромолекулах которых содержатся заряженные (ионизированные) или ионогенные (способные к ионизации) группы. Наиболее характерны три типа полиэлектролитов: поликислоты, полиоснования и полиамфолиты.
Поликислоты:
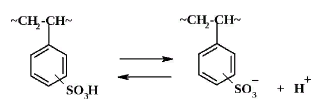 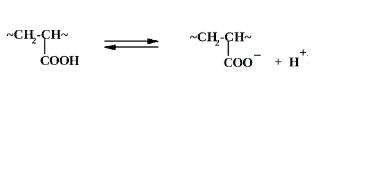
Полиоснования:
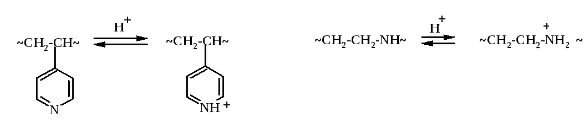
Кислотные и основные звенья:
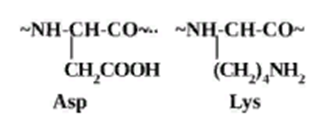
Вязкость растворов полиэлектролитов
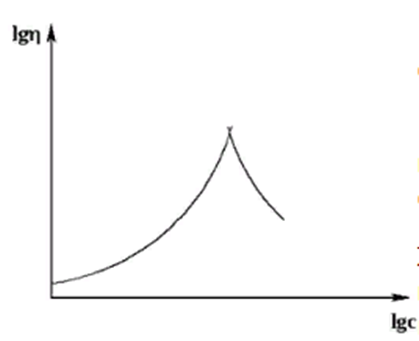
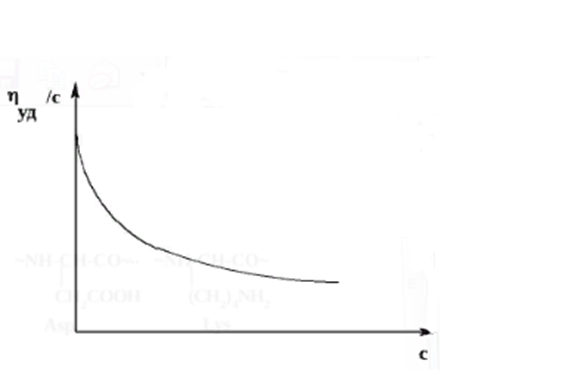
А. Зависимость вязкости от концентрации. В то время как приведенная вязкость «обычных» электронейтральных полимеров с увеличением концентрации растет, для полиэлектролитов картина обратная – она заметно падает с увеличением концентрации.
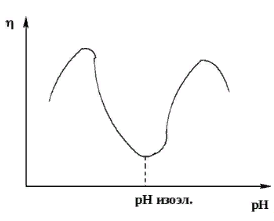
Б. Зависимость вязкости от рН. В разбавленных растворах слабых поликислот (таких, например, как полиакриловая кислота) при добавлении основания (т.е. при увеличении рН) вязкость растет. Причина очевидна: при этом возрастает количество ионизированных групп (например, групп СОО‾) и вследствие отталкивания между ними макромолекулы приобретают вытянутые конформации.
Полиэлектролитный эффект
Характерным свойством растворов высокомолекулярных соединений является высокая вязкость, которая значительно выше вязкости растворов низкомолекулярных веществ тех же концентраций. Для незаряженных полимеров приведенная вязкость ηпр большей частью линейно убывает с уменьшением концентрации раствора, стремясь при экстраполяции к нулевой концентрации, к пределу - характеристической вязкости [η].
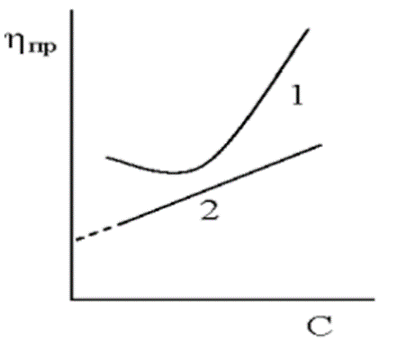 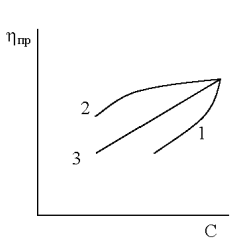
Зависимость вязкости от концентрации для растворов полиэлектролитов подчиняется эмпирическому уравнению Фуосса:

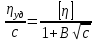
|
|
|
 Скачать 1.72 Mb.
Скачать 1.72 Mb.