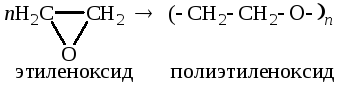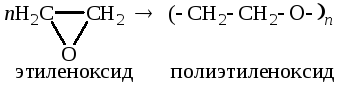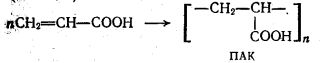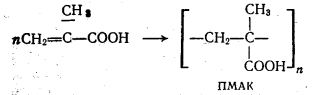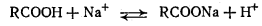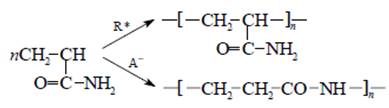|
|
Шпаргалки акрипол. Акрипол вопросы-1. 2. Классификация водорастворимых полимеров, примеры. Классификация
2.Классификация водорастворимых полимеров, примеры.
Классификация.
По молекулярной массе.
- В зависимости от молекулярной массы (ММ), полимеры делятся на:
мономеры (с небольшой ММ) акриламид
олигомеры (с ММ менее 540)
По количеству звеньев различают димер (два звена), тример (3), тетрамер (4), пентамер (5), гексамер (6), и т. д.
- полимеры (высокомолекулярные, с ММ от пяти тысяч до пятисот тысяч) полиакриламид и многие другие
- сверхвысокомолекулярные полимеры с ММ более полумиллиона – белки в основном.
По составу (гомополимер, сополимер, блок-сополимер).
По структуре – линейные, разветвлённые, сетчатые.
По строению основной цепи – гомоцепные, гетероцепные.
Гомоцепные имеют основную цепь из одинаковых атомов (С-С-С-С , S-S-S-S-)
Пример: Полиэтиленимин, полиэтиленоксид
По происхождению – природные, синтетические, искусственные.
Примеры, яичный белок, крахмал
Полимеры и сополимеры акриамида, полиэтиленоксид
Производные целлюлозы, хитозан и его производные.
Природа макромолекул – полярные, неполярные.
Фракционирование, полидисперсность.
3. Получение искусственных водорастворимых полимеров. Примеры.
искусственные полимеры – это высокомолекулярные вещества, которые получают на основе природных полимеров. Искусственные полимеры используют для получения пластмасс, волокон и других материалов.
Пример поливиниловый спирт искусственный, водорастворимый, термопластичный полимер.
В настоящее время промышленный синтез ПВС осуществляют путём полимераналогичных превращений, в частности, с использованием в качестве исходных полимеров простых и сложных поливиниловых эфиров, таких как ПВА. К основным способам получения ПВС можно отнести различные варианты омыления ПВА в среде спиртов или в воде в присутствии оснований и кислот. В зависимости от используемой среды и типа катализатора, процессы омыления ПВА можно представить следующей общей схемой:
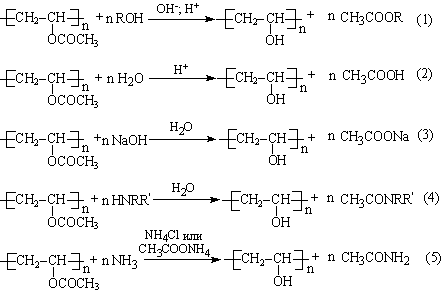
Приведённые схемы реакций можно разбить на три группы: алкоголиз (1), щелочной или кислотный гидролиз (2,3) и аминолиз (4,5). Синтез ПВС через реакцию полиальдольной конденсации из ацетальдегида до настоящего времени оканчивался получением низкомолекулярного полимера.
Основным и главным недостатком используемых технологий является образование жесткого геля в полном объёме реакционного аппарата при достижении конверсии порядка 50 % и неполная степень гидролиза ПВА.
Карбоксиметилцеллюлоза (КМЦ) является простым эфиром целлюлозы, ■содержащим карбоксильную группу. Это производное получается при действии монохлоруксусной кислоты СН2С1СООН или ее натриевой соли на щелочную целлюлозу
[С6Н702(0Н)3 • NaOH],, + п ■ CH2CICOONa —> [C6H702(0H)20CH2C00Na]„-f — п ■ NaCl + тг • Н20
Одновременно с основной реакцией протекает побочная реакция омыления натриевой соли монохлоруксусной кислоты щелочью
CH2ClCOONa-f NaOH CH2OHCOONa -f NaCl
4. Получение, структура и свойства полиоксиэтилена.
ПОЛИЭТИЛЕНОКСИД (полиоксиэтилен) - водорастворимый неионный синтетический термопластичный полимер, получаемый полимеризацией этиленоксида с использованием анионных, катионных или координационнo-анионных катализаторов с раскрытием цикла; общая формула HO[─CH2CH2─O─]nH; относится к полиэфирам простым.
В зависимости от средней молекулярной массы полимера — вязкая жидкость, гелеобразное или твёрдое вещество.
В зависимости от способа получения и молекулярной массы резко различается по свойствам и областям применения. Полиэтиленоксид широко используется в современных технологиях. Особенностью этой группы веществ является хорошая растворимость в воде и большинстве органических растворителей.
Хорошая растворимость и полная физиологическая индифферентность способствовали широкому применению полиэтиленоксидов в фармацевтической практике в качестве гидрофильных основ. Они также находят применение в качестве пластификаторов полиуретановых смол, для получения водорастворимых смол на базе шеллака, в производстве бумаги, кожи, целлофана, каучука и т.д.
Получение полиэтиленоксида(это полиоксиэтилен) полимеризацией окиси этилена.
1. Анионная полимеризация (в присутствии щелочи).
Существует два метода получения полимеров окиси этилена полимеризацией в присутствии щелочи:
Получение полиэтиленоксида в жидкой фазе под давлением.
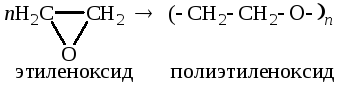
Технический продукт окрашен в коричневый цвет из-за наличия свободной щелочи.
Получение полиэтиленоксида барботированием газообразной окиси этилена в щелочные растворы гликоля.
Оба процесса осуществляются в автоклавах.
2. Катионная полимеризация (в присутствии кислот Льюиса).
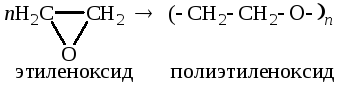
Просто условия разные, а реакция одна и та же, как я понял
Структура полиоксиэтилена
Полиэтиленоксид (полиоксиэтилен) СН2—СН2—О—СН2—СН2—О
– полимер этиленоксида. В зависимости от способа получения и молекулярной массы резко различается по свойствам и областям применения.
Низкомолекулярные полиэтиленоксиды (с молекулярной массой 200-40000): полиэтиленгликоли (ПЭГ), карбовакс;
Высокомолекулярные полиэтиленоксиды (с молекулярной массой 100 000-10 000 000): полиокс, алкокс.
Свойства полиоксиэтилена
В современных технологиях полиэтиленоксид применяют в порошковой металлургии, машиностроении, металлообработке и других отраслях. На основе ПЭО производят смазочные материалы, смазочно-охлаждающие жидкости, растворители, добавки для сыпучих материалов, его используют в археологии при консервировании мокрой древесины.
При внесении полимера (и синтетического, и природного биополимера) в неоднородное температурное поле в нем возникают электрические поля термического происхождения. В результате ориентационной поляризации на границе раздела с вакуумом или металлом на поверхности полимера возникают нескомпенсированные связанные заряды молекулярной природы, поверхностная плотность которых совпадает с нормальной проекцией вектора поляризованности.
По своим механическим свойствам высокомолекулярный полиоксиэтилен подобен полиэтилену среднего давления, но имеет значительно более ярко выраженную термопластичность. В области температур 65—70 °С полиокс резко теряет прочность, однако и выше температуры плавления сохраняет каучукоподобные свойства и исключительно высокие значения вязкости.
Полиэтиленоксид способен значительно (до 70%) снижать гидродинамическое сопротивление в водных и водно-органических растворах при концентрации полимера 0,001— 0,003%. Этот эффект возрастает с увеличением молекулярной массы, но снижается с повышением температуры. Полиэтиленоксид используют для снижения гидродинамического сопротивления в трубопроводах при перекачке жидкостей, растворов, пульп.
5. Получение , структура и свойства полиакриловой , полиметакриловой кислот и их солей.
Акриловая и метакриловая кислоты полимеризуются с образованием твёрдых полимерных кислот, которые в зависимости от молекулярного веса растворяются или набухают в воде.
Гомополимеры акриловой и метакриловой кислот и их щелочные соли неприменимы в качестве обычных пластиков, волокон или плёнок из-за водочувствительности.
Водорастворимые соли полиакриловой и полиметакриловой кислот, а также их сополимеры предложено использовать в качестве загустителей печатных красок, средств для повышения жёсткости в текстильной и ковровой промышленности, модификаторов камедей и крахмалов для получения специальных водных клеев, защитных коллоидов(стабилизаторов) и эмульгаторов, средств для обработки кожи.
Щелочные соли образуют вязкие водные растворы. Полиакрилат натрия совмещается с большей частью анионных и неионных дисперсий и, в отличие от многих природных камедей, не повреждается бактериями и стоек к гидролизу.
Полимер акриловой кислоты – твёрдый продукт белого цвета, нерастворим в мономере, бензоле, кумоле, толуоле, хлорированных углеводородах, ацетоне; растворяется во многих полярных и обычно связанных водородом растворителях, таких как вода, формамид, метанол, этанол, диоксан, этиленгликоль и уксусная кислота. Водный раствор полиакриловой кислоты является типичным полиэлектролитом.
Полиакриловая кислота адсорбирует до 5% влаги, которая оказывает пластифицирующее действие.
Наиболее вероятным представляется строение полимерной цепи «голова к голове»:
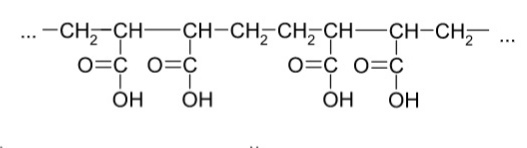
Полиакриловую кислоту получают полимеризацией акриловой кислоты в присутствии инициаторов радикального типа, под действием света, а также под действием γ-излучения.
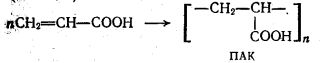
Во время полимеризации кислот выделяется значительное количество тепла.
Для облегчения отвода тепла процесс целесообразно проводить в растворах с концентрацией не выше 25%. В реакцию могут вступать только недиссоциированные молекулы акриловой кислоты. В водных растворах при рН > 6 полимеризация не идёт.
В органических растворах (бензол, толуол, ксилол и др.) полимеризация акриловой кислоты инициируется органическими перекисями, динитрилом азо-бис-изомаслянной кислоты. Ингибиторами могут служить гидрохинон, безводные производные мышьяка, аммония, олова, растворимые в мономере соли металлов, поршкообразная медь и другие соединения.
По химическим свойствам полиакриловую кислоту можно отнести к многоосновным насыщенным органическим кислотам, имеющим низкую степень диссоциации. Соли полиакриловых кислот образуются при действии на её водные растворы оснований или солей более сильных кислот. Полиакриловая кислота легко этерифицируется диазометаном с образованием полиметилкрилата. При обработке полиметакриловой кислоты большим избытком гидразингидрата образуется полиакрилгидразид. Полиакриловая кислота не реагирует с KMnO4, концентрированной HNO3.
Важнейшими свойствами ПАК являются прозрачность, высокая стойкость к старению и воздействию света, хорошая адгезия (в случае полиакрилатов) к различным материалам.
Полимеры АК образуют комплексные соединения с аминами (этилендиамином, пиридином, морфолином, диэтиламином, пиперидином и др.). Комплексы с полиаминами либо выпадают из водного раствора, либо растворяются в нем в зависимости от степени нейтрализации кислотных групп.
Полиметакриловая кислота
Полиметакриловая кислота – карбоцепной полимер; белый, непрозрачный, хрупкий продукт, растворимый в воде, бензоле, о-дихлорбензоле, метаноле, диоксане, тетрагидрофуране и растворах разбавленных щелочей; нерастворим в своём мономере и большинстве органических растворителей.
Получение
Атактическую полиметакриловую кислоту получают полмеризацией метакриловой кислоты по радикальному механизму в блоке (обычно используя в качестве инициаторов перекись бензоила, динитрил азо-бис-изомаслянной кислоты и др.) или в водном растворе (используя для инициирования перекись водорода или водорастворимые окислительно-восстановительные системы).
Изотактическую полиметакриловую кислоту получают гидролизом изотактического полиметилметакрилата.
Получают при полимеризации метакриловой кислоты:
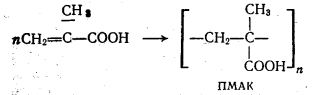
Те же условия, что и при получении ПАК.
Высокомолекулярные полимеры и сополимеры метакриламида, метакриловой кислоты, их солей получают эмульснонной полимеризацией в атмосфере инертного газа в среде вода — органический растворитель, образующий азеотропную смесь. После окончания полимеризацин смесь нейтрализуют бикарбонатом натрия и в виде азеотропа отгоняют воду. Полученный полимер хорошо растворяется в воде.
Полиметакриловая кислота слабый электролит. Свойства её в разбавленных растворах типичны для этого класса соединений, среди которых наиболее характерны реакции с образованием солей и сложных эфиров при участии карбоксильных групп полимерной кислоты.
В концентрированных растворах полиметакриловая кислота обнаруживает тенденцию к гелеобразованию. Особенностью гелей полиметакриловой кислоты является то, что макромолекулы в них находятся в глобулярной, свёрнутой форме, в отличие от обычных гелей других полимеров, образованных развёрнутыми цепями. Ультразвук, рентгеновские и γ-лучи, электронное излучение большой энергии при действии на полиметакриловую кислоту, находящуюся в растворе или в твёрдом состоянии, вызывают деструкцию полимера, более сильную в присутствии окисляющих агентов.
Водные растворы ПМАК имеют кислую реакцию (рН≈3), повышенную вязкость (полиэлектролитные свойства), снижающуюся при добавлении нейтральных солей.
ПМАК могут частично образовывать соли в присутствии ионов Nа+:
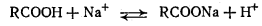
Так же и ПМК.
В нейтральной и слабощелочной средах образуются водорастворимые комплексы ПМАК с лизоцином, сальсолидоном, кумарином, инсулином и другими природными веществами. С поли-4-винилпириднном возникает полнэлектролитный комплекс глобулярного строения (размер глобул соответствует 2—10 макромолекулам).
Полиметакриловая кислота из-за большой гигроскопичности не находит широкого применения в чистом виде.
6. Получение , структура и свойства полимеров акриламида.
Важным химическим свойством акриламида является образование полиакриламида. Радикальная полимеризация на основе акриламида является основным методом синтеза полимеров и сополимеров. Реакцию можно проводить практически всеми известными способами: в растворе, эмульсии, суспензии, а также в массе кристаллических или расплавленных мономеров. Упрощенно радикальная полимеризация акриламида может быть представлена общей схемой:
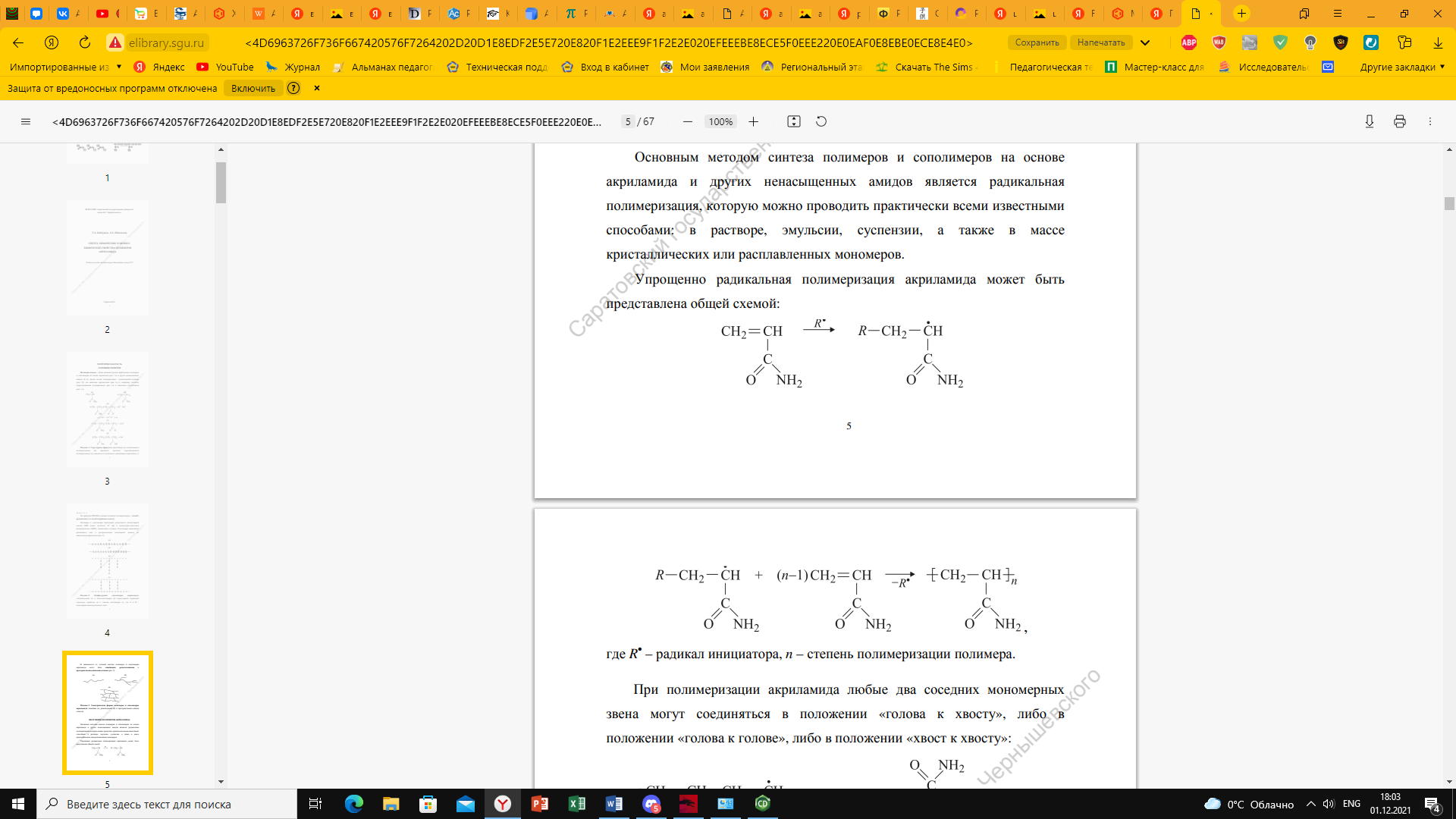

При полимеризации акриламида любые два соседних мономерных звена могут соединяться в положение «голова к хвосту», либо в положении «голова к голове», либо в положении «хвост хвосту».
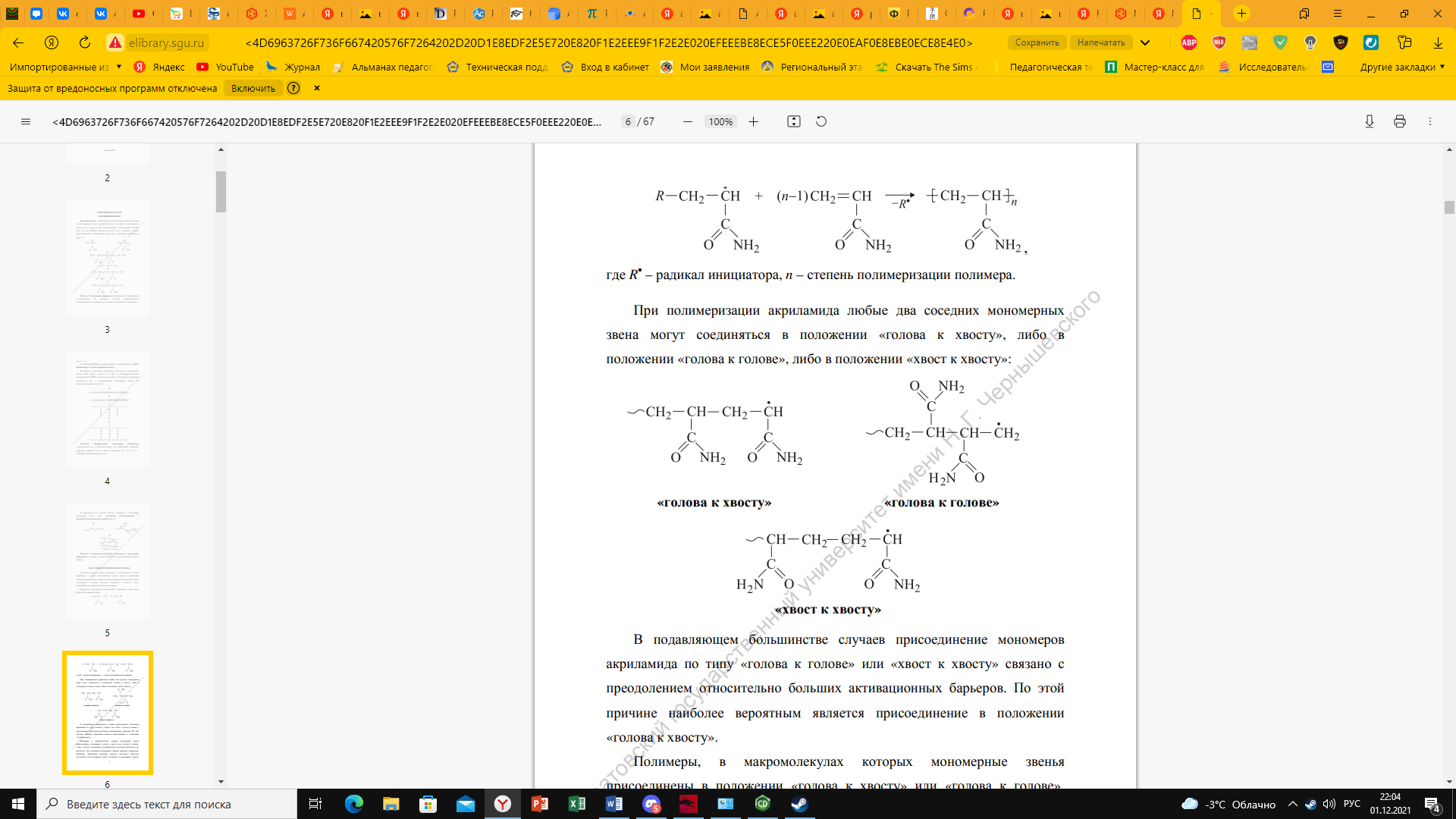
Обрыв цепи при радикальной полимеризации в основном происходит при взаимодействии двух растущих в результате их диспропорционирования:
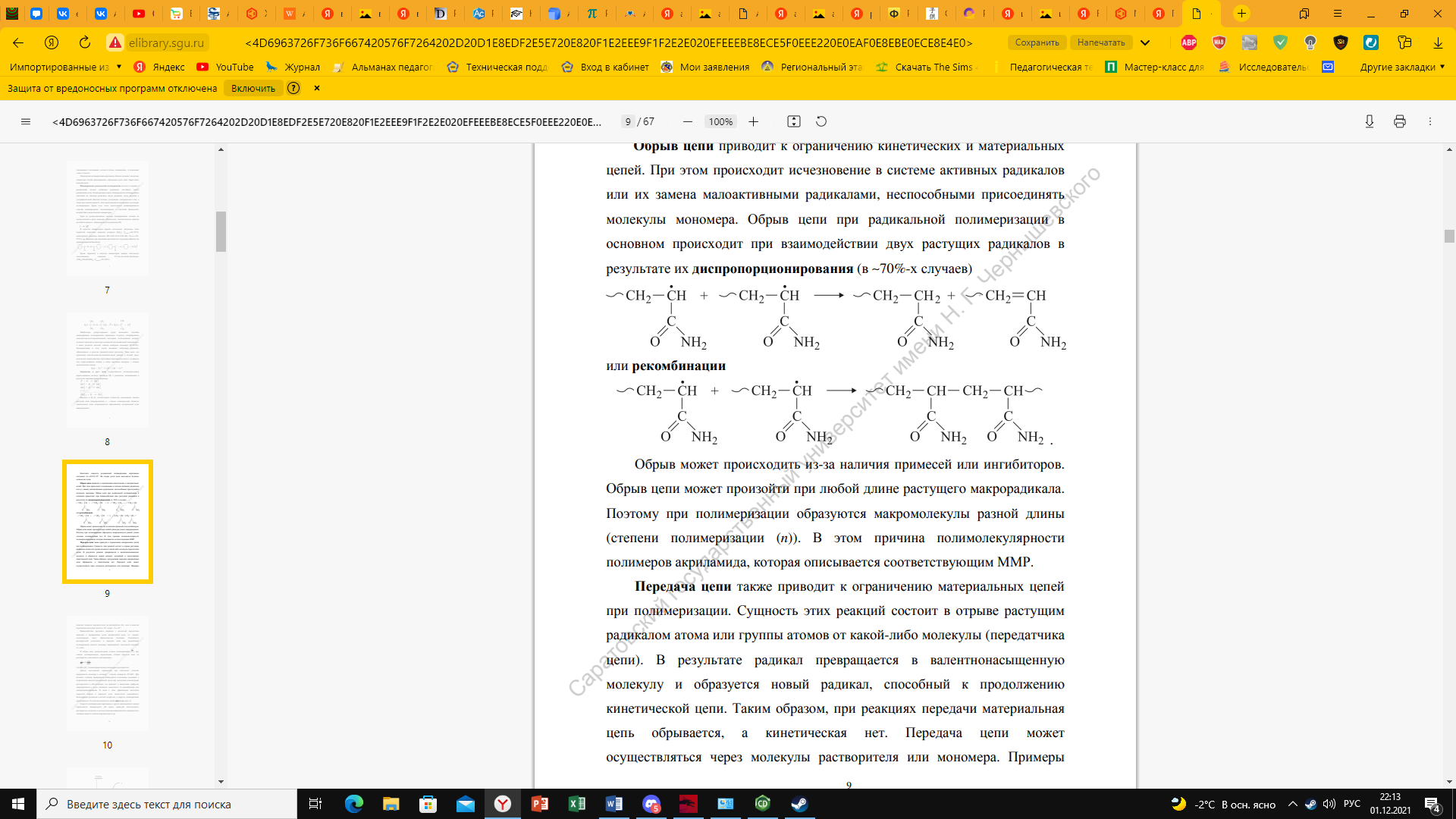
или рекомбинации:

Акриламид вступает в реакции сополимеризации. Пример сополимериации акриламида с акрилонитрилом:
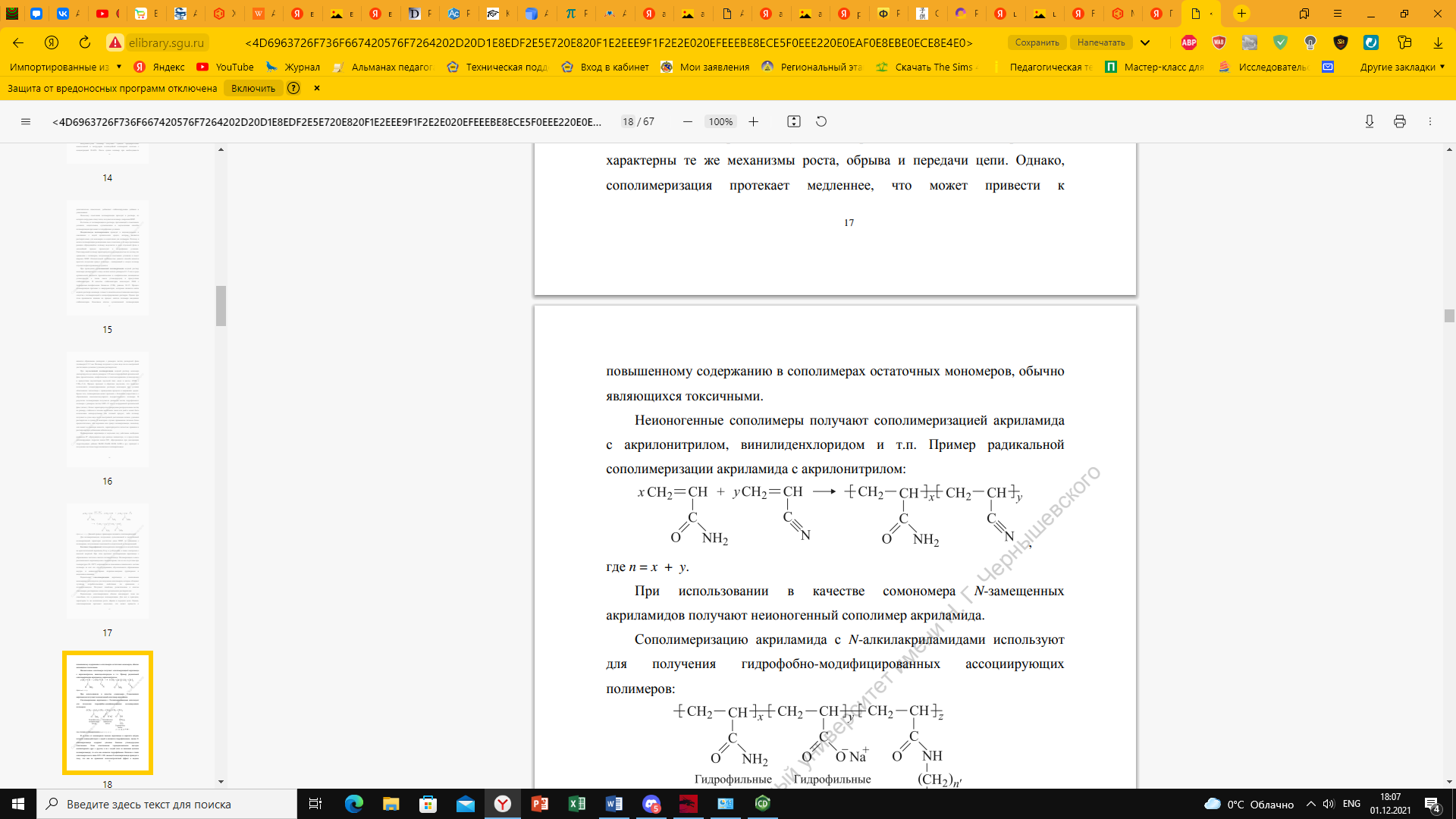
Передача цепи также приводит к ограничению материальных цепей при полимеризации. Сущность этих реакций состоит в отрыве растущим радикалом атома или группы атомов от какой-либо молекулы. При передаче цепи обрывается материальная цепь, а кинетическая продолжается за счет образования нового радикала.
Два пути полимеризации:
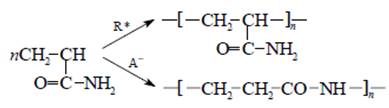
Знаками R* и A- соответственно обозначены радикал и анион. Радикальная полимеризация - основной промышленный метод получения водорастворимого ПАА. При анионной полимеризации образуется поли-β-аланин (найлон-3), нерастворимый в воде полимер, растворяющийся только в некоторых органических растворителях при нагреве.
Сополимеризация акриламида с N- алкилакриламидами используют для получения гидрофобно-модифицированных ассоциирующих полимеров:
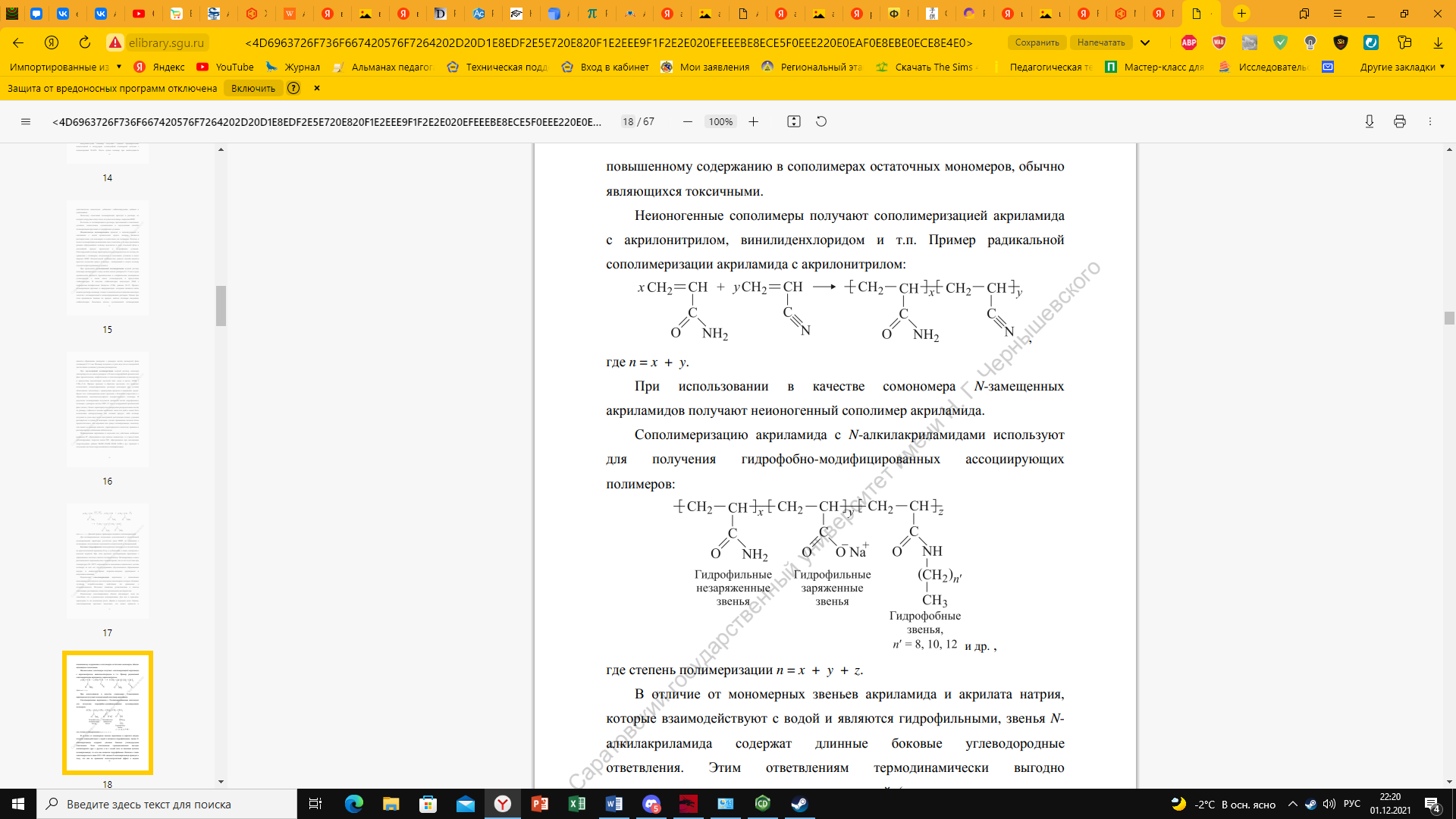
Химические свойства полиакриламида определяются наличием амидной группы. При нагревании или изменении рН его растворов происходит частичный гидролиз с образованием карбоксильных групп. Нагревание полиакриламида выше 100 °С приводит к уменьшению содержания азота вследствие имидизации и появлению сшитых структур. При взаимодействии полиакриламида с формальдегидом в водных растворах (20 °С, рН 8 – 10) или в неводной среде происходит метилолирование: – CONH2+CH2O → – CONHСН2ОН
При нагревании или подкислении полиметилолакриламида или его растворов образуются трехмерные структуры с эфирными (–CONHCH2–О–CH2NHCO-) и метиленовыми (–CONH–CH2–NHCO–) мостиками. К полиакриламиду присоединяется окись этилена: –CONH2 + C2H4О → –CONHCH2–СН2–ОН
Производные ионного характера получают из полиакриламида полимер аналогичными превращениями. Реакция с формальдегидом и бисульфитом в водном растворе приводит к частичному (на 50%) сульфометилированию:
Действие формальдегида и амина (50 – 75 °С, рН = 10,5) вызывает (по реакции Манниха) образование групп – CONHCH2NRR’, наряду с метилоламидными и карбоксильными. Обработка полиакриламида гипохлоритом в щелочной среде (20—30 °С) приводит (по Гофману) к образованию первичных аминогрупп (до 60% от теоретич.).
Наиболее широко используются водорастворимые полимеры АА в качестве флокулянтов для эффективной очистки природных и промышленных сточных вод, улавливания и выделения ионов тяжелых металлов и токсичных веществ, что способствует решению экологической проблемы защиты окружающей среды, и в частности природных водоемов от загрязнений. целлюлозно-бумажная промышленность
|
|
|
 Скачать 1.72 Mb.
Скачать 1.72 Mb.