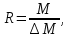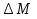Второй важной характеристикой процесса анализа массы являетсядостижимое разрешение (или массовая разрешающая мощность). Массовое разрешение определяется минимальной разницей между двумя значениями m/zдвух видов ионов, которая по-прежнему допускает различие, сделанное во время масс-анализа. Исторически, два пика равной интенсивности считались разрешенными если впадина между ними составляла 10% от максимальной интенсивности. Следовательно, решение разрешени было 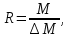 Где М это значение m/zчастичного ионного пика, и 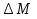 это ширина этого пика на 5% от его высоты. Более недавнее, более свободное (и гораздо более простительное) определение массовое разрешение было принято, используя это ширина этого пика на 5% от его высоты. Более недавнее, более свободное (и гораздо более простительное) определение массовое разрешение было принято, используя 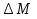 при 50% высоты пика. Несмотря на использованное определение, разрешение больше является функцией m/z, чемскорее «фиксированная» характеристика данного инструмента. при 50% высоты пика. Несмотря на использованное определение, разрешение больше является функцией m/z, чемскорее «фиксированная» характеристика данного инструмента. Наблюдение различных изотопных видов пептидов и белков прогрессивно возрастающего размера может быть достигнута за счет увеличения массовой разрешающей мощности анализатора (Рисунок 3.10). Сверхвысокое разрешение может позволить в некоторых случаях разделять изобарические виды и отчетливо обнаруживать. Разрешение является очень важным для точных измерений массы, как это позволяется во многих случаях точно измерить моноизотопную массу. Однако, очень низкая обогащённостьмоноизотопных пиков большого числа белков делает их детекцию практически невозможной. В таких случаях массовые измерения высокого разрешения не предлагают каких-либо значительных преимуществ сверх «обычной» масс-спектрометрии со скромным разрешением, за исключением возросшей обогащённостимоноизотопных пиков [например, используя изотопное истощение во время экспрессии белка]. Наконец, вопросы, касающиеся рабочего цикла масс-анализатора и его уровня получаемых данных должны быть взяты в рассмотрение, при отборе масс-анализатора имеющегося под рукой для специфических задач. MALDI, из определения, является импульсным процессом и наиболее хорошо сопряжен с анализаторами «быстрого циклирования», которые могут быть синхронизированы с лазером (например, TOF, ионная ловушка). Взаимодействие МАЛДИ со «сканирующими» устройствами, такими как магнитный сектор масс-спектрометра, приводит к значительным потерям к чувствительности и требует продленного времени получения. С другой стороны, ионизация электроспреем это продолжительный ионизационный процесс; следовательно здесь существует широкое разнообразие масс-анализаторов, с которыми он может быть провзаимодействован. До сих пор, накопление генерируемых ионизацией электроспреем ионов во внешнем хранящем устройстве позволяется импульсным введением в TOFили анализатор ловушки ионных масс значительно увеличивается рабочий цикл (и, следовательно, чувствительность) анализа по сравнению с обычной схемой, когда источник ионизации электроспреем взаимодействует непосредственно с медленно сканирующим анализатором. Очень важным преимуществом предлогаемым масс-спектрометрией, как аналитической техникой является способность реализовывать различные «переносимые» методы, непосредственного (онлайн) связывания масс-спектрометрии с разделительными методами для возросшей чувствительности и селективности анализа и реализации стратегий тандемной масс-спектрометрии (MS/MSи MSn) для структурного анализа. 3.3.2. Масс-спектрометрия, комбинированная с разделительными методами Комбинация разделительных техник с масс-спектрометрической детекцией это зрелая область, которая была рассмотрена недавно в нескольких превосходных статьях. В этом разделе мы только пересчитаем определенные функции этой комбинированной техники, которая частично соответствует биофизическим экспериментам, обсуждаемым в следующих главах. Ионизация электроспреем это частично привлекательный интерфейс между жидкостной хроматографией (LC) и масс-спектрометрией за счет продолжительной природы ионизационного процесса, который позволяет анализу элюируемого содержимого быть осуществленным в реальном времени (так называемая «онлайн» LC-MS). Интересно, что самые первый «онлайн» LC-ESIMSанализы пептидов были осуществленны в начале 1980х, предшествуя широкому признанию электроспрея, как надежного аналитического инструмента в биомолекулярном анализе. За двадцать лет, минувшие с этого первого случая, HPLC-ESIMSстала зрелой технологией, с множеством коммерческих инструментов, доступных как интегрированные LS-MSсистемы. Текущее развитие этой технологии идет по двум основным маршрутам, а именно уменьшение масштаба («меньшие колонки» для улучшения пределов детектирования) и уменьшение времени анализа («более быстрые» разделения, чтобы удовлетворить растущие требования высокопропускного анализа). |
 Скачать 102.87 Kb.
Скачать 102.87 Kb.