СЕПСИС-3. 3й международный консенсус определений для сепсиса и септического шока (Сепсис3). Полная версия
 Скачать 235.52 Kb. Скачать 235.52 Kb.
|
|
Рисунок 1. Рекомендации по практическому применению клинических критериев с целью идентификации пациента с сепсисом и септическим шоком 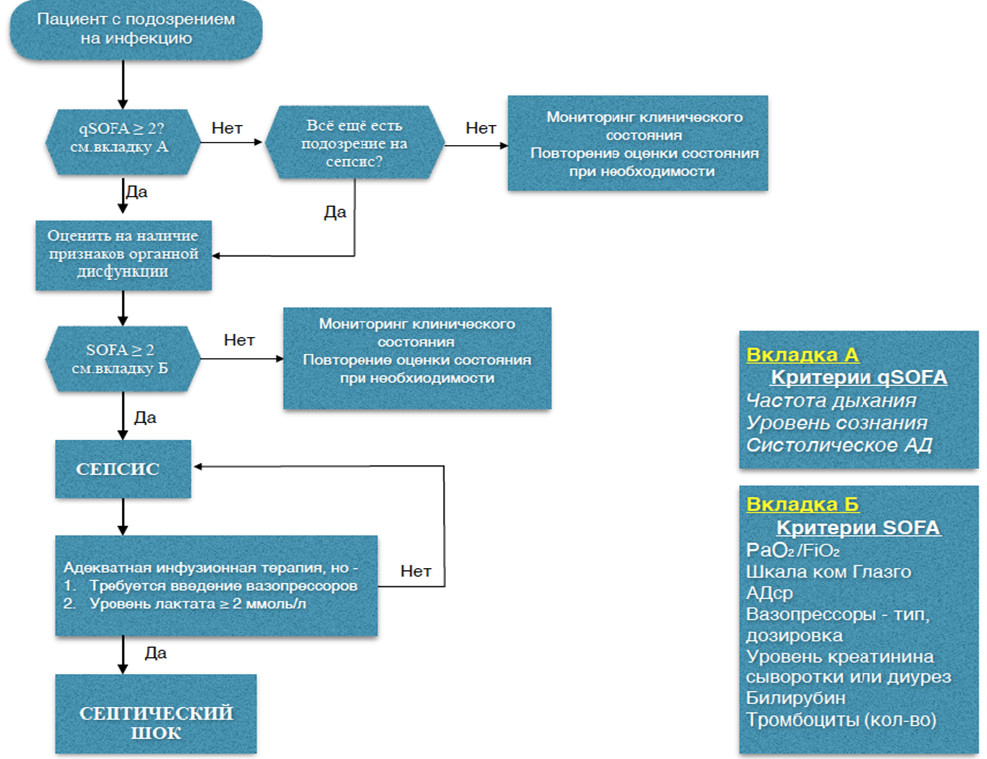 Ожидаемые последствия Рабочая группа сформировала новые определения, в которых объединила современные данные о биологии сепсиса, включая органную дисфункцию (Вкладка 3). Однако, отсутствие стандартных критериев, подобное ситуации и при других синдромах, исключает возможность достоверной оценки и требует приблизительных оценок эффективности через признание обоснованности в различных областях, как уже было сказано выше. Были разработаны и утверждены простые клинические критерии qSOFA, помогающие клиницистам, работающим вне ОРИТ, в идентификации пациентов с инфекцией, у которых плохой прогноз более чем вероятен. Такой подход имеет важные эпидемиологические и исследовательские последствия. Предложенные критерии должны помочь в первичной диагностической классификации, инициировать оценку и немедленное начало лечения. Критерии qSOFA и SOFA могут служить также и как критерии включения при клинических исследованиях. Здесь есть потенциальный конфликт с распространёнными на сегодня шкалами оценки органной дисфункции, шкалами раннего предупреждения и идущими в настоящий момент времени исследованиями. Многие из этих шкал были утверждены на основе консенсуса, в то время как важным аспектом данной работы является сбор данных, хоть и ретроспективно, но из огромной популяции пациентов. Рабочая группа настаивает на том, что стандартизация определений и клинических критериев является ключевым фактором в обеспечении коммуникации и более точной оценки масштабов такой проблемы, как сепсис. Дополнительные сложности вызваны тем, что очень редко инфекция подтверждается микробиологическим анализом до начала лечения. Даже когда микробиологические тесты завершены, сепсис с положительной культурой наблюдается только в 30-40% случаев. И сейчас, когда эпидемиология сепсиса оценивается и создаётся отчёт, в процесс вовлекаются такие косвенные показатели, как начало действия антибиотиков или клинические признаки вероятности инфекции. В будущих эпидемиологических исследованиях следует рассмотреть вопрос и предоставлении отчётности с указанием доли сепсиса с положительной микробиологической культурой. Большая прозрачность и последовательность будет содействовать проведению исследований и более точному кодированию. Изменения в кодировании МКБ и введение их в действие могут занять несколько лет, так что рекомендации, представление в Таблице 2 показывают, каким образом новые определения могут быть применены в рамках существующей МКБ. Дебаты и дискуссии, которые данная работа неизбежно вызовет, будут только поощряться. Аспекты новых определений действительно основаны только на мнении экспертов. Будущее понимание биологии сепсиса, появление новых подходов к диагностике и совершенствование сбора данных приведёт к новой их переоценке и ревизии. Выводы Обновлённые определения и новые клинические критерии смогут внести ясность в уже давно применяемые формулировки и поспособствуют ранней диагностике и своевременному лечению пациентов с сепсисом или с высоким риском развития сепсиса. Но этот процесс всё же остаётся незавершённым и непрерывным. Подобно тому, как это делается с обновлениями программного обеспечения, рабочая группа рекомендует называть новые определения как Сепсис-3, а определения 1991 и 2001 годов признать как Сепсис-1 и Сепсис-2 соответственно. Рабочая группа делает акцент на необходимость будущих изменений. Литература: 1. Torio CM, Andrews RM. National inpatient hospital costs: the most expensive conditions by payer, 2011. Statistical Brief #160. Healthcare Cost and Utilization Project (HCUP) Statistical Briefs. August 2013. http://www.ncbi.nlm.nih.gov/books /NBK169005/. Accessed October 31, 2015. 2. Iwashyna TJ, Cooke CR,Wunsch H, Kahn JM. Population burden of long-term survivorship after severe sepsis in older Americans. J AmGeriatr Soc.2012;60(6):1070-1077. 3. Gaieski DF, Edwards JM, KallanMJ, Carr BG. Benchmarking the incidence and mortality of severe sepsis in the United States. Crit Care Med. 2013;41(5):1167-1174. 4. Dellinger RP, Levy MM, Rhodes A, et al; Surviving Sepsis Campaign Guidelines Committee Including the Pediatric Subgroup. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock: 2012. Crit Care Med. 2013;41(2):580-637. 5. Rhee C, Gohil S, Klompas M. Regulatory mandates for sepsis care—reasons for caution.N Engl J Med. 2014;370(18):1673-1676. 6. Vincent J-L, Marshall JC, Namendys-Silva SA, et al; ICON Investigators. Assessment of the worldwide burden of critical illness: the Intensive Care Over Nations (ICON) audit. Lancet Respir Med. 2014;2(5):380-386. 7. Fleischmann C, Scherag A, Adhikari NK, et al; International Forum of Acute Care Trialists. Assessment of global incidence and mortality of hospital-treated sepsis: current estimates and limitations. Am J Respir Crit Care Med. 2015. 8. Iwashyna TJ, Ely EW, Smith DM, Langa KM. Long-term cognitive impairment and functional disability among survivors of severe sepsis. JAMA. 2010;304(16):1787-1794. 9. Bone RC, Balk RA, Cerra FB, et al. American College of Chest Physicians/Society of Critical Care Medicine Consensus Conference: definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. Crit Care Med. 1992;20(6):864-874. 10. Levy MM, Fink MP, Marshall JC, et al; International Sepsis Definitions Conference. 2001 SCCM/ESICM/ACCP/ATS/SIS International Sepsis Definitions Conference. Intensive Care Med. 2003; 29(4):530-538. 11. Vincent J-L, Opal SM, Marshall JC, Tracey KJ. Sepsis definitions: time for change. Lancet. 2013; 381(9868):774-775. 12. Seymour CW, Liu V, Iwashyna TJ, et al Assessment of clinical criteria for sepsis. JAMA. doi: 10.1001/jama.2016.0288. 13. Shankar-HariM, Phillips G, LevyML, et al Assessment of definition and clinical criteria for septic shock. JAMA.doi:10.1001/jama.2016.0289 14. Angus DC, van der Poll T. Severe sepsis and septic shock. N Engl J Med. 2013;369(9):840-851. 15. WiersingaWJ, Leopold SJ, Cranendonk DR, van der Poll T. Host innate immune responses to sepsis. Virulence. 2014;5(1):36-44. 16. Hotchkiss RS, Monneret G, Payen D. Sepsis-induced immunosuppression: from cellular dysfunctions to immunotherapy. Nat Rev Immunol. 2013;13(12):862-874. 17. Deutschman CS, Tracey KJ. Sepsis: current dogma and new perspectives. Immunity. 2014;40 (4):463-475. 18. Singer M, De Santis V, Vitale D, JeffcoateW. Multiorgan failure is an adaptive, endocrinemediated, metabolic response to overwhelming systemic inflammation. Lancet. 2004;364(9433): 545-548. 19. Hotchkiss RS, Swanson PE, Freeman BD, et al. Apoptotic cell death in patients with sepsis, shock, and multiple organ dysfunction. Crit Care Med. 1999;27(7):1230-1251. 20. Kwan A, Hubank M, Rashid A, Klein N, Peters MJ. Transcriptional instability during evolving sepsismay limit biomarker based risk stratification. PLoS One. 2013;8(3):e60501. 21. Iskander KN, Osuchowski MF, Stearns-Kurosawa DJ, et al. Sepsis: multiple abnormalities, heterogeneous responses, and evolving understanding. Physiol Rev. 2013;93(3):1247-1288. 22. Wong HR, Cvijanovich NZ, Anas N, et al. Developing a clinically feasible personalized medicine approach to pediatric septic shock. Am J Respir Crit Care Med. 2015;191(3):309-315. 23. Langley RJ, Tsalik EL, van Velkinburgh JC, et al. An integrated clinico-metabolomic model improves prediction of death in sepsis. Sci Transl Med. 2013;5 (195):195ra95. 24. Chan JK, Roth J, Oppenheim JJ, et al. Alarmins: awaiting a clinical response. J Clin Invest. 2012;122(8):2711-2719. 25. Churpek MM, Zadravecz FJ,Winslow C, Howell MD, Edelson DP. Incidence and prognostic value of the systemic inflammatory response syndrome and organ dysfunctions in ward patients. Am J Respir Crit Care Med. 2015;192(8):958-964. 26. Kaukonen K-M, BaileyM, Pilcher D, Cooper DJ, Bellomo R. Systemic inflammatory response syndrome criteria in defining severe sepsis. N Engl J Med. 2015;372(17):1629-1638. 27. Vincent JL, Moreno R, Takala J, et al;Working Group on Sepsis-Related Problems of the European Society of Intensive Care Medicine. The SOFA (Sepsis-related Organ Failure Assessment) score to describe organ dysfunction/failure. Intensive Care Med. 1996;22(7):707-710. 28. Vincent JL, de Mendonca A, Cantraine F, et al; Working Group on “Sepsis-Related Problems” of the European Society of Intensive Care Medicine. Use of the SOFA score to assess the incidence of organ dysfunction/failure in intensive care units: results of a multicenter, prospective study. Crit Care Med. 1998;26(11):1793-1800. 29. Rubulotta FM, Ramsay G, Parker MM, Dellinger RP, Levy MM, PoezeM; Surviving Sepsis Campaign Steering Committee; European Society of Intensive Care Medicine; Society of Critical Care Medicine. An international survey: public awareness and perception of sepsis. Crit Care Med. 2009;37(1): 167-170. 30. Le Gall J-R, Klar J, LemeshowS, et al; ICU Scoring Group. The Logistic Organ Dysfunction system: a new way to assess organ dysfunction in the intensive care unit. JAMA. 1996;276(10):802-810. 31. Shah RU, Henry TD, Rutten-Ramos S, Garberich RF, TighiouartM, Bairey Merz CN. Increasing percutaneous coronary interventions for ST-segment elevationmyocardial infarction in the United States: progress and opportunity. JACC Cardiovasc Interv. 2015;8(1 pt B):139-146. 32. Kraut JA, Madias NE. Lactic acidosis. N Engl J Med. 2014;371(24):2309-2319. 33. Casserly B, Phillips GS, Schorr C, et al. Lactate measurements in sepsis-induced tissue hypoperfusion: results from the Surviving Sepsis Campaign database. Crit Care Med. 2015;43(3):567-573. 34. Cecconi M, De Backer D, Antonelli M, et al. Consensus on circulatory shock and hemodynamic monitoring. Task Force of the European Society of Intensive Care Medicine. Intensive Care Med. 2014;40(12):1795-1815. 35. Czura CJ. “Merinoff symposium 2010: sepsis”—speaking with one voice. Mol Med. 2011;17(1-2):2-3. 36. Ait-Oufella H, Bige N, Boelle PY, et al. Capillary refill time exploration during septic shock. Intensive Care Med. 2014;40(7):958-964.Clinical Review & Education Special Communication Consensus Definitions for Sepsis and Septic Shock 810 |
