вариант. МОНОСАХАРИДЫ. Альдозы класс моносахаридов СnH2n
 Скачать 0.88 Mb. Скачать 0.88 Mb.
|
|
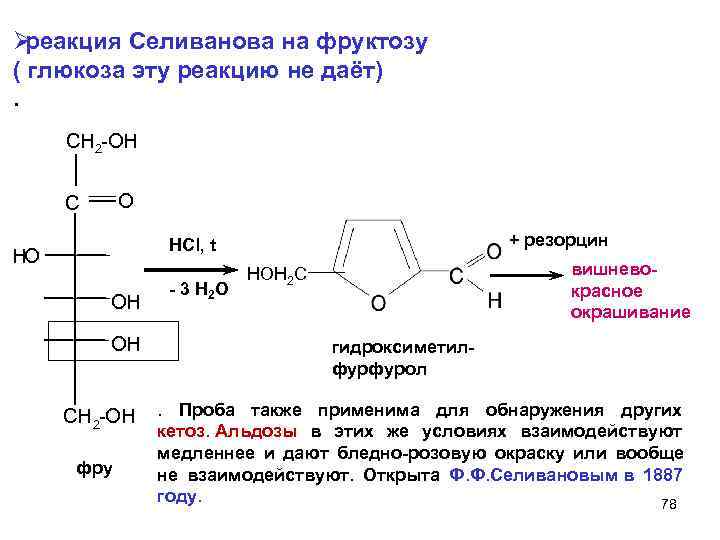
АЛЬДОЗЫ 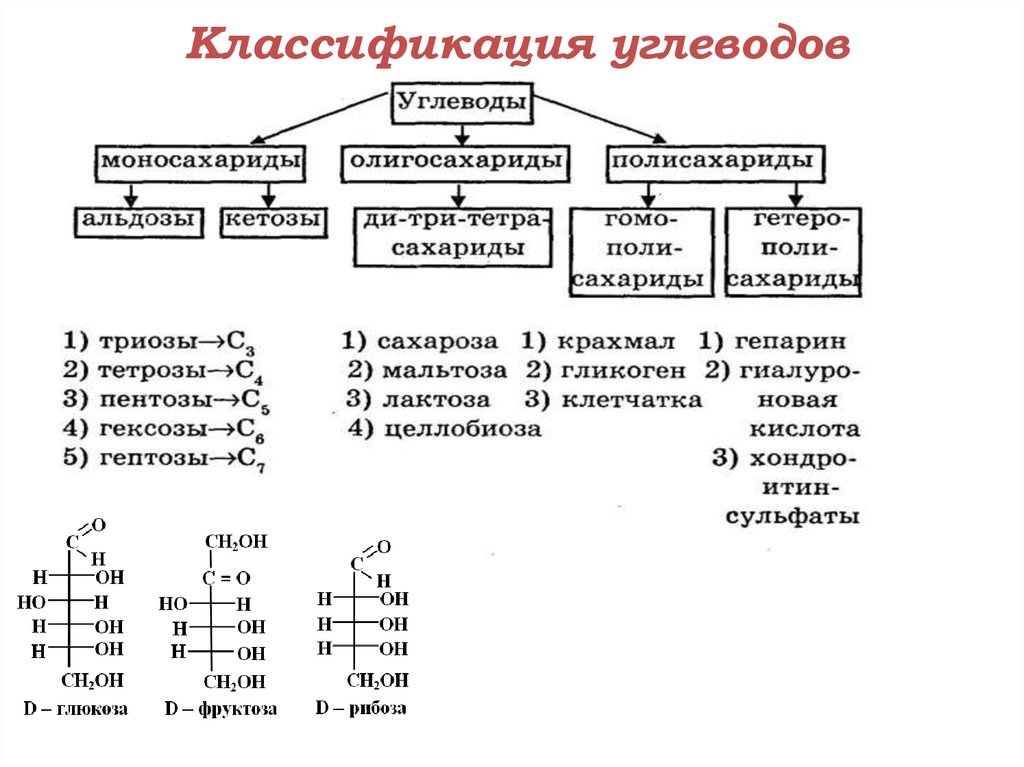 Класс моносахаридов СnH2nOn Общие химические свойства моносахаридов на примере глюкозы В силу своего строения глюкоза обладает химическими свойствами спиртов и альдегидов, а потому проявляет окислительно-восстановительную двойственность. Окислительные свойства глюкозы: гидрирование с образованием сорбита. Восстановительные свойства: с бромной водой, медное зеркало, серебряное зеркало, нитрование с образованием глюконовой кислоты или ее солей, с карбоновыми кислотами и ангидридами с образованием сложных эфиров. Реакции глюкозы по спиртовым группам 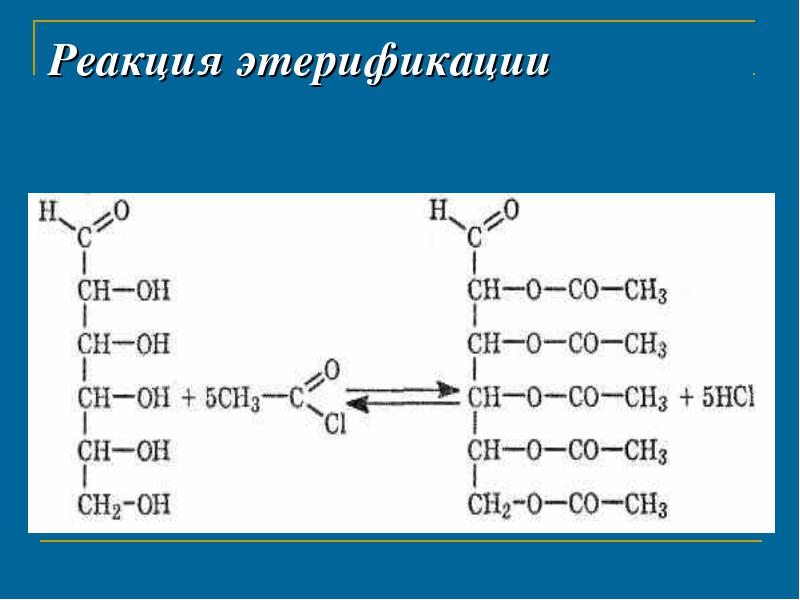 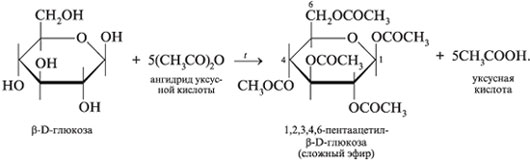 Билогическое значение имеют эфиры фосфорной кислоты – фосфаты, образующиеся по месту последнего звена с участием фермента фосфорилазы: 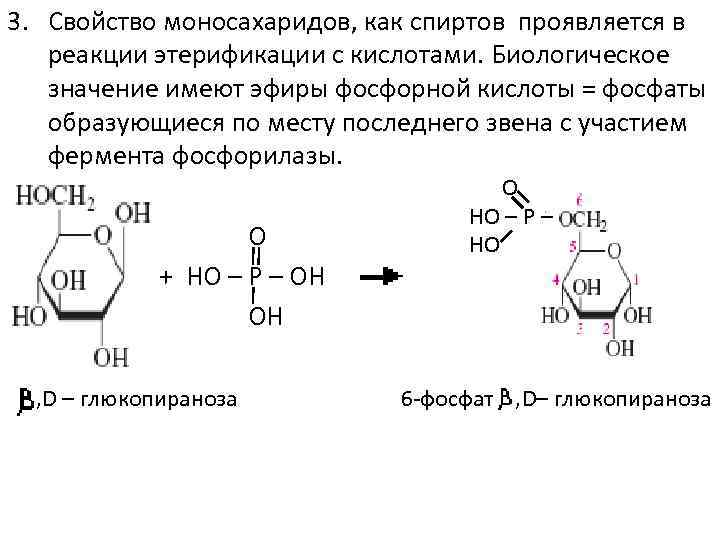 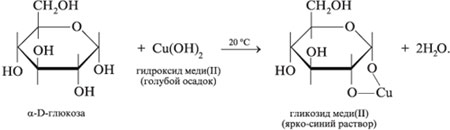
Реакции глюкозы по альдегидной группе 1. Восстановление водородом (гидрирование) и комплексными гидридами металлов (боргидрид натрия NaBH4, алюмогидрид лития LiAlH4) в шестиатомный спирт сорбит: 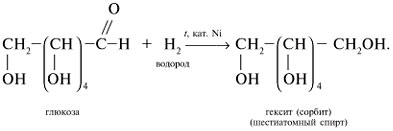  глюкоза сорбит 2. Окисление: в зависимости от типа окислителя и условий реакции моносахариды могут окисляться с образованием различных продуктов: А. В реакциях с мягкими окислителями (аммиакат серебра, реактив Фелинга, бромная вода) альдозы окисляются с участием альдегидной группы с образованием альдоновых кислот. 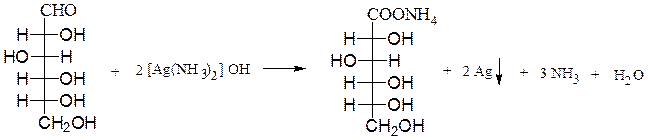 D- глюкоза аммониевая соль D-глюконовой кислоты или 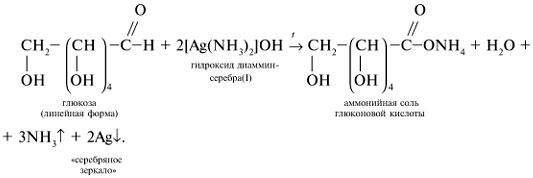 Реакция медного зеркала: окисление реактивом Фелинга (гидроксид медив щелочной среде) и нагревании реактив восстанавливается до красного осадка оксида меди (I), а глюкоза окисляется в глюконовую кислоту: 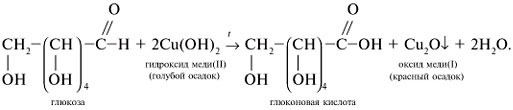 или 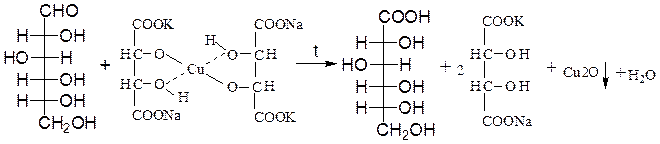 глюкоза глюконовая кислота Окисление бромной водой. Реакция сопровождается обесцвечиванием бромной воды, так как молекулярный бром восстанавливается в бесцветный бромид-анион:  глюкоза глюконовая кислота или CH2OH-(CHOH)4СОН + Br2 + H2O (НBrО +НBr) = CH2OH-(CHOH)4СООН + НBr Б. Сильные окислители (концентрированные азотная , серная кислота) окисляют, наряду с оксогруппой, последнюю гидроксильную группу, образуя двухосновные сахарные кислоты: 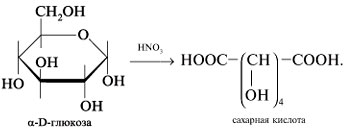 при окислении галактозы – галактаровую (слизевую) кислоту: 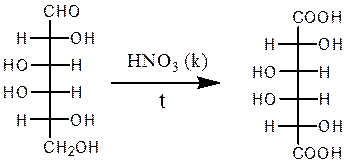 ПРИ ГОРЕНИИ УГЛЕВОДОВ ОБЪЕМЫ КИСЛОРОДА И УГЛЕКИСЛОГО ГАЗА РАВНЫ!!!!! Особые свойства глюкозы Ферментативное брожение: 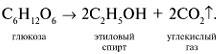 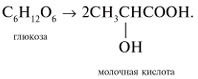 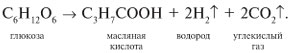 Фруктоза (кетоза, кетоноспирт)  4) Не дает серебряное и медное зеркало, но при обработке щелочью изомеризуется в глюкозу и дает эту реакцию. 5) дает вишнево-красное окрашивание при нагревании с крепкой соляной кислотой и резорцином, а при больших концентрациях фруктозы появляется красно-бурый осадок (реакция Ф.Ф. Селиванова,1887). 6) Не обесцвечивает бромную воду, как и все кетозы, поэтому реакция применяется для отличия кетоз от альдоз. 7) При восстановлении кетоз комплексными гидридами металлов (боргидрид натрия NaBH4, алюмогидрид лития LiAlH4), например D-фруктозы, возникает новый асимметрический углеродный атом, что приводит к образованию двух многоатомных спиртов: 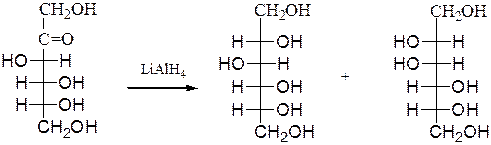 D-фруктоза D-сорбит D-маннит Способы получения моносахаридов 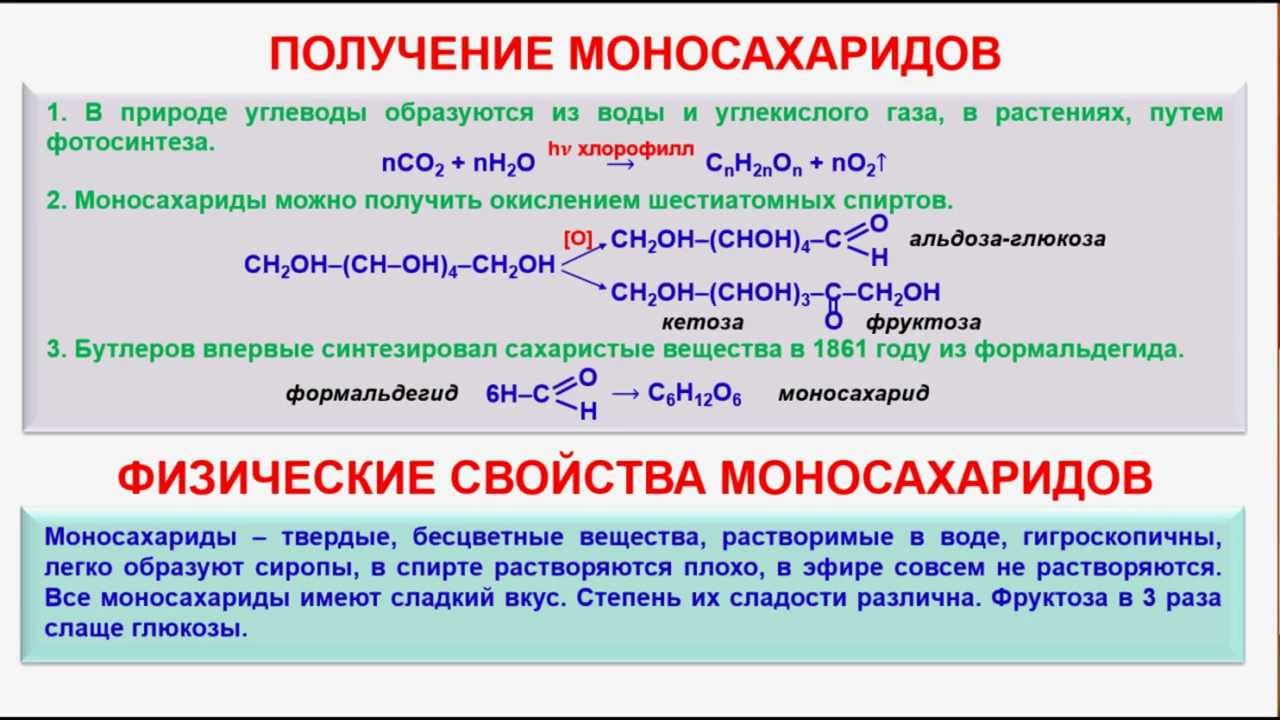 3. Гидролиз ди- и полисахаридов под действием кислот или ферментов:  а) С12Н22О11 + Н2О, Н+ 2С6Н12О6 а) С12Н22О11 + Н2О, Н+ 2С6Н12О6дисахарид моносахарид  б) (С6Н12О5)n + Н2О, Н+ nС6Н12О6 б) (С6Н12О5)n + Н2О, Н+ nС6Н12О6полисахарид Качественные реакции на моносахариды
|