Аналитический контроль показателя удельной поверхности при синтезе катодного материала NMC для ЛИА. Аналитический контроль показателя удельной поверхности при синтезе катодного материала nmc для лиа
 Скачать 181.44 Kb. Скачать 181.44 Kb.
|
1.2. Общая характеристика удельной поверхности катодных материаловУдельная поверхность – усреднённая характеристика размеров внутренних полостей (каналов, пор) пористого тела или частиц раздробленной фазы дисперсной системы. Для выражений этой величины используют отношение общей поверхности пористого или диспергированного в данной среде тела к его объему или массе. Удельная поверхность пропорциональна дисперсности или обратно пропорциональна размеру частиц дисперсной фазы. Измеряется данная величина в м2/г [4]. От величины зависит поглотительная способность адсорбентов, эффективность твердых катализаторов, свойства фильтрующих материалов. Удельная поверхность активных углей составляет 500-1500 м2/г, силикагелей – до 800, макропористых ионообменных смол – не более 70 м2/г. Удельная поверхность характеризует дисперсность порошкообразных материалов: минеральных вяжущих веществ, наполнителей, пигментов, пылевидного топлива и др. Величина их удельной поверхности обычно находится в пределах от десятых долей до нескольких десятков м2/г. Измеряемая величина удельной поверхности зависит от размеров сорбируемых молекул. Одно и то же вещество при сорбции крупных молекул имеет меньшую удельную поверхность, при сорбции мелких молекул имеет большую удельную поверхность. Для крупных молекул поверхность мелких пор, измеренная сорбцией мелких молекул, как бы и не существует. Поэтому, кроме удельной поверхности, важной характеристикой пористых тел является распределение поверхности пор по радиусам пор [5]. Разница удельной поверхности между двумя одинаковыми по иным физическим и химическим свойствам может отражаться в скорости химической реакции [6]. 1.3. Методы определения удельной поверхностиМетоды определения удельной поверхности делят на два вида: статистические и динамические. К первому виду относят объемный метод измерения адсорбции газов и паров, а также весовой метод измерения изотерм адсорбции газов и паров. Динамическим же методом является хроматографический метод термической десорбции – через колонку с адсорбентом (образцом) пропускают с постоянной скоростью поток смеси газа-носителя с адсорбтивом, обычно при низкокипящим газом, например азотом, аргоном, кислородом. В основе последнего метода лежит адсорбция. [4] Адсорбция – поглощение каких–либо компонентов из объема гомогенных сопредельных фаз на поверхности раздела этих фаз. Различие адсорбции и абсорбции в том, что первый процесс проходит на поверхности конденсированной фазы, а абсорбция – в ее объеме, примером такого процесса является растворение CO2 в воде или H2 в непористом металлическом палладии. Бывают случаи, когда разница между этими процессами неуловимо малы или механизм поглощения не ясен, для наименования используют более общий термин сорбция [7]. Адсорбцию делят на физическую и химическую, в свою очередь первую делят на основные типы взаимодействий Ван-дер-Ваальса: индукционное и ориентационное взаимодействия, и дисперсионные силы [8]. Индукционное взаимодействие основано на поляризации нейтральной частицы электрическим полем диполя. Ориентационное, в свою очередь, возникает на полярных молекулах с постоянным диполем (например, ионные кристаллы NaCl, NaJ, KCl, MgO, BaSO4) [8]. Наибольший вклад в ван-дер-ваальсово взаимодействие дают дисперсионные силы. Данное явление возникает между нейтральными частицами, не имеющими постоянных электрических дипольных моментов, т.е. атомов с заполненными электронными оболочками. Атомы обладают некоторым масштабом флуктуаций, именно поле флуктуации поляризует нейтральную частицу, в результате чего между ними возникают силы притяжения [9]. Химическая адсорбция в зависимости от условий может иметь различный характер. Может происходить настоящая гетерогенная реакция, в результате которой образуется новое химическое соединение, прочность связей в котором больше, чем прочность связей в твердом теле. Либо связи в твердом теле могут остаться неразрушенными, вследствие чего химическое взаимодействие происходит только между газами и поверхностными частицами [10]. Определить удельную поверхность ученые способны лишь с некоторыми допущениями, но с каждым разом их количество уменьшается. Изначально появилось уравнение изотермы сорбции Генри (формула 1), описывающее экспериментальные данные при малых степенях заполнения на однородных поверхностях [11]. α = K*P (1) где: 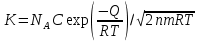 , K – константа равновесия, , K – константа равновесия, описывающая динамическое равновесие процессов адсорбции и десорбции; NA – число Авогадро; C – коэффициент пропорциональности; P – давление газа; T – температура газа; R – универсальная газовая постоянная; Q – энергия активации, необходимая для десорбции. 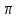 – число пи. – число пи.Условия эксперимента и отсутствие учета взаимодействия адсорбированных молекул выступали теми самыми допущениями. Данные допущения были приняты Ленгмюром (формула 2). И при K*P >> 1 закон Генри нарушается [11]. α = αm*K*P / (1 + K*P) (2) Где: αm – величина адсорбции, соответствующая полному заполнению поверхности. Даже такая формула не учитывает возможности адсорбции на слоях, следующих после монослоя, поэтому три ученых Брунауэр, Эммет и Теллер вывели собственное уравнение полимолекулярной физической адсорбции (формула 3) [11]. 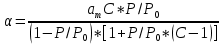 (3) (3)где: C = K/KL, KL – константа равновесия жидкость–пар.  Рисунок 2. Cхема катарометра Метод хроматографической термической десорбции реализован с помощью специального устройства, именуемого катарометр. Данный детектор измеряет теплопроводность и в его основе лежит принцип изменения сопротивления материалов от температуры [11]. 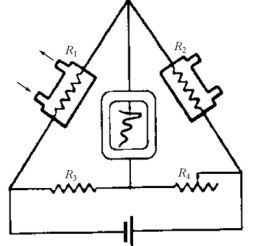 На рисунке 2 изображена схема катарометра. Данный детектор состоит из двух ячеек с помещенными в них металлическими нитями. Через одну из ячеек проходит поток газа перед входом в колонку, через другую – выходящий из колонки поток. Нагреваемые электрическим током нити являются двумя плечами моста Уинстона R1 и R2. К диагонали моста подключен потенциометр регистратор. Мост балансируется с помощью сопротивления R4 (т.е. добиваются отсутствия тока в его диагонали) при пропускании через обе ячейки смеси одинакового состава либо чистого газа носителя [12]. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ Методика проведения испытания. Методика измерения удельной поверхности катодного материала методом БЭТ.  Рисунок 2. Прибор Sorbi-MS Н  а работе катарометра основан прибор Sorbi-MS, используемый для анализа (рисунок 2). Исследуемый образец загружается в ампулу, которая закрепляется в держателе ампулы и помещается в адсорбер, снабженный встроенным нагревателем с датчиком температуры. Его конструкция, основанная на принципе сообщающихся сосудов, позволяет многократно в автоматическом режиме охлаждать ампулу с образцом до температуры жидкого азота, а затем нагревать до температуры десорбции. а работе катарометра основан прибор Sorbi-MS, используемый для анализа (рисунок 2). Исследуемый образец загружается в ампулу, которая закрепляется в держателе ампулы и помещается в адсорбер, снабженный встроенным нагревателем с датчиком температуры. Его конструкция, основанная на принципе сообщающихся сосудов, позволяет многократно в автоматическом режиме охлаждать ампулу с образцом до температуры жидкого азота, а затем нагревать до температуры десорбции. В режиме десорбции специальный клапан закрывает сообщение адсорбера с атмосферой, вследствие чего в нем увеличивается давление паров азота (из-за испарения жидкого азота) и происходит выталкивание жидкого азота из адсорбера, в котором давление продолжает оставаться атмосферным. В режиме адсорбции открытием клапана давление в адсорбере и вне его уравновешивается, как следствие, уровень азота повышается, а ампула с исследуемым образцом погружается в жидкий азот. Во время процессов состав газовой смеси, прошедшей через ампулу с образцом, регистрируется катарометром, снабженным схемой управления и термостабилизации. Прибор автоматизирован, подключается к ПК и имеет специальное программное обеспечение. Средства измерений, оборудование и реактивы Реактивы: NMC (NiCl2×6H2O, CoCl2×6H2O, MnCl2×4H2O). Посуда: проградуированный цилиндр, воронка, шпатель. Оборудование: прибор Sorbi-MS, станция пробоподготовки SorbiPrep, аналитические весы, барометр. Метод измерений. Измерение удельной поверхности катодного материала основано на определении состава газовой смеси, прошедшей через ампулу с образцом в приборе Sorbi-MS. Подготовка к выполнению измерений. Включить прибор Sorbi-MS. После успешной загрузки внутреннего ПО прибор издает два двойных звуковых сигнала. Начать прогревать азотную ловушку прибора. Для этого в появившемся диалоговом окне «Начать прогрев азотной ловушки?» программы SoftSorbi нажмите кнопку «Ок». Параметры прогрева выставлены автоматически и не подлежат к изменению студентами. Залить жидкий азот в прибор Sorbi-MS помещая воронку в заливную горловину прибора, адсорбер при этом должен быть открыт. Жидкий азот заливается до перелива. После следует убрать воронку, но закрывать горловину пробкой не нужно. Подготовка образца перед проведением испытания. Требуется взвесить (с аналитической точностью) и поместить необходимое количество образцов в ампулу. Прибор измеряет удельную поверхность в диапазоне от 4 до 12 м2. Для определения разумного количества образца требуется оценить его вес, полагая, что общая площадь должна быть порядка 8 м2. Поместить ампулу с образцом в головку держателя ампулы, при этом теплообменник не должен касаться образца. Установить держатель с ампулой, содержащей исследуемый образец, в станцию пробоподготовки SorbiPrep. Установить параметры пробоподготовки: Температура – 200 °С; Длительность – 20 минут. Запустить процесс нагрева длительным нажатием на кнопку канала А. После окончания пробоподготовки держатель с ампулой необходимо изъять из прибора SorbiPREP. Проведение испытания. Поместить ампулу с образцом в прибор Sorbi-MS. Запустить измерение. Для запуска измерения нажмите кнопку «Начать измерение без термотренировки». После запуска измерения откроется окно выбора метода измерения: необходимо выбрать метод «БЭТ». После этого откроется окно «Новый образец», в котором необходимо указать значение следующих параметров. Идентификация: «Название образца» – название, определяемое пользователем, с целью идентификации полученных данных: «Оператор» – наименование студента, выполняющего испытание образца; Параметры образца: «Масса образца, гр.» – масса образца в граммах, «Влажность образца, %) – 3% после проведения пробоподготовки. Параметры измерения: «Атмосферное давление» – после выбора единицы измерение следует вписать соответствующее значение, используя показания барометра. Обработка результатов измерений. Результат предоставить в виде (формула 4): 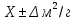 (4) (4)где Δ – предел допускаемой погрешности. В соответствии с ГОСТ 28794-90 Метод определения удельной поверхности хроматографических материалов термодесорбцией. Результаты измерений. Расчет удельной поверхности адсорбента проводится по формуле 5 в автоматическом режиме прибором Sorbi-MS и программным обеспечением SoftSorbi. 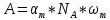 (5) (5)где: A – Величина удельной поверхности адсорбента; αm – Емкость монослоя; NA – число Авогадро; ωm – площадь приходящаяся на одну молекулу в монослое Площадь удельной поверхности синтезированного катодного материала NMC: При 900°C: A1 = 1,0434 м2/г A2 = 1,0438 м2/г При 1000°С A1 = 3,0776 м2/г A2 = 3,3973 м2/г Расчет погрешностей, сходимости и воспроизводимости анализов. Среднее арифметическое, 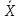 (формула 6). (формула 6).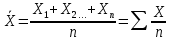 (6) (6)A900°C = (1,0434 + 1,0438) / 2 = 1,0436 м2/г A1000°C = (3,0776 + 3,3973) / 2 = 3,2375 м2/г Дисперсия измерений, S2 (формула 7). 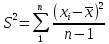 (7) (7)S2900°C = ((1,0434 – 1,0436)2 + (1,0438 – 1,0436)2) / (2 – 1) = 0,8 * 10-7 S21000°C = ((3,0776 – 3,2375)2 + (3,3973 – 3,2375)2) / (2 – 1) = 0,5 * 10-1 Стандартной отклонение, S (формула 8). 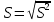 (8) (8)S900°C = √(0,8 * 10-7) = 0,283 * 10-3 S1000°C = √(0,5 * 10-1) = 0,224 * 100 Стандартное отклонение от среднего арифметического, 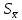 (формула 9). (формула 9).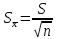 (9) (9)Sx 900°C = 0,283 * 10-3 / √(2) = 0,2 * 10-3 Sx 1000°C = 0,224 * 100 / √(2) = 0,16 * 100 Коэффициент Стьюдента при заданной вероятности и степени свободы (n – 1), который используют для вычисления точности определения, 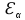 (формула 10). (формула 10).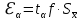 (10) (10)tαf = 12,706 Ɛα 900°C = 12,706 * 0,2 * 10-3 = 2,54 * 10-3 Ɛα 1000°C = 12,706 * 0,16 * 100 = 2,01 * 100 Отклонения, A0x (формулы 11,12). A01 = A1 – A2 (11) A02 = A2 – A1 (12) A0 900°C 1 = 1,0434 – 1,0438 = – 0,0004 A0 900°C 2 = 1,0438 – 1,0434 = 0,0004 A0 1000°C 1 = 3,0776 – 3,2375 = – 0,1599 A0 1000°C 2 = 3,3973 – 3,2375 = 0,1598 Относительная ошибка, ∆o (формула 13). 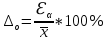 (13) (13)∆o 900°C = (2,54 * 10-3 / 1,0436) * 100% = 0,24% ∆o 1000°C = (2,01 * 100 / 3,2375) * 100% = 62,08% В таблице 1 приведены метрологические характеристики результатов определений показателя удельной поверхности. Таблица 1. Метрологические характеристики.
Окончательный результат NMC при 900°С = 1,0436 ± 0,0025 м2/г, ∆o = 0,24% и P = 0,95 NMC при 1000°С = 3,2375 ± 2,0098 м2/г, ∆o = 62,08% и P = 0,95 Результаты определения показателя удельной поверхности катодных материалов позволяют заключить следующее: Порошок, полученный при 900°C обладает высоким показателем однородности, что свидетельствует о правильно подобранном температуром режиме. Напротив, порошок при 1000°C на момент исследования был очень рассыпчатым, а пробоподготовка вызывала некоторые трудности. По результатам заключено, что порошок слишком неоднородный и мог разложиться в ходе второго этапа термосинтеза. Разница в значениях удельной поверхности при изменении температуры обуславливается характерным изменением кристаллической решетки: при 900°С образуется однородная слоистая решетка, а при 1000°С – структура нарушается появлением иных более стабильных оксидов d-элементов (CoMn2O4, Co3O4, NiO и т.д.), наблюдается характерная неоднородность [2]. | |||||||||||||||||||||||||||||||||||||||||||||||||||

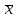 , м2/г
, м2/г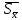 , м2/г
, м2/г