Опухоли у собак. Анатомотопографические особенности строения молочной железы у собак
 Скачать 192.5 Kb. Скачать 192.5 Kb.
|
ЭТИОЛОГИЯ ОПУХОЛЕЙ У ЖИВОТНЫХ.Доброкачественные опухоли в большинстве своем являются выражением реактивного роста вследствие повышенных функций (например, эндокринных желез, предстательной железы, молочной железы, матки) или они возникают как следствие хронического воспаления. Этиологические факторы злокачественных новообразований связаны со специфическим, опухолевым раздражением, в большинстве своем имеющим мультифакториальную природу. При известных условиях доброкачественные новообразования могут перерождаться и принимать злокачественный характер. Этиологическое значение в развитии злокачественных опухолей имеют следующие факторы. Физические факторы. Они могут быть подразделены на три группы: хроническая травма, например, при различных внедрившихся в тело осколков, давления на кость эндопротеза и т.д. Хроническое повреждение: например, при описторхозе плотоядных,при действии камней желчного пузыря на его стенку наблюдается хроническое его повреждение, которое может привести к возникновению опухолей. Хроническое лучевое воздействие (радиационный канцерогенез): ионизирующее излучение , как теперь стало известно, - универсальный канцерогенный агент.Частота и виды злокачественных и доброкачественных новообразований, индуцированных ионизирующими излучениями, зависят от многих факторов, в том числе от проникающей способности их зазных вилов, от характера воздействия – внешнего облучения или внутреннего ( включения радионуклидов, их органотропности), распределения дозы во времени (острое, хроническое, дробное облучение). Так ультрафиолетовое облучение может способствовать возникновению новообразований кожи, гамма-излучение – системы дыхания, внутреннее облучение может привести к развитию опухолей почек и печени (особенно высокое содержание стронция и тория). Молекулярные механизмы радиационного канцерогенеза не вполне ясны. Наиболее вероятно, что он осуществляется через превращение протоонкогенов клетки в онкогены в результате резкого повышения нестабильности генома, индицированного ионизирующим облучением, т.е. увеличения вероятности неопластического превращения клетки. Химические вещества. Известно более 800 химических веществ, обладающих канцерогенными свойствами. Большинство канцерогенов химического происхождения , встречающихся в окружающей среде, находится не в активной, в преканцерогенной форме. В активные (полные) канцерогены они превращаются в организме под влиянием активирующих веществ – коканцерогенов. Канцерогенные вещества, такие как полициклические ароматические углеводороды, ароматические амины, нитрозоамины, афлатоксины, в организме животных активируются монооксигеназами, локализующимися в микросомах клеток. В результате этого указанные вещества превращаются в эпоксидные соединения. Последние являются активными карциногенными метаболитами, вступающими в связь с макромолекулами клеток. Различают пять групп химических веществ, оказывающих канцерогенное действие: полициклические ароматические углеводороды, ароматические амины и амиды (азотокрасители, нафталин, инсектициды), азот-нитрозные соединения, алкилирующие агенты (бензилхлорид), органические канцерогены (арсентриоксид, асбест) и, кроме того растительные алкалоиды. Эти химические вещества находятся в сложном взаимодействии с гормонами, генетической и иммунной системой и вирусами. Само по себе химическое вещество иногда не обладает канцерогенным действием, но при влиянии дополнительных реализующих факторов становится таковым. У животных опухоли возникают в результате синергичного действия ряда канцерогенных факторов, инициирующих (сильные канцерогены) и активирующих (коканцерогены). Ряд веществ, не считающихся канцерогенами, в комбинации с другими факторами может способствовать развитию опухолей. Некоторые вещества могут содействовать развитию рака в эмбриональном периоде. Канцерогены могут образоваться и в самом организме; это в основном продукты обмена стеринов, аминокислот белков и др. они в разной степени обладают онкогенным действием. Так, холестерин в слабой степени, а его метаболиты холестадиены проявляют значительную бластомогенную активность. В эксперименте на мышах при введении этих канцерогенов в организм удалось вызвать у них аденомы легких, лейкозы и рак легких. Карцинолипин выделен из желтка. При введении его с пищей или под кожу мышам или крысам он вызвал у них развитие раковых опухолей. Карцинолипин стимулирует биосинтез белков. Канцерогенным действием обладают и производные желчных кислот: дезоксихолиевая и апохолиевая. Производные триптофана – орто- и аминофенолы (промежуточные продукты превращения триптофана в никотиновую кислоту), также обладают бластомогенным действием – с их помощью удалось вызвать бластому мочевого пузыря. Онкогенные вирусы. Этиологическая роль вирусов в происхождении опухолей у многих животных может считаться доказанной. Канцерогенные вирусы делятся на вирусы ДНК (полинома, папилома, аденовирусы и вирусы герпеса) и вирусы РНК или онковирусы. Последние по ультраструктуре делятся на типы А, В и С. В вирусах типа В находится фактор Биттнера, вызывающий карциномумолочной железы. Под влиянием вирусов в клетках может происходить несколько типов генетических изменений: интеграция вирусного генома в геном нориальной клетки, мутации, эпигеномные изменения. Интеграция вирусного генома. Под этим подразумевается соединение ДНК вируса с одним или несколькими участками ДНК хромосом нормальных клеток. Интегрированная вирусная ДНК реплицируется и передается дочерним клеткам вместе с ДНК клетки. Интеграции РНК вирусов в геном клетки предшествует образование ДНК, являющейся копией генома вируса, под влиянием специального фермента – обратной транскиптазы. Мутации. Гипотеза о роли мутации в онкогенезе была предложена в 1914 году Бовари. В настоящее время имеются доказательства, что в клетках опухоли происходит перестройка структуры хромосом. Эпигеномные изменения – это стойкие изменения генетических свойств, сопровождающие дифференцировку клеток в процессе эмбриогенеза. В отличие от мутаций и интеграции вирусных геномов эпигеномные изменения, по-видимому, не связаны с необратимыми изменениями ДНК клеток. Генетические факторы. Небольшое количество опухолей может встречаться как генетически обусловленные заболевания. Зависимость от «опухолевых» генов связана с появлением врожденных или наследственных новообразований. Они доказаны примерно для 50 видов опухолей. К доминантно наследуемым опухолям относятся базалиомы, невриомы, остеохондромы, множественные липомы, полипоз шейки матки, нейрофиброматозы. Наследственные новообразования могут встречаться как врожденные или развивающиеся сразу после рождения, но могут развиваться и у подрастающего молодняка или даже у взрослых животных. Гормональные факторы. Многие исследования показали, что высокие дозы гормонов (например, стероидов), имплантация или удаление эндокринных желез (кастрация, удаление щитовидной железы) могут приводить к возникновению различного рода опухолей. Так повышенное количество эстрогенов в крови у животных вызывает гиперплазию эндометрия, при длительном состоянии подобного рода может развиться карцинома эндометрия. Вообще, эстрогены родственны холестерину по своей химической структуре, имеют сходство с канцерогенными углеводородами.Эндогенные эстрогены могут вызвать бластоматозный рост тканей у животных прямым воздействием на ткани или опосредованно. Высокая дозировка гормонов при инволюции эндокринных желез может привести к возникновению миом матки, аденом эндокринных желез, а также способствовать развитию рака предстательной железы, матки, яичников. Во время беременности нередко образуются доброкачественные опухоли молочных желез. Развивающаяся или уже имеющаяся карцинома молочной железы, наоборот, растет медленно, а после родов животного может бурно распространяться. Возрастные факторы, влияние породы, пола, масти животного на возникновение новообразований в организме. С увеличением роста, развития и возраста животного наступают принципиальные изменения генетического аппарата. Опухоли возникают во все периоды жизни, но наиболее часто у взрослых или старых животных. Например, у собак и кошек опухоли чаще регистрируют в возрасте от 6 до 10 лет (в среднем 8 лет), у лошадей и крупного рогатого скота – от 5 до 13 лет ( в среднем 8 лет), у кур - в 2 года. Однако некоторые опухоли (вирусной этиологии) развиваются и у молодых животных. Так, папиллому у крупного рогатого скота, лошадей, собак наблюдают в возрасте не старше 2 лет, лимфосаркому – у собак в возрасте от 1 до 2 лет, остеосаркому – у собак в возрасте от 1 до 4 лет, а у кошек в более раннем возрасте. Определенное значение в возникновении опухолей имеют порода, масть и пол животных. Среди собак опухоли чаще регистрируют у боксеров и терьеров; у крупного рогатого скота герефордской породы отмечают плоскоклеточный рак глаз; меланомы встречаются преимущественно у лошадей серой масти. Более подвержены раковым заболеваниям самки, чем самцы, особенно часто поражаются у них матка, влагалище, молочная железа.Однако есть опухоли, которые одинаково поражают животных обеих полов. Дизонтогенетическая теория (греч. disonthogenesis – порочное развитие) предложена в прошлом веке немецким ученым Конгеймом (1839-1884). Согласно этой теории, причина возникновения опухолей кроется в нарушениях эмбриогенеза. Известно, что в процессе нормального развития организма клетки дифференцирутся в определенную ткань. Допускается, что некоторые клетки остаются в организме неопределенно долгое время в незрелом состоянии и при некоторых условиях начинают проявлять признаки опухолевого роста. Так, известна опухоль, которая развивается из остатков хорды, позвонков, жаберных дуг и т.д. Эта теория может объяснить происхождение только некоторых опухолей, но не раскрывает всех причин опухолевого роста. Полиэтиологическую теорию поддерживают большинство патологов и клиницистов. Сторонники этой теории полагают, что единой причины возникновения опухолей не существует, но любые факторы (физические, химические, вирусные, паразитарные, дисгормональные и др.), воздействуя на генетический аппарат клетки, вызывают мутацию – превращение нормальных клеточных элементов в опухолевые. ПАТОГЕНЕЗ ОПУХОЛЕЙ У ЖИВОТНЫХ.Опухолевая ткань возникает из нормальной путем трансформации последней. Различают три фазы этапа превращения нормальной ткани в опухолевую. Первый этап – трансформация нормальной клетки в предопухолевую, при этом только изменяется реактивность предопухолевых клеток, морфологически же они не отличаются от нормальной. В основе данного процесса лежит индуцирование канцерогенным раздражителем изменений хромосомных механизмов. Нарушается при этом генетическая информация, в первую очередь локусов, ответственных за формирование клеточных структур. Второй этап – превращение предопухолевой клетки в опухолевую, размножение этих клеток и образование опухолевого узла. Трансформация предопухолевой клетки в опухолевую обусловлена тем, что накопившееся коканцерогены индуцируют канцерогенный эффект и этим способствуют возникновению мутагенных изменений в клетках, выражающихся молекулярным изменением различных участков генома, изменением организации целых хромосом, нарушением механизмов редупликации хромосом. Вследствие извращенной генетической информации клетки теряют способность образовывать энзимы и белки, с характерной органной и тканевой специфичностью, и преобретают свойства синтезировать эмбриоспецифические и гетерологические антигены (в том числе и на своей поверхности), изменяется нормальная антигенная топография поверхности клеток. Все это и обуславливает в дальнейшем их злокачественные свойства. Третий этап – автоматический неограниченный рост опухолевой ткани, обусловленный в первую очередь выходом ее из-пол контроля регулирующих систем организма из-за отсутствия строгого соответствия между белковым составом и гомеостатирующими факторами Физиологические механизмы взаимодействия клетки со средой претерпевают существенные изменения в ходе малигнизации. Малигнизированная клетка утрачивает свои контактные связи с соседними клетками тканевой структуры и специализированные контакты с нервной системой. Установлено, что процесс малигнизации находится в прямой связи с выходом малигнизированной ткани из-под регулирующего влияния нервной системы. Опухолевая ткань по сравнению с нормальной бедна нервными элементами и нервными волокнами (афферентными) – они расположены на переферии опухолевой ткани. Не оказывают соответствующего блокикующего влияния на опухолевые клетки и гомеостатические факторы, в частности гормональные, тормозящие рост нормальных клеток. Таким образом, утеря регулирующих иннервационных влияний, обогащение высокоразвитым мембранным аппаратом (аппаратом активного энергетического взаимодействия клетки со средой существования), специфическое изменение функциональных свойств, высокая резистентность в отношении альтерирующего раздражителя определяют безудержность роста раковых клеток. Они выступают как самостоятельная, совершенная, саморегулирующаяся биологическая система с тенденцией к стойкому безудержному росту. В опухолевой трансформации, несомненно, играют роль и генетические факторы, однако прямое наследование истинных опухолей не установлено. Наследуется обычно предрасположенность к возникновению опухолей, что можно проявиться на протяжении жизни животного при воздействии на него канцерогенными факторами. Канцерогенные вещества сенсибилизируют ткани к развитию бластомогенеза. Имеется и ряд неспецифических факторов (актиномицин, витамины группы В – особенно В 12 и др.), создающих «почву» для проявления действия канцерогенов. Мутационный механизм химического и физического канцерогенеза. Воздействие канцерогенного фактора  Д  еполимеризация молекулы ДНК еполимеризация молекулы ДНКО  бразование свободных групп нуклеотидов (генов) бразование свободных групп нуклеотидов (генов)Рекомбинация генов  «  Самосборка» новой ДНК с новыми свойствами Самосборка» новой ДНК с новыми свойствамиВозникновение способности к безудержному росту клеток. ДИАГНОСТИКА ОПУХОЛЕЙ У ЖИВОТНЫХ.Поведение ветеринарного врача при диагностике опухолей должно включать максимальное количество мероприятий, направленных на то, чтобы обеспечить наиболее раннее выявление различного рода новообразований. Ветеринарная документация, тщательно составленная, облегчает статистическую и научную оценку клинического материала. Она включает: фамилию, имя, отчество, место жительства, телефон владельца животного, пол, возраст, породу, кличку, вес больного животного, точное и подробнейшее описание его общего состояния (температура, пульс, дыхание, общее состояние, сознание, состояние шерсти, кожных покровов, лимфатической, мышечной, сердечно-сосудистой, эндокринной систем, состояние костей и суставов, органов дыхания , органов пищеварения, системы органов мочевыделения, половых органов, глаз, ушей, описание нервно-психического состояния), дату поступления в клинику, диагноз при поступлении, диагноз основного заболевания, дату его постановки, указание локализации опухоли, определение вида и стадии ее, особенности лечения. Анамнез (anamnesis vitae) должен охватывать следующие данные: тип кормления, содержание, перенесенные заболевания и травмы у самок: количество родов, характеристика половых циклов; наследственные заболевания, в том числе чувствительность к медикаментам. Anamnesis morbi должен охватывать время возникновения настоящего заболевания и предполагаемые причины, ранее проводимая терапия (метод, сроки, эффективность.) Анализ симптомов при опухолях молочной железы. Объемное образование. - Боль или болезненность при надавливании. Втяжение соска. Покраснение кожи вокруг соска. Выделения из соска. Кровянистые выделения: внутрипротоковая папиломма (чаще всего), внутрипротоковый рак, мастопатия. Серо-зеленые выделения: мастопатия, расширение млечных протоков. Желтые выделения: серозные выделения – мастопатия, гнойные выделения – мастит. Молочно-белые выделения – галакторея: лактация, галактоцеле, гиперпролактинемия, побочное действие лекарственных средств, например хлорпромазина. Клинические исследования. Прежде всего производят осмотр больного животного, пальпацию области, где предполагается локализация опухоли. При недоступных для пальпации опухолях производят перкуссию для определения размера опухоли и аускультацию. При осмотре молочных желез у собаки обращают внимание на следующее: ассиметрия определенных пар молочныз желез или видимые образования, изменение состояния кожных покровов, состояние сосков (втяжение или изъязвление; расположение на разных уровнях; выделения из сосков – кровянистые, серозные, гнойные), втяжение кожи, зернистость (бугристость) молочных желез, расширенная венозная сеть (одностороннее расширение венозной сети характерно для рака молочной железы), симптом лимонной корки (резко выделяющиеся поры потовых желез при прорастании кожи опухолью). При поднятии лап животного на уровень головы сокращаются грудные мышцы, мышцы брюшного пресса – таким образом становится легче оценить связь объемного образования молочных желез с мышцами При пальпации молочных желез изучают состояние сосков, ареол: плотность, утолщение складки ареолы, наличие или отсутствие выделений. Осторожно собирая кожу железы в складки, выявляют кожные симптомы – морщинистость или втяжение, лимфостаз, синдром «лимонной корки». После поверхностной проводят более глубокую пальпацию, при которой изучают состояние железистых долек и определяют характер опухоли или другого образования в железе. Исследование проводят в начале кончиками пальцев обеих рук, а затем захватывают ткань железы между пальцами одной руки. Исследуют молочные железы у собак по порядку, последовательно прощупывая все их отделы по направлению от соска к периферии или наоборот. Такое прощупывание желез дает возможность определить опухоль. При выявлении опухоли производят более тщательную пальпацию соответствующей железы или ее области для определения размеров, формы, консистенции, подвижности молочной железы и опухоли, состояние кожи над опухолью. Ультразвуковой метод исследования молочной железы (УЗИ). Ультразвуковой метод сканирования применяется при подозрении на опухоль молочной железы у молодых сук. УЗИ показано в следующих случаях: щенность и лактация, дифференциальная диагностика кист и солидных опухолей, образования, расположенные по краю молочных желез (не видны при маммографии), перед пункцией объемного образования молочной желеы. Под контролем УЗИ можно производить пункцию и биопсию опухоли, что резко повышает точность исследований. Для ультразвукового метода исследования доступны опухоли, расположенные не глубже 10-12 см. Лабораторные исследования. Обязательны исследования крови, определение белков, ферментов (лактатдегидрогеназа), специфических ферментов печени (щелочная и кислая фосфотаза), содержание креатинина, мочевины, сахара в крови. Исследуют содержание гормонов (возможно повышение) при опухолях половых органов и молочной железы. Рентгенологическая диагностика является одним из основных методов диагностики опухолей. Производят рентгенологическое исследование грудной клетки и скелета (первичная опухоль? метастазы?), а также полых органов, кровеносных (ангиография) и лимфатических (лимфография) сосудов. Обследование рентгенологическим методом молочной железы называют маммографией. Различают контрастную и бесконтрастную маммографию. Контраст вводят в выводное отверстие на соске, из которого при надавливании появляются выделения (пораженных долей может быть несколько). Этот метод позволяет выявить локализацию патологического процесса и указывает, где следует производить секторальную резекцию в тех случаях, когда не удается прощупать уплотнения в молочной железе. Бесконтрастная маммография осуществляется при наличии уплотнений в молочных железах, которые клинически трудно отдифференцировать от раковых опухолей. При раковых опухолях определяется тень без четких контуров с отходящими в ткантходящими в ткан при мастопатии – диффузное, тяжистое затемнение молочной железы или ее отделов с просветлениями (кисты), при фиброаденомах – четко очерченное затемнение; могут выявляться тяжистость и мелкие просветления в тех случаях, когда одновременно имеется мастопатия. Мелкие точечные кальцинаты в зоне затемнения могут отображать малигнизацию на фоне мастопатии. Рентгенограммы молочной железы при мастопатии: а – маммограмма; стрелками указана однородная крупная тень кисты; б – пневмомаммограмма; стрелками указаны крупные кистозные образования с полициклическими контурами, заполненные газом. Биопсию проводят для определения гистологического, в некоторых случаях ферментативно-химического или иммуно-гистологического характера опухоли в виде эксцизии или взятия материала специальной иглой. Часто используется срочное (во время операции) гистологическое исследование биопсийного материала. Химическое исследование тканей опухоли молет быть произведено на стероидные рецепторы ( опухоли молочной железы). Точность пункционной биопсии повышается, если она производится под контролем ультразвукового или компьютерно-томографического исследования. Пункция обьемного образования молочнрй железы у собак – достаточно простое и широко распространенное исследование. Показания: для аспирации содержимого кист, для получения цитологического материала; диагнлстическая ценность этого метода при солидных образованиях 90-95% (выше, чем маммографии). Материал, полученный при пункции, отправляют для цитологического исследования. Методика пункции следующая: Готовят стерильную иглу диаметром 0,08 см и шприц объемом 10 мл. Кожу обрабатывают антисептиком. Местную анестезию можно не проводить. Объемное образование удерживают тремя пальцами свободной руки. Иглой прокалывают кожу и вводят ее в объемное образование. При проколе кисты игла проваливается. Если при потягивании за поршень в шприц поступает жидкость, то ее полностью удаляют. Если жидкости нет, то, слегка поттягивая поршень, несколько раз перемещают иглу в опухоли под разными углами (или вращают иглу), стараясь взять материал из нескольких участков. Чтобы материал не попал в шприц, его снимают с иглы. Иглу извлекают. Набирают в шприц 2 мл воздуха, одевают иглу и переносят ее содержимое на два предметных стекла. Одно предметное стекло фиксируют, а второе высушивают на воздухе. Препараты отправляют в цитологическую лабораторию. Т  актика ведения больных в зависимости от результатов цитологического исследования. актика ведения больных в зависимости от результатов цитологического исследования. 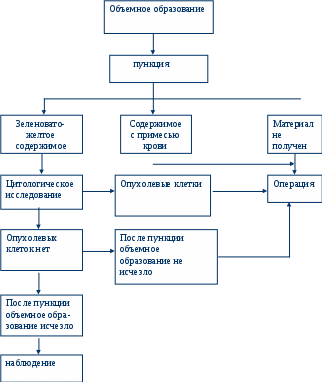  ЛЕЧЕНИЕ ОПУХОЛЕЙ МОЛОЧНОЙ ЖЕЛЕЗЫ.Лечение опухоли молочной железы проводится хирургическими и консервативными ( не хирургическими методами). Принципы лечения – в каждом конкретном случае заболевания необходим индивидуальный план лечения. А) Проверка готовности к лечению. Для этого уточняют состояние функций сердца и кровообращения, легких, почек, определяют показатели обмена веществ, электролитного и ионного баланса, уровень белков в крови, производят общий клинический анализ крови и мочи. Учитывают также возраст больного животного, сопутствующие заболевания. Б) Факторы планирования лечения. К этим факторам относятся морфологическая характеристика опухолей (гистологическая картина и степень злокачественности), стадия опухоли, мнение ветеринарного специалиста. На основании заключения специалистов определяют цель и рациональный способ лечения. При определении цели лечения имеют в виду излечение, клиническое излечение в течение 1 года, паллиативное или симптоматическое лечение. Результаты лечения зависят прежде всего от раннего распознавания и раннего начала, а также от радикализма лечения. Необходимо всегда знать и помнить, что лечение опухолей молочной железы (как и любых других органов) необходимо проводить комплексно, подключая все возможные и нужные в данном случае методы лечения. Оперативное (хирургическое) лечение. Хирургические методы лечения являются ключевыми, наиболее важными методами. Они направлены на удаление опухоли с помощью иссечения скальпелем, электроножом, лучом лазера или разрушение (некроз с последующим отторжением) с помощью холода (криохирургия). Эти методы наиболее эффективны в лечении начальных стадий развития опухоли. Хирургическому удалению доступны практически все локализации опухолей. Без учета паллиативных и пробных операций хирургические методы применяют более чем 80-85 % случаев. Показания к операции. Хирургическое удаление показано при всех видах опухолей молочных желез (ОМЖ), исключая случаи воспаленной карциномы, т.к. при ней неизбежен быстрый рецидив и распространение опухоли. В случае обнаружения отдаленных метастазов иссечение опухоли является паллиативной мерой, прогноз в этом случае неблагоприятный. При проведении одновременной овариогистероэктомии, последняя должна предшествовать мастоэктомии, с целью недопущения попадания опухолевых клеток в брюшную полость. Овариоэктомия не рекомендована кошкам, потому что большинство опухолей у них не являются гормонозависимыми. Противопоказания. Противопоказано радикальное лечение при диссеминации опухолевых клеток и появление отдаленных метастазов, неудалимых оперативным путем; при наличии тяжелых сопутствующих заболеваний жизненно-важных органов (легкие, сердце, почки, печень) с декомпенсацией их функции. Противопоказания для органосохраняющих операций на молочной железе: крупная опухоль в молочной железе (повышается вероятность негативного косметического результата) расположение первичных опухолей вблизи соска более 1 опухоли в молочной железе противопоказания к лучевой терапии запущенность заболевания ( например, стадия 2 и более) большая зона внутрипротокового поражения или наличие микрокальцификатов Основные принципы онкологического вмешательства предусматривают: иссечение пораженной части органа или ткани, из которых исходит опухоль, на таком расстоянии от опухоли, которое гарантирует проведение разреза в заведомо здоровых тканях. Обычно применяют частичную резекцию, субтотальное или тотальное удаление органа в зависимости от стадии и распространенности процесса. удаление регионарных лимфатических узлов на путях лимфооттока вместе с окружающей их жировой соединительной тканью. удаление части или всего органа, пораженного опухолью, вместе с регионарными лимфатическими узлами единым блоком. Выполнение онкологической операции требует знания особенности распространения опухоли в пределах пораженного органа, перехода на соседние органы и ткани и четкого представления о путях метастазирования по лимфатическим путям. Высокая эффективность отдаленных результатов достигается, если соблюдены принципы абластики, которая подразумевает недопущение хирургом распространения опухолевых клеток во время операции. Варианты мастэктомии (в зависимости от объема иссекаемой ткани). Иссекающая биопсия – удаление только опухолевого узла. Локальная (простая) мастэктомия – удаление только пораженной железы. Региональная мастэктомия – удаление пораженной железы и ее пары. Иссечение блоком – удаление пораженной железы, регионарного лимфоузла и всех желез и лимфатических сосудов, лежащих между ними. Односторонняя (унилатеральная) мастэктомия – удаление всех желез на пораженной стороне. Двусторонняя (билатеральная) мастэктомия – удаление всех желез (может быть одновременная или поэтапная). Доказано, что тип хирургической операции не влияет на время после операции, в течении которого не появляются рецидивы. Проведение операций. Операция по удалению опухоли молочной железы выполняется в несколько этапов: При локализации опухоли в 5-4-й паре, отступя не менее 3 см от края опухоли, двумя окаймляющими полуовальными разрезами рассекают кожу и отсепаровывают ее в сторону. Обнажают анатомические границы опухоли, рассекают жировую клетчатку до апоневроза. Лигитируют кетгутом питающие опухоль сосуды в краниальной и каудальной частях операционной раны, отступя от видимых границ опухоли на 3-5 см. Тупым путем отпрепаровывают блок тканей вместе с жировой клетчаткой и опухолью от апоневроза, обнажая питающую сосудистую ножку. Выделяют поверхностные паховые лимфатические узлы. Сосудистую ножку тщательно прошивают шелком и пересекают. Послойно и наглухо зашивают операционную рану, в каудальной ее части можно оставить дренаж на 1 сутки. При удалении опухоли, располагающейся в первых трех парах молочных желез, окаймляющий разрез кожи и жировой клетчатки продолжают до подмышечной впадины и выделяют единым блоком опухоль и лимфатические узлы с последующим послойным ушиванием тканей и кожи. Дренаж в этом случае вставляют в краниальный конец раны. Разберем более подробно отдельные варианты мастэктомии. Иссекающая биопсия кажется наиболее подходящей для удаления небольших опухолей. По краям опухоли вместе с ней удаляется здоровая ткань, рана зашивается в два слоя. Иссекающая биопсия не занимает много времени и не связана с риском осложнений после длительного наркоза. Более широкое иссечение можно сделать позже, после получения результатов биопсии, если есть к этому показания. Однако большинство опухолей молочных желез собак и кошек являются злокачественными и часто дают рецидивы, поэтому рекомендуется широкое иссечение. Локальная мастэктомия (рис. 12 В) осуществляется удалением одной молочной железы. Вокруг нее делаются два элиптических надреза, затем продолжают рассекать мягкие ткани до брюшной стенки. При необходимости мышечную фасцию удаляют вместе с опухолью. Рана закрывается в два слоя. Лимфатический узел, в котором совершается отток, служит барьером для прохождения метастазов, если он увеличен, то подлежит удалению вместе с опухолью. Региональная мастэктомия (рис. 12 В) осуществляется удалением двух или более желез вместе с соответствующим лимфоузлом. Этот прием выполняется чаще на смежных железах. Рассечение такое же, как и при локальной мастэктомии. Односторонняя мастэктомия (рис. 12 С) выполняется при удалении одной целой цепочки молочных желез. Рассечение проводится вдоль обеих сторон цепочки желез до пересечения краниально от первой железы и каудально от последней, недалеко от вульвы. Мягкие ткани рассекаются вниз вплоть до мышечной фасции. Из-за необходимости лигировать поверхностную надчревную артерию, иссечение обязательно начинать с последней железы. Зажимы Кохера накладываются на каудальную часть железы, железы отделяются от брюшной стенки с помощью комбинации приемов тупого и острого иссечения. Каудальные поверхностные надчревные артерия и вена изолируются и лигируются. Иссечение происходит легко до достижения реберной дуги, здесь план иссечения менее определен. Ассистент может начать закрывать каудальную часть раны. Паховый лимфоузел окружен жировой прослойкой. Подмышечный лимфоузел находится вентральнее широчайшей мышцы спины, рядом с латеральной грудной артерией, но если он не увеличен – его трудно найти, в таких случаях его не удаляют. Рану закрывают в 2 слоя. Дренаж Пенроуза полезен для предупреждения скопления жидкости в паховой области. Послеоперационная анальгезия может быть необходима в течение первых 24 часов. После операции на пациента рекомендуется надеть нежный бандаж для комфортного состояния пациента и защиты шва от разлизывания. Дренаж Пенроуза удаляется через 2-5 дней. Поэтапная двусторонняя мастэктомия применяется, если вся железистая ткань должна быть удалена. В основном она осуществляется проведением двух односторонних операций с интервалом в 6 недель. Таким образом, закрытие раны облегчается, благодаря уменьшению напряжения кожи, ее растягиванию и приспособлению. Каждая из операций занимает меньше времени, чем одновременная двусторонняя, но требуется два раза вводить животному наркоз. Поэтапную мастэктомию полезно проводить у таких пород как грейхаунд, у которых слишком мало кожи для закрытия большой раны без создания сильного напряжения. Одновременная двусторонняя мастэктомия (рис. 12 А) может быть выполнена у многих пород. При этом требуется одна анастезия и удаляется вся ткань молочных желез сразу. Близкое рассмотрение краев раны необходимо, чтобы убедиться, что вся периферическая железистая ткань иссечена. Такая операция показана для собак и кошек, у которых большая часть молочных желез затронута опухолью или некротическим и септическим процессом. Ее можно делать на молодых и жизнеспособных животных, поскольку старые и истощенные могут не выдержать стресса от длительной операции и анестезии. Чтобы определить, хватит ли кожи для закрытия раны, после двусторонней мастэктомии, необходимо положить собаку на спину, захватить руками кожу по каждому латеральному краю цепочек молочных желез и подтянуть их к срединной линии живота до соприкосновения. Рассечение проводится также, как и при односторонней операции, исключая сохранение треугольного участка кожи (клина) каудальнее мечевидного отростка. При сшивании раны края должны соединяться на срединной линии. Подкожная клетчатка должна сшиваться от каудального конца к краниальному. Кожа сшивается прерывистым узловым швом. Шов с валиком иногда необходим около мечевидного отростка, где нужно соединить три кожных участка, т.к. здесь создается наибольшее натяжение. Нередко именно в этом участке швы расходятся. Хирург должен знать, что чрезмерное натяжение кожи затрудняет нормальное дыхание. Анальгезия необходима в течение 1-2 дней после операции. Необходимо наложение мягкого, желательно подбитого ватой, бандажа. СВЕДЕНИЯ О НЕХИРУРГИЧЕСКИХ МЕТОДАХ ЛЕЧЕНИЯ. Лучевая и радиотерапия. Основной целью лучевой терапии является полное разрушение клеток путем воздействия как на основной очаг, так и на регионарные лимфатические узлы. Успешное лучевое лечение основывается на разной степени чувствительности к ионизирующему излучению клеток злокачественной опухоли и клеток здоровых тканей. Избирательность действия является основополагающим фактором как лучевой, так и химиотерапии при использовании цитотоксических препаратов. Чувствительность клеток к облучению тем выше, чем выше их репродуктивная активность и тем ниже, чем ниже ее морфологическая степень дифференцировки. Недостаток кислорода значительно повышает устойчивость к лучевому воздействию. В опухолевой ткани образование сосудов (капилляров) резко отстает от роста опухоли, поэтому бедные сосудами участки находятся в состоянии гипоксии, сохраняют устойчивость к облучению и могут дать рецидив опухоли. Механизм действия ионизирующего излучения на клетку обусловлен многими хакторами. Процесс начинается с ионизации молекул воды и образования активных Н- и ОН-радикалов. Последние выступают по соседству с субстратами, участвующими в процессе деления клеток и их метаболизме. В связи с этим подвергается расщеплению или изменению структура молекулы ДНК, разрушаются митохондрии, нарушается синтез белка, подавляется способность клеток к делению, нарушается ритм этого процесса (синхронизация клеточного цикла). При морфологическом исследовании в поврежденных клетках выявляются кариопикноз, кариолизис, нарушение соотношения ядро-цитоплазма, хромосомные аберрации, появляются многоядерные клетки. Предоперационное облучение опухоли применяется с целью уменьшения ее размеров, послеоперационное – применяется при неполном удалении опухоли во время оперативного вмешательства или для предотвращения локальных рецидивов. Радиотерапевтический метод лечения опухолей молочных желез собак не применяется широко. Основываясь на опыте медиков, его можно попробовать в лечении воспалительной карциномы у собак. Химиотерапия. Противоопухолевыми препаратами, применяемыми в химиотерапии, называют соединения, способные тормозить деление клеток. Они действуют как на опухолевые, так и на здоровые клетки (побочное действие). Химиотерапия в широком понимании включает также гормонотерапию, иммунотерапию, болеутоление и гипералиментацию. Показания к применению химиотерапии постепенно расширяются. Ее применяют в следующих случаях: при онкологических заболеваниях, излечение (или ремиссия ) которых может быть достигнуто только химиотерапией; при опухолях ряда органов (молочной железы, семенника, предстательной железы и др.), как дополнение к хирургическому и лучевому методам; для профилактики метастазирования (при раке молочной железы и семенников и др.) или перевода неоперабельной опухоли в операбельную за счет уменьшения размеров (например, при раке яичника); для паллиативного лечения злокачественных опухолей. Лекарственные препараты, применяемые для химиотерапии опухолей, классифицируют по механизму их действия: алкилирующие средства; антиметаболиты; антимитотические препараты; антибиотики; гормоны; неклассифицируемые соединения. Алкилирующие средства содержат радикалы, оказывающие действие на ДНК, РНК и гистоны. В результате химической реакции активного радикала (ядра) препарата с молекулой ДНК образуется перекрестная связь или разлом молекулы ДНК. В связи с этим измененная ДНК не способна выполнять свою функцию в процессе деления клеток. Наиболее выраженное тормозящее действие алкилирующие средства оказывают на быстроделящиеся клетки. Эти средства как клеточные яды могут также вызывать образование опухолей. Антиметаболиты разделяют на антипурины, антипиримидины, антагонисты фолиевой кислоты и т.д., в зависимости от того, какую группу соединений, необходимых для синтеза ДНК в клетке, они тормозят. Токсическое побочное действие антиметаболитов легче регулируется, а их канцерогенное действие незначительно. Антимитотические препараты останавливают клеточное деление в метафазе. Препараты этого ряда получают из растений. Антибиотики противоопухолевые имеют различный механизм действия. Одни из них влияют на цепочки ДНК, связывая определенные пары оснований (адриамицин), другие осуществляют свое действие за счет алкилирования (стрептозотоцин). Неклассифицируемые соединения обладают разным механизмом действия, отличающимся от указанных выше. Применение препаратов, обладающих цитотоксическим действием при лечении опухолей приводит к временному торможению деления клеток рака, либо даже к полному их уничтожению. Эффект принципиально зависит от свойств клеток опухоли и всей опухоли ( степень злокачественности, склонность к образованию некрозов), а также от состояния иммунной и гормональной систем больного животного. Антиэстрогенная химиотерапия при опухолях молочной железы в медицинской практике широко применяется как продолжение лечения после хирургического удаления опухоли в случае обнаружения метастазов в лимфоузлах или других органах. В ветеринарии этот метод не распространен за неимением окончательной информации об эффективности и безопасности такого лечения у собак. Осуществлялись попытки использовать комбинацию цитотоксина, винкристина, и метотрексата – положительных результатов не получено. Для послеоперационной химиотерапии опухолей молочной железы у женщин эффективно используется тамоксифен. Его антиэстрогенное действие связано с тем, что он блокирует эстрогенные рецепторы. Изучение действия тамоксифена на опухоли молочной железы к собак не дало однозначных результатов. Лечение было остановлено у 50% самок по причине возникновения побочных эффектов, таких, как аменорея, головокружение, тошнота, иногда вагинальные кровотечения. Наряду с антиэстрогенным действием на ткань молочной железы, появилось эстрогенное действие на матку и вагину, которое проявилось набуханием вульвы, проявлением интереса к самцам и другими признаками, характерными для позднего проэструса. Этот эффект объясняется образованием в организме метаболита Е, он составляет всего 6 %, но его эстрогенное действие наряду с другими побочными действиями препарата сильно ограничивает применение тамоксифена для химиотерапевтического лечения опухолей молочной железы собак. Гормональная терапия. Установлено, что стимулирование роста опухолей молочной железы зависит от тех же эндокринных влияний, что и пролифирация нормального эпителия этого органа. Подавление или выключение функции органов, стимулирующий пролиферацию железистого эпителия молочных желез, ведет к атрофии последнего, а также к регрессии опухоли.на этом основаны современные принципы гормонотерапии. Для достижения терапевтического эффекта следуею подавлять или выключать в организме продукцию гормонов, стимулирующих опухолевый рост. Достигнуть этого можно хирургическим, лучевым, гормональным воздействием. Наиболее доступными для любого лечебного учреждения, а поэтому наиболее распространенными являются методы, направленные на подавление функций яичников: овариоэктомия, облучение яичников, лечение андрогенами. К хирургическим методам можно также отнести адреналэктомию и гипофизэктомию. Лекарственная гормонотерапия включает лечение андрогенами, эстрогенами, кортикостероидами. Иммунотерапия. Имеются результаты опытов использования иммунотерапии в постоперационном периоде при раке молочной железы. Отмечалось продление времени выживания и регресс метастазов в легких. Предположительно вакцина BCG (bacillus Calmette-Guerin) обладает таким действием. При внутривенных инъекциях BCG с интервалами в 1,2,3,4, а затем 8 недель, отмечалось продление жизни в среднем до 100 недель по сравнению с 24 неделями в контрольной группе. Применение неспецифического иммуномодулятора левомизола у 76 прооперированных собак не показали положительных результатов. ПОСТОПЕРАЦИОННЫЕ ОСЛОЖНЕНИЯ И РЕЦИДИВЫ ПРИ ПРОВЕДЕНИИ ОПЕРАЦИЙ НА ОРГАНАХ БРЮШНОЙ ПОЛОСТИ И МОЛОЧНОЙ ЖЕЛЕЗЫ.Осложнения в постоперационный период могут наблюдаться после любой операции, но чаще они развиваются после обширных, травматических оперативных вмешательств на грудной и на брюшной полостях. Различают ближайший и отдаленный послеоперационный периоды. В ближайшем послеоперационном периоде наиболее ответственным и критическим является ранний период – первые 2-3 дня. В это время в максимальной степени проявляются изменения, которые являются прямым следствием операционной травмы и общего наркоза. Это зависит от особенностей патологического процесса, общего состояния организма до операции, а так же от наличия сопутспвующих заболеваний, возраста, характера вмешательства, осложнений в ходе операций, от течения наркоза и т.д. основными задачами терапии в ранний период являются: поддержание сердечно-сосудистой деятельности, функции внешнего дыхания, борьба с гипоксией, нарушениями водно-электролитного баланса, метаболизма и кислотно-щелочного равновесия. Послеоперационный период при операциях на органах брюшной полости и молочной железе имеет три особенности: развитие бронхолегочных осложнений, возникновение пареза желудочно-кишечного тракта и большая вероятность развития сердечной недостаточности. Бронхолегочные осложнения обусловлены гиповентиляцией легких за счет ограничения диафрагмального дыхания на фоне метеоризма, послеоперационных болей. Из осложнений со стороны дыхательной системы встречаются ателектазы легкого и пневмонии с преобладанием симптома дыхательной недостаточности которая, как правило, развивается на 3-4 день. Решающим для постановки диагноза является рентгенологическое исследование. Лечение комплексное: антибиотики, сульфаниламиды, оксигенотерапия и прочее. Сердечная недостаточность как послеоперационное осложнение начинается с левожелудочковой недостаточности, которая быстро переходит в недостаточность обоих желудочков. Провоцирующим фактором обычно бывает внутривенное введение больших количеств жидкости, особенно на фоне имеющихся патологий сердечно-сосудистой системы (кардиосклероз, аортального порока и пр.). Клинически сердечная недостаточность проявляется цианозом видимых слизистых оболочек, тахикардией, выделением кровянистой мокроты, болезненным увеличением печени и тд. При возникновении этого осложнения назначают сердечные гликозиды и диуретики. В качестве профилактики необходимо проводить предоперационную подготовку (премедикацию) пациентов с учетом имеющейся патологии и индивидуальное определение объемов внутривенных инфузий. Дисфункции желудочно-кишечного тракта как правило развиваются в первые дни после операции, при этом наблюдаются тошнота и рвота. Однократная рвота не требует специальных лечебных мероприятий, при повторной рвоте используют противорвотные препараты фенотиазинового ряда (аминазин, пипольфен и др.), производят зондирование желудка для эвакуации его содержимого. В случае упорной рвоты в желудок вводят тонкий зонд для постоянной асптрации содержимого. Важно вести количественный и качественный анализ удаленного содержимого желудка, т.к. с ним выделяются минеральные соли. Для предотвращения развития гиповолемии и нарушения водно-электролитного баланса необходимо проводить внутривенную инфузию солевых растворов. Симптомами пареза желудочно-кишечного тракта являются срыгивание или рвота застойным желудочным содержимым, вздутие живота, задержка стула, неотхождение газов, резкое ослабление перестальтических шумов. Парез развивается на 2-3 сутки после операции. Для профилактики и лечения такого рода патологий на следующий день после операции проводят зондирование желудка 2-3 раза в день. Применяют лекарственную стимуляцию моторной функции желудочно-кишечного тракта. Используют ганглиоболкаторы: димеколин, прозерин, питуитрин. Хорошие результаты дает внутривенное введение электролитов, особенно калия, который стимулирует перистальтику. В экстренных случаях производят гастростомию на фолиевском катетере или различные варианты интубации кишечника. При полном удалении опухолей из нижних молочных желез после операции могут образоваться серотомы или гематомы. Эти осложнения чаще всего вызываются недостаточным заживанием подкожного слоя. При возникновении серотом проводится пункция, и жидкость отсасывается с помощью иглы; на несколько дней накладывается давящая повязка. Для того, чтобы ускорить рассасывание гематом, три раза в день делают горячие компрессы, которые накладывают на 15 минут. После неполного удаления злокачественных опухолей происходит нарушение заживления раны, и прогрессирующее разбухание опухолевых тканей приводит в течение нескольких дней к спаечным уплотнениям краев раны. В таких случаях прогноз неблагоприятным и животное рекомендуется подвергнуть эутаназии. Рецидивами называются новые гистологически идентичные опухоли на том же месте. Они наблюдаются примерно в 20% случаев. Почти половина рецидивирующих опухолей оцениваются как доброкачественные, и показано проведение повторной операции. ПРОГНОЗ ПРИ ОПУХОЛЯХ МОЛОЧНОЙ ЖЕЛЕЗЫ У СОБАК.Если собаки умирают от последствий опухолей молочной железы, то это, как правило, происходит в течение первых 2 лет после операции. Распространено гистопатологическое деление прогнозов по результатам биопсии опухолей молочной железы на: « благоприятный» и «осторожный» - при доброкачественных опухолях «сомнительный» и «неблагоприятный» при злокачественных опухолях. Проведенное Kalin, Suter & Lott-Stolz (1985) ретроспективное исследование биологических свойств опухолей молочной железы дало такие показатели относительно выживаемости через два года после операции: при опухолях с благоприятным прогнозом в живых осталось 76% прооперированных собак, с осторожным прогнозом - 70%, с сомнительным прогнозом – 46% и с неблагоприятным – 14%. |
