Лекции по дисциплине Металловедение. Атомнокристаллическая структура металлов
 Скачать 453.5 Kb. Скачать 453.5 Kb.
|
|
Тема № 1 АТОМНО-КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА МЕТАЛЛОВ Классификация металлов Под металлами понимают определенную группу элементов, расположенную в левой части Периодической таблицы Д.И.Менделеева. Особенность строения металлических веществ заключается в том, что они все построены в основном из таких атомов, у которых внешние электроны слабо связаны с ядром. Это обусловливает и особый характер химического взаимодействия атомов металла, и металлические свойства. Теория металлического состояния рассматривает металл как вещество, состоящее из положительно заряженных ионов, окруженных отрицательно заряженными частицами - электронами, слабо связанными с ядром. Эти электроны непрерывно перемещаются внутри металла и принадлежат не одному какому-то атому, а всей совокупности атомов. Характерной особенностью атомно-кристаллического строения металлов является наличие электронного газа внутри металла, слабо связанного с положительно заряженными ионами. Все металлы можно разделить на две большие группы - черные и цветные металлы. Черные металлы имеют темно-серый цвет, большую плотность (кроме щелочноземельных), высокую температуру плавления, относительно высокую плотность и во многих случаях обладают полиморфизмом. Наиболее типичным металлом этой группы является железо. Цветные металлы чаще всего имеют характерную окраску: красную, желтую, белую. Обладают большой пластичностью, малой твердостью, относительно низкой температурой плавления, для них характерно отсутствие полиморфизма. Наиболее типичным металлом этой группы является медь. Текже металлы можно подразделить следующим образом: 1. Железные металлы - железо, кобальт, никель и близкий к ним по своим свойствам марганец. Кобальт, никель и марганец часто применяют как добавки к сплавам железа, а также в качестве основы для соответствующих сплавов, похожих по своим свойствам на высоколегированные стали. 2. Тугоплавкие металлы, температура плавления которых выше, чем железа (т.е. 1539 С). Применяют как добавки к легированным сталям, а также в качестве основы для соответствующих сплавов. 3. Редкоземельные металлы (РМЗ) - лантан, церий, неодим, празеодим и др., объединяемые под названием лантаноидов, и сходные с ними по свойствам иттрий и скандий. 4. Щелочноземельные металлы в свободном металлическом состоянии не применяются, за исключением специальных случаев. Цветные металлы подразделяются на: 1. Легкие металлы - бериллий, магний, алюминий, обладающие малой плотностью. 2. Благородные металлы - серебро, золото, металлы платиновой группы. 3. Легкоплавкие металлы - цинк, кадмий, ртуть, олово, свинец, висмут, таллий, сурьма и элементы с ослабленными металлическими свойствами - галлий, германий. Кристаллическое строение металлов Всякое вещество может находится в трех агрегатных состояниях -твердом, жидком и газообразном. Кристаллическое состояние прежде всего характеризуется определенным, закономерным расположением атомов в пространстве. В кристалле каждый атом имеет одно и то же количество ближайших атомов - соседей, расположенных на одинаковом от него расстояние. Расположение атомов в кристалле изображается в виде пространственных схем, в виде так называемых кристаллических ячеек. Под элементарной кристаллической ячейкой подразумевается наименьший комплекс атомов, который при многократном повторение в пространстве позволяет воспроизвести пространственную кристаллическую решетку . 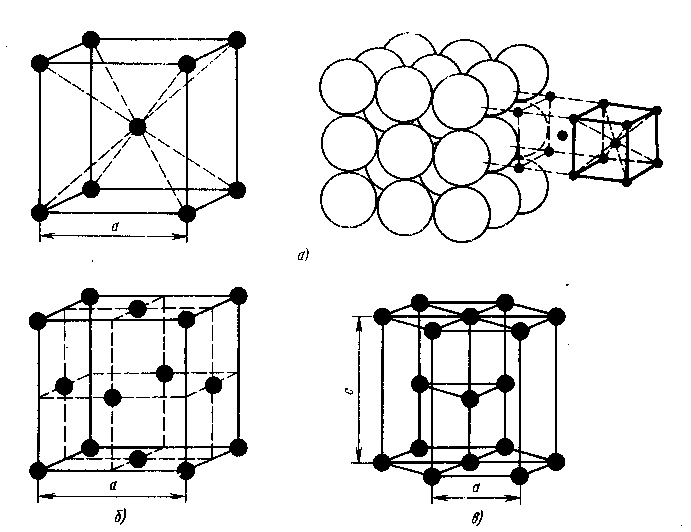 Простейшим типом кристаллической ячейки является кубическая решетка. В простой кубической решетке атомы расположены (упакованы) недостаточно плотно. Простейшим типом кристаллической ячейки является кубическая решетка. В простой кубической решетке атомы расположены (упакованы) недостаточно плотно.Рис.1. Типы кристаллической ячейки: а - кубическая объемно-центрированная, б – кубическая гранецентрированная; с - гексагональная плотноупакованная Стремление атомов металла занять места, наиболее близкие друг к другу, приводят к образованию решеток следующих типов (рис. 1): кубической объем-ноцентрированной, кубической гранецентрированной и гексагональной плотноупакованной (рис.1 ). В кубической объемно-центрированной решетки (ОЦК) атомы расположены в углах куба и один атом в центре объема куба. в гранецентрированной кубической решетке (ГЦК) -атомы расположены в углах куба и в центре каждой грани, в гексагональной решетке атомы расположены в углах и центре шестигранных оснований призмы и три атома в средней плоскости призмы. Кубическую ОЦК решетку имеют металлы:Na, Li, W, V, Cr и др. Кубическую ГЦК решетку имеют Pb, Ni, Ag, Au, Cu и др. Размеры кристаллической решетки характеризуются параметрами, или периодами решетки. Кубическую решетку определяет один параметр - длина ребра куба. Параметры имеют величины порядка атомных размеров и измеряются в ангстремах. Некоторые металлы имеют тетрагональную решетку; она характеризуется тем, что ребро с не равно ребру а. Отношение этих параметров характеризует так называемую степень тетрагональности. Число атомов, находящихся на наиболее близком расстояние от данного атома, называется координационным числом. Так например, атом в простой кубической решетке имеет шесть ближайших равноотстоящих соседей, т.е. координационное число этой решетки равно 6 (рис. 2 ). Центральный атом в объемноцентрированной решетке имеет восемь ближайших равноотстоящих соседей, т.е. координационное число этой решетки равно 8. Координационное число для гранецентрированной решетки равно 12. В случае гексагональной плотноупакованной решетки координационное число равно 12. Реальное строение металлических кристаллов Металлическое изделие состоит из очень большого числа кристаллов. Подобное строение называется поликристаллическим. Кристаллы неправильной формы в поликристаллическом агрегате называются зернами, или кристалликами. Различие отдельных зерен состоит в различной пространственной ориентации и наименьшем расстоянии от данного атома для различных решеток. В общем случае ориентация кристаллической решетки в зерне случайна, с разной степенью вероятности может встретится любая ориентация ее в пространстве. При очень медленном отводе тепла при кристаллизации, а также с помощью других специальных способов может быть получен кусок металла, представляющий собой один кристалл, называемый монокристалл. Несовершенства структуры металлов Одним из видов несовершенств кристаллического строения является наличие незанятых мест в узлах кристаллической решетки, или иначе - вакансии, или атомных дырок (рис. 2). Такой "точечный" дефект решетки играет важную роль при протекание диффузионных процессов в металлах.  Рис. 2. Точечные дефекты кристаллической решетки Число вакансий при комнатной температуре очень мало по сравнению с общим числом атомов (примерно 1 вакансия на 1018 атомов), несильно увеличивается с повышением температуры, особенно вблизи температуры плавления (1 вакансия на 104 атомов). Также возможно наличие межузельных (дислоцированных) атомов. 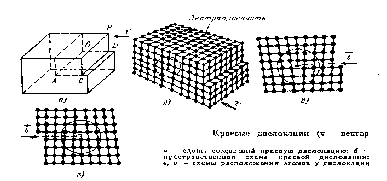 Рис. 3. Краевые дислокации Другим важнейшим видом несовершенства кристаллического строения являются так называемые краевые (линейные) дислокации (рис.3). Связанны с образованием в кристаллической решетке по каким-либо причинам появилась лишняя полуплоскость атомов, так называемая экстраплоскость. Край такой плоскости образует линейный дефект (несовершенство) решетки, который называется краевой дислокацией. Краевая дислокация может простираться в длину на многие тысячи параметров решетки, может быть прямой, но может и выгибаться в ту или иную сторону. В пределе она может закрутиться в спираль, образуя винтовую дислокацию (рис 4). Вокруг дислокации возникает зона упругого искажения решетки. Расстояние от центра, дефекта до места решетки без искажения принимают равным ширине дислокации, она невелика и равна нескольким атомным расстояниям. 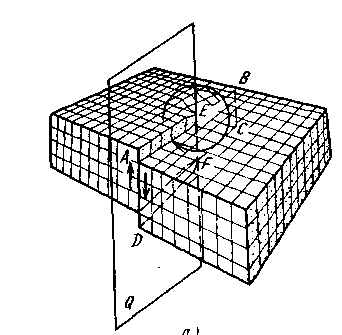 Рис. 4. Винтовая дислокация Рис. 4. Винтовая дислокацияВакансии непрерывно перемещаются в решетке, когда соседствующий в ней атом переходит в "дырку", оставляя пустым свое старое место. Повышение температуры, тепловой подвижности атомов увеличивает число таких актов и увеличивает число вакансий. Линейные дефекты не двигаются самопроизвольно и хаотически, как вакансии. Однако достаточно небольшого напряжения, чтобы дислокация начала двигаться, образуя плоскость, а в разрезе - линию скольжения С. Различие свойств в зависимости от направления испытания носит название анизотропии. Все кристаллы анизотропные. Тема № 2 КРИСТАЛЛИЗАЦИЯ В чистых металлах при определенных температурах происходит изменение агрегатного состояния: твердое состояние сменяется жидким при температуре плавления, жидкое состояние переходит в газообразное при температуре кипения. Температуры перехода зависят от давления, но при постоянном давлении они вполне определены. Энергетические условия процесса кристаллизации При переходе из жидкого состояния в твердое образуется кристаллическая решетка, возникают кристаллы. Такой процесс называют кристаллизацией. В природе все самопроизвольно протекающие превращения, а следовательно, кристаллизация и плавление обусловлены тем, что новое состояние в новых условиях является энергетически более устойчивым, обладает меньшим запасом энергии. Энергетическое состояние системы, имеющей огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией F, называемой свободной энергией (свободная энергия F = U - TS, где U - внутренняя энергия системы; Т - абсолютная температура; S - энтропия). При температуре, равной ts, свободные энергии жидкого и твердого состояний равны, металл в обоих состояниях находится в равновесии. Эта температура ts и есть равновесная или теоретическая температура кристаллизации. Для начала кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Температура, при которой практически начинается кристаллизация, называется фактической температурой кристаллизации. Охлаждение жидкости ниже равновесной температуры кристаллизации называется переохлаждением. Разность Δt между температурой ts и температурой tk, при которой протекает кристаллизация, называется степенью переохлаждения: Δ t = ts - tk. При медленном охлаждении степень переохлаждения невелика, и кристаллизация протекает при температуре, близкой к равновесной. На кривых охлаждения при температурах кристаллизации отмечаются горизонтальные площадки (остановка в падении температуры), образование которых объясняется выделением скрытой теплоты кристаллизации. С увеличением скорости охлаждения степень переохлаждения возрастает. Процесс кристаллизации начинается с образования кристаллических зародышей (центров кристаллизации) и продолжается при их росте. Пока образовавшиеся кристаллы растут свободно, они могут иметь геометрически относительно правильную форму. При столкновении же растущих кристаллов их правильная форма нарушается. В результате растущие кристаллы, имеющие сначала геометрически правильную форму, после затвердевания получают неправильную внешнюю форму, их называют кристаллитами или зернами. В процессе кристаллизации возникают зародыши разного размера, однако не все они способны к росту. Минимальный размер зародыша Rk, способного к росту при данных температурных условиях, называется критическим размеров зародыша. C увеличением степени переохлаждения размер критического зародыша уменьшается, следовательно, число зародышей, способных к росту, возрастает. Скорость процесса кристаллизации и строение металла после затвердевания зависят от числа зародышей, возникающих в единицу времени в единице объема и от скорости роста зародышей. Чем больше центров кристаллизации (зародышей)и меньше скорость их роста, тем мельче кристалл, выросший из одного зародыша (зерно металла). Величина зерна может меняться в пределах от 0,4 до 0,001 мм. При небольшой степени переохлаждения число зародышей мало и скорость роста велика. В этих условиях будет получено крупное зерно. С увеличением степени переохлаждения число зародышей возрастет в большей мере, чем скорость их роста и размер зерна в затвердевшем металле уменьшается. Чем больше размер зерна, тем ниже пластичность и прочность металла. Для получения мелкого зерна часто используют процесс модифицирования. При модифицировании в расплавленный металл вводят небольшое количество специальных веществ (модификаторов), которые, практически не изменяя его химического состава, вызывают при кристаллизации измельчение зерна и тем способствуют улучшению механических свойств. Строение металлического слитка Чаще всего в процессе кристаллизации образуются разветвленные или древовидные кристаллы, получившие название дендритов (рис. 5). При образовании кристаллов первоначально образуются длинные ветви - так называемые оси первого порядка (главные оси). Одновременно с удлинением осей первого порядка на их ребрах происходит зарождение и рост перпендикулярных к ним таких же ветвей второго порядка. В свою очередь на осях второго порядка зарождаются и растут оси третьего порядка. Правильная форма дендритов искажается в результате столкновения и срастания частиц на поздних стадиях кристаллизации. 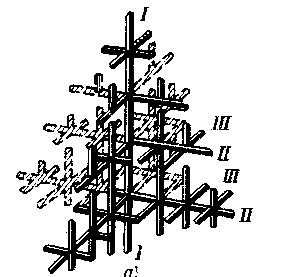 Рис. 5. Древовидные кристаллы Полиморфные превращения Значительное число металлов в зависимости от температуры может существовать в разных кристаллических формах или в разных полиморфных модификациях. В результате полиморфного превращения атомы кристаллического тела, имеющие решетку одного типа, перестаиваются таким образам, что получается кристаллическая решетка, другого типа. Полиморфную модификацию, устойчивую при более низкой температуре, для большинства. металлов принять обозначать буквой α, при более высокой β , а затем γ и т.д. Известны полиморфные превращения Fe α - Feγ и др. Полиморфное превращение осуществляется образованием зародышей и последующим их ростом в результате перехода атомов из старой модификации в новую. Зародыши часто возникают на границах исходных зерен. В результате превращения получаются новые кристаллические зерна, имеющие другой размер и форму. Переход металла из одной аллотропической, модификации в другую в условиях равновесия (малой степени переохлаждения) протекает при постоянной температуре и сопровождается выделением тепла, если превращение протекает при охлаждении, и поглощением тепла в случае нагрева. Поэтому на кривых охлаждения (рис. 6) при температуре полиморфного превращения (несколько ниже tn ) отмечается площадка. В реальных условиях полиморфные превращения протекают лишь при значительном переохлаждении (перегреве) относительно равновесной температуры полиморфного превращения tn. И  зменение компактности кристаллической решетки при переходе из одной полиморфной формы в другую влечет за собой изменение объема вещества и его свойств. Тема № 3 ПЛАСТИЧЕСКАЯ ДЕФОРМАЦИЯ И МЕХАНИЧЕСКИЕ СВОЙСТВА Под механическими свойствами металла (или другого материала) понимают характеристики, определяющие его поведение под действием приложенных к нему внешних механических сил в виде статической, динамической или знакопеременной нагрузок. К механическим свойствам относят прочность - сопротивление металла (сплава) деформации и разрушению и пластичность - способность металла к необратимой без разрушения деформации (остающейся после удаления деформирующих сил). Деформацией называется изменение размеров и формы тела под действием приложенных сил. Деформация вызывается внешними силами, приложенными к телу, или происходящими в самом теле физико-механическими процессами (например, изменение объема отдельных кристаллитов при фазовых превращениях или вследствие температурного градиента). Виды напряжений В случае одноосного растяжения возникающие в теле напряжения равны. Сила Р, (рис. 7) приложенная к некоторой площадке F, обычно направлена к ней под некоторым углом. Поэтому в теле возникают нормальные и касательные напряжения. Образование внутренних напряжений связано в основном с неоднородным распределением деформаций (в том числе и микродеформаций) по объему тела. Наличие в испытуемом образце механических надрезов, трещин внутренних дефектов металла приводит к неравномерному распределению напряжений, создавая у основания надреза пиковую концентрацию нормальных напряжений (нормальные напряжения бывают растягивающими и сжимающими) (см. рис. 7). Действие надрезов, сделанных в образце, аналогично конфигурации изделий, имеющих сквозные отверстия, резьбу и т.п., или влиянию внутренних дефектов металла (неметаллических включений, графитных выделений в чугуне, трещин и др.), нарушающих его цельность. Поэтому всевозможные надрезы, отверстия, галтели и другие источники концентрации напряжений называют концентраторами напряжений. |
