Биомембраны. Биомембраны. Структура и функциональная роль
 Скачать 138 Kb. Скачать 138 Kb.
|
|
Биомембраны. Структура и функциональная роль.
Функции и задачи биомембран. Биомембраны выполняют двойную функцию:
Изучение биомембран важно для понимания жизнедеятельности организма в норме, для выяснения механизма патологии и для верного подхода к созданию комплекса врачебных мероприятий. Задачи биомембран:
Различают клеточную (плазматическую) и внутриклеточные биомембраны. Размеры, химический состав и строение биомембран. Биомембраны – надмолекулярные структуры. Их толщина очень мала (10 нм). Они представляют собой двумерные структуры. Химический состав: липиды (40%) и белки (60%) – количественное соотношение варьирует. Биомембраны, в большинстве своём, гетерогенны. Но есть и относительно простые биомембраны. Например, белковая часть внутриклеточных мембран палочек сетчатки содержит всего один белок – родопсин. Структурной основой биомембран являются липиды, большую часть которых составляют фосфолипиды. Общая структура фосфолипида:
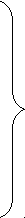 О О|| ОН Р О Х | О | Гидрофильная СН2 СН СН2 часть | | О О | | С = О С = О 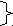 | | | |R1 R2 Гидрофобная часть Все фосфолипиды содержат полярную гидрофильную головку и два неполярных гидрофобных хвоста, следовательно, проявляют амфофильные свойства. В 1972 году Зингер и Николсон предложили Мозаичную модель биомембран, популярную и по настоящее время. Согласно этой теории, структурной основой биомембран является двойной липидный слой, в котором гидрофобные хвосты обращены внутрь биомембран и образуют единую углеводородную фазу, а полярные головки находятся снаружи, по обе поверхности билипидного слоя. Схематически: 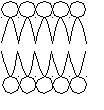 Этот билипидный слой инкрустирован молекулами белка, которые делят на периферические и интегральные. Периферические белки – белки, которые целиком расположены на гидрофильной части слоя, т.е. только на поверхности мембран. Интегральные белки – белки, имеющие участки гидрофобной поверхности, они погружены на различную глубину в билипидный слой. Некоторые белки пронизывают мембрану насквозь и называются прошивающими. С учётом белкового компонента, схема примет вид: 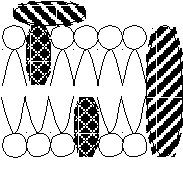  - периферический белок - периферический белок - интегральный белок - интегральный белок - прошивающий белок - прошивающий белокАсимметрия биомембран. Как белковый, так и липидный состав биомембран неодинаков. Фосфолипидные слои отличаются относительным содержанием компонентов, а расположение белков в зависимости от слоя имеет принципиальные, качественные отличия. Например, в плазматических мембранах к внутренней стороне примыкает больше белков-ферментов, а к наружной – больше белков узнавания и оборонительных белков. Сравним Мозаичную модель Зингера-Николсона с «Бутербродной» моделью Даниэли и Дайсона: принцип расположения липидов одинаковый. Однако в «Бутербродной» модели все белки – гидрофилы, а, следовательно, расположены только на поверхности мембраны, по обе стороны от билипидного слоя, т.е. возникает двусторонняя симметрия. Схема «Бутербродной» модели: 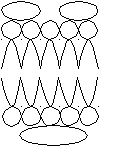 Силы, стабилизирующие мембранные структуры. Различают следующие силы взаимодействия:
Отдельная сильная связь прочнее слабой; чтобы её разрушить, необходимо приложить больше энергии. Однако кооперативный вклад слабых взаимодействий зачастую равен вкладу сильных. Целостность биомембран поддерживается слабыми связями, а определяющую роль играют гидрофобные взаимодействия между неполярными группировками в результате отталкивания молекул воды. В биомембране они возникают между хвостами липидов, а также между хвостами липидов и интегральными белками. Полярные головки липидов связываются с периферическими белками электростатическими силами. Физическое строение биомембран. Физическое строение биомембран определяется свойствами билипидного слоя. А они – жидкостные. Доказательства: 1. Мембранные липиды не закреплены жёстко и постоянно меняются местами. Различают 2 вида перемещений:
Для молекул липидного слоя характерен коэффициент диффузии Латеральную диффузию могут совершать мембранные белки. В данном случае коэффициент будет зависеть от глубины погружения белка и вязкости среды. Для периферических белков 2. Большинство мембранных липидов содержит двойные связи, т.е. являются ненасыщенными, с низкой температурой физиологического плавления. 3. Метод калориметрии. Микрокалориметрическими измерениями установлено, что при определённых условиях мембранно-фазовый переход соответствует плавлению липидов, т.е. температура плавления очень низка (нередко - отрицательна). Однако мембраны не растекаются, а поддерживают объём клетки. Это становится возможным благодаря сложной пространственной структуре, напоминающей кристаллическую, характерную для твёрдых тел. В биомембранах сочетается упорядоченность и подвижность, т.е. биомембраны находятся в жидко-кристаллическом состоянии, «белковые айсберги плавают в липидном море». Часть белковых молекул закреплено на цитоплазматических структурах клетки микротрубочками и микрофиламентами, являющимися стабилизаторами клеточной поверхности. Методы анализа структуры биомембран.
В организме практически нет парамагнетиков и сильно флуоресцирующих веществ, следовательно, 3-ий и 4-ый методы используются в определённой модификации: в организм вводят парамагнитные или флуоресцирующие метки и зонды. Метка – молекула, встраивающаяся в мембрану и удерживающаяся в ней ковалентными связями. Зонд - молекула, встраивающаяся в мембрану и удерживающаяся в ней слабыми взаимодействиями. С помощью меток удаётся установить структуру молекул и взаимную ориентацию их частей. А с помощью зондов можно также установить вязкость – физическое состояние окружения молекул. Недостаток данных методов – они влияют на свойства объекта. ЯМР позволяет установить структуру молекул, подвижность отдельных группировок в них. Применяется в клинической диагностике болезней, связанных с изменением структурного состояния органов и тканей (в т.ч. онкологических). Производится сканирование (послойный просмотр участка) – ЯМР-интраскопия. Преимущества: не оказывает вредного воздействия на организм. Искусственные липидные мембраны (БЛМ) – получают при контакте смеси липидов, растворённых в органике с водой. Различают плоские и сферические (везикулярные) искусственные мембраны. Они также имеют 2-х-слойное строение. Физические свойства БЛМ близки к свойствам биомембран (толщина, электроёмкость). Но БЛМ не обладают метаболической активностью, так как не имеют в своём составе белков. Применяются для изучения проницаемости и транспорта веществ. Многослойные везикулярные мембраны (липосомы) – замкнутые частицы, образованные рядами концентрических билипидных слоёв, раздёлённых водным пространством. Толщина каждого билипидного слоя в 3-4 раза больше, чем у водной прослойки. Диаметр липосомы 5-50 мкм. Используются в терапии как капсулы для доставки лекарственных препаратов в органы и ткани (липосома + антитело – транспорт к ткани-антигену). Преимущества: нетоксичны, полностью усваиваемы, способны преодолевать ряд барьеров. Схема: 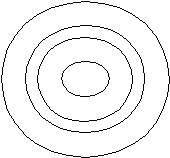 Биомембраны. Мембранный транспорт.
Проницаемость биомембран. Виды трансмембранного переноса веществ. Проницаемость – свойство мембран пропускать различные вещества. Селективность (избирательность) – различная проницаемость для разных соединений. У биомембран селективность высокая. Существует два принципиально различных типа переноса вещества через мембрану:
Градиент – характеризует быстроту изменения параметра в пространстве (вдоль выбранного направления). Градиент – векторная характеристика. В биофизике принято градиент направлять от большего значения к меньшему. Пример: ГС – градиент концентраций, Г Свободная энергия F – характеризует способность системы совершать работу. Виды химических реакций:
Пассивный транспорт – перемещение вещества по концентрационному и электрическому градиентам. Характерные черты (критерии):
Активный транспорт – перенос против градиента, концентрационного или электрического. Характерные черты (критерии):
Пассивный мембранный транспорт: способы и математическое описание. Пассивный перенос растворённого вещества осуществляется путём диффузии, а растворителя – путём осмоса и фильтрации (физический смысл - диффузия). Диффузия – самопроизвольное перемещение вещества по его концентрационному или электрическому градиенту за счёт хаотического теплового движения его молекул (ионов). Диффузия в растворе нейтральных молекул описывается уравнением Фика: m – масса вещества t – время D – коэффициент диффузии (зависит от свойств переносимого вещества) С – концентрация вещества S – площадь поверхности, через которую идёт перенос «-» показывает, что градиент концентрации уменьшается. 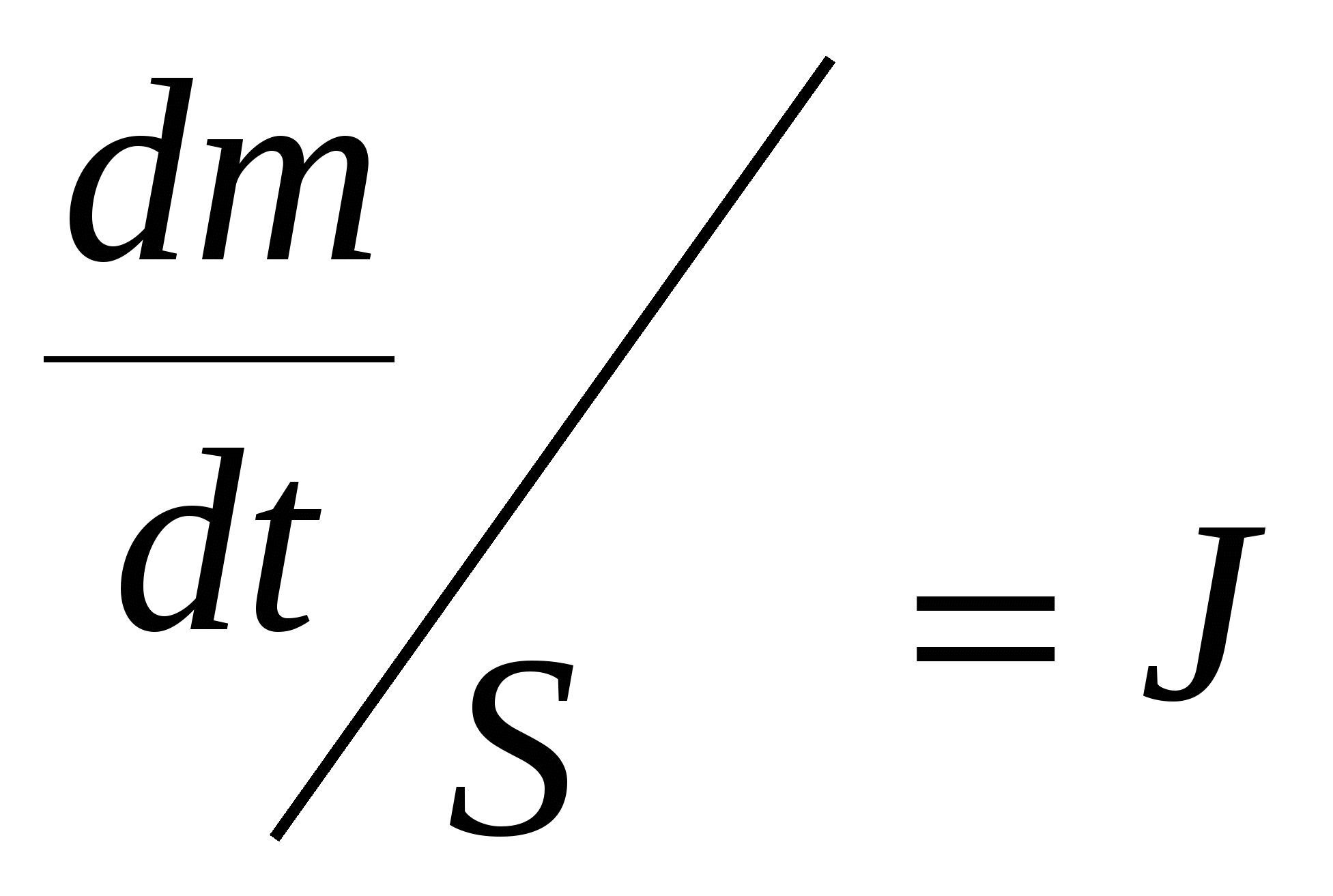 - плотность потока вещества – масса вещества, переносимая в единицу времени через единицу площади мембраны. - плотность потока вещества – масса вещества, переносимая в единицу времени через единицу площади мембраны. Диффузия через мембрану нейтральных молекул:  b b – толщина мембраны С1 < С2 – концентрации переносимого вещества С1 мембрана С2 Заменим коэффициент D, зависящий от свойств субстрата на коэффициент a, зависящий от свойств мембраны: Р – коэффициент проницаемости, зависящий от свойств мембраны. Диффузия через мембрану ионов: Пусть Z – заряд переносимого иона [элементарные единицы] F – число Фарадея = 9,65*107 Кл/кмоль R – универсальная газовая постоянная T – абсолютная температура [К]. Молекулярные механизмы пассивного мембранного транспорта. П   ассивный перенос (диффузия) ассивный перенос (диффузия)П    ростая Облегчённая ростая ОблегчённаяЧ   ерез липидный слой По каналам ерез липидный слой По каналам ГФБ, липиды, жировые клетки ГФЛ, аминокислоты, сахара, спирты, минеральные вещества, мочевина *** ГФБ – гидрофобные, ГФЛ – гидрофильные вещества. Способ передачи зависит от полярности молекул вещества. Простая диффузия (неопосредованный перенос):
Облегчённая диффузия (опосредованный перенос):
V 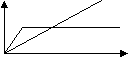 простая простаяоблегчённая C Сквозные каналы имеют белковую природу, их стенки выстланы полярными группировками. Диссоциация, адсорбция ионов из раствора приводит к появлению на внутренней поверхности каналов фиксированных зарядов, преимущественно отрицательных. Факторы, лимитирующие проникновение веществ через каналы:
Больше всего проницаемость для небольших и электронейтральных молекул воды. Причём для воды существует дополнительный, особый механизм проникновения через подвижные поры липидной природы. Мембранные липиды могут находится в двух основных пространственных конфигурациях – конформациях:
  Кинки Кинки могут перемещаться через мембрану при движении хвостов и самих липидов. Вода попадает в них и мигрирует вместе с ними. При облегчённой диффузии: специфический переносчик – компонент мембраны, имеющий центр связывания субстрата. Варианты:
Эстафетная передача – молекулы интегральных белков передают субстрат друг другу как эстафетную палочку. Активный мембранный транспорт. Характеристика бионасосов. В основе активного транспорта лежит сопряжение противоградиентных потоков вещества с гидролизом АТФ. Молекулярный механизм, локализованный в мембране и способный транспортировать вещества за счёт энергии гидролиза АТФ, называется биологическим насосом. В природе только ионные насосы:
Молекулярная организация и этапы работы Калий - Натриевого насоса. В основе устройства лежит фермент: калий, натрий – активируемая АТФ-аза. Функциональная единица состоит из 2-х полипептидных цепей: Связывание ионов происходит в петле между 2-ой и 3-ей спиралями цепи, а фосфата – между 4-ой и 5-ой спиралями. Вместе обе субъединицы образуют компактную глобулу – протомер. При гидролизе АТФ четыре протомера взаимодействуют, объединяясь в олигомерный комплекс. В основе работы фермента в качестве насоса – его способность к изменению конформаций. Их две: Е1 – исходная конформация – фермент способен взаимодействовать с АТФ и ионами натрия с внутренней стороны мембраны. Его активные центры связывают и удерживают ионы натрия и терминальный фосфат АТФ. Переход в конформацию Е2 состоит в перемещении отдельных частей белковой глобулы и перестройке ионных центров. В результате петля, содержащая ионный центр связывания оказывается не в цитоплазме, а внутри мембраны, между спиралями 2 и 3, причём сам центр обращён наружу, во внеклеточную среду. Структура и свойства этого центра меняются: он теряет способность удерживать натрий и приобретает высокое сродство к калию. Минимуму свободной энергии отвечает исходная конформация Е1, поэтому переход в конформацию Е2 требует дополнительной энергии, а обратное превращение осуществляется самопроизвольно. Работа насоса осуществляется в 5 стадий:
Сопряжённый активный транспорт. ПВ – питательное вещество, ПМ – продукт метаболизма. Активный транспорт любых веществ сопряжён с ионным транспортом. Различают:
В основе сопряжённого активного транспорта – наличие ионных градиентов, созданных насосами. Энергия АТФ тратится именно на создание градиентов, поэтому ионный активный транспорт называют первичным, сопряжённый – вторичным. Распространённый вид сопряжения – сопряжение на переносчике. При этом происходит пассивный перенос ионов натрия и активный перенос ПВ или ПМ. Переносчиками являются пермеазы – мембранные прошивающие белки, имеющие 2 центра связывания:
Схема: связывание с субстратом => изменение конформации => перенос (ионов натрия с ПВ – Симпорт, а с ПМ - антипорт) |
