электив по фармакологии. Фармакотерапия в восстановительной медицине
 Скачать 174.8 Kb. Скачать 174.8 Kb.
|
Лекарственная реабилитация (коррекция дислипидемий, возможных осложнений)Медикаментозное лечение дислипопротеинемий проводится в том случае, если строгая гиполипопротеинемическая диета, соблюдавшаяся не менее 6 месяцев, нормализация или снижение массы тела и физические нагрузки (тренировки) не приводят к адекватному снижению уровня липидов в крови. Для этого ориентируются на содержание в крови холестерина липопротеинов низкой плотности. Европейское общество по изучению атеросклероза рекомендует начинать одновременную медикаментозную терапию гиперхолестеринемии и диетотерапию при уровне холестерина в крови 250 мг/дл (6,5 ммоль/л). Задачей лечащих врачей является снижение уровня холестерина в плазме крови до 200 мг/дл (5,2 ммоль/л). Медикаментозная терапия дислипопротеинемий производится с учетом имеющегося у больного типа гиперлипидемии. Следует сказать, что нормальное или сниженное содержание в крови холестерина не является абсолютным показателем отсутствия активности атеросклеротического процесса в коронарных артериях. (См. табл. 1) Таблица 1. Нормальные значения показателей липидного спектра крови 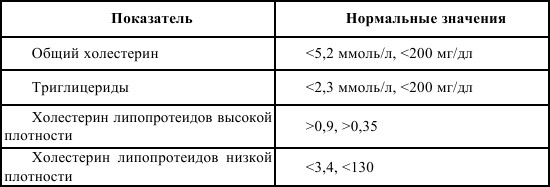 До начала медикаментозной терапии дислипопротеинемий необходимо определить содержание в крови холестерина, триглицеридов и произвести фенотипирование гиперлипопротеинемий. Учитывая необходимость коррекции дислипидемий, лекарственная реабилитация после перенесенного инфаркта миокарда проводится гипохолестеринемическими препаратами из группы статинов – симвастатин (зокор), правастатин (липостат), флувастатин (лескол), а также никотиновой кислотой, гемфиброзилом, пробурколом. Гиполипидемические (снижающие в крови уровень холестерина и триглицеридов) препараты в России включены в «Перечень жизненно необходимых и важнейших лекарственных средств». Классифицируется данная группа препаратов на пять групп: 1) ингибиторы 3-гидроксиметил-глютарил-коэнзим-А-редуктазы, или вастатины (или статины); 2) анионообменные смолы или секвестраты желчных кислот и средства, подавляющие абсорбцию холестерина в кишечнике; 3) никотиновая кислота и ее производные; 4) пробуркол; 5) фибраты, или производные фибровой кислоты. Гиполипидемические средства также подразделяются с учетом их основного механизма действия: 1) препараты, препятствующие образованию атерогенных липопротеинов; 2) препараты, тормозящие всасывание холестерина в кишечнике; 3) физиологические корректоры липидного обмена, содержащие эссенциальные фосфолипиды и ненасыщенные жирные кислоты, повышающие уровень липопротеинов высокой плотности. Все перечисленные препараты назначаются пациентам с повышенным содержанием в крови холестерина и триглицеридов (соответственно гиперлипидемией и гипертириглицеридемией) на длительный период. Препараты позволяют снизить риск возникновения повторных сердечных приступов и других сердечно-сосудистых событий, а в случае их возникновения уменьшают риск смерти в первый год после развития инфаркта миокарда. Механизм действия секвестратов желчных кислот заключается в следующем. Эти препараты, являясь анионообменными смолами, в кишечнике связываются с желчными кислотами, образуя с ними комплексы, и таким образом изолируют их (секвестрируют). Это приводит к затруднению обратного всасывания желчных кислот и увеличению выведения их с каловыми массами. Меньшее количество желчных кислот возвращается в печень, и возникает необходимость в образовании новых желчных кислот из холестерина. Соответственно увеличивается потребность в холестерине. Данная потребность обеспечивается увеличением синтеза холестерина в гепатоцитах и количества рецепторов, захватывающих из крови холестерин. Рецепторы и липопротеины низкой плотности, которые транспортируют холестерин, взаимодействуют друг с другом. Так происходит усиленное извлечение из крови холестерина, связанного с липопротеинами низкой плотности. Секвестраты не оказывают серьезных побочных действий и не всасываются из просвета кишечника в кровь. Препараты, замедляющие всасывание холестерина в кишечнике, уменьшают всасывание холестерина в кровь и, следовательно, снижают уровень холестерина в крови. К данным препаратам относятся диаспоний, или полиспонин, трибуспонин, гуарем. Полиспонин является сухим экстрактом из корней и корневищ диоско-реи ниппонской. В его состав входят водорастворимые стероидные сапонины, нарушающие всасывание холестерина из кишечника. Трибуспонин является препаратом, содержащим стероидные сапонины из травы якорцев стелющихся. Гипохолестеринемический эффект препарата выражен незначительно. Гуарем – препарат, являющийся естественной пищевой добавкой растительного происхождения. В его состав входят пищевые волокна, полученные из эндоспермы семян гиацинтовых бобов. Химической характеристикой данного вещества является его водорастворимость и то, что препарат является полисахаридом растительного происхождения. Гуаровые волокна при контакте с водой образуют вязкое желе, которое не всасывается из желудочно-кишечного тракта. Под влиянием кишечных бактерий гуаровые волокна распадаются на короткие цепочки жирных кислот. Все это задерживает опорожнение желудка и время прохождения пищи по желудочно-кишечному тракту, а также желеобразная масса снижает процессы абсорбции. Механизм гипохолестеринемического эффекта препарата гуа-рема объясняется следующим образом: гуарем снижает реабсорбцию холестерина путем удаления его молекул с поверхности слизистой оболочки кишечника; препарат связывает желчные кислоты в кишечнике, уменьшая обратное поступление желчных кислот в печень, тем самым стимулируя их синтез в гепатоцитах; далее увеличивается количество рецепторов липопротеинов низкой плотности на поверхности гепатоцитов, это приводит к повышению захвата холестерина из плазмы крови; препарат снижает аппетит и количество потребляемой пищи, следовательно, приводит к снижению массы тела. Выявлено и гипогликемическое действие гуарема, так как он уменьшает реабсорбцию углеводов в кишечнике. В процессе клинических исследований препарата установлены также побочные эффекты гуарема: метеоризм, боли в области кишечника, тошнота, редко – рвота или жидкий стул. Никотиновая кислота – водорастворимый витамин группы В, обладающий гиполипидемическим действием. Механизм ее действия заключается в подавлении мобилизации СЖК из жировой ткани, уменьшении образования в печени липопротеидов очень низкой плотности, снижении содержания в крови триглицеридов. Наряду с этим никотиновая кислота уменьшает образование и содержание в крови липопротеинов низкой плотности и холестерина. В отличие от других гиполипидемических средств никотиновая кислота снижает содержание в крови разновидности липопротеинов низкой плотности – липопротеина-а. Данный препарат активирует систему фибринолиза и увеличивает размер липопротеинов низкой плотности, что значительно затрудняет инфильтрирование их в интиму артерий. Никотиновая кислота повышает уровень холестерина липопротеинов высокой плотности (атиатерогенных липопротеинов), в том числе и при нормолипидемии; установлено, что этот эффект выражен больше, чем у всех других гиполипидемических средств. Применение никотиновой кислоты с секвестрантами желчных кислот способствует стабилизации и регрессии стенозов коронарных артерий. При терапии никотиновой кислотой могут наблюдаться побочные явления со стороны функции печени, желудка, у большинства больных в начале применения может наблюдаться гиперемия кожи, возможно развитие гипергликемии. Разработана новая пролонгированная форма никотиновой кислоты – эндурацин. Этот препарат хорошо всасывается из желудочно-кишечного тракта и почти не дает побочных эффектов. Эндурацин обладает гиполипидемическим и антиагрегатным действием, а также расширяет коронарные артерии. Пробуркол является эффективным гипохолестеринемическим средством, снижающим содержание в крови холестерина, но на уровень триглицеридов пробуркол практически не влияет. Пробуркол активирует нерецепторный путь удаления из крови липопротеинов низкой плотности соответственно холестерина; увеличивает содержание в крови протеина, переносящего эфиры холестерина, благодаря чему активируется «обратный» транспорт холестерина, т. е. перенос его из клеток органов и тканей в печень с последующим удалением его из организма. Выявлено его антиоксидантное действие, препарат уменьшает способность липопротеинов низкой плотности проникать в субэндотелиальный слой, окисляться. Фибраты – производные фибровой кислоты. К ним относятся гиполипидемические средства, оказывающие преимущественно гипотриглицеридемическое действие. Данная группа препаратов представлена гемфиброзилом, фенофибратом, безафибратом, кло-фибратом. В исследованиях установлено, что данные лекарственные вещества снижают уровень холестерина липопротеинов низкой плотности на 5-15 %. Гемфиброзил (лопид, гевилон) – фибрат II поколения, не только снижающий содержание в крови триглицеридов и в меньшей степени холестерина, но также повышающий уровень в крови холестерина ЛПВП. К сожалению, в Российскую Федерацию оригинальный гемфиброзил не поставляется, есть только его генерическая копия – изолипан. Показания к назначению гемфиброзила: 1) основное показание – уменьшение риска развития ИБС у лиц с ПБ типом гиперлипопротеинемии без признаков заболеваний коронарных артерий в настоящем или прошлом с триадой липидных нарушений: низкий холестерин, липопротеины низкой плотности, повышенный холестерин ЛПНП, высокий уровень триглицеридов в крови; 2) резкое увеличение содержания в крови триглицеридов (до 11,3 ммоль/л и более); 3) гиперлипопротеинемия III типа с увеличением содержания в крови липопротеинов промежуточной плотности, при этом в крови повышено содержание холестерина и триглицеридов; 4) гипертриглицеридемия и снижение содержания в крови холестерина ЛПВП у больных инсулиннезависимым сахарным диабетом. Гемфиброзил принимают за 30 мин до завтрака и ужина по 450–600 мг (суточная доза 900-1200 мг). Побочные действия гемфиброзила проявляются поражением мышц (повышенная чувствительность, боли, слабость в мышцах, повышение креатинкиназы в крови), в этом случае лечение следует прекратить; способностью усиливать камнеобразование в желчных путях; диспептическими расстройствами (тошнота, иногда рвота), болями в животе; ухудшением функции печени, при печеночной патологии гемфиброзил не применяется. В редких случаях возможно развитие лейкопении, тромбоцитопении, анемии. Безафибрат (безалип) – применяется значительно реже, чем гемфиброзил, так как уступает последнему по степени снижения триглицеридов в крови. Имеет те же показания, что и фенофибрат. Рекомендуемая суточная доза – 200 мг 3 раза в день, а при приеме пролонгированной формы – 400 мг один раз в день. У больных с любым типом гиперлипопротеидемии препарат повышает уровень холестерина ЛПВП, что отмечается как у больных с первичной гиперлипидемией, так и с вторичной, обусловленной сахарным диабетом или заболеванием почек. При длительном применении безафибрата (от 2 до 4 лет) отмечаются стабильные результаты, развития толерантности не наблюдается. По гиполипидемической эффективности препарат не уступает клофибрату, фенофибрату, а степень повышения уровня холестерина липопротеинов высокой плотности выше. Хорошо всасывается в желудочно-кишечном тракте. Побочные эффекты: в основном это желудочно-кишечные расстройства, реже – кожные реакции и др. Случаев гепатотоксичности за период клинического использования препарата не зарегистрировано, нет и доказательств более частого образования желчных камней у пациентов, длительно лечащихся безафибратом. Фенофибрат (липантил) – назначается по 100 мг три раза в день. Имеется пролонгированная форма препарата, принимаемая один раз в день. Установлено, что лечение фенофибратом позволяет добиться снижения содержания холестерина на 13 %. Препарат снижает также содержание триглицеридов в крови. Побочные действия те же, что у гемфиброзила. Положительная особенность его по сравнению с другими фибратами – снижение уровня мочевой кислоты на 10–28 %, что позволяет отдавать предпочтение фенофибрату при лечении больных с сочетанием гиперлипиде-мии и гиперурикемии. Кроме того, этот препарат наряду с ципро-фибратом наиболее эффективно снижает уровень триглицеридов в липопротеидах очень низкой плотности. Используется при всех типах гиперлипидемии за исключением I типа. Побочные эффекты наблюдаются нечасто (от 2 % до 15 % случаев). Это желудочно-кишечные расстройства (запоры или диарея), редко – кожные проявления (зуд, покраснение, сыпь), которые быстро самостоятельно проходят после отмены препарата. В единичных случаях отмечаются миалгия, сопровождавшаяся повышением уровня креатинфосфокиназы, импотенция, общая слабость, головная боль, головокружение, бессонница. В некоторых случаях повышается уровень трансаминаз в крови, в то время как содержание у-глутамилтранспептидазы и щелочной фосфатазы часто снижается. Есть данные о возрастающей литогенности желчи по сравнению с тем, что наблюдалось до лечения фенофибратом. До настоящего времени нет данных, свидетельствующих об увеличении частоты образования желчных камней на фоне терапии этим препаратом. Липантил 200М – микроионизированная капсульная форма фенофибрата, обладающая продленным действием. Препарат назначается один раз в сутки в дозе 200 мг во время вечернего приема пищи. Лечение может проводиться в течение нескольких месяцев. Препарат показан при 11А, 11В, III и IV типах гиперлипопротеинемии, особенно при выраженной гипертриглицеридемии, высоком уровне в крови холестерина ЛПНП. Клофибрат (мисклерон) – первый препарат из группы фибратов. Клофибрат активирует ли-попротеинлипазу и ускоряет метаболизм ЛПОНП и ЛППП, снижая их содержание в плазме крови. Влияние на уровень ЛПНП непостоянно. В настоящее время клофибрат практически не используется в связи с увеличением частоты образования камней в желчном пузыре, а также вследствие повышения смертности от внесердечных причин. В связи с выраженным побочным действием применяют клофибрат относительно редко. В основном препарат эффективен при III типе гиперлипопротеинемии. Назначается внутрь. Основными побочными эффектами являются тошнота, рвота, диарея, холелитиаз, мышечные боли, сердечные аритмии, кожные высыпания, импотенция. Ципрофибрат – фибрат III поколения, применяется в суточной дозе 100–200 мг. Обладает теми же побочными действиями, что и гемфиброзил. Таким образом, фибраты (производные фибровой кислоты) применяются при лечении очень высоких уровней триглицеридов в крови (IV тип гиперлипопротеинемии), для лечения больных семейной гиперлипопротеинемией III типа, при комбинированной гиперлипопротеинемии и у больных сахарным диабетом с повышенным уровнем триглицеридов в крови. Ингибиторы 3-гидрокси-3-метилглутарил-коэнзима-А-редуктазы (статины). Ингибиторы 3-гидрокси-глютарил-коэнзим-А-редуктазы (ГМК-КоА-редуктазы), или вастатины (статины). Статины являются наиболее активными гипохолестеринемическими средствами. Механизм действия: 1) установлено, что в процессе образования холестерина в клетке участвует фермент ГМГ-КоА-редуктаза. Статины блокируют активность этого фермента, что приводит к уменьшению образования холестерина; 2) снижение синтеза холестерина в гепатоцитах сопровождается увеличением синтеза большого количества рецепторов для липопротеинов низкой плотности, и происходит повышенное извлечение из крови и дальнейшее снижение уровня липопротеинов низкой плотности; 3) увеличение числа рецепторов липопротеина низкой плотности способствует снижению в крови уровня и их предшественников – ЛПОНП, что также способствует снижению и ЛПНП, и общего холестерина. Ловастатин (мевакор) – это неактивный лактон, выделенный из гриба Aspergillus terreus. В печени это лекарственное вещество превращается в активное соединение, которое захватывается гепатоцитами, и в них осуществляет свое ингибирующее влияние на фермент ГМГ-КоА-редуктазу, в результате чего снижается синтез холестерина и ЛПНП. В начале лечения препарат назначается по 20 мг один раз в сутки во время ужина. Однократный прием вечером более эффективен по сравнению с утренним приемом. Это объясняется тем, что холестерин синтезируется главным образом в ночные часы. Установлено, что снижение общего холестерина крови достигает 30 %, увеличивается уровень холестерина ЛПВП, уменьшается содержание в крови триглицеридов. Лечение ловастатином можно продолжать длительно (несколько месяцев и даже лет), так как препарат является достаточно безопасным. Симвастатин (зокор) – как и ловастатин, получен из грибов, является неактивным соединением, в печени превращается в активное вещество, ингибирующее ГМГ-КоА-редуктазу. Симвастатин применяется в суточной дозе 20–40 мг. Правастатин – является активной формой, оказывает антилипидемическое действие без предварительного метаболизма в печени. Является производным грибковых метаболитов. Суточная доза правастатина составляет 20–40 мг. Под влиянием лечения правастатином количество ХС ЛПНП снижается, уровень ХС ЛПВП повышается. Установлено замедление прогрессирования коронарного атеросклероза, положительное влияние на клиническое течение ишемической болезни сердца, инфаркта миокарда и уменьшение случаев смертности как от ИБС, так и «несердечной» смерти. Переносимость препарата хорошая. Лечение может продолжаться несколько месяцев и даже лет. Флувастатин (лескол) – новый, полностью синтетический ингибитор ГМГ-КоА-редуктазы. В отличие от ловастатина, симвастатина и правастатина, этот препарат не является производным грибковых метаболитов, основа его молекулы – индольное кольцо. Данный препарат – исходно активный препарат в отличие от других статинов. Флувастатин назначается в вечернее время в суточной дозе 20–40 мг; переносимость и эффективность его не зависят от времени приема пищи. Гиполипидемический эффект флувастатина развивается уже в течение первой недели, достигает максимума через 3–4 недели и сохраняется на достигнутом уровне при продолжении лечения. Аторвастатин является новым синтетическим ингибитором ГМГ-КоА-редуктазы с выраженным гипохолестеринемическим эффектом, а также препарат значительно снижает уровень триглицеридов. Применяется при гиперлипопротеинемии НА, ПБ, IV типов в дозе 5-10 мг/сут. Статины (вастатины) являются достаточно безопасными, хорошо переносимыми гиполипидемическими средствами. Однако иногда могут возникать побочные явления. Влияют на печень. Статины действуют избирательно в клетках печени. Поэтому примерно у 1 % больных возможно повышение содержания в крови АлАТ, обычно при применении больших доз препаратов. Вероятность поражения печени возрастает при сочетанном применении статинов и фибратов. Указанные изменения быстро проходят после прекращения приема препаратов. Влияют на мышечную ткань. У некоторых больных может наблюдаться боль в мышцах, мышечная слабость, повышение содержания в крови креатинфосфокиназы. Опасность поражения мышц возрастает при одновременном использовании статинов и фибра-тов. Желудочно-кишечные расстройства: тошнота, снижение аппетита, запоры, метеоризм. Могут наблюдаться расстройства сна, преимущественно при применении ловастатина и симвастина. При лечении правастатином возможна головная боль. Не выявлено отрицательного воздействия статинов на углеводный и пуриновый обмен, что позволяет активно применять эти средства при лечении гиперлипопротеинемии у больных сахарным диабетом, ожирением, подагрой, бессимптомной гиперурикемией. Главной характеристикой действия статинов является антиатерогенный эффект. Статины обладают множеством дополнительных свойств, не связанных с воздействием на уровень липидов. Большая их часть улучшает течение атеросклеротических заболеваний, участвует в быстром (в течение месяца) снижении смертности. Поэтому статины рекомендуются независимо от уровня липидемии всем больным с острым инфарктом миокарда. В основном эти свойства связаны с восстановлением нарушенной при атеросклерозе функции эндотелия коронарных артерий. Дополнительные эффекты в той или иной мере присущи всем статинам и, в меньшей степени, другим липидкорригирующим средствам. Гиполипидемические средства необходимо назначать с учетом типа гиперлипидемии, а также уровня в крови общего холестерина и триглицеридов. В некоторых случаях применяется комбинированная медикаментозная гиполипидемическая терапия. Комбинированная терапия проводится при ярко выраженной гиперхолестеринемии, в целях снижения уровня холестерина липопротеинов низкой плотности часто используют диетотерапию и два препарата, рекомендуют сочетание секвестрантов желчных кислот с никотиновой кислотой или ловастатином. При одновременном повышении уровня холестерина липопротеинов низкой плотности и триглицеридов рекомендуется сочетание секвестрантов желчных кислот с никотиновой кислотой или гемфиброзилом. К гиполипидемическим средствам относятся также бензафлавин, эссенциале и липостабил. Вензафлавин – производное рибофлавина-2,3,4,5-тетра-бензоил-5-ацетил-1,5-дигидрорибофлавина. Препарат повышает содержание в печени флавинов и восстанавливает энергетический обмен в митохондриях печени. Кроме того, бензафлавин понижает содержание в крови глюкозы, холестерина, триглицеридов, липопротеинов. Начало гиполипидемического действия препарата отмечается уже на 2-4-й день лечения. Вензафлавин назначается внутрь по 0,04-0,06 г 1–2 раза в день. Переносимость препарата хорошая, побочных эффектов нет, лечение продолжается несколько месяцев. Эссенциале является комплексным препаратом, содержащим эссенциальные фосфолипиды, ненасыщенные жирные кислоты, витамины В12, никотинамид, натрия пантотенат. Установлено, что препарат усиливает катаболизм холестерина. Наиболее эффективен при ИЛ и ИВ типах гиперлипопротеинемии. Назначают по две капсулы три раза в день в течение 2–3 месяцев 3–4 раза в год. Эссенциальные фосфолипиды улучшают способность липопротеинов высокой плотности извлекать из артерий и транспортировать холестерин, т. е. эссенциале повышает антиатероген-ные холестерин-акцепторные и холестерин-транспортные свойства липопротеинов высокой плотности. Липостабил – это препарат, близкий по механизму действия к эссенциале. Применяется для лечения гиперхолестеринемии и ги-пертриглицеридемии, но чаще при НА и ПБ типах гиперлипопротеинемии. Применяется внутрь в капсулах – 1–2 капсулы три раза в день в течение трех месяцев. Целесообразна в комплексном лечении больных атеросклерозом поливитаминотерапия, так как она способствует катаболизму атерогенных липопротеинов и улучшает метаболические процессы в миокарде, печени, головном мозге. Основными предпосылками для поливитаминотерапии при инфаркте миокарда являются следующие: 1) повышенная потребность в витаминах у больных атеросклерозом, ИБС; 2) снижение активности витаминсодержащих ферментов, что ведет к нарушению аэробного, анаэробного гликолиза, цикла Кребса с накоплением в организме пировиноградной и молочной кислот; 3) нарушение липидного обмена и белкового обмена, усиление перекисного окисления липидов; 4) снижение сократительной способности миокарда у больных ИБС. Поливитаминотерапия больных инфарктом миокарда проводится курсами по 1–2 месяца, которые повторяют 3–4 раза в год, особенно в сезоны дефицита витаминов в рационе больного. Применяются препараты «Ундевит», «Декамевит», «Олиговит», «Фор-тевит» и др. Витаминотерапия больных атеросклерозом должна проводиться с учетом межвитаминных взаимоотношений. Установлено, что моновитаминотерапия может проводиться только витаминами, не обладающими антагонистическим действием друг на друга. Такими витаминами являются В2, Н (биотин), С, пантотеновая кислота. Витаминотерапия при атеросклерозе должна применяться в виде сбалансированных поливитаминных комплексов, которые способствуют ассимиляции витаминов, обеспеченность которыми в организме снижена, нивелированию конкурентных отношений между витаминами и нормализации метаболических процессов. Максимальное терапевтическое действие витаминных комплексов достигается после 3-4-недельного курса лечения и сохраняется в течение 2–4 недель. Рекомендуется через 1,5–2 месяца проводить повторные курсы витаминотерапии. Лечение пароксизмальной желудочковой тахикардии Пароксизмальная желудочковая тахикардия встречается у 10 % больных инфарктом миокарда. Согласно В. Н. Захарову (1990 г.), с точки зрения терапевтической тактики, выделяют три типа пароксизмальной желудочковой тахикардии. 1-й тип – кратковременная (залп из 3–6 желудочковых экстрасистол). 2-й тип – длительная, без нарушения гемодинамики. 3-й тип – длительная, с признаками острой левожелудочковой недостаточности или аритмической формы кардиогенного шока. Медикаментозное купирование пароксизмальной желудочковой тахикардии производится при первом и втором типах. Н. М. Шевченко и А. А. Гросу (1992 г.) рекомендуют купировать пароксизмальную желудочковую тахикардию следующим образом. 1. Вводится внутривенно струйно в течение 1 мин 100 мг лидокаина (5 мл 2 %-ного раствора). Купирующий эффект лидокаина не превышает 30 %, однако имеются следующие преимущества лидокаина: быстрота и кратковременность действия, невысокая токсичность. 2. При отсутствии эффекта от лидокаина вводится внутривенно медленно новокаинамид в дозе 1 г (10 мл 10 %-ного раствора в 10 мл изотонического раствора натрия хлорида) в течение 5–6 мин под тщательным контролем артериального давления. Менее опасно внутривенное капельное введение 10 мл новокаинамида в 100 мл изотонического раствора натрия хлорида в течение 30–40 мин. В процессе введения новокаинамида возможно дополнительное введение болюсом лидокаина (2,5 мл 2 %-ного раствора), так как при сочетании лидокаина и новокаинамида антиаритмический эффект усиливается. Вместо новокаинамида вторым препаратом (т. е. препаратом второй очереди) может быть: 1) дизопирамид, или ритмилен, назначаются внутривенно в дозе 150 мг за 3 мин; 2) этмозин применяется внутривенно в дозе 150 мг за 3 мин (6 мл 2,5 %-ного раствора); 3) гилуритмал, или аймалин – в дозе 50 мг за 3 мин (2 мл 2,5 %-ного раствора). Купирующий эффект препаратов новокаинамида, дизопира-мида, этмозина, гилуритмала приблизительно одинаков. 3. При отсутствии желаемого клинического эффекта от препаратов первого и второго рядов следует применить кордарон в дозе 150–300 мг (3–6 мл 5 %-ного раствора в 20 мл изотонического раствора натрия хлорида внутривенно медленно в течение 5– 10 мин). 4. В некоторых случаях при отсутствии эффекта от применения вышеназванных препаратов можно вводить обзидан. Обзидан вводится внутривенно медленно в количестве 5-10 мг со скоростью 1 мг/мин (т. е. 5-10 мл 0,1 %-ного раствора в 10 мл изотонического раствора натрия хлорида со скоростью 2 мл/мин). Может быть эффективным внутривенное введение ритмонорма в дозе 20 мл (70 мг) в течение 5–6 мин. После купирования пароксизмальной желудочковой тахикардии с профилактической целью можно назначить внутрь новокаинамид в суточной дозе 3 г, кордарон – по 0,2 г 1 раз в день 5 дней в неделю, аймалин – 300 мг в сутки и др. Лечение при нарушениях атриовентрикулярной проводимости Атриовентрикулярная блокада I ст. (замедление атриовентрикулярной проводимости) возникает у 4-14 % больных инфарктом миокарда преимущественно задней стенки левого желудочка и обусловлена ишемией атриовентрикулярного соединения. Обычно атриовентрикулярная блокада I ст. имеет преходящий характер и благоприятный прогноз, а также не требует специального лечения. Следует учесть, что иногда замедление атриовентрикулярной проводимости может быть обусловлено лечением а-адреноблокаторами, сердечными гликозидами, верапамилом (финоптином, изоптином). После отмены этих препаратов атриовентрикулярная проводимость нормализуется. Атриовентрикулярная блокада II ст. I типа Мобитца (с периодами Венкебаха) возникает у 4-10 % больных инфарктом миокарда. Данный тип атриовентрикулярной блокады обусловлен ишемией атриовентрикулярного узла и чаще обнаруживается при диафрагмальном (нижнем) инфаркте миокарда, носит обычно преходящий характер, практически не влияет на прогноз и не требует специального лечения. Как правило, эта блокада проходит самостоятельно в течение 24–48 ч, но иногда может отмечаться в течение нескольких суток. Атриовентрикулярная блокада II ст. II типа Мобитца наблюдается менее чем у 1 % больных инфарктом миокарда, чаще всего при локализации в передней стенке левого желудочка. При этом замедление проводимости происходит в нижних отделах ствола пучка Гиса. Как правило, изменения носят необратимый характер. Этот тип блокады может сопровождаться выраженной брадикардией (при частом регулярном выпадении желудочковых комплексов), возможно внезапное развитие полной атриовентрикулярной блокады. Наиболее часто полная атриовентрикулярная блокада развивается у больных с удлиненным интервалом Р(5 в сочетании с полной блокадой левой ножки пучка Гиса или с блокадой правой и ветвей левой ножки пучка Гиса. Если атриовентрикулярная блокада II ст. II типа Мобитца характеризуется выраженной брадикардией и, в особенности, если она сочетается с передним инфарктом миокарда, блокадой ножки пучка Гиса, необходимо срочно производить трансвенозную эндокардиальную электрокардиостимуляцию (кардиостимулятором типа «деташЗ», т. е. функционирующего только при снижении ЧСС ниже определенной, фиксированной для данного пациента величины 50–70). При нижнем инфаркте миокарда с нерасширенными желудочковыми комплексами, нормальной ЧСС, отсутствием признаков недостаточного кровоснабжения жизненно важных органов электрокардиостимуляцию не проводят, но важным является нахождение больного под постоянным наблюдением. В случае замедления ЧСС, снижения АД, появления стенокардии и головокружений производится электрокардиостимуляция. Атриовентрикулярная блокада III ст. (полная атриовентрикулярная блокада) развивается в 5–8 % случаев при инфаркте миокарда. При поражении ветви правой коронарной артерии, снабжающей кровью атриовентрикулярный узел, полная атриовентрикулярная блокада сочетается с инфарктом миокарда задненижней стенки левого желудочка. При этом полной блокаде предшествует атриовентрикулярная блокада I ст. или блокада II ст. типа Мобитца, водитель ритма желудочков расположен в атриовентрикулярном узле. Приблизительно у 70 % больных ЧСС превышает 40 ударов в 1 мин, не возникают приступы Морганьи-Адамса– Стокса, комплексы С›К8 не расширены. Этот вид блокады может исчезнуть в течение нескольких дней. Летальность при этом варианте блокады составляет около 15 %. При поражении ветви левой коронарной артерии, которая снабжает кровью левожелудочковую перегородку, развивается инфаркт передней стенки левого желудочка и переднеперегородочной области. При этом полная атриовентрикулярная блокада возникает внезапно в первые сутки, ЧСС составляет менее 40 ударов в минуту, возникают приступы Морганьи-Адамса-Стокса, комплекс 01К8 расширен и деформирован (водитель ритма находится ниже бифуркации пучка Гиса). При этом типе блокады часто развивается тяжелая левожелудочковая недостаточность, возможен и кардиогенный шок. При полной атриовентрикулярной блокаде с широкими комплексами ОД8 у больных инфарктом миокарда передней стенки летальность достигает 80 % (А. Л. Сыркин, 1991 г.). При развитии полной атриовентрикулярной блокады в первые часы от начала инфаркта миокарда в ее происхождении может иметь значение высокий тонус блуждающего нерва (обычно это блокада с частотой сокращений желудочков более 40 в минуту, с узкими комплексами ОД8). Такая блокада, как правило, исчезает в первые несколько часов или суток. Лечение полной атриовентрикулярной блокады заключается в следующем. 1. Если при полной атриовентрикулярной блокаде число сокращений желудочков составляет 40–60 в минуту, нет нарушений гемодинамики и комплексы СЯК8 на ЭКГ не расширены, то специальное лечение не проводится. Этот вид блокады чаще наблюдается при задненижнем инфаркте миокарда и в некоторых случаях исчезает самостоятельно. 2. Если у больного имеется передний инфаркт миокарда с полной атриовентрикулярной блокадой с широкими комплексами С)К8 (водитель ритма расположен ниже бифуркации пучка Гиса), но число сокращений желудочков не менее 40 в минуту и нет нарушений гемодинамики, приступов Морганьи-Адамса-Стокса, необходимо только профилактическое введение эндокардиального электрода в полость правого желудочка без проведения кардиостимуляции. Целесообразность превентивного введения таким больным электрода и подключения кардиостимулятора, работающего «по требованию», объясняется возможностью внезапного ухудшения их состояния из-за уменьшения автоматизма желудочкового водителя ритма. Превентивное введение электрода при инфаркте миокарда бывает необходимо также в случае развития бифасцикулярной внутрижелудочковой блокады и сочетания внутрижелудочковой блокады с атриовентрикулярной блокадой I–II ст. 3. Основным методом лечения полной атриовентрикулярной блокады при инфаркте миокарда является эндокардиальная кардиостимуляция. Показаниями для проведения электрокардиостимуляции являются: редкий ритм желудочковых сокращений (менее 40 в минуту) при отсутствии эффекта от медикаментозной терапии; приступы Морганьи-Адамса-Стокса; появление признаков левожелудочковой недостаточности; артериальная гипотензия. 4. Медикаментозная терапия, направленная на ускорение ритма желудочков, проводится при появлении показаний для ускорения ритма желудочков (т. е. уменьшении числа сокращений желудочков менее 40–50 в минуту, артериальной гипотензии, при начальных проявлениях левожелудочковой недостаточности, приступах Морганьи-Адамса-Стокса), отсутствии возможности произвести эндокардиальную электростимуляцию, а также для ускорения ритма желудочков можно применять следующие лекарственные средства. Атропин – периферический М-холинолитик, понижает тонус блуждающего нерва, вводится внутривенно или подкожно в дозе 0,6–0,75 мл 0,1 %-ного раствора 3–4 раза в сутки. Эффект от лечения атропином наблюдается нечасто. Изадрин – стимулятор в-адренорецепторов миокарда, повышает активность идиовентрикулярного водителя ритма. Рекомендуется внутривенное капельное введение препарата (1 мг препарата растворяется в 250 мл 5 %-ного раствора глюкозы, вводится со скоростью 0,25 мл/мин). При отсутствии изадрина для внутривенного введения можно воспользоваться приемом изадрина в таблетках под язык (по 1 таблетке каждые 2 ч до учащения ритма желудочков). После достижения частоты сокращения желудочков 50–60 в минуту можно перейти к приему алупента внутрь в дозе 0,02 г каждые 6 ч. Алупент, или астмопент – стимулятор в-адренорецепторов, повышает активность идиовентрикулярного водителя ритма, вводится внутривенно по 1 мл 0,05 %-ного раствора в 20 мл изотонического раствора натрия хлорида 2–3 раза в день с последующим переходом на прием внутрь по 0,02 г каждые 4–6 ч. При лечении стимуляторами в-адренорецепторов необходимо контролировать уровень АД и ЭКГ (возможно появление желудочковой экстрасистолии). Дозу в-адреномиметиков необходимо подбирать так, чтобы не было экстрасистол или их количество не превышало 2 за 1 мин. Лечение при нарушениях внутрижелудочковой проводимости. Приблизительно у 15–20 % больных инфарктом миокарда развивается блокада ножек или ветвей левой ножки пучка Гиса. Полная блокада правой ножки пучка Гиса регистрируется у 2 % больных, но в 40–45 % случаев может перейти в полную атриовентрикулярную блокаду, при этом летальность может достигать 46 %. Полная блокада левой ножки пучка Гиса развивается у 2–5 % больных и в 20 % случаев может привести к развитию полной атриовентрикулярной блокады, сопровождается высокой летальностью (около 45 %). Блокада левой передней ветви наблюдается у 3–5 % больных инфарктом миокарда, а левой задней ветви – у 1–2 %. Изолированная блокада левой задней ветви пучка Гиса наблюдается обычно при обширном инфаркте миокарда и летальность при этом достигает 42 %. Блокада правой ножки в сочетании с блокадой задней левой ветви при инфаркте миокарда возникает в 1 % случаев, но часто прогрессирует в полную атриовентрикулярную блокаду (более чем в 40 % случаев), причем летальность может составить 57 %. Таким образом, блокады ножек пучка Гиса, а также ветвей левой ножки при инфаркте миокарда имеют серьезное прогностическое значение. Особенно плохой прогноз имеют двух– и трехпучковые блокады. Основным лечебным мероприятием при блокадах ножек пучка Гиса является профилактическая, или превентивная, электрокардиостимуляция. Изолированная блокада передней или задней ветви левой ножки пучка Гиса крайне редко осложняется полной атриовентрикулярной блокадой и поэтому не требует профилактической электрокардиостимуляции. Полная блокада правой или левой ножки пучка Гиса, а также блокада правой ножки в сочетании с блокадой передней или задней ветви левой ножки является показанием к профилактической установке электрокардиостимулятора. При трехпучковой блокаде лечебная тактика та же, что и при полной атриовентрикулярной блокаде. Чрезвычайно важным остается вопрос о показаниях к временной эндокардиальной электрокардиостимуляции при инфаркте миокарда. У некоторых больных, при наличии показаний, профилактически используются наружные кардиостимуляторы. Лечение хронической ишемической болезни сердца у пожилых пациентов очень часто сочетается с другой важной кардиологической проблемой – лечением сердечных аритмий. С одной стороны, сердечные аритмии в большинстве случаев возникает на фоне хронической ишемической болезни сердца, с другой, они оказывают существенное влияние на ее течение и прогноз, ухудшая их, в ряде случаев являясь непосредственной причиной смерти. Все это диктует необходимость их лечения. К сердечным аритмиям, требующим обязательного лечения, относят пароксизмальные тахикардии, желудочковые и суправентрикулярные, полную атриовентрикулярную блокаду, дисфункцию синусового узла с асистолией более 3–5 с. К прогностически неблагоприятным относят также частую пароксизмальную фибрилляцию предсердий, желудочковые экстрасистолии высоких градаций по классификации Лауна. Многолетние наблюдения ученых позволяют сделать вывод, что у пациентов пожилого возраста наиболее часто встречается фибрилляция предсердий, желудочковая экстрасистолия высоких градаций, синдром слабости синусового узла. Фибрилляция предсердий у большинства пациентов начинается с пароксизмов различной продолжительности и темпа сокращений предсердий. На ранних этапах желательно купировать пароксизмы фибрилляции предсердий, используя для этого различные противоаритмические препараты. В медицинской литературе даны рекомендации к их применению. Некоторые пациенты со временем начинают улавливать по ощущениям пароксизм фибрилляции предсердий и в первые же минуты принимают внутрь один из препаратов, самостоятельно купируя пароксизм. После восстановления синусового ритма целесообразно продолжение приема противоаритмического препарата для предупреждения возможного рецидива фибрилляции предсердий. В практике, как правило, используется препарат, купирующий пароксизм, а при его неэффективности – какой-либо другой. Наиболее часто применяются следующие препараты: амиодарон, пропафенон, атенолол, дизопирамид, хинидин. Доза препаратов, длительность противорецидивного курса лечения подбираются индивидуально, но у пожилых пациентов должны быть минимальными. Среди нарушений сердечного ритма, имеющих большое значение для врача общей практики, по контингенту лиц пожилого возраста является синдром слабости синусового узла, обозначаемый в литературе также терминами «болезнь синусового узла», «дисфункция синусового узла». На раннем этапе синдром слабости синусового узла проявляется эпизодами немотивированной общей слабости, головокружением. Позднее присоединяется прогрессирующая брадикардия, синдром «тахибради», пароксизм фибрилляции предсердий. Но основным симптомом являются эпизоды асистолии 3–5 с и более. Для подтверждения синдрома слабости синусового узла можно проводить пищеводную электростимуляцию предсердий. Но в практическом здравоохранении ограничиваются суточным мониторированием ЭКГ, во время которого выявляются эпизоды асистолии по удлинению интервала R-R. Многолетние попытки лечения синдрома слабости синусового узла лекарственными препаратами не давали желаемого результата, и больные умирали, как правило, от прогрессирующей сердечной недостаточности. Поэтому сегодня единственным эффективным методом лечения, улучшающим состояние и способствующим сохранению жизни больного, является постоянная электростимуляция сердца, причем целесообразно осуществлять ее как можно раньше. Никаких возрастных ограничений для имплантации электростимулятора нет, при этом пациенты могут вести активный образ жизни. Лечение тромбоэмболических осложнений Тромбоэмболические осложнения при инфаркте миокарда клинически диагностируются у 10 % больных, однако при аутопсии частота их выявления достигает 45 %, что свидетельствует о частом бессимптомном течении тромбоэмболий. Тромбоэмболические осложнения могут стать причиной смерти больных инфарктом миокарда. Одним из наиболее опасных для жизни тромбоэмболических осложнений является тромбоэмболия легочной артерии. При инфаркте миокарда могут наблюдаться также тромбоэмболии артерий большого круга кровообращения. Тромбоэмболия церебральных артерий может быть причиной инсульта, селезеночной артерии – инфаркта селезенки, почечной артерии, следствием этого является инфаркт почки. Возможна также тромбоэмболия артерий нижних конечностей. Около 30 % больных инфарктом миокарда с акинезией или дискинезией передневерхушечной зоны миокарда имеют внутри желудочковые тромбы. Однако большая часть тромбов остается неподвижной, поэтому эмболии в артерии большого круга наблюдаются редко. Лечение тромбоэмболических осложнений при инфаркте миокарда заключается, прежде всего, в гепаринотерапии. При отсутствии противопоказаний в течение 5–7 дней проводится лечение гепарином – вначале 10,000 ЕД внутривенно струйно, затем по 1000 ЕД/ч или по 5000–7000 ЕД каждые четыре часа под контролем частичного активированного тромбопластинового времени. Терапевтическая доза гепарина соответствует увеличению этого показателя в 1,5–2,5 раза по сравнению с исходным. В дальнейшем гепарин постепенно отменяют, за 3–5 дней до его отмены назначаются антикоагулянты непрямого действия, лечение которыми продолжается около трех месяцев под контролем протромбинового времени (при оптимальной дозе антикоагулянтов протромбиновый индекс должен быть в пределах 50–60 %). Однако в последние годы некоторые специалисты предлагают вместо непрямых антикоагулянтов применять длительно действующие антиагреганты (аспирин в малых антиагрегантных дозах, тиклопидин). При развитии тромбоэмболии артерий конечностей производят эмболэктомию, если позволяет общее состояние больного. Операция проводится под местной анестезией с использованием катетера Фогарта. |
