Реферат. Синез Фишера-Тропша. Реферат. Химизм процесса
 Скачать 0.96 Mb. Скачать 0.96 Mb.
|
|
Оглавление Введение…………………………………………………………………….3 1 Химизм процесса…………………………………………………………6 1.1 Основные реакции образования углеводородов……………………..6 1.2 Побочные реакции……………………………………………………...8 1.3 Механизм реакций……………………………………………………...9 2 Катализаторы……………………………………………………………12 3 Факторы, влияющие на процесс……………………………………….17 3.1 Качество сырья………………………………………………………..17 3.2 Температура…………………………………………………………...18 3.3 Давление…………………………………………………………….....19 3.4 Объемная скорость газа……………………………………………....20 4 Разновидности технологических схем………………………………...21 4.1 Схема с многотрубным реактором и стационарным слоем катализатора……………………………………………………………………...21 4.2 Схема с псевдоожиженным слоем катализатора…………………....23 4.3 Схема с циркулирующим взвешенным порошкообразным катализатором…………………………………………………………………....25 4.4 Схема с барботажным реактором…………………………………....26 5 Современные производства…………………………………………….29 5.1 Sasol 1, 2, 3. PetroSA…………………………………………………..29 5.2 Oryx…………………………………………………………………….30 5.3 SMDS…………………………………………………………………..31 5.4 Pearl…………………………………………………………………….31 5.5 Escravos………………………………………………………………...32 Заключение………………………………………………………………..34 Список использованных источников…………………………………....38 Введение История знает немало примеров, когда в силу острой необходимости рождались новые оригинальные подходы к решению давно существующих жизненно важных проблем. Так, в предвоенной Германии, лишенной доступа к нефтяным источникам, назревал жесткий дефицит топлива, необходимого для функционирования мощной военной техники. Располагая значительными запасами ископаемого угля, Германия была вынуждена искать пути его превращения в жидкое топливо. Эта проблема была успешно решена усилиями превосходных химиков, из которых, прежде всего, следует упомянуть Франца Фишера, директора Института кайзера Вильгельма по изучению угля. В 1926 году была опубликована работа Франца Фишера и Ганса Тропша «О прямом синтезе нефтяных углеводородов при обыкновенном давлении» [1]. В ней сообщалось, что при восстановлении водородом монооксида углерода при атмосферном давлении в присутствии различных катализаторов (железо-оксид цинка или кобальт-оксид хрома) при 270ºС получаются жидкие и даже твердые гомологи метана. Так возник знаменитый синтез углеводородов из монооксида углерода и водорода, называемый с тех пор синтезом Фишера-Тропша (ФТ). Смесь CO и H2 в различных соотношениях, называемая синтез-газом, может быть получена как из угля, так и из любого другого углеродсодержащего сырья. После изобретения процесса германскими исследователями было сделано множество усовершенствований и исправлений и название «Фишер-Тропш» сейчас применяется к большому количеству сходных процессов. Справедливости ради следует отметить, что синтез Фишера-Тропша возник не на пустом месте - к тому времени существовали научные предпосылки, которые базировались на достижениях органической химии и гетерогенного катализа. Еще в 1902 году П. Сабатье и Ж. Сандеран впервые получили метан из СО и H2. В 1908 году Е. Орлов открыл, что при пропускании монооксида углерода и водорода над катализатором, состоящим из никеля и палладия, нанесенных на уголь, образуется этилен [2]. Первый промышленный реактор был пущен в Германии в 1935 году, использовался Co-Th осажденный катализатор. В 1930-40-е годы на основе технологии Фишера-Тропша было налажено производство синтетического бензина (когазин-I, или синтин) с октановым числом 40÷55, синтетической высококачественной дизельной фракции (когазин-II) с цетановым числом 75÷100 и твердого парафина. Сырьем для процесса служил уголь, из которого газификацией получали синтез-газ, а из него углеводороды. Промышленность искусственного жидкого топлива достигла наибольшего подъема в годы второй мировой войны. К 1945 г. в мире имелось 15 заводов синтеза Фишера-Тропша (в Германии, США, Китае и Японии) общей мощностью около 1 млн. т углеводородов в год. Они выпускали в основном синтетические моторные топлива и смазочные масла. В Германии синтетическое топливо почти полностью покрывало потребности немецкой армии в авиационном бензине. Годовое производство синтетического топлива в этой стране достигло более 124 000 баррелей в день, т.е. около 6,5 миллионов тонн в 1944 году [3]. После 1945 года в связи с бурным развитием нефтедобычи и падением цен на нефть отпала необходимость синтеза жидких топлив из СО и Н2. Наступил нефтехимический бум. Однако в 1973 году разразился нефтяной кризис - нефтедобывающие страны ОПЕК (Organization of Petroleum Exporting Countries, Организация стран-экспортеров нефти) резко повысили цены на сырую нефть, и мировое сообщество вынуждено было осознать реальную угрозу истощения в обозримые сроки дешевых и доступных нефтяных ресурсов. Энергетический шок 70-х годов возродил интерес ученых и промышленников к использованию альтернативного нефти сырья, и здесь первое место, бесспорно, принадлежит углю. Мировые запасы угля огромны, они, по различным оценкам, более чем в 50 раз превосходят нефтяные ресурсы, и их может хватить на сотни лет [2]. Кроме этого, в мире имеется значительное количество источников углеводородных газов (как непосредственно залежи природного газа, так и попутный нефтяной газ), которые по тем или иным причинам не используются по экономическим причинам (значительная удаленность от потребителей и, как следствие, большие затраты на транспортировку в газообразном состоянии). Однако мировые запасы углеводородов иссякают, потребности в энергии растут, и в этих условиях расточительное использование углеводородов недопустимо, о чем свидетельствует неуклонный рост мировых цен на нефть с начала 21 века. В этих условиях синтез Фишера-Тропша снова приобретает актуальность. 1 Химизм процесса 1.1 Основные реакции образования углеводородов Суммарные реакции синтеза углеводородов из оксидов углерода и водорода в зависимости от катализатора и условий процесса можно представить разными уравнениями, но все они сводятся к двум основным [1]. Первая основная реакция - собственно синтез Фишера-Тропша: Вторая основная реакция - равновесие водяного газа. Этот процесс особенно легко протекает на железных катализаторах как вторичный: С учетом этой вторичной реакции для ФТ-синтеза на железных катализаторах получается суммарное уравнение: Реакции (1) и (3) при стехиометрическом, исчерпывающем превращении позволяют получить максимальный выход 208,5 г углеводородов на 1 м3 смеси CO + Н2 при образовании только олефинов. Реакция (2) может подавляться при низких температурах, малом времени контакта, циркуляции синтез-газа и удалении воды из циркулирующего газа, так что синтез может протекать частично по уравнению (1) с образованием воды и частично по уравнению (3) с образованием СO2. Из уравнения (1) при удвоенном превращении по уравнению (2) получается суммарное уравнение синтеза углеводородов из СО и Н2O по Кёльбелу-Энгельгардту: Стехиометрический выход равен 208,5 г [-СН2-] на 1 м3 смеси СО + Н2. Образование углеводородов из СО2 и Н2 обусловлено уравнением (1) и реакцией, обратной (2): Стехиометрический выход 156,25 г. [-СН2-] на 1 м3 смеси СO2 + Н2. В общем виде уравнения выглядят следующим образом: Для синтеза парафинов Для синтеза олефинов 1.2 Побочные реакции Нежелательными реакциями следует считать гидрирование СО в метан, разложение СО и окисление металла водой или диоксидом углерода. Метан образуется в присутствии кобальтовых и никелевых катализаторов: Стехиометрический выход 178,6 г СН4 на 1 м3 смеси СО + Н2. Вода, образующаяся при этом, конвертируется затем (особенно на железных катализаторах) в присутствии СО в смесь СО2 + Н2, поэтому суммарная реакция образования метана иная: Стехиометрический выход 178,6 г СН4 на 1 м3 смеси СО + Н2. При температурах выше 300°С метан образуется также при гидрировании СО2 по суммарному уравнению: Стехиометрический выход 142,9 г СН4 на 1 м3 смеси СO2 + H2. Процесс синтеза осложняется образованием углерода по реакции Будуара: ФТ-синтез может быть направлен в сторону преимущественного образования спиртов или альдегидов, которые при синтезе углеводородов образуются как побочные продукты. Основные уравнения в случае спиртов следующие а альдегиды образуются так: Уравнения для других продуктов, образующихся в небольшом количестве (кетоны, карбоновые кислоты, эфиры), опущены. 1.3 Механизм реакций В настоящее время рассматриваются три различных механизма реализации этого процесса. Первый механизм, называемый карбидным, впервые предложенный Фишером и Тропшем и в дальнейшем нашедший поддержку у других исследователей, предполагает образование С–С-связей в результате олигомеризации метиленовых фрагментов на поверхности катализатора. На первой стадии происходит адсорбция СО и образуется поверхностный карбид (соединения углерода с металлами, а также с бором и кремнием), а кислород превращается в воду или СО2 : 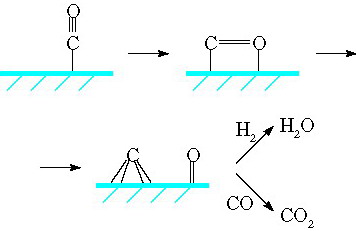 На второй стадии поверхностный карбид гидрируется с образованием фрагментов СНx (х = 1–3): 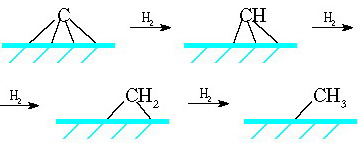 Удлинение цепи происходит в результате реакции поверхностных метила и метилена и далее путем внедрения метиленовых групп идет рост цепи: 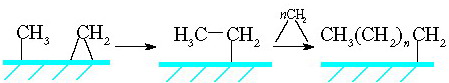 Стадия обрыва цепи происходит в результате десорбции алкена с поверхности катализатора: 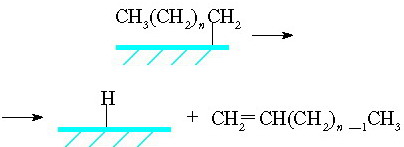 Второй механизм, названный гидроксикарбеновым, предполагает также гидрирование координированного на металле СО с образованием поверхностных гидроксикарбеновых фрагментов, в результате конденсации которых и происходит образование С–С–связей: 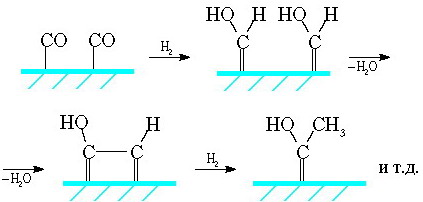 Третий механизм, который можно назвать механизмом внедрения, предполагает образование С–С–связей в результате внедрения СО по связи металл–углерод: 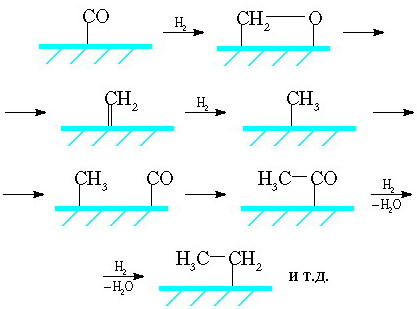 2 Катализаторы ФТ-синтез начинается с одновременной хемосорбции СО и Н2 на атомах металла. Для образования такой хемосорбционной связи особенно пригодны переходные металлы с 3d- и 4f-электронами или их соединения внедрения (карбиды, нитриды и т.д.). Катализаторами служат металлы VIII группы: наиболее активен Ru, затем Co, Fe, Ni. Для увеличения поверхности их часто наносят на пористые носители, например, силикагель и глинозем. В промышленности нашли применение только Fe и Co. Рутений слишком дорог, кроме того, его запасы на Земле слишком малы для использования в качестве катализатора в многотоннажных процессах. На никелевых катализаторах при атмосферном давлении образуется в основном метан, при повышении же давления никель образует летучий карбонил и вымывается из реактора [5]. Кобальтовые катализаторы были первыми катализаторами, используемыми в промышленности (в Германии, а затем во Франции и Японии в 1930-1940-е годы). Типичными для их работы являются давление 1÷50 атм и температура 180÷250°С. В этих условиях образуются, главным образом, линейные парафины. Кобальт обладает значительной гидрирующей активностью, поэтому часть СО неизбежно превращается в метан. Эта реакция резко ускоряется с повышением температуры, поэтому кобальтовые катализаторы не могут использоваться в высокотемпературном процессе ФТ. Железные катализаторы с середины 1950-х годов используются на заводах синтеза ФТ в ЮАР. По сравнению с кобальтовыми они гораздо более дешевы, работают в более широком интервале температур (200÷360°С), и позволяют получать более широкий спектр продуктов: парафины, низшие α-олефины, спирты. В условиях синтеза ФТ железо катализирует реакцию водяного газа, что позволяет эффективно использовать получаемый из угля синтез-газ, в котором соотношение СО: Н2 ниже стехиометрического 1: 2. Железные катализаторы имеют более низкое сродство к водороду по сравнению с кобальтовыми, поэтому метанирование не является для них большой проблемой. Однако в силу той же низкой гидрирующей активности поверхность железных контактов быстро зауглероживается. Кобальтовые контакты способны работать без регенерации значительно дольше. Еще одним недостатком железных контактов является их ингибирование водой. Поскольку вода является продуктом синтеза, конверсия СО за один проход невысока. Для достижения высокой степени превращения необходимо организовывать рецикл газа [6]. И железные, и кобальтовые катализаторы крайне чувствительны к отравлению серой. Поэтому синтез-газ должен быть предварительно очищен от серы, по крайней мере, до уровня 2 мг/м3 [7]. Остаточная сера адсорбируется поверхностью катализатора, так что в итоге продукты синтеза ФТ практически ее не содержат. Это обстоятельство делает синтетическое дизельное топливо, полученное по технологии ФТ, весьма привлекательным ввиду современных жестких экологических требований к транспорту. При воздействии различных агентов на свежеприготовленные катализаторы группы железа изменяется состав и структура катализаторов, появляются фазы, действительно активные в ФТ-синтезе. В то время как число таких фаз в случае кобальта и никеля относительно небольшое, для железа их много, поэтому каталитическая система усложняется. Железо образует с углеродом или другими металлоидами (азот, бор и т.д.) соединения внедрения различного состава, не утрачивая при этом «металлического» характера, необходимого для ФТ-сннтеза. Многие исследования подтвердили, что железные катализаторы в ходе ФТ-синтеза изменяются по фазовому составу, степени окисления и углеродным структурам внедрения. Железо восстановленного катализатора к началу синтеза переходит в карбид Fe2C (карбид Хэгга). Одновременно, но медленнее, образуется оксид Fe3O4, доля которого (в расчете на исходное железо) постоянно повышается, в то время как содержание карбида Fe2C в зависимости от времени работы и температуры меняется мало. Содержание свободного углерода возрастает с увеличением времени синтеза. В условиях эксплуатации фазовый состав катализатора находится в равновесии с составом реакционной смеси и только в малой степени зависит от способа его приготовления или предварительной обработки (восстановление, карбидирование) [1]. В работе Бартоломью показано, что на Co- и Ni - катализаторах СО гидрируется в метан по двум маршрутам, каждый из которых связан с определенными участками на поверхности [8]. А.Л. Лапидус с сотрудниками выдвинули двухцентровую модель Co-катализатора синтеза ФТ. Согласно этим представлениям, центрами первого типа являются кристаллиты металлического Со. На них СО адсорбируется диссоциативно и затем гидрируется в метан. На этих же центрах происходит реакция диспропорционирования CO, приводящая к зауглероживанию катализатора. Центры второго типа представляют собой границу между металлическим Со и оксидной фазой на поверхности катализатора. Они ответственны за рост углеводородной цепи. Оксид углерода адсорбируется на СоO в слабосвязанной ассоциативной форме, затем перемещается на носитель, где образует с водородом поверхностные комплексы типа CHxO. Эти комплексы взаимодействуют друг с другом, образуя полимерные структуры на поверхности. Их гидрирование на СоO дает углеводороды. Два типа адсорбции СО на поверхности обнаруживаются по спектру термопрограммированной десорбции (ТПД) СО, в котором центрам первого типа отвечает пик с Tmax в области 250-350°С, центрам второго - Tmax < 250°C. По соотношению площадей пиков можно судить о доле каждого из типов центров и, соответственно, предсказывать каталитическое действие контакта. Эксперименты показали хорошую корреляцию между выходом углеводородов и количеством центров слабосвязанной адсорбции СО на поверхности контакта [5]. Оксидная фаза Со-катализаторов обычно формируется в процессе их предварительной термообработки (прокаливания и / или восстановления) вследствие взаимодействия оксидного носителя (SiO2, Al2O3 и др.), оксида кобальта и промотора. Катализаторы, не содержащие оксидной фазы, не способны катализировать образование жидких углеводородов из СО и Н2, поскольку не имеют на своей поверхности центров полимеризации. Таким образом, оксидная фаза катализаторов синтеза ФТ играет определяющую роль в образовании жидких углеводородов, и для создания эффективных катализаторов этого процесса необходимо особое внимание уделять подбору носителя и проведению предварительной термообработки катализатора. Воздействуя на активную часть катализатора путем предварительной термообработки, приводящей к усилению взаимодействия активной фазы с носителем, или вводя в состав катализатора модифицирующие оксидные добавки, можно усилить полимеризационные свойства катализатора и, следовательно, увеличить селективность реакции в отношении образования жидких углеводородов. Промоторы по принципу действия подразделяются на две группы - структурные и энергетические. В качестве структурных промоторов используются трудно восстанавливаемые оксиды тяжелых металлов, например Аl2О3, ThO2, MgO и СаО. Они способствуют образованию развитой поверхности катализатора и препятствуют рекристаллизации каталитически активной фазы. Подобную функцию выполняют и носители - кизельгур, доломит, диоксид кремния (в форме свежеосажденного геля гидроксида или силиката калия). Энергетические промоторы, которые также называют химическими, электронными или активирующими добавками, согласно электронному механизму реакции, увеличивают ее скорость и влияют на селективность. В качестве энергетических промоторов могут действовать также химически активные структурные промоторы. Энергетические промоторы (особенно щелочи) значительно влияют и на текстуру катализатора (поверхность, распределение пор). В качестве энергетических промоторов для железных катализаторов (независимо от способа получения) чаще всего используют карбонаты щелочных металлов. Железным катализаторам, получаемым разными способами, соответствует неодинаковая оптимальная концентрация щелочной добавки. Осажденные катализаторы не должны содержать более 1% К2СО3 (в расчете на Fe); для определенных осажденных катализаторов оптимум составляет 0,2% К2СО3 (отклонение в 0,1% заметно влияет на активность и селективность). Для плавленых катализаторов указана оптимальная концентрация ≈ 0,5% К2О. К промоторам, обусловливающим и структурное, и энергетическое влияние, можно отнести медь. Медь облегчает восстановление железа, причем этот процесс в зависимости от количества меди может протекать при температуре, более низкой (вплоть до 150°С), чем без добавки. Далее эта добавка при сушке гидроксида железа (II и III) способствует окислению его до Fe2O3. Медь благоприятствует образованию соединений железа с углеродом и вместе со щелочью ускоряет восстановление железа, образование карбида и углерода. На селективность ФТ-синтеза медь не влияет [1]. |
