ВКР Сотина. Исследование фазовых эффектов и методов разделения азеотропных смесей, утверждена приказом ргу имени С. А. Есенина от 20 г
 Скачать 1.21 Mb. Скачать 1.21 Mb.
|
2.6.1. Ректификационный метод получения бутилацетата из метилацетата и бутанола-1Метод получения бутилацетата из метилацетата и бутанола-1 имеет широкое распространение по ряду причин. Бутилацетат является хорошим растворителем, который получают в промышленности этерификацией уксусной кислоты бутанолом-1. В России потребность в бутилацетате выше чем имеющиеся производственные мощности. Для сравнения, таким же высоким спросом пользуется уксусная кислота, которая идет на получение поливинилового спирта: 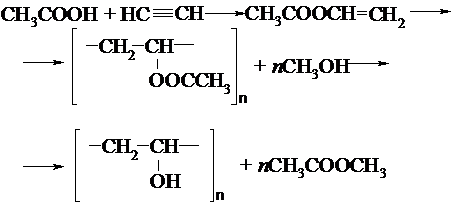 Метилацетат, получающийся при образовании поливинилового спирта, подвергается кислотному гидролизу: СН3СООСН3 + Н2О ↔ СН3СООН + СН3ОН Сформированные при гидролизе метанол и уксусная кислота успешно применяются на стадиях синтеза поливинилового спирта и винилацетата. Для их получения необходимы реагенты высокой химической чистоты, что напрямую влияет на качество полимеров. Восстановленные уксусная кислота и метанол могут содержать нежелательные микропримеси и по этой причине не вполне отвечают заданным требованиям. В таком случае наиболее эффективно прибегать к использованию восстановленной свежей уксусной кислоты. Более предпочтительным сырьем относительно уксусной кислоты для получения бутилацетата является метилацетат. Так как при использовании метилацетата скорость коррозии уменьшается, данная реакция протекает в более щадящих температурных условиях, потому что температура кипения метилацетата в два раза меньше температуры кипения уксусной кислоты при атмосферном давлении. Эти достоинства находят применение при осуществлении реакции в присутствии сильнокислотных ионообменников. Операция протекает при температурах, не снижающих стабильность ионитов, при этом коррозийная активность не увеличивается. В качестве катализатора данного процесса используется катионообменная смола. Таблица 6. Некоторые физико-химические свойства отдельных веществ и их смесей.
Данные, указанные в таблице 6, доказывают, что концентрационный симплекс, в этом случае представляющий собой тетраэдр, делиться на четыре участка непрерывной четкой ректификации (рис. 25). 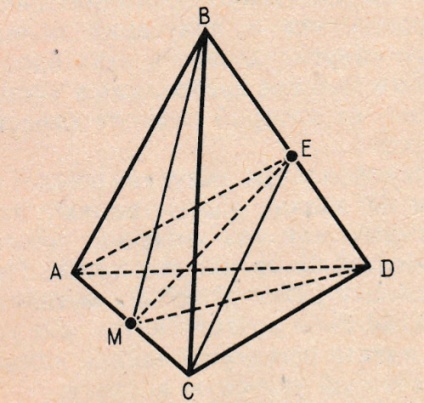 Рис. 25. Области ректификации четырехкомпонентной системы с двумя азеотропами. При повторном разделении как нижний продукт для областей AEDM и MEDC выделяется чистый бутилацетат, а в качестве нижнего образуются трехкомпонентные системы метилацетат-бутанол-бутилацетат, метанол-бутанол-бутилацетат, также может выделяться бинарная смесь бутанол-бутилацетат. Установление фазового равновесия жидкость-пар в рассматриваемой системе, дает возможность уточнить состояние разделяющей поверхности областей четкой ректификации АЕС. [12] Имеются два варианта построения процесса, которые соответствуют стационарным состояниям с максимальной степенью превращения реагентов. В первой реакции конверсия бутанола (рис. 26) равняется 100%, во втором (рис. 27) - степень превращения метилацетата также эквивалентна 100%. Равновесная степень превращения во второй реакции будет меньше. 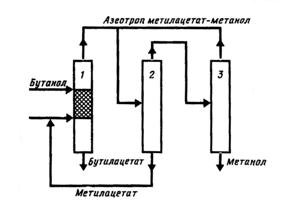 Рис. 26. Технологическая схема получения бутилацетата из метилацетата и бутанола: 1– совмещенный аппарат; 2 – колонна выделения метилацетата; 3 – колонна выделения метанола На рис. 26 показан метод разделения бинарной азеотропной смеси метилацетата с метанолом, проходящий в двухколонной установке (колонны 2 и 3). Во второй колонне обеспечивается постоянное повышенное давление, около 0,8105-1,0132 МПа. Процент метилацетата в азеотропе колеблется в пределах 45-47 %. При температуре 130 °С в колонне 2 происходит экстракция чистого метилацетата. Также следует отметить, что в присутствии катионов металлов активность катализатора снижается. Образование метанола происходит при обычном атмосферном давлении, однако при давлении немного ниже атмосферного, например, 0,0400 МПа, процесс оказывается экономически более выгодным. В таком случае, содержание метилацетата в азеотропе повышается с 62-64 % при атмосферном давлении до 70-72 % при пониженном. Это приводит к снижению затрат энергии на разделение, так как относительная летучесть компонентов смеси возрастает. Отмечу, что колонны 3 работают под вакуумом и в холодное время года, из-за того, что целостность конденсации сравнительно легко обеспечивается охлаждением промышленной оборотной водой. 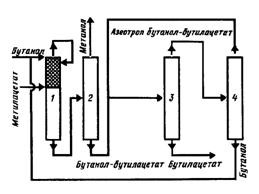 Рис. 27. Технологическая схема получения бутилацетата: 1 – реакционно-ректификационная колонна; 2 – колонна выделения метанола; 3– колонна выделения бутилацетата; 4 – колонна выделения бутанола. На рис. 27 изображена технологическая схема разделения бинарной азеотропной смеси бутилацетат - бутанол в двухколонной установке (колонны 3 и 4). В данном процессе, снижение давления приводит к обогащению азеотропа спиртом, а не эфиром, то есть прослеживается обратное смещение состава азеотропа. При давлении 0,0220 МПа в азеотропе имеется около 50% бутанола. Для указанного давления температура кипения азеотропа - 76,4 °С, соответственные значения для 0,0067 МПа - 37 % и 50,7 °С. Исходная смесь содержит 25 % бутанола при совмещенном процессе. При таких условиях степень превращения бутанола и метилацетата будет составлять 66 и 22 %, а в предельном стационарном состоянии 100 и 32 % соответственно. При раздельном процессе исходная смесь имеет 80,7% бутанола. В случае химического равновесия конверсии бутанола и метилацетата соответственно равны 17,2 и 72%. В условиях предельного стационарного состоянии эти значения составляют 23,9 и 100% соответственно. [33] Степень превращения реагентов за однократное пропускание смеси через аппарат намного ниже при несовмещенном процессе, чем в случае стационарного состояния. Таким образом можно сделать вывод, что принцип совмещения давно и с успехом применяется в промышленности. Использование совмещенных методов незаменимо при получении особо чистых веществ, разделении комплексных многокомпонентных смесей. Реакционно-массобменные технологии являются ключевым фактором для возникновения малоотходных технологий, так как предоставляют возможность повысить степень преобразования реагентов, увеличить селективность, а также уменьшить расход материалов и энергоемкость производства. [6]. |
