химия. производство метанола. Историческая справка
 Скачать 364.58 Kb. Скачать 364.58 Kb.
|
|
Историческая справка Впервые метанол был найден в древесном спирте в 1661 г., но лишь в 1834 г. был выделен из продуктов сухой перегонки древесины Думасом и Пелиготом. В это же время была установлена его химическая формула. До промышленного освоения каталитического способа метанол получали в основном сухой перегонкой древесины. Метанол, полученный этим способом, был загрязнен ацетоном и другими трудноотделимыми примесями. В настоящее время этот метод получения метанола практически не имеет промышленного значения. Способ, основанный на сухой перегонке древесины, до 1913 года оставался единственным освоенным процессом получения метанола, а в 1913 г. был разработан синтетический способ получения метанола из окиси углерода и водорода на цинк-хромовом катализаторе при давлении 250—350 кГс/см2. Позднее, в 1923 г. этот процесс был осуществлен в Германии в промышленном масштабе и в дальнейшем интенсивно развивался и совершенствовался. История развития отечественного промышленного синтеза метанола началась в 1934 г. на двух небольших агрегатах Новомосковского химического комбината совокупной мощностью около 30 тонн в сутки при давлении 25 МПа на Zn-Cr катализаторе. В соответствии с Директивами XXIV съезда КПСС об ускоренном развит и химической промышленности и расширении ассортимента химической продукции производство метанола росло бурными темпами. Выпуск метанола за указанный период значительно превышал темпы роста производства многих продуктов химической промышленности. Увеличение выпуска метанола проводилось путем интенсификации процесса, за счет расширения существующих и строительства новых производств. Каталитический синтез метанола из оксида углерода и водорода в настоящее время является практически единственным промышленным методом получения метанола, а все используемые в настоящее время процессы отличаются друг от друга вариантами технологических схем, целью которых является достижения максимальной эффективности использования ресурсов. Поиски других способов синтеза метанола продолжаются до сих пор, однако, ощутимых результатов они пока не дали. Одним из таким направлений можно назвать прямое окисление метана, однако, для экономической целесообразности этого процесса, доля метана, превращающегося в метанол, должна превышать по крайней мере 77%. Этот показатель достигался далеко не всегда, и сколь бы то ни было значимого промышленного применения он пока не нашел. Функциональная схема производства метанолаТехнологический процесс получения метанола из оксида углерода и водорода включает ряд операций, обязательных для любой технологической схемы синтеза. Газ предварительно очищается от карбонила железа, сернистых соединений, подогревается до температуры начала реакции и поступает в реактор синтеза метанола. По выходе из зоны катализа из газов выделяется образовавшийся метанол, что достигается охлаждением смеси, которая затем сжимается до давления синтеза и возвращается в процесс. Функциональная схема производства метанола приведена на рисунке 1.1 [1]. 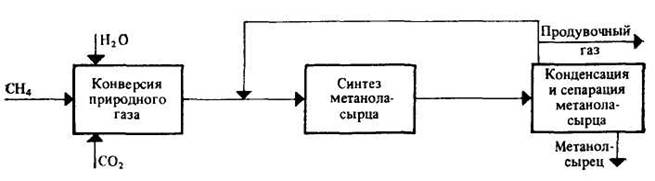 Функциональная схема производства метанола Функциональная схема производства метанолаФизико-химические основы процесса Синтез метанола основан на обратимых реакциях, описываемых уравнениями: CO + 2H2 CH3OH; DH = –90.8 кДж CO2 + 3H2 CH3OH + H2O; DH = –49.6 кДж Обе реакции экзотермичны и протекают с уменьшением объема. Из этого следует, что для достижения максимальных значений выхода метанола и степени превращения синтез-газа необходимо проведение процесса при низких температурах и высоких давлениях. Максимально достижимая степень превращения синтез-газа при этом ограничена условиями равновесия реакций получения метанола, которые изучены экспериментально и теоретически. На основании полученных практических данных можно при приближенных расчетах ограничится только первой реакцией, так как доля оксида углерода (IV) в исходной смеси незначительна. Для увеличения скорости реакции необходимо повышение температуры. При этом, выбирая оптимальный температурный режим, следует учитывать образование побочных соединений: метана, высших спиртов, кислот, альдегидов, кетонов и эфиров [1]. Эти реакции обусловливают бесполезный расход синтез-газа и удорожают очистку метанола. Применяемый для синтеза метанола катализатор должен обладать высокой селективностью, т. е. максимально ускорять образование метанола при одновременном подавлении побочных реакций. Катализаторы синтеза метанола Применяемый для синтеза метанола катализатор должен обладать высокой селективностью, т. е. максимально ускорять образование метанола при одновременном подавлении побочных реакций. Для синтеза метанола предложено много катализаторов. Лучшими оказались катализаторы, основными компонентами которых являются оксид цинка или медь (применяется при давлении 5,5 МПа) [1]. На первых крупнотоннажных установках процесс осуществлялся при давлении около 30 МПа на цинк-хромовом катализаторе. В последующие годы получили широкое распространение схемы синтеза при пониженном давлении на низкотемпературных медьсодержащих катализаторах. Катализаторы синтеза метанола весьма чувствительны к каталитическим ядам, поэтому первой стадией процесса является очистка газа от сернистых соединений. Сернистые соединения отравляют цинк-хромовые катализаторы обратимо, а медьсодержащие катализаторы – необратимо. Необходима также тщательная очистка газа от карбонила железа, который образуется в результате взаимодействия оксида углерода с железом аппаратуры. На катализаторе карбонил железа разлагается с выделением элементного железа, что способствует образованию метана. Режимные параметры процесса синтеза метанола Зависимость выхода метанола от температуры не линейна и имеет выраженный максимум. Кривая зависимости количества образовавшегося метанола от температуры проходит через экстремум при всех составах газа, причем максимальный выход метанола наблюдается при 255–270 °С. Интервал оптимальных температур, соответствующих наибольшему выходу продукта, определяется активностью катализатора, объемной скоростью газовой смеси и давлением. Процессы низкого давления (5–10 МПа) на медьсодержащих катализаторах осуществляют при температурах 220–280 °С. Для цинк-хромового катализатора характерны более высокие давления (20–30 МПа) и температуры (350–400 °С). Максимальное давление, применяемое в промышленных синтезах, составляет 40 МПа; выше этого давления ускоряются побочные реакции и, кроме того, увеличение затрат на компрессию газа ухудшает экономические показатели процесса. В синтезах низкого давления повышение давления ограничено термической стабильностью медных катализаторов. С возрастанием объемной скорости газа выход метанола падает. Это справедливо для синтеза как при высоком, так и при низком давлении. Такая закономерность основана на том, что с увеличением объемной скорости уменьшается время контакта газа с катализатором и, следовательно, концентрация метанола в газе, выходящем из реактора [1]. Состав газовой смеси существенно влияет на степень превращения сырья и производительность катализатора. В промышленных условиях всегда работают с некоторым избытком водорода; максимальная производительность наблюдается при молярном отношении Н2:СО = 4, на практике поддерживают отношение 2,15–2,25. Технологические схемы производства метанола Технологический процесс получения метанола из оксида углерода и водорода включает ряд операций, обязательных для любой технологической схемы синтеза. Газ предварительно очищается от карбонила железа, сернистых соединений, подогревается до температуры начала реакции и поступает в реактор синтеза метанола. По выходе из зоны катализа из газов выделяется образовавшийся метанол, что достигается охлаждением смеси, которая затем сжимается до давления синтеза и возвращается в процесс. Технологические схемы различаются аппаратурным оформлением главным образом стадии синтеза, включающей основной аппарат колонну синтеза и теплообменник. Ниже представлена схема агрегата синтеза метанола под давлением 5.5 МПа  Схема производства метанола при давлении 5 МПа Схема производства метанола при давлении 5 МПа1, 10 – турбокомпрессоры; 2 – подогреватель природного газа; 3 – реактор гидрирования сернистых соединений; 4 – адсорбер; 5 – трубчатый конвертор; 6 – котел-утилизатор; 7, 11, 12 – теплообменники; 8, 14 – холодильники (АВО); 9, 15 – сепараторы; 13 – колонна синтеза; 16 – сборник Природный газ сжимается турбокомпрессором 1 до давления 3 МПа, подогревается в подогревателе 2 за счет сжигания в межтрубном пространстве природного газа и направляется на сероочистку в аппараты 3 и 4, где последовательно осуществляется каталитическое гидрирование органических соединений серы и поглощение образующегося сероводорода адсорбентом на основе оксида цинка. После этого газ смешивается с водяным паром и диоксидом углерода в соотношении СН4 : Н2О : СО2 = 1 : 3,3 : 0,24. Смесь направляют в трубчатый конвертор 5, где на никелевом катализаторе происходит пароуглекислотная конверсия при 850-870 °С. Теплоту, необходимую для конверсии, получают в результате сжигания природного газа в специальных горелках. Конвертированный газ поступает в котел-утилизатор 6, где охлаждается до 280–290 °С. Затем теплоту газа используют в теплообменнике 7 для подогрева питательной воды, направляемой в котел-утилизатор. Пройдя воздушный холодильник 8 и сепаратор 9, газ охлаждается до 35-40 °С. Охлажденный конвертированный газ сжимают до 5 МПа в компрессоре 10, смешивают с циркуляционным газом и подают в теплообменники 11, 12, где он нагревается до 220–230 °С. Нагретая газовая смесь поступает в колонну синтеза 13, температурный режим в которой регулируют с помощью холодных байпасов. Теплоту реакционной смеси используют в теплообменниках 11, 12 для подогрева поступающего в колонну газа. Далее газовая смесь охлаждается в холодильнике-конденсаторе 14, сконденсировавшийся метанол-сырец отделяется в сепараторе 15 и поступает в сборник 16. Циркуляционный газ возвращают на синтез, продувочные и танковые газы передают на сжигание в трубчатую печь. Вследствие снижения температуры синтеза при низком давлении процесс осуществляется в условиях, близких к равновесию, что позволяет увеличить производительность агрегата. Конструкции реакторов синтеза метанола Колонна синтеза метанола, работающая в установке при высоком давлении, показана на рисунке.  Колонна синтеза метанола при высоком давлении Колонна синтеза метанола при высоком давлении1 – теплообменник; 2 – холодный байпас; 3 – электроподогреватель; 4 – катализатор Смешанный газ, пройдя кольцевой зазор между катализаторной коробкой и корпусом колонны, поступает в межтрубное пространство теплообменника, расположенного в нижней части колонны. В теплообменнике газ нагревается до 330–340 С и по центральной трубе, в которой размещен электроподогреватель, поступает в верхнюю часть колонны и проходит последовательно пять слоев катализатора. После каждого слоя катализатора, кроме последнего, в колонну вводят определенное количество холодного циркуляционного газа для поддержания необходимой температуры. После пятого слоя катализатора газ направляется в теплообменник, где охлаждается с 300–385 до 130 °С. Размещение теплообменника внутри корпуса колонны значительно снижает теплопотери в окружающую среду, что улучшает условия автотермичной работы агрегата, исключает наличие горячих трубопроводов, т. е. делает эксплуатацию более безопасной и снижает общие капиталовложения. Кроме того, за счет сокращения длины трубопроводов снижается сопротивление системы, что позволяет использовать турбо- циркуляционные компрессоры вместо поршневых. Конструкция и изготовление реакторов для проведения процесса при низком давлении проще благодаря более мягким условиям синтеза. При этом применяют реакторы как шахтные, так и трубчатые. В реакторах для синтеза при низком давлении особое внимание уделяют теплосъему, так как медьсодержащие катализаторы по сравнению с цинкхромовыми значительно более чувствительны к колебаниям температуры. Реактор, используемый при давлении синтеза 5,5 МПа показан на рисунке 1.2  Колонна синтеза метанола при низком давлении Колонна синтеза метанола при низком давлении1 – фарфоровые шары; 2 – катализатор В шахтных реакторах температурный режим регулируют с помощью байпасов, холодный газ вводят через специальные распределительные устройства. В трубчатых реакторах катализатор находится в трубках, охлаждаемых кипящей водой. Температуру катализатора поддерживают постоянной по всей длине реактора с помощью регуляторов давления, причем перегревы катализатора практически исключены. Выгрузка отработанного катализатора протекает тоже достаточно просто – путем снятия колосниковых решеток. Диаметр реакторов достигает 6 м при длине 8–16 м [1]. Проектируемый реактор синтеза метанола представляет собой вертикальный цилиндрический аппарат высотой около 18 метров и диаметром 3.2 м, установленный на опоре.  Конструкция реактора синтеза метанола Конструкция реактора синтеза метанола1 – днище; 2 – обечайка; 3 – штуцер; 4 – катализатор; 5 – патрубки; 6 – штуцер байпасного потока; 7 – штуцер выгрузки катализатора; 8 – штуцер выхода метанола; 9 – опора. Исходный газ подается в аппарат через штуцер в верхнем днище 1 и далее последовательно проходит через катализатор 4, на поверхности которого осуществляется синтез метанола. Продукты реакции выводятся через штуцер 8 снизу аппарата. Слой катализатора разделен на две секции по 3,5 м. Для байпасного потока предусмотрен штуцер 6, расположенный между слоями катализатора. Загрузка катализатора осуществляется через штуцер 3 на верхнюю полку. Нижняя полка соединена с верхней патрубками 5, через которые катализатор загружается на нижнюю полку. Выгрузка катализатора осуществляется через штуцер 7. Аппарат состоит из цилиндрической обечайки и двух эллиптических днищ. Внутри аппарата на двух опорных тарелках расположен слой катализатора, который закрывается сверху решетками. Верхнее днище является съемным и крепится к обечайке при помощи фланцевого соединения. Нижнее днище приваривается к обечайке. Для обслуживания внутренних устройств колонны над опорными тарелками размещены два люк-лаза. Аппарат установлен на цилиндрической опоре, в которой предусмотрены отверстия для штуцеров выгрузки насадки, вывода метанола и доступа внутрь опоры для обслуживания колонны. Вверху опоры есть небольшое отверстие для выхода газов, скапливающихся под колонной. Современные технологические тенденции Каталитический синтез метанола из оксида углерода и водорода является единственным промышленно значимым способом получения метанола. В качестве сырья в настоящее время во всех (или почти во всех) случаях выступает природный газ, однако, могли бы использоваться и другие виды водородосодержащего сырья – это коксующийся уголь, отходы нефтепереработки, газы производства ацетилена пиролизом природного газа и др. Сам процесс производства метанола можно разделить на три этапа. 1. На первом этапе проводится очистка газа от серы. Этот процесс называют гидродесульфуризацией. За ним следует поглощение выделившегося при гидродесульфуризации сероводорода цинковыми поглотителями. Очистка от серы необходима, т.к. сера является ядом для никелевых катализаторов конверсии природного газа. 2. На втором этапе осуществляется конверсия природного газа в синтез-газ (в основном паровая или пароуглекислотная). После охлаждения и конденсации водяных паров газ компримируют. 3. На третьем этапе осуществляется каталитический синтез метанола. Газ на выходе из реактора содержит 3-5% CH3OH, затем газ охлаждают и конденсируют продукты реакции, а оставшийся газ смешивают с исходным газом и направляют снова в реактор. Получаемый метанол-сырец содержит также воду (не более 9% по ТУ 113-05-323-77), этанол, пропанол, бутиловые и амиловые спирты, диметиловый эфир и др. 4. Если метанол-сырец не является товарным продуктом, то его подвергают ректификации, на первом этапе отделяя легколетучие фракции, на втором – от воды и высококипящих элементов. Обычно содержание воды в товарном метаноле не превышает 0,08%. Перечисленные стадии применимы ко всем (почти ко всем) типам производств, и общая схема процесса верна вне зависимости от технологических решений. На рисунке ниже представлена классическая схема производства метанола. Рис. 1. Классическая схема производства метанола  Представленная схема является классической. Рассмотрим технологические решения, предлагаемые основными мировыми лицензиаторами метанольных производств. Одной из главных мировых тенденций в производстве метанола является переход на мега-установки, которые в большом количестве стали строится в период 1990-2006 гг. За это время на Ближнем Востоке и в Латинской Америке появились 22 новых завода, суммарной мощностью почти 20 млн. тонн метанола в год. Мощность установок увеличилась с 1500 тонн в сутки до 5000 тонн. Одним из примеров такого рода производств служит завод в Тринидаде, построенный One Synergy Alliance (Johnson Matthey Catalysts and Davy Process Technology). На заводе действует установка М5000 и используется традиционный паровой риформинг метана. Метод повышения производительности установки парового риформинга без увеличения ее размеров заключается в использовании установки пред-риформинга. Это хорошо отработанная технология, впервые примененная компанией British Gas под названием процесса «Каталитического обогащения газа» при производстве бытового газа из лигроина в 1960-х гг. В компании Toyo Engineering создали схему «TAS –R», позволяющую увеличить силу реакции парового риформинга в адиабатических условиях с помощью разделения пред-риформера на два реактора и возврата технологического газа в конвекционную зону установки для промежуточного дополнительного нагревания (Рис.2). Рис. 2. Схема синтеза метанола «TAS –R», разработанная Toyo Engineering  Из-за очень большого размера традиционных установок парового риформинга, на мега-заводах были предприняты попытки найти им альтернативу. Компания One Synergy предложила альтернативную установку, известную как «Compact Reformer» («Компактный Риформер»), в которой теплота сгорания подается к каталитической трубе конвекцией, а не излучением. Она представляет собой вертикальный теплообменник, установленный на верху камеры сгорания. Некоторые лицензиаторы предлагают автотермический риформинг, в котором теплота обеспечивается за счет сгорания части технологического газа в адиабатическом реакторе вместо внешнего сжигания. АТР может действовать при более высоком давлении, чем обычная печь, что позволяет экономить на необходимости компрессии на следующих этапах процесса. Рис. 3. Схема синтеза метанола на основе автотермического риформинга, разработанная Topsøe 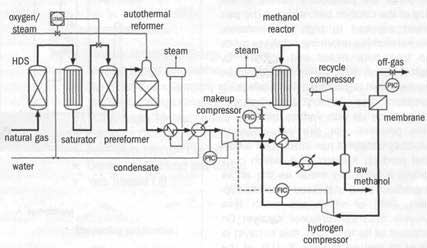 На рис.3 показан процесс производства метанола по Haldor Topsøe на основе АТР. В этой технологической схеме также используется пред-риформер. Процесс включает в себя следующие основные этапы: поступающий природный газ десульфурируется и насыщается паром. Затем технологический газ подвергается пред-риформингу и повторному нагреванию до 650ºС в печи прямого нагрева. Эта температура имеет большое значение, т.к. если подать технологический газ в установку АТР при более низкой температуре, потребление кислорода (около 0,6 т на 1 т метанола) увеличится. В установке АТР газ вступает в реакцию с паром и кислородом, в результате чего образуется крайне реактивный синтез-газ. На рис. 4 представлена схема комбинированного риформинга, предложенный Lurgi. Рис. 4. Схема комбинированного риформинга (Lurgi)  Модернизация реакторного блока также позволяет существенно увеличить производительность завода. В 1970-х гг. были популярны осевые реакторы. Современные реакторы, такие как ARC, разработанный Casale в сотрудничестве с ICI (ныне Johnson Matthey), а также реактор CMD, разработанный Haldor Topsøe, являются оптимизированными многослойными охлаждающими осевыми моделями, созданными для модернизации реакторами первых поколений. Существуют различные варианты реакторов такого типа. На рис. 5 представлен реактор MRF-Z (Toyo). В данном случае синтез-газ проникает через верхнюю часть реактора и проходит сквозь решетки вертикальных байонетных водных труб к центральной коллекторной трубе, выходя из сосуда через нижнее отверстие. Как и у всех центробежных реакторов, перепад давления очень низок. Использование байонетных труб позволяет избежать проблем, вызываемых тепловым напряжением, а также делает возможным свободный сток. Осмотр труб в процессе эксплуатации также несложен, поскольку внутренняя труба может выниматься из реактора. Мощность преобразователя MRF-Z можно увеличивать до очень больших величин (до 10 000 т/день) простым увеличением его высоты. Правда, естественная циркуляция питающей котел воды невозможна при таких масштабах, поэтому придется использовать циркуляционные насосы. Рис. 5. Реактор синтеза метанола MRF-Z, разработанный Toyo  В реакторе Lurgi с водяным охлаждением катализатор находится внутри труб, а вода – в межтрубном пространстве. Температура процесса контролируется регулировкой давления пара. Для очень крупных заводов компания Lurgi предусмотрела последовательное соединение реактора с водяным охлаждением и газоохлаждаемого реактора (Рис.1.5). Газ подогревается в газоохлаждаемом реакторе, а затем проходит в реактор с водяным охлаждением, где и происходит реакция. Нагретый технологический газ возвращается затем в реактор, охлаждаемый газом, где реакция заканчивается при менее интенсивных условиях. Рис. 6. Каскадная система реакторов для мега-установок (Lurgi)  Компания Methanol Casale, заключившая альянс с известной компанией по конструированию печей для риформинга Foster Wheeler, в начале нынешнего десятилетия представила свой реактор с водяным охлаждением. Коммерческий выпуск идет с 2002 г. Данный реактор отличается от других расположенными по радиусу вместо труб вертикальными пластинами – элементами теплообменника, призванных обеспечивать охлаждение (Рис.6). Сообщается, что такое устройство более эффективно и компактно, чем трубное охлаждение, сокращает количество катализатора и, следовательно, размер реактора, необходимого для достижения заданной производительности. Casale продолжили работу над данным типом реактора и недавно выпустили еще два изотермических реактора, доклад о которых будет зачитан на конференции Nitrogen & Syngas 2007 в Бахрейне в конце февраля. Разработчики технологических схем синтеза метанола, применяемых в России Институт «Химтехнология», г. Северодонецк, Украина Государственный научно-исследовательский и проектный институт химических технологий («Химтехнология») является комплексной организацией, включающей научно-исследовательское, проектное подразделения и опытный завод. Свою деятельность институт начал в 1950 г. как филиал Государственного научно-исследовательского и проектного института азотной промышленности (ГИАП). После принятия в 1958 г. постановления правительства о необходимости ускоренного развития химической промышленности и широкого внедрения химической продукции в народное хозяйство страны к 1967 г. он стал крупной комплексной организацией, работающей в области азотных удобрений и производств органического синтеза. В 1981 году институт стал самостоятельной организацией, а в настоящее время входит в холдинг «АЛВИГО». По проектам Института «Химтехнология» построены производства метанола: - на цинк-хромовых катализаторах под давлением синтеза 32 МПа г.Северодонецк (Украина), г.Новочеркасск (Россия), г.Новгород (Россия), г.Ионава (Литва) - на медьсодержащих катализаторах под давлением синтеза 5 МПа мощностью 100 тыс. тонн в год г.Северодонецк (Украина), г.Щекино (Россия), г.Новомосковск (Россия), г.Невинномысск (Россия) и 40 тыс тонн в год г.Харбин (Китай). Институт «Химтехнология» выполнял базовый и детальный проект на строительные работы, надзор за строительством и монтажом агрегатов мощностью 750 тыс. тонн в год в городах Томск и Губаха (Россия) по проекту ICI. Институт «Химтехнология» Выполняет разработку проектов реконструкции действующих производств метанола с целью снижения энергопотребления г.Ионава (Литва), г.Щекино (Россия), г.Новочеркасск (Россия). Также разработаны проекты производства метанола: - М-400 – мощностью 400 тыс. тонн в год. - КТЛМ-2500 – мощностью 825 тыс. тонн в год. Также разработана технология двустадийного синтеза метанола, которая при реконструкции действующих производств позволяет увеличить мощность производства почти в 1,5 раза и снижает энергопотребление на 15-20%. Кроме того, разработана совместная технология получения диметилового эфира (ДМЭ) с метанолом. В настоящее время она проходит опытную проверку. Такая технология сейчас особенно актуальна, так как ДМЭ сейчас всерьез рассматривается как альтернатива дизельному топливу. Более того, принятая Правительством Москвы программа предусматривает внедрение ДМЭ для автотранспорта Москвы к 2010 году, подразумевающая строительство производств ДМЭ. Однако на начальном этапе ДМЭ целесообразно получать на реконструированных установках синтеза метанола. Johnson Matthey (ICI) Процессы синтеза метанола, разработанные в свое время компанией Synetix, одним из подразделений компании ICI, которое в 2002 году приобрела компания Johnson Matthey, в мире являются наиболее распространенными. Их технология синтеза метанола при низком давлении (Low Pressure Methanol) используется более чем на 60% мировых производств (По данным компании Johnson Matthey Catalysts). По ее проектам было осуществлено строительство производств в Томске (1983 год) и Губахе (1984 год), где сейчас используются катализаторы этой компании. Помимо разработки технологических процессов компания Johnson Matthey Catalysts производит катализаторы для всех типов синтеза. Methanol Casale Компания образована в 1994 году и входит в группу компаний Casale. Штаб-квартира группы расположена в Швейцарии, а представительства компании расположены в 14 странах мира, в том числе и в России. Основная специализация компании – повышение эффективности (увеличение мощности и снижение потребления синтез-газа) имеющихся реакторов синтеза метанола и строительство новых. В сотрудничестве со специалистами компании ICI, таким образом, была проведена модернизация нескольких производств, в т.ч. на ОАО «Тольяттиазот». Также в сотрудничестве с Methanol Casale была проведена реконструкция цеха метанола на Невинномысском Азоте. Одним из последних достижений компании является разработка технологии конверсии производств аммиака для производства метанола или одновременного выпуска аммиака и метанола. |
