ДОКЛАД КАШАЕВ АНТОН. Изопроцессами. Если неизменным параметром является температура
 Скачать 72.25 Kb. Скачать 72.25 Kb.
|
|
СЛАЙД 1. ТИТУЛЬНЫЙ ЛИСТ Процессы, в которых масса идеального газа и один из параметров - давление, объем или температура - остается постоянным, а изменяются только остальные два, называют изопроцессами. Если неизменным параметром является температура, то соответствующий изопроцессназывается изотермическим, если объем - изохорным, а если давление - изобарным. Экспериментально законы для этих условий изменения состояния газа были открыты учеными физиками в XVII – XIX веках. Выбор темыпроекта определяется желанием и возможностью экспериментально с помощью лабораторного оборудования школьного кабинета физики воспроизвести эксперименты ученых и доказать справедливость газовых законов для реального газа – воздуха. Главной особенностью выбранной темы проекта является доступность оборудования и исследуемых материалов. СЛАЙД 2. Проблема проекта – экспериментальное исследование газовых законов различными способами, получение графических зависимостей: р(V) при изотермическом, р(Т) при изохорном, V(Т) при изобарных процессах на основании экспериментальных данных и доказательство справедливости газовых законов для реального газа – воздуха. Решив данную проблему, я получу конкретный образовательный результат: экспериментально исследую изотермический, изохорный и изобарный процессы различными способами и докажу справедливость газовых законов для реального газа - воздуха. Тема проекта актуальна, т.к. в разделе «Молекулярная физика и термодинамика» (10 класс) молекулярно – кинетической теории газа посвящена целая глава, а лабораторная работа предлагается только одна - по исследованию закона Бойля-Мариотта с помощью мензурки с водой, пробирки и измерительной ленты. При выполнении этой работы получается большая погрешность измерения не позволяющая доказать равенство р1V1=р2V2. Лабораторное оборудование школьного кабинета физики: набор для исследования изопроцессов в газах (автор изделия к.п.н. Степанов С.В., 2011 г.) и прибор для изучения газовых законов (ПГЗ-1, 1991 г.), напротив, позволяют с большой точностью провести проверку всех трех газовых законов. Цель проекта: решить проблему экспериментальной проверки разными способами справедливости газовых законов: Бойля-Мариотта, Шарля и Гей-Люссака. Достижение цели проекта позволит решить исходную проблему, т.к. полученные экспериментально данные при исследовании газовых законов различными способами позволят получить графические зависимости: р(V) при изотермическом, р(Т) при изохорном, V(Т) при изобарном процессах, согласующиеся с теоретическими данными параграфа учебника и доказать справедливость газовых законов для реального газа – воздуха. Проектные продукты - дидактический материал «Способы экспериментального исследования и проверки газовых законов» для школьного кабинета физики.Этот продукт поможет достичь цели проекта, т.к. будет содержать описание эксперимента по проверке справедливости каждого из законов: Бойля-Мариотта, Шарля и Гей-Люссака двумя способами, дающими одинаково верный результат. СЛАЙД 3. На достижение поставленной цели направлено решение следующих задач: 1. используя первоисточник – школьный учебник физики, сформировать представление о газовых законах; 2. выполнить эксперименты № 1-6 «Опытная проверка закона Бойля-Мариотта», «Опытная проверка закона Гей-Люссака», «Опытная проверка закона Шарля»; 3. сравнить полученные результаты, представить результаты измерений с помощью таблицы и графика; 4. сделать вывод о справедливости газовых законов для реального газа – воздуха; 5. познакомить одноклассников со способами исследования газовых законов, не описанных в учебнике, и результатами экспериментов. Новизной работы является совершенствование исследовательских навыков при проведении экспериментов различными способами, позволяющих получить одинаковые результаты, доказывающие справедливость газовых законов для реального газа – воздуха. СЛАЙД 4. ИССЛЕДОВАНИЕ ИЗОТЕРМИЧЕСКОГО ПРОЦЕССА Цель работы: экспериментально проверить соотношение между объемом и давлением газа определенной массы при его изотермическом расширении V1р1 = V2р2 в соответствии с законом Бойля-Мариотта. Оборудование: мановакуумметр, сифон для изучения свойств газов, резиновый шланг. Указания к работе. Объектом изучения является воздух, находящийся внутри сифона. В начале работы при закрытых кранах мановакуумметра сифон максимально сжат, его верхний торец устанавливается на уровне 4-го деления шкалы сифона. Открыв правый кран мановакуумметра, измеряют давление p1 (1 кг·с/см2 = 0,98066·105 Па) сжатого воздуха. Правый кран закрывают. Параметры воздуха в начальном состоянии: давление р1измеряется с помощью мановакуумметра, объем V1 равен объему внутренней полости сифона, температура Т соответствует температуре воздуха в помещении класса. Параметры воздуха при постепенном расширении: объемы V2-4 равны объемам внутренней полости сифона после его растягивания с помощью винта до уровня 5, 6, 7-го делений шкалы сифона. При этом для каждого нового объема воздуха фиксируется значение давлений p2-4, температура Т не изменится. Объем внутренней полости сифона определяется по формуле V = hS, т.к. поперечное сечение сифона одинаково по всей длине, объем воздуха удобно вычислять в условных единицах по длине воздушного столба с помощью шкалы. Завершив измерения, находят произведения h1р1,h2р2, h3p3, h4p4 сравнивая полученные значения, делают вывод о справедливости закона Бойля-Мариотта.  СЛАЙД 5. ИССЛЕДОВАНИЕ ИЗОБРАНОГО ПРОЦЕССА Цель работы: экспериментально проверить соотношение между объемом и температурой газа определенной массы при его изобарном нагревании V1/Т1 = V2/Т2 в соответствии с законом Гей-Люссака. Оборудование: мановакуумметр, сифон для изучения свойств газов, резиновый шланг, сосуд с кипящей водой на электрической плитке, лабораторный термометр. Объектом изучения является воздух, находящийся внутри сифона. В начале работы при открытых кранах мановакуумметра верхний торец сифона устанавливается на уровне 5-го деления шкалы. Закрыв краны, проверяют устанавливание стрелки мановакуумметра на отметке «0» (т.е. давление внутри сифона равно атмосферному давлению). Параметры воздуха в начальном состоянии: давление р равно атмосферному давлению, объем V1 равен объему внутренней полости сифона, температура Т1соответствует температуре воздуха в помещении класса. Сифон опускают в сосуд с водой комнатной температуры и ставят сосуд на электрическую плитку. При нагревании воды в сосуде и воздуха в сифоне его давление постепенно начинает увеличиваться. Помешивая воду в сосуде, измеряют ее температуру несколько раз, например, через каждые 20°С. Поворачивая винт, изменяют объем сифона, а следовательно, и объем воздуха таким образом, чтобы давление оставалось постоянным, т.е. равнялось атмосферному. Параметры воздуха при постепенном расширении: температура Т измеряется через каждые 20°С, объемы V равны объемам внутренней полости сифона после его растягивания с помощью винта, давление р поддерживается постоянным.Объем внутренней полости сифона определяется по формуле V = hS, т.к. поперечное сечение сифона одинаково по всей длине, объем воздуха удобно вычислять в условных единицах по длине воздушного столба с помощью шкалы. Завершив измерения, находят отношения V1/Т1, V2/Т2, V3/Т3, V4/Т4 сравнивая полученные значения, делают вывод о справедливости закона Гей-Люссака.  СЛАЙД 6. ИССЛЕДОВАНИЕ ИЗОХОРНОГО ПРОЦЕССА Цель работы: экспериментально проверить соотношение между давлением и температурой газа определенной массы при его изохорном нагревании р1/Т1 = р2/Т2 в соответствии с законом Шарля. Оборудование: мановакуумметр, сифон для изучения свойств газов, резиновый шланг, сосуд с кипящей водой на электрической плитке, лабораторный термометр. Объектом изучения является воздух, находящийся внутри сифона. В начале работы при открытых кранах мановакуумметра верхний торец сифона устанавливается на уровне 5-го деления шкалы. Закрыв краны, проверяют устанавливание стрелки мановакуумметра на отметке «0» (т.е. давление внутри сифона равно атмосферному давлению). Затем левый кран открывают. Параметры воздуха в начальном состоянии: давление р равно атмосферному давлению, температура Т1соответствует температуре воздуха в помещении класса. Сифон опускают в сосуд с водой комнатной температуры и ставят сосуд на электрическую плитку. При нагревании воды в сосуде и воздуха в сифоне его давление постепенно начинает увеличиваться. Помешивая воду в сосуде измеряют ее температуру несколько раз, например, через каждые 20°С. Поворачивая винт, изменяют объем сифона, а следовательно и объем воздуха таким образом, чтобы давление оставалось постоянным, т.е. равнялось атмосферному. Параметры воздуха при постепенном расширении: температура Т измеряется через каждые 20°С, давления р определяют по показаниям мановакуумметра, объем Vподдерживается постоянным.Объем внутренней полости сифона определяется по формуле V = hS, т.к. поперечное сечение сифона одинаково по всей длине, объем воздуха удобно вычислять в условных единицах по длине воздушного столба с помощью шкалы. Завершив измерения, находят отношения р1/Т1, р2/Т2, р3/Т3, р4/Т4 сравнивая полученные значения, делают вывод о справедливости закона Шарля.  СЛАЙД 7. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ ПРОЕКТА Результаты исследования изотермического процесса
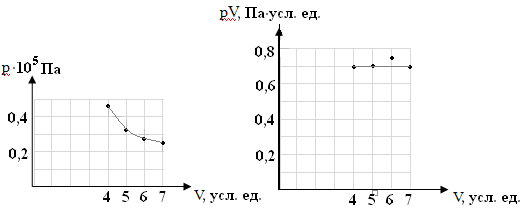 Вывод: подтвердили справедливость закона Бойля-Мариотта. Слайд 8. Результаты исследования изобарного процесса
6. Графики зависимости давления от объема  Вывод: подтвердили справедливость закона Гей-Люссака. Слайд 9. Результаты ихохорного процесса
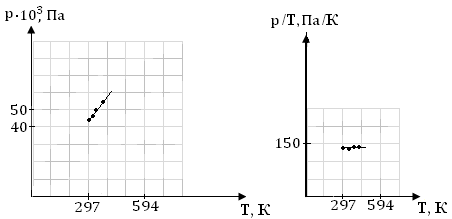 Вывод: подтвердили справедливость закона Шарля. Общий вывод по результатам эксперимента: газовые законы Бойля-Мариотта, Гей-Люссака и Шарля справедливы для реального газа – воздуха. Слайд 10. Закончив свой проект, я испытал удовлетворение от проделанной работы, поскольку все, что было задумано, получилось: мне удалось выбрать актуальную тему проекта, сформулировать проблему, касающуюся школьников, интересующихся физикой и желающих развить компетентность проводить эксперименты и оценивать полученные результаты. 2. По материалу учебника физики 10 класса изучены изопроцессы, происходящие с идеальным газом, газовые законы Бойля-Мариотта, Гей-Люссака и Шарля и графики зависимостей р(V), р(Т) и V(Т). 3. Изученные инструкции к проведению лабораторных работ для исследования газовых законов различными способами помогли определиться с оборудованием и порядком проведения экспериментов для решения задач проекта по достижению поставленной цели. 4. Проведенные эксперименты позволили решить проблему проекта – экспериментальное исследовать газовые законы различными способами, получить графические зависимости: р(V) при изотермическом, р(Т) при изохорном, V(Т) при изобарных процессах на основании экспериментальных данных и доказать справедливость газовых законов для реального газа – воздуха. 5. Цель проекта достигнута решением поставленных задач. |
