1. СРОП 247 группа Кабенов Куаныш. Кабенов Куаныш 247 группа
 Скачать 1.44 Mb. Скачать 1.44 Mb.
|
|
Билет 3 Кабенов Куаныш 247 группа. 1.Написать гексапептид с нейтральным зарядом, определить его ИЕТ, как изменится его заряд в кислой или в щелочной среде. 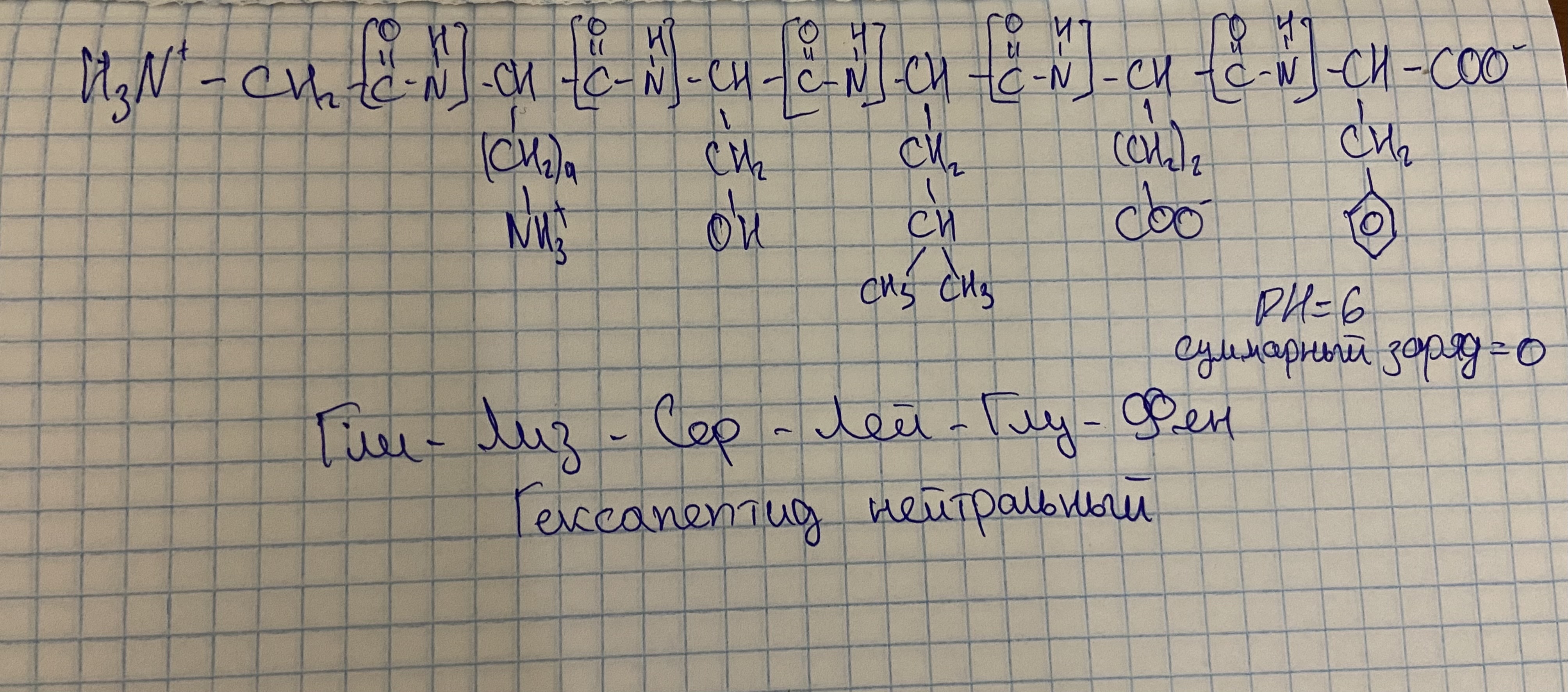 Гли-Лиз-Сер-Лей-Глу-Фен. Гексапептид нейтральный. Изменение pH в кислую сторону (повышение в сред конц. H+) приводит к подавлению диссоциации кислотных групп. В напротив увелечение конц OH- групп вызывает отщепление H+ от основных функциональных групп, что приводит к уменьшению положительного заряда. 2.Оптические свойства; коллоидность. Характеристика, примеры. Оптические свойства это (рассеивание света дифракция лучей эффект Тиндаля нефелометрия турбидиметрия). К оптическим свойствам коллоидов относятся: опалесценция, эффект Тиндаля и окраска. Эти свойства обусловлены явлениями рассеяния и поглощения света коллоидными частицами. Рассеяние падающего на золь света — это изменение направления распространения прошедшего через вещество излучения. Белки обладают коллоидными свойствами, образуя коллоидные растворы, т.к. их молекулы крупные и не могут проходить через полупроницаемые мембраны. Характерными признаками коллоидных свойств белковых растворов являются их своеобразный блеск и светорассеивание. Поскольку радиус молекулы белка больше, чем длина волны света, то имеет место дифракция света. На этих свойствах белка основаны методы диализа и ультрафильтрации, используемые для очистки белков от низкомолекулярных примесей. Для коллоидных систем хар-на интенсивное браувское движение частиц десперсной фазы. По степени взаимодействия между молекулами десперсионой фазы и среды:делятся на Лиофильные и Лиофобные. 3.Растворимость белковых молекул; гидратная оболочка. Характеристика, применение. Белки бывают растворимые и нерастворимые в воде. Растворимость белков зависит от их структуры, величины рН, солевого состава раствора, температуры и других факторов и определяется природой тех групп, которые находятся на поверхности белковой молекулы. К нерастворимым белкам относятся кератин (волосы, ногти, перья), коллаген (сухожилия), фиброин (щелк, паутина). Многие другие белки растворимы в воде. Растворимость определяется наличием на их поверхности заряженных и полярных группировок (-СОО-, -NH3+, -OH и др.). Заряженные и полярные группировки белков притягивают к себе молекулы воды, и вокруг них формируется гидратная оболочка, существование которой обусловливает их растворимость в воде.Так же на растворимость белка влияет наличие нейтральных солей (Na2SO4, (NH4)2SO4) в растворе. Гидратная оболочка это -окружение молекулы диполями воды и взаимодействие их с полярными и заряженными группами на поверхности глобулы белка. Чем больше полярных и/или заряженных аминокислот в белке, тем больше гидратная оболочка. Чем больше гидрофильных свойств у белковой молекулы, чем больше в ее составе и на ее поверхности аминокислот с полярными радикалами, тем сильнее выражена и прочнее удерживается гидратная оболочка и тем больше в ней слоев. Вода гидратной оболочки обладает особыми свойствами: она не является свободной, а связана с белковой молекулой. Это - “связанная” вода. Она принадлежит белку, и поэтому имеет особые свойства. |
