биохим экз 2,15,28,41 (1). Классификация по составу белковой молекулы
 Скачать 41.65 Kb. Скачать 41.65 Kb.
|
|
Классификация и биологические функции белков. Сложные белки. Структурная организация белков Классификация по составу белковой молекулы Белки по составу можно разделить на две группы: простые и сложные белки. Простые белки состоят только из аминокислотных остатков и не содержат других химических составляющих. Сложные белки, помимо полипептидных цепей, содержат другие химические компоненты. К простым белкам относятся РНКаза и многие другие ферменты. Фибриллярные белки коллаген, кератин, эластин по своему составу являются простыми. Запасные белки растений, содержащиеся в семенах злаков, – глютелины, и гистоны – белки, формирующие структуру хроматина, принадлежат также к простым белкам. Среди сложных белков различают металлопротеины, хромопротеины, фосфопротеины, гликопротеины, липопротеины и др. Металлопротеины К металлопротеинам относят белки, в составе которых имеются ионы металлов. В их молекулах встречаются такие металлы, как медь, железо, цинк, молибден, марганец и др. Некоторые ферменты по своей природе являются металлопротеинами Хромопротеины В составе хромопротеинов в качестве простетической группы присутствуют окрашенные соединения. Типичными хромопротеинами являются зрительный белок родопсин, принимающий участие в процессе восприятие света, и белок крови гемоглобин. Фосфопротеины Фосфопротеины в своем составе содержат остатки фосфорной кислоты, связанные с гидроксильной группой аминокислотных остатков сложноэфирной связью. Гликопротеины Гликопротеины содержат в качестве простетической группы ковалентно связанный углеводный компонент. Гликопротеины разделяют на истинные гликопротеины и протеогликаны. Углеводные группировки истинных гликопротеинов содержат обычно до 15 – 20 моносахаридных компонентов, у протеогликанов они построены из очень большого числа моносахаридных остатков. Классификация по функциям По выполняемым функциям белки можно разделить на структурные, питательные и запасные белки, сократительные, транспортные, каталитические, защитные, рецепторные, регуляторные и др. Структурные белки К структурным белкам относятся коллаген, эластин, кератин, фиброин. Белки принимают участие в формировании клеточных мембран, в частности, могут образовывать в них каналы или выполнять другие функции Питательные и запасные белки Питательным белком является казеин, основная функция которого заключается в обеспечении растущего организма аминокислотами, фосфором и кальцием. К запасным белкам относятся яичный белок, белки семян растений. Эти белки потребляются во время развития зародышей. В организме человека и животных белки в запас не откладываются, они должны систематически поступать с пищей, в противном случае может развиться дистрофия. Сократительные белки Сократительные белки обеспечивают работу мышц, движение жгутиков и ресничек у простейших, изменение формы клеток, перемещение органелл внутри клетки. Такими белками являются миозин и актин. Эти белки присутствуют не только в мышечных клетках, их можно обнаружить в клетках практически любой ткани животных. Транспортные белки Гемоглобин, рассмотренный в начале параграфа, является классическим примером транспортного белка. В крови присутствуют и другие белки, обеспечивающие транспорт липидов, гормонов и иных веществ. В клеточных мембранах находятся белки, способные переносить через мембрану глюкозу, аминокислоты, ионы и некоторые другие вещества Белки-ферменты Каталитические белки, или ферменты, представляют собой самую многообразную группу белков. Почти все химические реакции, протекающие в организме, протекают при участии ферментов. К настоящему времени открыто несколько тысяч ферментов. Более подробно они будут рассмотрены в следующих параграфах. Защитные белки К этой группе относятся белки, защищающие организм от вторжения других организмов или предохраняющие его от повреждений. Иммуноглобулины, или антитела, способны распознавать проникшие в организм бактерии, вирусы или чужеродные белки, связываться с ними и способствовать их обезвреживанию. Рецепторные белки Клеточная мембрана является препятствием для многих молекул, в том числе и для молекул, предназначенных для передачи сигнала внутрь клеток. Тем не менее клетка способна получать сигналы извне благодаря наличию на ее поверхности специальных рецепторов, многие из которых являются белками. Регуляторные белки Белки, участвующие в управлении биологическими процессами, относят к регуляторным белкам. К ним принадлежат некоторые гормоны. Инсулин и глюкагон регулируют уровень глюкозы в крови. Гормон роста, определяющий размеры тела, и паратиреоидный гормон, регулирующий обмен фосфатов и ионов кальция, являются регуляторными белками. К этому классу белков принадлежат и другие протеины, участвующие в регуляции обмена веществ. 15. Строение и функции гликогена. Биосинтез гликогена, его регуляция. Нарушения обмена гликогена. Гликогенозы и агликогенозы. Гликоген – резервный полисахарид животных тканей, в наибольшей мере содержится в печени и мышцах. Структурно он схож с амилопектином, но, во-первых, длина веточек меньше – 11-18 остатков глюкозы, во-вторых, более разветвлен – через каждые 8-10 остатков. За счет этих особенностей гликоген более компактно уложен, что немаловажно для животной клетки. СИНТЕЗ ГЛИКОГЕНА Синтез гликогена начинается с образования глюкозо-6-фосфата под действием глюкокиназы в печени или других гексокиназ в остальных тканях. Как уже говорилось, глюкокиназа обладает низким сродством к глюкозе, и в гепатоцитах глюкоза будет задерживаться только при ее высоких концентрациях. Непосредственно синтез гликогена осуществляют следующие ферменты: 1. Фосфоглюкомутаза – превращает глюкозо-6-фосфат в глюкозо-1-фосфат; 2. Глюкозо-1-фосфат-уридилтрансфераза – фермент, осуществляющий ключевую реакцию синтеза. Необратимость этой реакции обеспечивается гидролизом образующегося дифосфата; 3. Гликогенсинтаза – образует α-1,4-гликозидные связи и удлиняет гликогеновую цепочку, присоединяя активированный С1 УДФ-глюкозы к С4 концевых остатков гликогена; 4. Амило -1.4--1,6-гликозилтрансфераза, "гликоген-ветвящий" фермент – переносит фрагмент с минимальной длиной в 6 остатков глюкозы на соседнюю цепь с образованием- 1,6-гликозидной связи. РЕГУ ЛЯЦИЯ ОБМЕНА ГЛИКОГЕНА Метаболизм гликогена в печени регулируется несколькими гормонами, одни из которых активируют ферменты синтеза гликогена, а другие – ферменты распада гликогена. Основные ферменты метаболизма гликогена активны либо в фосфорилированной, либо в дефосфорилированной форме. Присоединение фосфатов к ферменту производят протеинкиназы, источником фосфора является АТФ: *фосфорилаза гликогена активируется после присоединения фосфатной группы, *синтаза гликогена после присоединения фосфата инактивируется. Скорость фосфорилирования указанных ферментов повышается после воздействия на клетку адреналина, глюкагона и некоторых других гормонов. В результате адреналин и глюкагон вызывают гликогенолиз, активируя фосфорилазу гликогена. Дефосфорилирование ферментов осуществляют протеинфосфатазы. Активатором протеинфосфатаз выступает инсулин. Вместе с этим, инсулин и глюкокортикоиды ускоряют синтез гликогена, увеличивая количество молекул гликогенсинтазы. В клетке осуществляется реципрокная (взаимоисключающая) регуляция. При работе клетки и/или гормональных влияниях активируется протеинкиназа и, как следствие, активируется фосфорилаза гликогена и ингибируется гликогенсинтаза. Идут реакции катаболизма глюкозы, и образуется энергия. При отдыхе или в покое работают протеин-фосфатазы, которые освобождают ферменты от фосфорной кислоты: в результате гликоген-фосфорилаза дефосфорилируется и становится не активной, активируется гликогенсинтаза. Начинается запасание глюкозы в виде гликогена. Для регуляции активности фосфорилазы и синтазы гликогена используется особый каскадный аденилатциклазный механизм. ГЛИКОГЕНОЗЫ В настоящее время гликогенозы делят по патогенетическому признаку на печеночные, мышечные и смешанные формы. Следует отметить, что при гликогенозах количество гликогена не всегда изменено, изменения могут быть только в структуре его молекулы. Печеночные гликогенозы Самый частый гликогеноз I типа или болезнь фон Гирке обусловлен аутосомнорецессивным дефектом глюкозо-6-фосфатазы. Из-за того, что этот фермент есть только в печени и почках, преимущественно страдают эти органы, и болезнь носит еще одно название – гепаторенальный гликогеноз. Даже у новорожденных детей наблюдаются гепатомегалия и нефромегалия, обусловленные накоплением гликогена не только в цитоплазме, но и в ядрах клеток. Кроме этого, активируется синтез липидов с возникновением стеатоза печени. Так как фермент необходим для дефосфорилирования глюкозо-6-фосфата с последующим выходом глюкозы в кровь, у больных отмечается гипогликемия, и, как следствие, ацетонемия, метаболический ацидоз, ацетонурия. Гликогеноз III типа или болезнь Форбса-Кори или лимит-декстриноз – это аутосомно-рецессивный дефект амило-α-1,6-глюкозидазы, "деветвящего" фермента, гидролизующего α-1,6-гликозидную связь. Болезнь имеет более доброкачественное течение, и частота ее составляет примерно 25% от всех гликогенозов. Для больных характерна гепатомегалия, умеренная задержка физического развития, в подростковом возрасте возможна небольшая миопатия. Строение и обмен углеводов 198 Еще два печеночных гликогеноза – гликогеноз IV типа (болезнь Андерсена), связанный с дефектом ветвящего фермента и гликогеноз VI типа (болезнь Херса), связанный с дефицитом печеночной фосфорилазы гликогена встречаются довольно редко. Мышечные гликогенозы Для этой группы гликогенозов характерны изменения ферментов мышечной ткани. Это приводит к нарушению энергообеспечения мышц при физической нагрузке, к болям в мышцах, судорогам. Гликогеноз V типа (болезнь Мак-Ардля) – отсутствие мышечной фосфорилазы. При тяжелой мышечной нагрузке возникают судороги, миоглобинурия, хотя легкая работа не вызывает каких-либо проблем. Смешанные гликогенозы Эти заболевания касаются и печени, и мышц, и других органов. Гликогеноз II типа (болезнь Помпе) – поражаются все гликогенсодержащие клетки из-за отсутствия лизосомальной α-1,4-глюкозидазы. Происходит накопление гликогена в лизосомах и в цитоплазме. Заболевание составляет почти 10% всех гликогенозов и является наиболее злокачественным. Больные умирают в грудном возрасте из-за кардиомегалии и тяжелой сердечной недостаточности. АГЛИКОГЕНОЗЫ Агликогенозы – состояния, связанные с отсутствием гликогена. В качестве примера агликогеноза можно привести наследственный аутосомнорецессивный дефицит гликоген-синтазы. Симптомами является резкая гипогликемия натощак, особенно утром, появляется рвота, судороги, потеря сознания. В результате гипогликемии наблюдается задержка психомоторного развития, умственная отсталость. Болезнь несмертельна при адекватном лечении (частое кормление), хотя и опасна. 28. Пути обезвреживания аммиака: амидирование, восстановительное аминирование, аммониогенез. Обезвреживание в обмене аминокислот.Обезвреживаниебиогенных аминов. Трансаминирование является этапом как катаболизма (распада), так синтеза аминокислот Трансаминирование – заключительный этап синтеза заменимых АК из соответствующих кетокислот. Трансаминирование – первая стадия дезаминирования большинства аминокислот, т.е. начальный этап их катаболизма. Образующиеся при этом кетокислоты окисляются в ЦТК или используются для синтеза глюкозы и кетоновых тел. В результате дезаминирования аминокислот образуется аммиак, который является клеточным ядом, при высоких концентрациях он повреждает главным образом нервные клетки. Поэтому аммиак должен быстро инактивироваться и выводиться из организма. У разных видов позвоночных обезвреживание и выведение аммиака производится различными способами. 1. Образование глутамина - процесс идев в мозге, сетчатке, почках, печени и мышцах. 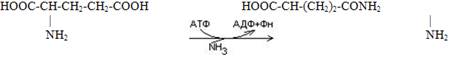 Глутамин выделяется с мочой. 2. Восстановительное аминирование -кетоглутаровой кислоты -кетоглутарат+NH3 + НАДН глутамат + НАД+ Эта реакция обратная окислительному дезаминированию глутяминовой кислоты. Дальше глутамат связывает еще одну молекулу NH3 и дают глутамин. Глу+NH3 Глн. Глутамин используется почками как резервный источник аммиака, необходимый для нейтрализации кислых продуктов обмена при ацидозе. 3. Образование аммонийных солей. Аммиак в почках акцептирует протон кислоты, образуя аммонийную соль. Одновременно этот процесс обеспечивает сбережение организмом ионов Na+, которые в отсутствие ионов аммония выводились бы с анионами кислот. NH3+Н+Cl- NH4C 4. Биосинтез мочевины. Мочевина - главный конечный продукт обмена азота в организме. С мочой за сутки выводится 25-30 г мочевины. Синтез мочевины идет в печени. Превращение аммиака в мочевину осуществляется в форме цикла. Пернвая аминогруппа, поступающая в цикл мочевины, получается в виде свободного аммиака при окислительном дезаминировании глутамата в митохондриях клеток печени. Эта рекция катализируется глутаматдегидрогеназой, для действия которой требуется НАД+ Глутамат+НАД++Н2О-кетоглутарат + +НАДН+Н+. Аммиак соединяется с двуокисью углерода с образованием карбомоилфосфата. Реакция требует затраты АТФ. Катализирует эту реакцию карбомоилфосфатсинтетаза. На следующей стадии карбомоилфосфат взаимодействует с орнитином с образованием цитрулина. Образовавшийся цитрулин переходит из митохондрий в цитозоль клеток печени. Цитрулин взаимодействует с аспартатом в присутствии АТФ с образованием аргининсукцината. Эта реакция катализируется аргининсукцинатсинтетазой. На следующей стадии аргининсукцинат расщепляется с образованием аргинина и фумарата. Фумарат возвращается в пул промежуточных продуктов цикла лимонной кислоты. На последней стадии аргинин под действием аргиназы расщепляется на мочевину и орнитин. Синтез заменимых аминокислот 1. Аминирование 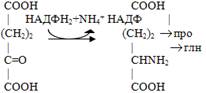 2. Переаминирование 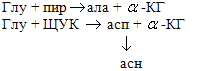 Глюсергли 41. Глюкокортикоиды, влияние на метаболизм. Гипо- и гиперфункции коры надпочечников. Стероидный диабет ГОРМОНЫ КОРЫ НАДПОЧЕЧНИКОВ В коре надпочечников образуются из холестерина стероидные гормоны: кортикостероиды (глюкокортикоиды и минералокортикоиды) и половые гомоны (женские и мужские). ГЛЮКОКОРТИКОИДЫ Представителями глюкокортикоидов являются гидрокортизон (кортизол, кортизон и кортикостерон Ткани-мишени для этой группы гормонов: печень, мышцы, жировая, лимфоидная и соединительная ткани. Причем в печени глюкокортикоиды повышают проницаемость мембран для транспорта веществ в клетку и активируют анаболические процессы (то есть синтез веществ), а в остальных тканях – понижают проницаемость мембран и стимулируют катаболизм (то есть распад веществ). Действие глюкокортикоидов на метаболизм Углеводный обмен. Во всех тканях-мишенях глюкокортикоиды тормозят гликолиз. В печени гормоны усиливают глюконеогенез и синтез гликогена, в остальных тканях – уменьшают транспорт глюкозы в клетку, в мышцах – снижают синтез гликогена. При избытке глюкокортикоидов (применение их для лечения в больших дозах или длительно, а также повышенное образование глюкокортикоидов в организме) развивается гипергликемия вследствие активации глюконеогенеза в печени и понижения утилизации глюкозы в периферических тканях. Длительная гипергликемия может привести к срыву инсулярного аппарата поджелудочной железы и развитию стероидного диабета -Липидный обмен. В печени глюкокортикоиды повышают синтез триглицеридов, липопротеинов очень низкой плотности (ЛПОНП) и кетоновых тел. В жировой ткани гормоны увеличивают распад жира на конечностях, но усиливают отложение жира на туловище и лице. Поэтому при избытке глюкокортикоидов наблюдается так называемое паукообразное ожирение и повышение уровня кетоновых тел в крови. - Белковый обмен. В печени глюкокортикоиды увеличивают синтез белка, в остальных тканях – снижают синтез и стимулируют распад тканевых белков. В связи с этим при избытке глюкокортикоидов наблюдаются замедление заживления ран, атрофия и слабость мышц, в костях – остеопороз (разрежение кости, что сопровождается легко возникающими переломами, например, компрессионными переломами позвонков и длинных костей уже при минимальной травме). В лимфоидной ткани избыток глюкокортикоидов приводит к угнетению синтеза антител и уменьшению образования лимфоцитов, поэтому при стрессе (когда вырабатывается много глюкокортикоидов) снижается иммунная защита организма и повышается восприимчивость к инфекционным заболеваниям. Указанный механизм действия глюкокортикоидов на лимфоидную ткань лежит в основе их применения при лечении аллергии и при трансплантации для подавления реакции отторжения пересаженного органа |
