КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ АНТИОКСИДАНТОВ. Клиническая фармакология антиоксидантов
 Скачать 3.89 Mb. Скачать 3.89 Mb.
|
|
КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ АНТИОКСИДАНТОВ Патологические сдвиги гипоксического и свободнорадикального генеза очень часто встречаются совместно, так как все виды гипоксии обязательно сопровождаются активацией свободнорадикальных процессов. Однако избыточное усиление перекисного окисления белков и липидов может представлять и первичное звено патологии без предшествующей гипоксии, например, в начальной стадии лучевого поражения, при некоторых интоксикациях и др. Расстройства гипоксического и свободнорадикального происхождения по мере их нарастания могут привести к деструкции клеток и, следовательно, часто определяют судьбу органа, ткани и в конечном счете - всего организма. Отсюда вытекает актуальность разработки высокоэффективных антигипоксантов и антиоксидантов и их рационального применения. Избыточная активация реакций свободнорадикального окисления представляет типовой патологический процесс, встречающийся при самых различных заболеваниях и повреждающих воздействиях на организм. Свободные радикалы - молекулы с неспаренными электронами, находящимися на внешней оболочке атома или молекулы, обладающие очень высокой реакционной способностью и, как следствие, выраженным повреждающим действием на клеточные структуры. В понятие свободного радикала не включаются ионы металлов пе- ременной валентности, неспаренные электроны которых находятся на внутренних оболочках. Доказано участие свободных радикалов в патогенезе очень многих заболеваний (шок различного генеза; атеросклероз; нарушения мозгового, коронарного и периферического кровообращения; сахарный диабет и диабетическая ангиопатия; ревматоидные, воспалительные и дегенеративные заболевания опорно-двигательной системы; поражения глаз; легочные заболевания; онкологическая патология; термические поражения; различные интоксикации; реперфузионные поражения) и преждевременного старения. Кроме того, к повышенному образованию свободных радикалов в организме приводят прием препаратов с прооксидантными свойствами, проведение ряда лечебных процедур (кислородотерапия, гипербарическая оксигенация, ультра- фиолетовое облучение, лазерная коррекция зрения, лучевая терапия), а также различные экологически неблагоприятные факторы окружающей среды. Начальным этапом развития окислительного стресса является избыточное образование высокоактивных свободнорадикальных форм кислорода. Причинами этого могут быть во-первых, нарушение функций митохондрий с прекращением образования молекул воды (конечного продукта кислородного метаболизма) и накоплением промежуточных свободнорадикальных форм кислорода, во-вторых, подавление эндогенных антиоксидантных систем, нейтрализующих свободные радикалы. Образовавшиеся свободнорадикальные формы кислорода подвергают перекисной модификации фосфолипиды, а точнее, ненасыщенные жирные кислоты, входящие в их состав и высвобождающиеся при распаде фосфолипидов. В ходе этого окисления образуются свободнорадикальные формы указанных кислот с повреждающими свойствами и токсичные продукты окисления. В результате происходит деструкция клеточных структур вплоть до гибели клеток. Последовательность реакций свободнорадикального окисления представлена на схеме 9.1. Процессы перекисного окисления липидов (ПОЛ) постоянно происходят в организме и имеют важное значение для обновления состава и поддержании функциональных свойств биомембран, энергетических процессов, клеточного деления, синтеза биологически активных веществ, внутриклеточной сигнализации. Через стадию перекисных производных ненасыщенных жирных кислот осуществляется биосинтез простагландинов и лейкотриенов, а тромбоксаны, оказывающие мощное влияние на адгезивно-агрегационные свойства форменных элементов крови и микроциркуляцию, сами являются гидроперекисями. Образование гидроперекисей холестерина - одно из звеньев в синтезе некоторых стероидных гормонов, в частности, прогестерона.
Избыточная активация процессов цепного свободнорадикального окисления липидов может привести к накоплению в тканях таких продуктов, как липоперекиси, радикалы жирных кислот, кетоны, альдегиды, кетокислоты, что, в свою очередь, повреждает и увеличивает проницаемость клеточных мембран, модифицирует структурные белки, ферменты, биологически активные вещества. Происходит активация процессов апоптоза - либо за счет прямого повреждения клеточных белков, либо за счет изменения характера транскрипции определенных генов. Наконец, свободные радикалы 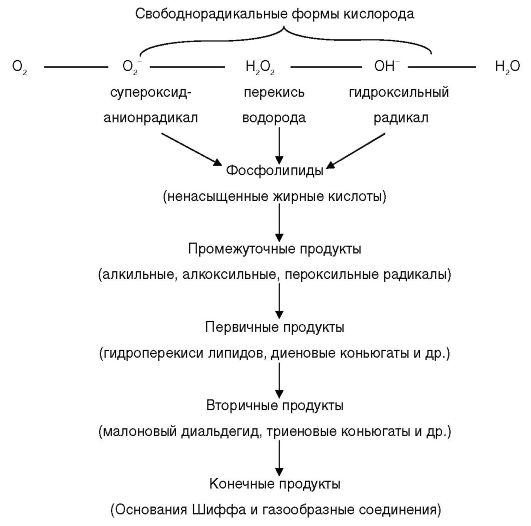 Схема 9.1. Последовательность реакций свободнорадикального окисления могут играть роль сигнальных молекул, напрямую стимулирующих выход кальция из депо. Некоторые высокоактивные формы и соединения кислорода, азота и хлора, образующиеся в организме, представлены на схеме 9.2. В реакциях одноэлектронного восстановления кислорода (в дыхательной цепи митохондрий, при аутоокислении избытка катехоламинов и др.) обычно участвует, наряду с молекулой, из которой радикал образуется, ион металла переменной валентности, выполняющий функцию донора или акцептора одного электрона. В результате образуется супероксидный анион-радикал, способный свободно мигриро- 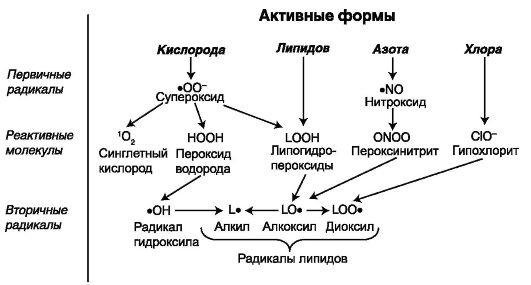 Схема 9.2. Активные формы кислорода, азота и хлора (Владимиров Ю. А., 1998) вать от места своего образования через мембраны по анионным каналам, что обеспечивает его широкую распространенность в клеточных структурах. Типичный пример реакции, в которой образуется радикал, - это реакция Фентона - взаимодействие пероксида водорода с ионом двухвалентного железа: При высоких температурах или под действием ультрафиолетового излучения радикалы могут образовываться также в результате разрыва химической связи (гомолитическое расщепление), однако в обычных условиях такие реакции в нормальных живых клетках практически не имеют места.
Присоединение к супероксидному анион-радикалу еще одного электрона (двухэлектронное восстановление кислорода) приводит к образованию перекиси водорода. Это происходит либо в результате спонтанной дисмутации:  При взаимодействии перекиси водорода и молекулы супероксиданион-радикала, являющегося донором третьего электрона, в присутствии металлов с переменной валентностью образуется гидроксильный радикал, наиболее значимый для процессов пероксидации как самая агрессивная окисляющая форма восстановленного кислорода. Одним из основных субстратов свободнорадикальных реакций являются насыщенные жирные кислоты, широко представленные в составе липидов мембран. В ходе первой, инициирующей ПОЛ, реакции образуется перекись водорода и радикал жирной кислоты:  Регулятором уровня ПОЛ в организме является антиоксидантная система, в составе которой достаточно условно можно выделить эндогенные антиоксиданты, металлсвязывающие белки и пищевые антиоксиданты. Некоторые компоненты антиоксидантной системы (Percival M., 1998) Эндогенные антиоксиданты Неферментные: • Билирубин. • Тиолы (глутатион, α-липоевая кислота, N-ацетилцистеин). • Тиоредоксин. • НАДФ и НАДН. • Убихинон (кофермент Q10). • Мочевая кислота. Ферментные: • Медь/цинк- и магнийзависимая супероксиддисмутаза. • Железозависимая каталаза. • Селензависимая глутатионпероксидаза. • Селензависимая тиоредоксинредуктаза. • Тиоредоксинпероксидаза. Металлсвязывающие белки • Альбумин (медь). • Церулоплазмин (медь). • Металлотионеин (медь). • Ферритин (железо). • Миоглобин (железо). • Трансферрин (железо). Пищевые антиоксиданты • Аскорбиновая кислота (витамин С). • α-токоферол (витамин Е).
• β-каротин и другие каротиноиды и оксикаротиноиды, в том числе ликопин и лютеин. • Полифенолы, в том числе флавоноиды, флавоны, флавонолы и проантоцианидины. К одним из основных ферментов, оказывающих антиоксидантное действие, относятся супероксиддисмутаза, каталаза, ферменты системы глутатиона. Супероксиддисмутаза и каталаза являются высокоспецифичными ферментами и нейтрализуют такие активные формы кислорода, как супероксидный анион-радикал и перекись водорода: 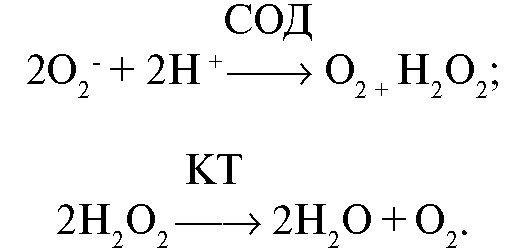 Помимо этих ферментов в разрушении активных форм и соединений кислорода принимают участие тиоредоксинпероксидаза (перок- сиредоксин), тиоредоксин и тиоредоксинредуктаза. Важной составляющей антиоксидантной защиты является система глутатиона, нейтрализующая перекиси липидов и поддерживающая в восстановленном состоянии SH-группы белков, что обеспечивает их функциональную активность. Глутатионпероксидаза (ГП, GSH-пероксидаза) - фермент, восстанавливающий перекись водорода и липоперекиси с одновременным окислением глутатиона (GSH): 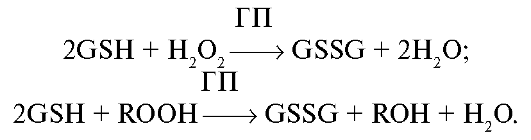 ГП обладает в 1000 раз бóльшим сродством к перекиси водорода по сравнению с каталазой, поэтому ГП рассматривают в качестве антиоксидантного фермента, имеющего первоочередное значение в защите клетки от постоянно образуемой перекиси водорода. Активность ГП прогрессивно возрастает в зависимости от количества возникающих липопероксидов. При этом накапливается окисленный глутатион, смешанные дисульфиды глутатиона и белков, снижается уровень NADPH, а затем и восстановленного глутатиона (GSH). Глутатионредуктаза (ГР, GSH-редуктаза) катализирует восстановление окисленного глутатиона (GSSG), используя в качестве восстановительного эквивалента NADPH: 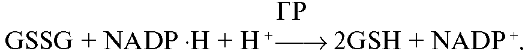 Окисление глутатиона в глутатионпероксидазной реакции, сопряженное с его восстановлением глутатионредуктазой, является определяющим фактором, поддерживающим восстановительный потенциал глутатиона.
Антиоксидантная активность восстановленного глутатиона (GSH) тесно связана с работой защитных ферментов системы глутатиона. В условиях активации перекисного окисления GSH снижается, а окисленного глутатиона - возрастает. На рисунке представлена нейтрализация свободных радикалов и перекисей системой глутатиона (схема 9.3). Глутатион-S-трансферазы (ГST) - семейство мультифункциональных белков, использующих GSH для конъюгации с гидрофобными веществами, их восстановления или изомеризации. Биологическая роль ГST в организме заключается: а) в биотрансформации ксенобиотиков:  Роль некоторых эндогенных антиоксидантных ферментов представлена на схеме 9.4. В наиболее общем виде спектр биологической активности некоторых естественных антиоксидантов представлен в табл. 9.1. 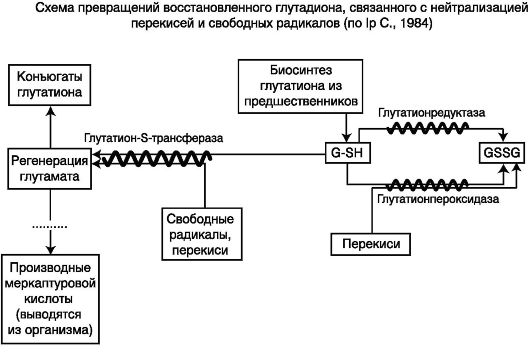 Схема 9.3. Нейтрализация свободных радикалов и перекисей системой глутатиона 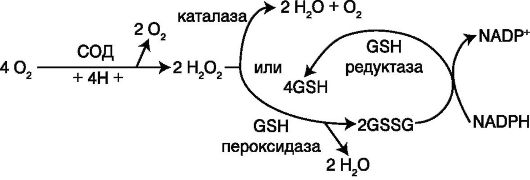 Схема 9.4. Участие некоторых эндогенных антиоксидантных ферментов в антиоксидантной защите (Proctor P. H., Reynolds E. S., 1984) Таблица 9.1. Некоторые высокоактивные формы и соединения кислорода и нейтрализующие их естественные антиоксиданты (Percival M., 1998, с изменениями и дополнениями) 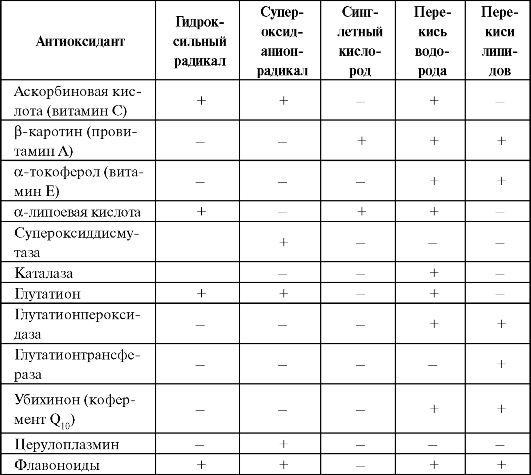 Препаратами, ограничивающими активность процессов свободнорадикального окисления, являются антиоксиданты. Классификация антиоксидантов 1. Антирадикальные средства. 1.1. Эндогенные соединения. 1.2. Синтетические препараты. 2. Антиоксидантные ферменты и их активаторы. 2.1. Препараты супероксиддисмутазы. 2.2. Препараты ферроксидазы (церулоплазмина). 2.3. Активаторы антиоксидантных ферментов. 3. Блокаторы образования свободных радикалов. 9.1. АНТИРАДИКАЛЬНЫЕ СРЕДСТВА Эндогенные соединения • α-токоферол (витамин Е). • β-каротин (провитамин А). • Карнозин. • Кислота аскорбиновая (витамин С).
• Глутатион восстановленный (Татионил). • Кислота α-липоевая (Тиоктацид). • Убихинон (Убинон). • Ретинол (витамин А). Механизм действия антирадикальных средств («скэвенджеров») заключается в непосредственном взаимодействии данных препаратов со свободными радикалами с их нейтрализацией. Наиболее изученное антирадикальное средство - α-токоферол (витамин Е). Строго говоря, термин «витамин Е» является собирательным названием для группы токоферолов - α, β и γ, которые обладают сходной биологической активностью. Наибольшая витаминная и антиоксидантная активность присуща α-токоферолу, в связи с чем именно он нашел применение в медицине. Витамин Е является природным антиоксидантом, содержащим фенольное кольцо с системой сопряженных двойных связей, защищающим различные вещества от окислительных изменений, участвующим в биосинтезе гема и белков, пролиферации клеток, тканевом дыхании и других важнейших процессах клеточного метаболизма. Он может выполнять структурную функцию, взаимодействуя с фосфолипидами биологических мембран, одновременно тормозя ПОЛ и пре- дупреждая их повреждение. Поток протонов от фонда NADPH и NADH к α-токоферолу осуществляется цепью антирадикальных эндогенных соединений (глутатион, эрготионин-аскорбат) при участии соответствующих редуктаз и дегидрогеназ. Механизм антиоксидантного действия препарата заключается в переносе водорода фенильной группы на перекисный радикал: 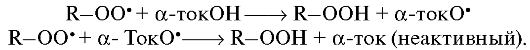 Феноксил - радикал, который образуется при этом, сам по себе достаточно стабилен и в продолжении цепи не участвует. Синергичный эффект оказывает аскорбиновая кислота, восстанавливающая продукт окисления α-токоферола - α-токофероксид в α-токоферол. Как и другие жирорастворимые витамины, витамин Е хорошо всасывается в верхних отделах тонкой кишки и поступает в кровяное русло через лимфатическую систему. В крови связывается с β-липопротеидами. Около 80% введенного в организм α-токоферола через неделю экскретируется желчью, а небольшая часть выводится в виде метаболитов с мочой.
Суммарный антиоксидантный эффект α-токоферола не слишком выражен, так как в процессе нейтрализации свободных радикалов данным веществом образуются соединения с остаточной радикальной активностью. Другой недостаток α-токоферола заключается в его липофильности, что затрудняет создание лекарственных форм для парентерального введения, необходимых при оказании неотложной помощи. Выход здесь может быть в создании липосомальных форм α- токоферола, более эффективных и потенциально пригодных для парентерального введения. Главное достоинство α-токоферола - очень малая токсичность, как у эндогенного соединения. Эмпирически витамин Е применяют при самых разнообразных заболеваниях, однако большинство сообщений об эффективности α-токоферола базируется на единичных клинических наблюдениях и экспериментальных данных. Контролируемые исследования практически не проводились. В настоящее время нет четких данных о роли витамина Е в предупреждении опухолевых заболеваний, хотя показана способность препарата снижать образование нитрозаминов (потенциально канцерогенные вещества, образующиеся в желудке), уменьшать образование свободных радикалов и оказывать антитоксическое действие при применении химиотерапевтических средств. Наиболее крупное исследование, посвященное изучению профилактического антиканцерогенного эффекта α-токоферола у мужчин- курильщиков - АТВС (The Alpha-Tocopherol Beta-Carotene Cancer Prevention, 2002 г). Его результаты продемонстрировали, что ежедневный профилактический прием витамина Е (50 мг) в течение 5-8 лет не влияет на заболеваемость раком легкого, толстой кишки, желудка, поджелудочной и предстательной железы. Более того, исследование VITAL (VITamins And Lifestyle, 2008 г.), в которое было включено более 77 000 человек в возрасте 50-76 лет, продемонстрировало, что риск развития рака легких увеличивается при 10-летнем дополнительном назначении 100 мг витамина Е в сутки примерно на 7%, а при использовании дозировки в 400 мг - на 28%. Наиболее часто этот негативный эффект проявляется у курящих.
Данные Кембриджского исследования CHAOS по применению антиоксидантов в кардиологии, опубликованные в 1996 г., позволяют го- ворить, что у больных с достоверным (ангиографически подтвержденным) коронарным атеросклерозом прием витамина Е (суточная доза 544-1088 мг (400-800 МЕ)) снижает риск нефатального инфаркта миокарда. Общая же смертность от сердечно-сосудистых заболеваний в этом случае не снижается. Благоприятный эффект проявляется лишь после годичного приема α-токоферола. В то же время в исследовании HOPE (Heart Outcomes Prevention Evaluation, 1993-1999 гг.), в котором изучалось наряду с рамиприлом действие витамина Е (400 МЕ/сут) у бессимптомных больных старше 54-летнего возраста с низкой фракцией выброса левого желудочка и высоким риском сердечно-сосудистых осложнений, установлено, что применение этого антиоксиданта в течение примерно 4,5 лет не оказывало никакого влияния на первичную (инфаркт миокарда, инсульты и смерти от сердечно-сосудистых заболеваний, рак и смерти от рака) точку исследования. При исследовании вторичных точек (случаи развития сердечной недостаточности (СН), нестабильной стенокардии и операции реваскуляризации сердца) оказалось, что прием витамина Е сопровождался даже некоторым повышением риска развития СН и госпитализаций по поводу СН. Исследование HOPE-TOO (HOPE-The Ongoing Outcomes) явилось продолжением исследования HOPE (за 738 пациентами из вклю- ченных в исследование HOPE проводилось пассивное наблюдение). Исследование подтвердило эффективность длительного применения ингибитора ангиотензинпревращающего фермента рамиприла для вторичной профилактики сердечно-сосудистых заболеваний; среди больных, получавших витамин Е, различий в первичных или вторичных точках не было получено.
Таким образом, достаточно убедительно показано, что применение витамина Е у больных с высоким риском сердечно-сосудистых осложнений не предотвращает их развитие, так же как и возникновение случаев рака. Более того, учитывая возрастание риска развития сердечной недостаточности при длительном приеме витамина Е, необходимо более тщательное клиническое изучение так называемых натуральных продуктов (витаминов, пищевых добавок), широко используемых в профилактических целях. В другом крупном исследовании по первичной профилактике атеросклеротических заболеваний у людей, по крайней мере с одним фактором риска (гипертензия, гиперхолестеринемия, ожирение, преждевременный ИМ у ближайшего родственника или преклонный возраст), витамин Е (300 МЕ/сут) применялся на протяжении 3,6 лет и не оказал никакого действия ни на одну из конечных точек (частота случаев сердечно-сосудистой смерти и всех сердечно-сосудистых событий). Не подтвердилась эффективность витамина Е и в большинстве других случаев (гиперхолестеринемия, тренированность спортсменов, сексуальная потенция, замедление процессов старения и многие другие). В то же время получены достаточно убедительные данные, что при неонатальном гемохроматозе (тяжелое, часто фатальное нарушение метаболизма железа у новорожденных, приводящее к развитию острой печеночной недостаточности) раннее лечение антиоксидантами (витамин E, деферроксамин, селен и N-ацетилцистеин) и трансплантация печени, в дополнение к оптимальному медицинскому обслуживанию, могут привести к благоприятным результатам (подробнее см. далее). α-токоферол в дозе 294-441 МЕ (450-600 мг) в сутки оказывает терапевтический эффект у больных с синдромом перемежающейся хромоты, что, возможно, связано с улучшением реологических свойств крови. Терапевтические дозы витамина Е могут защищать генетически дефектные эритроциты при талассемии, недостаточности глутатионсинтетазы и глюкозо-6-фосфатдегидрогеназы.
В табл. 9.2 представлены основные показания к применению препарата при заболеваниях, в патогенезе которых предполагается повышенная липопероксидация. Как правило, препарат назначается перорально, а инъекции обычно производят в случаях нарушения всасывания и обмена витамина Е в организме. Дозы такие же, как при приеме внутрь. Таблица 9.2. Основные показания к применению и схемы назначения α-токоферола 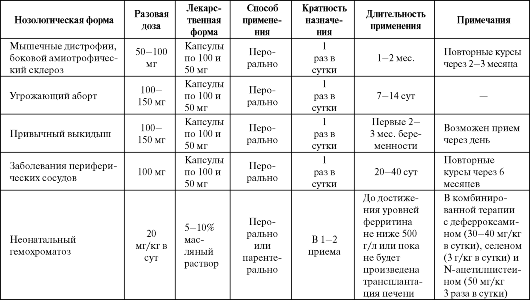 Длительный прием витамина Е в дозах от 100 до 800 мг не вызывает побочных реакций. Возможные проявления токсического действия α-токоферола появляются при парентеральном введении больших доз (табл. 9.3). Следует отметить, что α-токоферол является индуктором изоферментов цитохрома Р-450 3А4. Совместно с витамином Е в организме действует и аскорбиновая кислота (витамин С), способная образовывать окислительно-восста- новительную пару аскорбиновая кислота/дегидроаскорбиновая кислота. Вероятно, на границе раздела липиды/водная фаза аскорбиновая кислота обеспечивает защиту α-токоферола или восстанавливает его окисленную форму после действия свободных радикалов. Кроме того, предполагается, что витамин С может предотвращать или делать обратимым процесс окисления восстановленного глутатиона (GSH) до его функционально неактивной формы (GSSG). Весьма важным обстоятельством является то, что аскорбиновая кислота проявляет выраженный антиоксидантный эффект только в отсутствие металлов переменной валентности (ионов железа и меди); в присутствии же активной формы железа (Fe3+) она может восстанавливать его до двухвалентного железа (Fe2+), которое способно высвобождать гидроксильный радикал по реакции Фентона, проявляя свойства прооксиданта. Фактически достаточно 10 мг витамина С в день, чтобы избежать его дефицита в организме, но для того чтобы аскорбиновая кислота могла активно функционировать как антиоксидант, дозы должны составлять 80-150 мг/сут.
В одном из первых хорошо спланированных исследований по влиянию длительного регулярного приема аскорбиновой кислоты на кардиоваскулярную летальность (NHANES-I (First National Health and Nutrition Examination Survey)) было установлено, что под влиянием витамина С происходит уменьшение смертности от сердечно-сосудистых причин на 48% и от всех причин на 26%. Однако в других исследованиях не удалось повторить этот успех. Также неудачей окончилась попытка добиться снижения уровня холестерина в крови или выраженности коронарного стеноза путем длительного назначения аскорбиновой кислоты в дозах >250 мг/сут. Не получено до настоящего времени и убедительных данных по снижению онкологической или кардиоваскулярной заболеваемости под влиянием монотерапии аскорбиновой кислотой в относительно высоких дозах (400-1000 мг/ сут). В крупном исследовании VITAL (VITamins And Lifestyle) не подтверждена способность витамина С при длительном приеме умень- шать риск развития рака легких. Таблица 9.3. Побочные эффекты и противопоказания к применению некоторых антиоксидантов 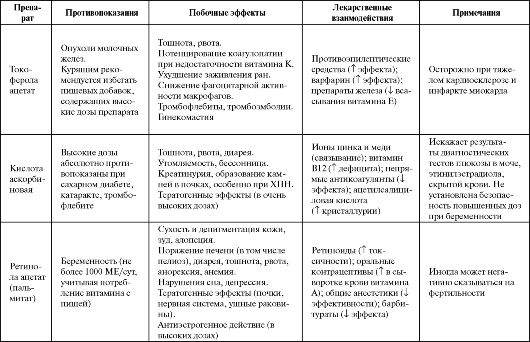 Продолжение табл. 9.3 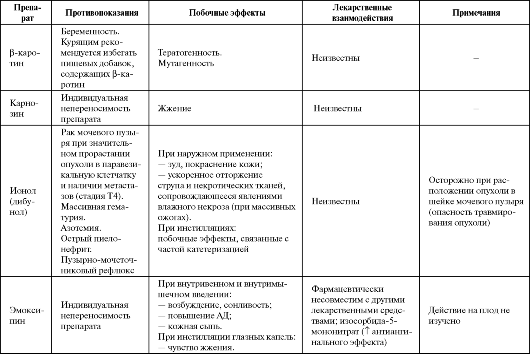 Продолжение таблицы 9.3 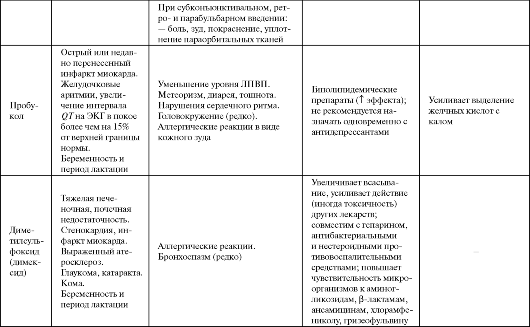 Продолжение табл. 9.3 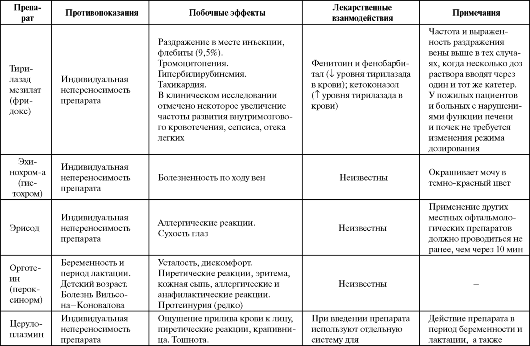 Продолжение таблицы 9.3 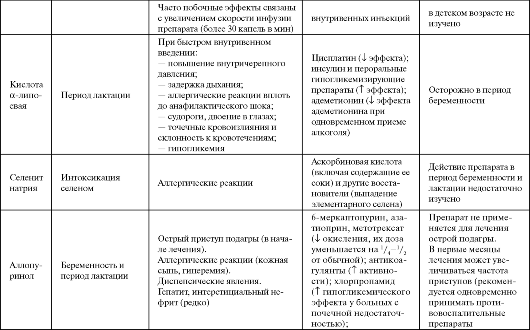 Окончание табл. 9.3  Остается открытым вопрос о безопасности использования больших доз аскорбиновой кислоты. Это связано с несколькими причинами. Во-первых, увеличенные дозы витамина С приводят к увеличению потерь организмом витаминов В12, В6 и В2. Во-вторых, применение высоких доз препарата запрещено у больных катарактой и глаукомой (в силу снижения проницаемости капилляров и нарушения обмена жидкости в передней камере глаза), у больных диабетом и тромбофлебитом. В-третьих, высокие дозы аскорбиновой кислоты также небезопасны при беременности (вследствие повышения уровня эстрогенов).
Помимо этого следует учитывать, что аскорбиновая кислота в процессе метаболизма образует две окисленные формы - дегидроаскорбиновую и дикетогулоновую кислоты, обладающие собственной прооксидантной активностью. Возможные побочные реакции, развивающиеся при приеме препарата, представлены в табл. 9.3. Ретинол (витамин А) и β-каротин (провитамин А) являются составной частью естественной антиоксидантной системы клетки и оказывают определенное антиоксидантное действие, однако оно под- тверждено преимущественно в экспериментальных исследованиях на животных. Согласно мембранной теории действия витамина А, ретинол способен проникать в гидрофобную зону биомембран и взаимодействовать с лецитино-холестериновыми монослоями на границе раздела фаз, вызывая перестройку мембран клетки, лизосом и митохондрий. Несмотря на достаточно убедительные теоретические и экспериментальные данные об антиоксидантной активности ретинола, в настоящее время отсутствуют подтвержденные в рандомизированных клинических исследованиях (РКИ) данные по влиянию монотерапии ретинолом на развитие онкологических заболеваний или снижение кардиоваскулярной заболеваемости. β-каротин, а также каротиноиды, не способные к образованию витамина А, выполняют антиоксидантные функции за счет наличия изопреноидных участков в своей формуле. Они являются достаточно эффективными ловушками для синглетного кислорода, в особенности при низком парциальном давлении кислорода. Кроме того, в этом случае они могут действовать и по другому механизму, выступая в качестве антиоксидантных соединений, обрывающих цепи ПОЛ. В то же время при высоком содержании кислорода β-каротин может проявлять прооксидантную активность. Рекомендуемая доза для мужчин составляет 1000 мкг ретинола или 6 мг β-каротина, тогда как для женщин эта доза меньше и составляет 800 мкг ретинола или 4,8 мг β-каротина.
В 5 РКИ было показано, что прием β-каротина (в дозах 20-30 мг/сут или 50 мг через день) не снижает заболеваемость раком легкого, предстательной и поджелудочной железы, толстой кишки и немеланомного рака кожи. В 4 исследованиях не удалось обнаружить у β-каротина способности снижать кардиоваскулярную летальность. Кроме того, имеются определенные ограничения в применении лекарственных средств, содержащих витамин А и каротиноиды, связанные с их возможной тератогенной активностью. Есть сообщения об увеличении частоты развития рака легких у курильщиков на 18-28% при использовании β -каротина. Известный риск несет применение этих препаратов у беременных, поэтому норма при беременности и лактации уста- новлена соответственно 200 мкг и 400 мкг ретинола. Особый интерес представляет комбинированное применение эндогенных антирадикальных антиоксидантов. В РКИ CARET изучали применение комбинации β-каротина (30 мг/сут) и ретинола (25 000 МЕ/сут) среди людей группы высокого риска (курильщики, рабочие, контактирующие с асбестом). Через 4 года было выявлено статистически значимое увеличение заболеваемости раком легкого, смертности от этого заболевания и общей смертности. Исследование АТВС также не выявило пользы от комбинированного приема в течение 5-8 лет β-каротина (20 мг/сут) и α-токоферола (50 мг/сут) в плане снижения заболеваемости раком легкого, толстой кишки, желудка, поджелудочной и предстательной железы. В исследовании HPS (Heart Protection Study) наряду с изучением эффективности симвастатина исследовалось и профилактическое действие антиоксидантов. Применение комплекса витаминов (600 мг витамина Е, 250 мг витамина С и 20 мг β-каротина в сутки) продолжалось в среднем 5,5 лет и не показало каких-либо отличий в групах плацебо и у принимавших витамины. Более того, если и имелась какая-то тенденция, то в сторону превышения числа сосудистых событий в группе антиоксидантного вмешательства.
Наконец, в исследовании HATS (HDL Atherosclerosis Treatment Study) - лечение атеросклероза в зависимости от уровня холестерина липопротеидов высокой плотности (ХС ЛПВП), у 160 больных с коронарной болезнью сердца с подтвержденными стенозами коронарных артерий и низким ХС ЛПВП была использована более высокая, чем в HOPE и HPS, доза витамина Е (800 МЕ/сут). В комбинацию были также включены 1000 мг витамина С, 25 мг β-каротина и 100 мг селена. Действие антиоксидантов сравнивалось с эффектом комбинированного применения симвастатина и никотиновой кислоты (ниацин). Кроме того, одна из групп получала симвастатин + ниацин и антиоксиданты. Исследование продолжалось 3 года и выявило, что антиоксиданты никак не влияли на уровень ХС ЛПВП, а в комбинации с гипохолестеринемическими препаратами уменьшали эффект последних на ХС ЛПНП и особенно ХС ЛПВП. Также неутешительными, в плане применения антиоксидантов, оказались ангиографические и клинические данные этого исследования. В двух исследованиях изучали возможность применения аскорбиновой кислоты в комбинации с α-токоферолом для профилактики опухолей толстой кишки. Через 2 или 4 года относительный риск рецидива аденоматозных полипов толстой кишки среди получавших комбинацию витамина С (400 или 1000 мг/сут) и витамина Е (400 мг/ сут), по сравнению с плацебо, не снизился. В то же время в одном небольшом исследовании через 3 года одновременного применения витаминов С (1000 мг/сут), Е (30000 МЕ/сут) и А (70 мг/сут) было отмечено уменьшение частоты рецидивов полипов толстой кишки. Таким образом, в настоящее время нет достаточного количества убедительных данных о выраженной антирадикальной активности эндогенных препаратов при различной патологии у человека. Другие эндогенные антиоксиданты с антирадикальным действием, которые уже рассматривались и в качестве антигипоксантов, - это идебенон и убихинон (см. лекцию «Клиническая фармакология антигипоксанатов»). Важнейшая биологическая роль убихинона (ко- фермента Q) определяется участием в митохондриальной цепи электронного транспорта в качестве кофермента. В настоящее время можно считать доказанным, что убихинон, кроме переноса электронов и протонов в митохондриях, выполняет еще одну важную функцию, образуя окислительно-восстановительную систему убихинол-убихинон, а его восстановленная форма является хорошим антиоксидан- том. Кофермент Q является единственным жирорастворимым антиоксидантом, который синтезируется в клетках, а также постоянно регенерируется из окисленной формы с помощью ферментных систем организма. Антиоксидантная активность убихинона проявляется в следующем:
- в фазе инициации цепи ПОЛ восстановленная форма кофермента Q (убихинон) вступает в конкурирующую реакцию с активным соединением и препятствует образованию алкильных радикалов; - может реагировать с пероксильным радикалом и не дает образоваться новым алкильным радикалам, что ведет к обрыву цепи ПОЛ; - в клеточных мембранах восстановленный кофермент Q обеспечивает эффективную защиту мембранных липидов, белков и ДНК от разрушительного действия активных форм кислорода; - кофермент Q восстанавливает витамин Е, взаимодействуя с его токофероксильным радикалом. Главным образом антиоксидантное действие кофемента Q заключается в предотвращении образования и устранении свободных липидных радикалов, а при концентрациях убихинона, существующих в митохонд- риях, он способен быть ловушкой супероксидного анион-радикала: 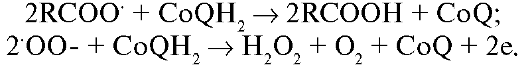 В целом в качестве антиоксиданта убихинон пока менее изучен, чем α-токоферол. Но главное его достоинство в качестве антиоксидантов - относительно небольшая токсичность. Новым направлением в антиоксидантной терапии стало использование препаратов восстановленного глутатиона, являющегося важным компонентом антиоксидантной системы организма, нейтрализующим высокоактивные перекиси липидов и поддерживающим в восстановленном состоянии сульфгидрильные группы белков, обеспечивая их функциональную активность. Истощение пула восстановленного глутатиона в организме происходит при старении, заболеваниях, в патогенезе которых большую роль играют гипоксия и ишемия. В частности, пилотное исследование по применению препарата восстановленного глутатиона (татионила) в офтальмологии при идеопатической сенильной катаракте дало первые обнадеживающие результаты (табл. 9.4). Получен неплохой эффект при использовании татионила у больных, находящихся на гемодиализе (для предупреждения гемолитической анемии), в спортивной медицине. Однако для широкого внедрения препарата в клиническую практику потребуется еще большое число экспериментальных и клинических исследований.
|
