Конспект лекций СДВС 2014. Конспект лекций по курсу двс (сдвс) Николаев 2014 Содержание
 Скачать 4 Mb. Скачать 4 Mb.
|
|
Тема 7. Процесс сгорания. Условия выделения и использования тепла при сгорании топлива. Количество воздуха необходимое для сгорания топлива. Факторы, влияющие на эти процессы. Процесс расширения. Параметры рабочего тела в конце процесса. Работа процесса. Процесс выпуска отработавших газов. Сгорание топлива – основной процесс расчетного цикла, при котором происходит выделение теплоты, преобразуемой в двигателе в полезную механическую работу. Самовоспламенение и сгорание топлива представляют сложный процесс химического соединения горючих элементов топлива с кислородом воздуха, сопровождаемый выделением теплоты. При расчете процесса сгорания топлива промежуточные физико-химические изменения не рассматривают, а учитывают лишь конечные результаты химических реакций. Процесс сгорания рассчитывают исходя из 1 кг сжигаемого топлива. Для удобства расчета количество воздуха и образующихся газообразных продуктов сгорания измеряют в киломолях, под которым подразумевается количество газа, масса которого в килограммах равна молекулярной массе данного газа. Для определения конечных параметров процесса сгорания – максимальных значений давления Рz и температуры Тz – необходимо прежде всего определить количество воздуха L, которое вводится в цилиндр для сгорания 1 кг топлива, и количество образовавшихся продуктов сгорания М. Примем элементарный массовый состав топлива где массовые доли условно обозначены химическими символами соответствующих элементов. Теоретически необходимое количество воздуха при сгорании 1 кг топлива Lo определяется стехиометрическими соотношениями, т. е. уравнениями окисления составных частей топлива при полном сгорании. Из этих условий определяют количество кислорода, необходимое для полного сгорания. В качестве примера рассмотрим уравнение реакции окисления С в СО2: 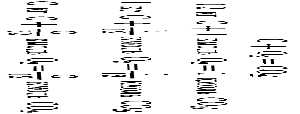 Из последнего равенства следует, что для полного сгорания С кг углерода требуется С/12 кмоль кислорода и в результате сгорания будет получено С/12 кмоль углекислого газа. Аналогично можно определить количество кислорода для сгорания водорода и серы и количество продуктов их сгорания. Общее количество кислорода, необходимое для сгорания, определяют в результате суммирования количеств кислорода, необходимого для сгорания каждого из горючих элементов. Учитывая, что в 1 кг топлива содержится О/32 кмоль кислорода, необходимое его мольное количество следует уменьшить на величину О/32 кмоль. Таким образом, теоретически необходимое мольное количество кислорода для сжигания 1 кг топлива будет равно Воздух по объему состоит из 21 % О2 и 79 % N2. Следовательно, теоретически необходимое мольное количество воздуха для сжигания 1 кг топлива составит, кмоль/кг То же значение в килограммах на 1 кг топлива будет где μв = 28,97 – масса 1 кмоль воздуха. Для дизельного топлива среднего состава (С = 0,87, Н = 0,126, О = 0,004) получим Lo = 0,495 кмоль/кг и L'o = 14,3 кг/кг. Следует заметить, что сгорание топлива при теоретически необходимом количестве воздуха является частным случаем, встречающимся только в карбюраторных двигателях, в которых пары легкого топлива и воздуха перемешиваются более интенсивно. Из-за ограниченного времени на смесеобразование в дизелях и недостаточно полного перемешивания топлива с воздухом топливовоздушная смесь в камере сгорания оказывается неоднородной. Чтобы обеспечить качественное сгорание топлива в дизелях, приходится вводить в цилиндр воздух в количестве, превышающем теоретически необходимое, т.е. действительное количество воздуха L > Lo. Отношение действительного количества воздуха L, участвующего в процессе сгорания, к теоретически необходимому Lo называется коэффициентом избытка воздуха: Согласно опытным данным α изменяется в следующих пределах: α =1,8...2,7 для МОД, α =1,6...2,2 для СОД и α = 1,5...2,0 для ВОД. В состав смеси газов, образующихся в цилиндре в конце процесса сгорания, кроме продуктов сгорания СО2, Н2О и SO2 входят кислород О2 (вследствие его избытка) и азот N2 (в горении не участвует). Количество продуктов сгорания, образующихся при сгорании 1 кг топлива, определяется приведенными ранее стехиометрическими уравнениями сгорания, кмоль/кг Количество избыточного кислорода О2 в продуктах сгорания может быть определено по количеству избыточного воздуха: следовательно, Оставшееся количество молей в продуктах сгорания приходится на инертный азот N2, входящий в состав воздуха: Общее количество М продуктов полного сгорания 1 кг топлива при а > 1 определяется суммированием всех составляющих: Если обозначить через Мα= 1 количество продуктов сгорания 1 кг топлива с теоретически необходимым количеством воздуха (α = 1), то Из последнего выражения следует, что продукты сгорания 1 кг топлива данного состава при а > 1 представляют собой смесь одного и того же количества чистых продуктов сгорания (ЧПС) Ма= [ с избыточным количеством воздуха (α – 1)L0. Масса продуктов сгорания равна сумме масс количеств воздуха и топлива до сгорания, тогда как объемные количества рабочей смеси до сгорания и после него не равны. Приращение объема продуктов сгорания (количества молей) происходит вследствие увеличения суммарного количества молекул газообразных продуктов сгорания и может быть определено разностью Таким образом, приращение объема при сгорании не зависит от L, а определяется содержанием в топливе Н и О. В качестве критерия, оценивающего приращение объема (числа молей) продуктов сгорания, используется введенный Е. К. Мазингом теоретический (химический) коэффициент молекулярного измененияβо, который представляет отношение количества молей газообразных продуктов сгорания М к количеству молей воздуха L без учета остаточных газов в цилиндре: Например, для дизельного топлива среднего состава Кроме перечисленных выше компонентов в составе продуктов сгорания содержатся остаточные газы Мr, которые остаются в цилиндре от предыдущего цикла и влияют па изменение объема продуктов сгорания. Поэтому вводится понятие расчетного (действительного) коэффициента молекулярного изменения β, который представляет собой отношение числа молей газа после сгорания к числу молей воздуха с учетом наличия остаточных газов, т. е. Значение расчетного коэффициента молекулярного изменения лежит в пределах β = 1,03…1,04. Расчетный коэффициент молекулярного изменения в промежуточный момент процесса сгорания определяется с учетом доли топлива х, сгоревшего к моменту времени t от начала воспламенения, по формуле Из этой формулы следует, что на линии сжатия и в начальный момент воспламенения, т. е. при х = 0, βх = 1, а в конце процесса сгорания при х = 1 достигает максимального значения, равного β. Для повышения точности расчета процесса сгорания и других процессов цикла следует учитывать зависимость теплоемкости рабочего тела от его температуры и химического состава. В расчетах рабочего цикла (по методу Гриневецкого – Мазннга) используются понятия средней мольной изобарной теплоемкости ср и средней мольной изохорной теплоемкости сv. Средняя мольная изохорная теплоемкость сухого воздуха может быть определена по формуле Средняя мольная изохорная теплоемкость ЧПС для топлива среднего элементарного состава Погрешность в расчете теплоемкостей по этим эмпирическим формулам не превышает 1 %. Температура рабочего тела в конце видимого сгорания определяется из решения уравнения первого закона термодинамики, которое применительно к процессу сгорания может быть выражено в конечных разностях в виде Преобразуя уравнение в итоге получим зависимость для определения температуры конца сгорания Преобразовав уравнения и подставив все известные значения получим Это уравнение удобнее всего решается методом последовательных приближений, для чего задаются в первом приближении произвольные значения температуры в пределах Tz = = 1700…2000 К. Для судовых ДВС значения температуры в конце видимого сгорания Tz лежат в пределах: 1700...1800 К для МОД, 1800…1900 К для СОД и 1900...2000 К для ВОД. Повышение температуры Tz более 2000 К нежелательно из-за возможности значительной диссоциации газов, которая до 2000 К не превышает 2 %. Значение максимального давления сгорания pz обычно принимается на основании опытных данных по прототипам проектируемого двигателя или определяется из выражения pz = λpc после предварительного выбора степени повышения давления λ. Объем цилиндра Vz в конце видимого сгорания определяется в зависимости от степени предварительного расширения Степень предварительного расширения может быть определена в результате совместного решения уравнения состояния газа в точках z и с: У судовых ДВС значение ρ находится в пределах 1,2…1,6. Расширение продуктов сгорания в цилиндре происходит при движении поршня от ВМТ к НМТ в течение такта, называемого рабочим ходом. На участке yz (рис. 7.1) расчетного цикла увеличение объема рабочего тела сопровождается подводом к нему теплоты. Давление в цилиндре принимают постоянным. 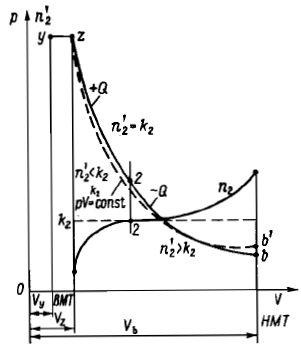 Рис. 7.1. Схема процесса расширения в теоретическом и расчетном циклах В расчетном цикле считается, что процесс расширения начинается в конце видимого сгорания в точке z, в результате чего происходит политропическое понижение давления и температуры газов. В действительном цикле расширение заканчивается в момент открытия выпускных окон или клапанов. В расчетном цикле конец расширения относят к точке b, расположенной в НМТ у четырехтактных двигателей и на уровне верхней кромки выпускных окон – у двухтактных. На процесс расширения влияют теплообмен расширяющихся газов со стенками цилиндра, догорание в первой части процесса, иногда растягивающееся на весь процесс, возможность утечки части газов через неплотности поршневых колец и восстановление (рекомбинация) некоторого количества продуктов диссоциации, возникающих в процессе сгорания. Все эти факторы обусловливают изменение показателя политропы расширения. В первой части процесса вследствие подвода теплоты от догорания и восстановления продуктов диссоциации показатель политропы расширения n2’ меньше показателя адиабаты k2 и достигает значений, меньших единицы. Политропа расширения приобретает более пологий характер, чем адиабата. По мере перемещения поршня к НМТ процесс догорания топлива становится менее интенсивным, а отдача теплоты стенкам из-за большой поверхности охлаждения возрастает. При этом показатель политропы расширения непрерывно увеличивается. При некотором положении поршня подвод теплоты за счет догорания топлива и восстановления продуктов диссоциации становится равным отдаче теплоты стенкам цилиндра, а мгновенное значение показателя политропы n2’ достигает значения показателя адиабаты (точка 2), т. е. n2’ = k2. Это и есть точка мгновенного теплового равновесного состояния газов и стенок цилиндра. При дальнейшем расширении преобладающее значение имеет отвод в стенки цилиндра и показатель n2’ становится выше показателя адиабаты и по мере приближения поршни к НМТ увеличивается до 1,4...1,5; на этом отрезке политропа идет круче адиабаты. Таким образом, процесс расширения в реальном двигателе осуществляется по политропе с переменным показателем от 1,1 до 1,5. В связи с трудностью учета всех факторов, сопровождающих процесс расширения, для определения параметров газов в процессе расширения используют политропу с усредненным показателем n2, постоянным за процесс и дающим такую же работу, как н при действительном расширении с переменным показателем политропы. Среднее значение показателя политропы расширения в расчетах рабочих процессов определяют из уравнения первого закона термодинамики, которое применительно к процессу расширения на участке zb. В результате преобразований получим: 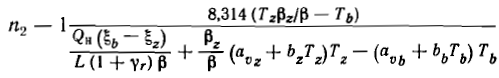 Температура и давления конца процесса расширения определяется из выражения соответственно: В процессе выпуска продукты сгорания удаляются из цилиндра, за счет чего обеспечивается осуществление последующих рабочих циклов. Процесс выпуска у четырехтактных и двухтактных двигателей протекает по-разному. В четырехтактных двигателях процесс выпуска делят на три фазы (рис. 7.2): фаза I – после открытия выпускного клапана примерно до НМТ газы вытекают из цилиндра за счет перепада давлений в цилиндре и выпускном коллекторе; фаза II – при движении поршня от НМТ к ВМТ газы выталкиваются из цилиндра перемещающимся поршнем на протяжении всего хода; фаза III – при одновременном открытии выпускного и впускного клапанов в районе ВМТ (перекрытие клапанов) осуществляются одновременно очистка цилиндра за счет динамического действия выпускных газов, движущихся по выпускному трубопроводу, и заполнение его некоторым количеством свежего воздуха – продувка камеры сгорания. 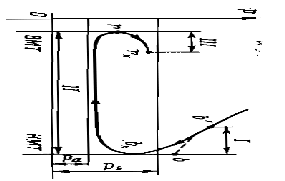 Рис. 7.2. Схема процесса выпуска в четырехтактном двигателе В двухтактных двигателях удаление продуктов сгорания из цилиндра и его наполнение свежим зарядом происходят одновременно за счет поступающего из ресивера продувочного воздуха. Особенности процессов очистки и наполнения цилиндров двухтактных двигателей сводятся к следующему (рис. 7.3): – процессы газообмена происходят лишь в конце рабочего хода поршня и в начале хода сжатия, занимая всего 140...150° ПКВ; – для газообмена необходимо предварительное сжатие воздуха в наддувочном агрегате до давления, превышающего давление газов в выпускном коллекторе в период продувки цилиндра; – функции управления процессами газообмена выполняет поршень, открывающий и закрывающий выпускные и продувочные окна. При прямоточно-клапанной системе газообмена выпуском управляют выпускные клапаны.  Рис. 7.3. Схема процесса выпуска в двухтактном двигателе Процесс выпуска в двухтактных двигателях можно разделить на три фазы: фаза I – свободный выпуск продуктов сгорания, при котором газы из цилиндра удаляются за счет перепада давлений между цилиндром и выпускным трубопроводом. Свободный выпуск газов начинается с момента открытия поршнем выпускных окон (точка b) и заканчивается в момент открытия поршнем продувочных окон. Свободный выпуск по продолжительности составляет относительно небольшую долю по отношению ко всему периоду выпуска. Но за этот, относительно небольшой отрезок времени, давление в цилиндре быстро падает от значения в начале выпуска рb до значения ps, при котором начинается продувка. фаза II – поступление из продувочного ресивера в цилиндр воздуха (процесс продувки рабочего цилиндра) и истечение в выпускной трубопровод вытесняемых продувочным воздухом продуктов сгорания (принужденный выпуск, который охватывает период от начала поступления воздуха в цилиндр до момента закрытия продувочных окон). Эта фаза протекает при стабильно сохраняющемся соотношении давлений ps > рц > рт. фаза III – потеря заряда, если выпускные органы закрываются после продувочных (в бесклапанных системах), или дозарядка, если выпускные окна закрываются раньше продувочных (в асимметричных системах продувки). Эта фаза может отсутствовать, если продувочные и выпускные окна закрываются одновременно. Процесс выпуска аналогично процессу наполнения сопровождается газодинамическими потерями давления Δрг: где Δр’ – потери давления в выпускном клапане (или клапанах) и газоотводном канале в крышке; Δр" – потери давления в выпускном коллекторе и выпускном тракте; Δр"' – потери давления в специальных устройствах выпускного тракта – глушителе, утилизационном парогенераторе. По опытным данным общая потеря давления в выпускной системе у выполненных двигателей составляет Δрг = 0,005... 0,025 МПа. Увеличение противодавления в выпускном тракте приводит к возрастанию коэффициента остаточных газов и уменьшению коэффициента наполнения. |
