Коррозия. Контрольная работа по дисциплине Физикохимические основы коррозии
 Скачать 57.02 Kb. Скачать 57.02 Kb.
|
|
Министерство образования и науки РФ Федеральное государственное бюджетное образовательное учреждение высшего образования «Уфимский государственный нефтяной технический университет» Контрольная работа по дисциплине: «Физико-химические основы коррозии» Выполнил ст.гр. БМТз-16-01 М.А. Комышев Проверил к.т.н. профессор В.В. Кравцвов Уфа, 2018 Содержание
Введение Коррозия — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это разрушение любого материала, будь то металл или керамика, дерево или полимер. Более всего подвержены коррозии чистые металлы. Сплавы, пластики и прочие материалы в этом отношении характеризуются термином «старение». Вместо термина «коррозия» также часто применяют термин «ржавление». Виды коррозии. Коррозионный процесс портит жизнь людям многие века, поэтому он изучен достаточно широко. Существуют различные классификации коррозии в зависимости от типа окружающей среды, от условия использования коррозирующих материалов (находятся ли они под напряжением, если контактируют с другой средой, то постоянно или переменно и пр.) и от множества других факторов. Электрохимическая коррозия Коррозировать могут два различных металла, соединенных между собой, если на их стык попадет, например, конденсат из воздуха. У разных металлов различные окислительно-восстановительные потенциалы и на стыке металлов образуется фактически гальванический элемент. При этом металл с более низким потенциалом начинает растворяться, в данном случае, коррозировать. Это проявляется на сварочных швах, вокруг заклепок и болтов. Для защиты от такого вида коррозии применяют, например, оцинковку. В паре металл-цинк коррозировать должен цинк, но при коррозии у цинка образуется оксидная пленка, которая сильно замедляет процесс коррозии. Химическая коррозия Если поверхность металла соприкасается с коррозионно-активной средой, и при этом нет электрохимических процессов, то имеет место т.н. химическая коррозия. Например, образование окалины при взаимодействии металлов с кислородом при высоких температурах.
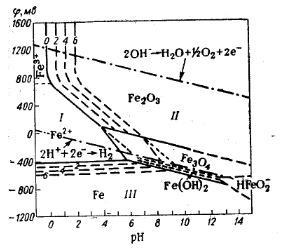 Рисунок 1 Диаграмма Пурбе для системы Fe-H2O I-активная область (коррозия); II-пассивная область; III-неативная область. На диаграмме «потенциал-рН» системы железо-вода показаны области термодинамической устойчивости металлического железа, ионов Fe2+ , Fe3+, НFeО-2, в растворе и нерастворимых соединений Fe(ОН)2, Fe3О4, Fe2О3. Эти области отвечают неактивному (металлическое железо), активному (ионы в растворе) и пассивному (нерастворимые соединения) состояниям железа. Две штрих пунктирные линии показывают зависимость потенциалов кислородного (верхняя линия) и водородного (нижняя линия) электродов от рН раствора. Область. Заключенная между этими линиями, отвечает термодинамически устойчивому состоянию воды. Области термодинамической устойчивости разграничены равновесными кривыми: числа, стоящие около них, показывают логарифмы активности соответствующих ионов. Диаграмма дает возмоджность установления условий (рН и потенциал) пассивного состояния железа. Кроме того, при наложении этой диаграммы на аналогичную диаграмму хрома, молибдена и др. можно выяснить действие пассиваторов и предсказать коррозионные и пассивирующие реакции.
Ненаполненные и неармированные реактопласты могут корродировать по нескольким механизмам, которые можно разделить на две главных группы — физические и химические. Физическая коррозия заключается в том, что полимер взаимодействует с окружающей средой так, что его свойства изменяются, но химической реакции не происходит. Типичным примером является диффузия жидкостей в полимерный материал. Во многих случаях физическая коррозия обратима: после удаления жидкости восстанавливаются первоначальные свойства. Если поглощение полимером жидкости или газа приводит к пластификации или набуханию полимерной сетки, это означает, что имела место физическая коррозия. Набухание сшитых полимеров, вызванное поглощением растворителя, максимально, когда параметры растворимости растворителя и полимера совпадают. Суть химической коррозии заключается в том, что в результате химической реакции реактопласта с окружающей средой разрушаются химические связи. Несколько различных форм химической коррозии могут происходить одновременно. Чаще всего химическая коррозия необратима. Результатом химической коррозии могут являться различные изменения материала. Например, полимер может становиться хрупким, размягчаться, обугливаться, растрескиваться, расслаиваться, обесцвечиваться, покрываться пузырями или разбухать. Действие корродентов более или менее одинаково для всех термоотверждающихся полимеров. Однако определенные химически стойкие сорта полимеров практически не подвергаются воздействию широкого ряда жестких коррозионных условий или подвергаются ему со значительно меньшей скоростью. Такие свойства обусловлены структурой полимера; примером группировки, придающей полимеру подобные свойства, является сложноэфирная группа. Отверждение смол очень сильно влияет на химическую стойкость термоотверждающихся полимеров. Неправильное отверждение приведет к ухудшению коррозионной стойкости. Конструкция ламината (слоистого материала) и используемые армирующие наполнители также влияют на его коррозионную стойкость. Сила и природа связи полимера с армирующим материалом также играет важную роль. Различные механизмы атаки по-разному влияют на прочность слоистого материала в зависимости от условий его эксплуатации, в частности, окружающей среды, а также от механизма (или комбинации механизмов) воздействия корродента.
Почвенная коррозия – разрушение металла в почве. Ежегодные потери металла вследствии протекания почвенной коррозии достигают 4%. Почвенной коррозии подвергаются различного назначения трубопроводы, резервуары, сваи, опоры, кабеля, обсадные трубы скважин, всякого рода металлоконструкции, эксплуатируемые в почве. Почва – очень агрессивная среда. Она состоит из множества химических соединений и элементов, многие из них только ускоряют коррозионный процесс. Агрессивность почвы (грунта) зависит от некоторых факторов: влажность, аэрация, пористость, рН, наличие растворенных солей, электропроводность. Классификация грунтов по коррозионной активности: - высококоррозионные грунты (тяжелые глинистые, которые длительное время удерживают влагу); - среднекоррозионные грунты; - практически инертные грунты в коррозионном отношении (песчаные почвы). Влияние влажности грунта на почвенную коррозию металла. Влага в почве присутствует почти везде. Где-то ее больше, а где-то меньше. Именно влажность грунта очень сильно влияет на скорость почвенной коррозии, превращая почву в электролит. Она же вызывает электрохимическую коррозию находящихся в грунте металлоконструкций. Вода в грунте может быть: капиллярной, гравитационной, связанной. Капиллярная влага собирается в порах грунта. Высота подъема ее по капилляру зависит от диаметра пор. Капиллярная влага сильно влияет на скорость почвенной коррозии. Связанная влага на скорость почвенной коррозии не влияет, т.к. находится в виде гидратированных химических соединений. Под действием силы тяжести в грунтах и почвах постоянно перемещается вода, которая оказывает, как и капиллярная, значительное влияние на скорость почвенной коррозии. Максимальная скорость почвенной коррозии наблюдается при влажности грунта 15 – 25%. Это объясняется уменьшением омического сопротивления коррозионных элементов. С повышением влажности почвы анодный процесс проходит легче (за счет затруднения пассивации поверхности металла), а катодный – труднее (грунт насыщается влагой, затрудняется его аэрация). Влажность, при которой наблюдается наибольшая скорость коррозии, называют критическим показателем влаги для грунта. Для глинистых грунтов он составляет около 12 – 25%, для песчаных 10 – 20%. Пористость (воздухопроницаемость) грунта. Пористость (воздухопроницаемость) грунта влияет на способность длительное время сохранять влагу и аэрацию. Воздухопроницаемость зависит от состава грунта, его плотности, влажности. Грунты, хорошо пропускающие воздух (песчаные), более агрессивны. В песчаных грунтах катодный процесс протекает с облегчением. На практике бывают случаи, когда подземный трубопровод большой протяженности проходит через разного вида грунты. Если он проходит последовательно в песчаной, а потом глинистой почве, где условия аэрации металлической поверхности очень различаются, то возникают аэрационные микрогальванические коррозионные зоны. Поверхность трубопровода в песчаной зоне будет играть роль катода, а глинистой – анода. Разрушение металла будет происходить на анодных участках, где затруднен доступ кислорода к поверхности. Интересно, что катодная и анодная зоны могут находится на расстоянии больше сотни метров. При этом коррозионный процесс будет отличаться омическим торможением. Кислотность грунта. Для большинства грунтов значение рН составляет 6,0 – 7,5. Высококоррозионными являются почвы, рН которых сильно отличается от данного значения. К ним относятся торфяные, болотистые грунты, значение рН которых составляет 3 – 6. А также щелочные солончаки и суглинки, с рН почвы 7,5 – 9,5. Очень агрессивной средой по отношению к сталям, свинцу, меди, цинку является чернозем, содержащий органические кислоты. Одна из самых агрессивных почв – подзол. Сталь в подзоле корродирует в 5 раз быстрее, чем в других грунтах. Кислотность грунтов ускоряет почвенную коррозию, т.к. вторичные продукты коррозии становятся более растворимы, существует возможность дополнительной катодной деполяризации ионами водорода. Электропроводность грунта. Электропроводность грунта зависит от его минералогического состава, количества влаги и солей в почве. Каждый вид грунта имеет свое определенное значение электропроводности, оно может колебаться от нескольких единиц до нескольких сотен Ом на метр. Соленость грунта оказывает огромное влияние на его электропроводность. С увеличением содержания солей легче протекают анодный и катодный электродные процессы, что снижает электросопротивление. Почти всегда определив электропроводность грунта можно судить о его степени коррозионной агрессивности (для стали, чугуна). Исключение составляют водонасыщенные почвы. Минералогический состав и неоднородность грунта. Минералогический состав и неоднородность грунта оказывают большое влияние (как и влажность) на омическое сопротивление. В глинисто-песчаном влажном грунте удельное сопротивление почвы составляет около 900 Ом•см, а в таком же грунте, только сухом – 240000 Ом•см. С уменьшением удельного сопротивления грунта его агрессивность увеличивается. Минерализация почвы может колебаться в пределах 10 – 300 мг/л. Неоднородность грунта приводит к возникновению гальванопар, которые только усиливают почвенную коррозию, делают разрушение неравномерным. Влияние температуры грунта на почвенную коррозию металлов. Температура может колебаться в очень больших пределах. Зимой, когда свободная вода, заполняющая капилляры в почве замерзает - скорость почвенной коррозии немного уменьшается. Это также связано с плохой аэрацией поверхности металла. В летнее время, когда на улице стоит жара, скорость почвенной коррозии может замедлятся также, что объясняется высыханием почвы. Самый большой ущерб почвенная коррозия наносит в межсезонье, когда грунт достаточно влажный, созданы оптимальные условия для протекания коррозионного процесса. Температура грунта зависит от времени года, географической широты, времени суток, погоды. Значительное различие температур на конструкции, имеющей большую протяженность (подземный трубопровод) может быть причиной образования термогальванических коррозионных пар, которые обеспечивают усиление местной почвенной коррозии. Влияние микроорганизмов на почвенную коррозию металлов. В почве живут и развиваются два вида микроорганизмов: аэробные (могут существовать только при наличии кислорода), анаэробные (для обеспечения их жизнедеятельности кислород не требуется). Они оказывают огромное влияние на почвенную коррозию металлов. Почвенная коррозия металлических сооружений, вызванная жизнедеятельностью живых микроорганизмов носит название биологическая (биокоррозия) либо биохимическая. Аэробные микроорганизмы (почвенные) существуют двух видов: одни принимают непосредственное участие в осаждении железа, другие – окисляют серу. Оптимальными условиями для существования анаэробных серобактерий является кислая среда (3 – 6 рН). Серобактерии окисляют сероводород в серу, а потом - серную кислоту по следующим уравнениям: 2H2S + O2 = 2H2O + S2; S2 + 2H2O + 3O2 = 2H2SO4. В местах наибольшего количества серобактерий концентрация серной кислоты может достигать 10%. Это очень сильно ускоряет почвенную коррозию, особенно стали. При рН грунта около 4 – 10 развиваются бактерии, перерабатывающие железо. Эти бактерии в процессе своей жизнедеятельности поглощают ионы железа, а выделяют нерастворимые соединения, содержащие Fe. В местах скопления железобактерий наблюдается большое количество нерастворимых железистых соединений, которые увеличивают гетерогенность поверхности. Это явление также оказывает большое влияние на скорость почвенной коррозии. Анаэробные микроорганизмы могут вырабатывать углеводороды, сероводород, угольную кислоту и множество других химических соединений. Они могут разрушать защитные покрытия, воздействовать на ход анодной и катодной реакции, менять характеристики почвы. Среди анаэробных микроорганизмов самыми опасными можно считать сульфатредуцирующие бактерии. Оптимальные условия для их существования, почва со значением рН 5,5 – 8 (болотные, глинистые, илистые грунты). Бактерии восстанавливают сульфаты, содержащиеся в почве. Этот процесс можно описать следующим уравнением: MgSO4 + 4H = Mg(OH)2 + H2S + O2. Выделившийся кислород обеспечивает протекание реакции на катоде. Сероводород и сульфиды в почве являются причиной появления на поверхности эксплуатируемой конструкции рыхлого слоя сульфида железа. Коррозия носит питтинговый характер. Механизм и особенности почвенной коррозии металлов. Почвенная коррозия почти всегда протекает по электрохимическому механизму (исключения составляют лишь очень сухие грунты). Анодный процесс при почвенной коррозии – разрушение металла. На катоде же проходит кислородная деполяризация. Чаще всего кислородная деполяризация проходит с затрудненным доступом кислорода к поверхности корродирующего изделия. Подвод кислорода может осуществятся несколькими способами: диффузией в жидкой или газообразной среде или направленным течением этих фаз, перемешиванием фаз при помощи конвекции. Во влажном грунте процесс проходит с преимущественно катодным контролем, а сухих рыхлых почвах - анодным. Иногда, при работе протяженных микропар может наблюдаться катодно-омический контроль. На катоде также может проходить и водородная деполяризация (только в условиях кислых грунтов). Существенно изменить ход коррозионного процесса могут и микроорганизмы. Подземную коррозию делят на грунтовую коррозию и электрокоррозию (коррозию блуждающими токами). Подземная коррозия менее опасна, чем разрушение под воздействием блуждающих токов. Особенности почвенной коррозии металлов: - значительное влияние омического сопротивления грунта; - возникновение коррозионных микро и макропар; - язвенный характер разрушения. 4. Влияние адгезии полимерных покрытий на защитные свойства. Для изучения влияния адгезии полимерных покрытий на их защитные свойства была использована методика измерения емкости и сопротивления металла с защитным покрытием, погруженного в электролит. Данная методика позволяет достаточно полно охарактеризовать основные свойства покрытия. Его емкость определяется суммарно1 пористость покрытия, при этом чем она ниже и меньше меняется с частотой, а сопротивление выше и в большей степени зависит от частоты, тем выше защитная способность покрытия; чем выше зависимость сопротивления от емкости. Тем выше его адгезионные свойства.
одготовка поверхности перед нанесением защитного покрытия обязательна! На чистый металл, без каких-либо загрязнений, слой металла, ЛКМ и др. ложится равномерно, хорошо сцепляясь с поверхностью, и в дальнейшем не отслаивается. Даже самое хорошее и качественное покрытие не будет обладать высокими защитными свойствами, если неправильно произведена предварительная подготовка поверхности! Подготовка поверхности металла очень сильно влияет на коррозионную стойкость изделия. Подготовка поверхности металла включает в себя очистку от жировых загрязнений, оксидных пленок, грязи и т.д. Осуществляется подготовка поверхности следующими способами: механической очисткой, обезжириванием и травлением. Иногда достаточно лишь одного метода удаления загрязнений, в других же случаях – применяются все. Каждый этап очистки, в зависимости от тяжести загрязнения, может повторяться несколько раз, например, стальные болты, которые хранились в смазочных материалах, могут подвергать процессу обезжиривания два-три раза. Механическая очистка Механическая обработка поверхности применяется для очистки металла от окалины, ржавчины, оксидных пленок, литейной корочки, старого лакокрасочного материала и т.п. При механической очистке удаляются вышеперечисленные загрязнения, зачастую, вместе с верхним слоем металла. Подготовка поверхности механическими методами включает в себя: абразивную обработку (пескоструйная, гидропескоструйная, дробеструйная и др.), шлифование, полирование, крацевание и т.п. Чаще всего применяется для очистки крупногабаритных изделий и объектов средних размеров, с довольно толстым поперечным сечением. Осуществляется механическая обработка в специальных аппаратах барабанного, камерного и других типов. Их изготавливают из чугуна или сплавов высокой твердости. В качестве абразивного материала используется кварцевый песок, корунды, стальная или чугунная дробь и многое другое. Под высоким давлением сжатый воздух (либо жидкость) с абразивным материалом выходит из сопла, направленного на обрабатываемую поверхность. Частички абразива, ударяясь о металл, очищают его. Обработанная поверхность металла отличается чистотой и равномерной шероховатостью. Пескоструйная обработка – очень хороший способ подготовки поверхности практически для всех покрытий (которые не требуют отполированной поверхности). Пескоструйная обработка с использованием сухого кварцевого песка сейчас уже не популярна, т.к. отличается большой вредностью для мастера, который ее проводит (развивается профессиональное заболевание – силикоз). Вместо обычной пескоструйной обработки широко используется обработка металлическим песком, стальной дробью, абразивными порошками, а также гидропескоструйная очистка. Обработка металлическим песком получила очень широкое распространение, т.к. это один из самых эффективных методов. Для его реализации используется металлический песок или стальная дробь с размером частиц от 0,15 до 1,5 мм. Металлическим песком или мелкой дробью обрабатывают практически все металлы (кроме алюминия и его сплавов). При этом размер частицы и сила потока воздуха устанавливается в зависимости от толщины стенки металлического изделия. Обработка абразивными порошками также является достаточно эффективным методом очистки поверхности от старого защитного покрытия и т.п. Данный метод – альтернатива сухой пескоструйной очистки, т.к. для его реализации используются сухие абразивы. Кроме того, оборудование используется то же самое. Шлифование и полирование проводят для придания металлу блеска, а так же удаления неровностей. Реализуются эти способы на специальных станках, либо вручную (при помощи наждачной бумаги и т.д.). Рыхлую окалину и шлам можно удалить при помощи щетки, которая изготавливается из тонкой латунной проволоки. Этот процесс получил название крацевание (кварцевание). Шлифование – это способ подготовки поверхности перед нанесением защитного покрытия, для реализации которого необходимы абразивные инструменты (ленты, вращающиеся шлифовальные круги, бруски и т.п.). Для грубого шлифования (обдира) часто используют круги, которые полностью состоят из абразивного материала (шлифовального или точильного камня). Грубым шлифованием можно удалить с поверхности толстый слой окалины, наплывы металла, заусенцы, бугры, раковины и т.д. Абразивом часто служат крупные фракции корунда (Al2O3), карбида кремния (карборунда SiC), наждака (30-35% Fe2O3 и 60-70% Al2O3). Размер зерна составляет около 250–1200 мкм. В качестве связующего используются жидкое стекло, а также различного рода глины, смолы. Декоративное шлифование (или тонкое) проводится с использованием уже не цельного круга, а специальных эластичных кругов, которые состоят из основы и абразивного материала. В качестве абразива служат мелкие фракции кварца, корунда, наждака. Их наносят на основание при помощи связующих веществ (жидкого стекла, клеев и т.д.). Основу (эластичный круг) изготавливают из брезента, кожи, войлока, хлопчатобумажной ткани, фетра и других материалов, которые дальше прессуют, склеивают и прошивают (один эластичный круг зачастую состоит из нескольких слоев). Зерно абразивного материала для тонкого шлифования по размерам составляет около 75 – 200 мкм. После операции декоративного шлифования и перед последующим полированием часто проводят матирование. Матирование – это процесс шлифования, только для его реализации используют не круги с абразивом, а эластичные круги со специальными пастами. Если поверхность ровная, то можно использовать простой круг с маленьким ворсом или без него. Изделия, которые имеют сложную форму, матируют на специальных кругах, которые изготовлены из полимерных материалов (нейлон, капрон и т.п.) или морской травы (сизаль, фибер). Для матирования цветных металлов и черных могут быть использованы следующие составы: а) 10% парафина, 80,8% маршаллита, 9% солидола Т и 0,2% церезина; б) 43,4% солидола Т, 43,4% парафина, 13,2% очищенного петролатума; в) 76,1% кирпичной пыли, 13,5% стеарина, 1,4% наждак№3, 0,9% венской извести, 8,1% солидола Т. Круги из войлока, фетра, кожи, наждачного полотна изготавливаются наборным способом. В качестве основы при этом служит деревянная либо металлическая основа. Матерчатые круги изготавливают путем сшивания некоторого количества заранее подготовленных дисков. Эти диски могут быть вырезаны из парусины, фланели, брезента, байки, бязи и т.п. Наружный диаметр зачастую не превышает 25 – 40 см. В состав круга для шлифования или полирования входит от 12 до 15 секций, в свою очередь, в каждой из них 15 – 20 сшитых или склеенных между собой дисков. На крупномасштабных производствах диски вырезают при помощи прессов, а на мелких предприятиях и вручную. Твердость круга очень сильно зависит не только от материала, используемого для его изготовления, но и от способа прошивки. Чем чаще швы – тем тверже получается круг. Широкое распространение получили концентрический и спиральный способы прошивки. Способы прошивки матерчатых кругов: - радиальный; - концентрический; - крестообразный; - тангенциальный; - спиральный и др. После того, как круг прошили, его балансируют и центрируют на специальных машинах. Далее, когда поверхность стала уравновешенной, шлифовальный или полировальный круг обрабатывают клеящим составом (столярным или казеиновым). Клей сначала подогревают, и только потом наносят равномерным слоем на круг. Затем на специальных станках накатывают (вручную или автоматически) подогретый до 40 – 45 °С абразивный материал. Кроме шлифовальных кругов могут использоваться еще и шлифовальные ленты. Это бесконечные ремни с абразивным материалом, тканевые ленты, склеенные между собой полосы шлифовальной шкурки на бумажной или матерчатой основе и т.п. Обезжиривание Обезжиривание проводят для удаления маслянистых и жировых загрязнений. Для этого применяют специальные растворители: керосин, уай-спирит, трихлорэтилен, бензин, растворы различных солей и щелочей. Изделие погружают в ванну с растворителем, омывают им или просто протирают поверхность металла. Обезжиривание подразделяется на: химическое и электрохимическое, ультразвуковое, термическое. Травление Травление применяется для удаления ржавчины, окалины и других продуктов коррозии с поверхности многих металлов. Зачастую травление проводят в растворах различных кислот с добавками ингибиторов кислотной коррозии, иногда в щелочах. Замедлители коррозии способствуют удалению загрязнения, сводя при этом потери основного металла к минимуму. Подразделяется травление также на: химическое и электрохимическое. Химическое травление проводят в растворенных или концентрированных кислотах и их смесях. Иногда рабочий травильный раствор подогревают до определенной температуры для интенсификации процесса удаления загрязнений. Концентрированную соляную кислоту, подогретую до температуры 40°С применяют для травления углеродистых сталей. Процесс длится от пяти минут до получаса (зависит от загрязнения). Электрохимическое травление чаще всего применяется для анодного либо катодного травления углеродистых и легированных сталей. Может проводиться в подкисленных растворах солей железа или растворах солей щелочных металлов, соляной, серной кислотах и их смесях. Во время катодного травления восстанавливаются ионы водорода, образующие на поверхности металла множество пузырьков. При отрыве пузырьков от металла загрязнение удаляется механически. Анодное травление применяется реже, т.к. ускоряет растворение основного металла. Ювелирные изделия подвергают электрохимическому или химическому полированию, мелкие детали очищают ультразвуком. После травления металлическое изделие необходимо тщательно промыть, и просушить перед нанесением защитного покрытия. Список использованных источников 1) А.Я. Шаталов. Электрохимические основы теории коррозии металлов. Изд. Воронежского Университета. Воронеж. 1971г. 180 стр. 2) Ф.А. Швейцер. Коррозия пластмасс и резин. Изд. НОТ. Спб. 2010г. 640 стр. 3) В.И. Сафрончик. Защита подземных трубопроводов антикоррозионными покрытиями. Стройиздат. Ленинград. 1977г. 120 стр. 4) http://www.okorrozii.com/podgotovka-poverhnosti.html |
